Documentos de Académico
Documentos de Profesional
Documentos de Cultura
10 Apunte Ley de Decaimiento Radioactivo
10 Apunte Ley de Decaimiento Radioactivo
Cargado por
Felipe Harvez SanchezTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
10 Apunte Ley de Decaimiento Radioactivo
10 Apunte Ley de Decaimiento Radioactivo
Cargado por
Felipe Harvez SanchezCopyright:
Formatos disponibles
Universidad de Chile
Facultad de Medicina
Departamento de Tecnología Médica
Física de Radiaciones y Dosimetría
Ley de Decaimiento Radioactivo
T.M. Macarena Cubillos Mesías, MSc
1. Constante de decaimiento
Considérese un número N de átomos radioactivos iguales. Se define λ como la constante
de decaimiento radioactivo total, que tiene dimensiones s-1. El producto de λ por un
tiempo determinado en segundos << 1/ λ es la probabilidad que un átomo individual
decaiga durante ese intervalo de tiempo.
Se asume que λ es independiente de la edad del átomo y de las condiciones físicas y
químicas como temperatura, presión, concentración, etc.
El valor esperado del número total de átomos en el grupo que se desintegran por unidad de
tiempo mucho menor a 1/ λ se conoce como la actividad de la muestra λN. La tasa de
cambio de N en cualquier tiempo t es equivalente a la actividad:
𝑑𝑁
− = 𝜆𝑁
𝑑𝑡
Al separar variables e integrar desde t = 0 (cuando N = N0) a t:
𝑁 𝑡
𝑑𝑁
= − 𝜆 𝑑𝑡
𝑁0 𝑁 0
ln 𝑁 − ln 𝑁0 = −(𝜆𝑡 − 0)
𝑁
ln = −𝜆𝑡
𝑁0
𝑁
= 𝑒 −𝜆𝑡
𝑁0
Así se puede escribir la razón de las actividades a tiempo t:
𝜆𝑁
= 𝑒 −𝜆𝑡
𝜆𝑁0
Lo que coincide con la ley de decaimiento radioactivo observada experimentalmente
1 Ley de Decaimiento Radioactivo – Física de Radiaciones y Dosimetría
Tecnología Médica – Universidad de Chile
Si un núcleo tiene más de un modo de desintegración posible (es decir, diferentes núcleos
hijos), la constante de decaimiento total puede ser escrita como la suma de las constantes de
decaimiento parciales λi:
𝜆 = 𝜆𝐴 + 𝜆𝐵 + 𝜆𝐶 + …
Y la actividad total se expresa como:
𝑁𝜆 = 𝑁𝜆𝐴 + 𝑁𝜆𝐵 + 𝑁𝜆𝐶 + …
2. Unidades de actividad
Se han definido varias unidades para la definición de actividad. La unidad antigua de
actividad era el curie (Ci), originalmente definido como el número de desintegraciones por
segundo que ocurren en una masa de 1 g de 226Ra. Posteriormente se definió simplemente
como equivalente a 3.7 x 1010 s-1.
Recientemente, debido a estándares internacionales, se definió el becquerel (Bq) como
equivalente a 1 desintegración por segundo, en unidades de s-1. Por lo tanto:
1 Ci = 3.7 x 1010 Bq
1 mCi = 3.7 x 107 Bq
1 μCi = 3.7 x 104 Bq
3. Vida media y período de semidesintegración
La vida promedio τ de una muestra es el valor esperado del tiempo requerido para que una
población inicial de núcleos radioactivos N0 decaiga a 1/e de de su número original. Por lo
tanto:
𝑁 1
= = 0.3679 = 𝑒 −𝜆𝑡
𝑁0 𝑒
ln 𝑒 −1 = −1 = −𝜆𝜏
1
𝜏=
𝜆
La vida promedio τ representa el tiempo de vida promedio de un núcleo individual desde un
tiempo de inicio t0 hasta que decae en el tiempo t. El intervalo t – t0 puede ir desde 0 a
infinito.
2 Ley de Decaimiento Radioactivo – Física de Radiaciones y Dosimetría
Tecnología Médica – Universidad de Chile
El período de semidesintegración o vida media 𝒕𝟏/𝟐 es el valor esperado del tiempo
requerido para que la mitad de los núcleos iniciales se desintegre, por lo tanto, decreciendo
la actividad a la mitad:
𝜆𝑁
= 0.5 = 𝑒 −𝜆𝑡1/2
𝜆𝑁0
ln 0.5 = −0.6931 = −𝜆𝑡1/2
0.6931
𝑡1/2 = = 0.6931 𝜏
𝜆
4. Cadenas de decaimiento radioactivo
Si se tiene que 1 → 2 (2 estable) con N1(0) = N0 y N2(0) = 0, es decir, el número inicial de
partículas de 1 (N1) a tiempo 0 es igual a N0 y el número inicial de partículas de 2 (N2) es
igual a cero:
𝑁1 𝑡 = 𝑁0 𝑒 −𝜆 1 𝑡
𝑁2 𝑡 = 𝑁0 (1 − 𝑒 −𝜆 1 𝑡 )
Ya que 𝑁1 (𝑡) + 𝑁2 (𝑡) = 𝑁0
Un caso particular importante se da cuando 1 → 2 → 3 (3 estable). N1(t) está dado por
𝑁1 𝑡 = 𝑁0 𝑒 −𝜆 1 𝑡 , mientras que N2(t):
𝜆1
𝑁2 𝑡 = 𝑁0 (𝑒 −𝜆 1 𝑡 − 𝑒 −𝜆 2 𝑡 )
𝜆2 − 𝜆1
Y 𝑁3 𝑡 = 𝑁0 − [𝑁1 𝑡 + 𝑁2 (𝑡)]. El máximo de actividad en 2 se alcanza en:
(𝜆2 /𝜆1 )(𝜆2 − 𝜆1 )−1
𝑡𝑚𝑎𝑥 = ln
Como:
𝜆2 𝑁2 (𝑡) 𝜆2
= 1 − 𝑒 [− 𝜆 2 − 𝜆 1 𝑡]
𝜆1 𝑁1 (𝑡) 𝜆2 − 𝜆1
Se comprueba que:
𝜆2 𝑁2 𝑡𝑚𝑎𝑥 = 𝜆1 𝑁1 𝑡𝑚𝑎𝑥
3 Ley de Decaimiento Radioactivo – Física de Radiaciones y Dosimetría
Tecnología Médica – Universidad de Chile
La situación más interesante se presenta cuando 𝜆2 ≫ 𝜆1 : para tiempos 𝑡 ≫ 𝜆−1
2 se llega al
denominado equilibrio secular:
𝜆2 𝑁2 𝑡 = 𝜆1 𝑁1 𝑡
Y por lo tanto la actividad de 2 será igual a la actividad de 1.
5. Reacciones nucleares
En una típica reacción nuclear de un experimento de laboratorio, un haz de partículas x
incide sobre un blanco X. Después de la reacción, se observa que una partícula y sale,
dejando un núcleo residual Y, lo que puede escribirse como:
𝑥+𝑋 →𝑦+𝑌
Como una reacción química, una reacción nuclear debe estar balanceada, es decir, el
número total de protones debe ser igual antes y después de la reacción, al igual que el
número total de neutrones. Debido a que una reacción nuclear tiene lugar bajo la influencia
de fuerzas internas del proyectil y el blanco, sin otras fuerzas externas, la reacción
conservará la energía, el momento lineal y el momento angular.
En la mayoría de los experimentos se observa solamente la partícula y; el núcleo residual Y
generalmente pierde toda su energía cinética (debido a colisiones con otros átomos), por lo
tanto se detiene dentro del blanco.
5.1 Cinemática de las reacciones nucleares
Se asumirá que las velocidades de las partículas son lo suficientemente pequeñas, de modo
de poder usar cinemática no relativista. Si se considera un proyectil x moviéndose con
momento px y energía cinética Kx, el blanco se encuentra en reposo, y los productos de la
reacción poseen momentos py y pY y energías cinéticas Ky y KY. Como en el caso del
decaimiento radioactivo, se usa la conservación de la energía para computar el valor Q para
esta reacción:
𝑚𝑁 (𝑥)𝑐 2 + 𝐾𝑥 + 𝑚𝑁 (𝑋)𝑐 2 = 𝑚𝑁 (𝑦)𝑐 2 + 𝐾𝑦 + 𝑚𝑁 (𝑌)𝑐 2 + 𝐾𝑌
La letra m representa las masas nucleares de las partículas de la reacción. Sin embargo,
como se mencionó anteriormente, en una reacción nuclear el número de protones debe estar
balanceado:
𝑍𝑥 + 𝑍𝑋 = 𝑍𝑦 + 𝑍𝑌
Reescribiendo la primera ecuación al ignorar la energía de ligadura de electrones, las masas
nucleares se convierten en masas atómicas sin correcciones adicionales:
4 Ley de Decaimiento Radioactivo – Física de Radiaciones y Dosimetría
Tecnología Médica – Universidad de Chile
𝑚 𝑥 + 𝑚 𝑋 − 𝑚 𝑦 − 𝑚 𝑌 𝑐 2 = 𝐾𝑦 + 𝐾𝑌 − 𝐾𝑥
La diferencia de energías de reposo entre las partículas iniciales y las finales se define
como el valor Q de la reacción:
𝑄 = 𝑚𝑖 − 𝑚𝑓 𝑐 2 = 𝑚 𝑥 + 𝑚 𝑋 − 𝑚 𝑦 − 𝑚 𝑌 𝑐 2
Por la ecuación anterior se ve que el valor Q es equivalente a la diferencia en energías
cinéticas entre las partículas finales y la partícula inicial:
𝑄 = 𝐾𝑦 + 𝐾𝑌 − 𝐾𝑥
6. Producción de radioisótopos
A menudo se utilizan reacciones nucleares para producir isótopos radioactivos. En este
procedimiento, un isótopo estable no radioactivo X se irradia con una partícula x para
formar un isótopo radioactivo Y. En este caso no se observan las partículas Y mientras son
producidas en la reacción, en cambo, estas partículas permanecerán en el blanco, y después
de la irradiación se observa el decaimiento radioactivo del núcleo Y.
Para calcular la actividad del radioisótopo Y que es producido en un intervalo de tiempo t,
sea R la razón constante a la cual Y es producido, la que está relacionada con la sección
eficaz y la intensidad del haz x. En un intervalo dt, el número de núcleos Y producidos es
Rdt. Debido a que Y es radioactivo, el número de núcleos de Y que decaen en el intervalo dt
es λNdt, donde λ es la constate de decaimiento y N es el número de núcleos Y presentes.
El cambio neto dN en el número de núcleos Y es:
𝑑𝑁 = 𝑅 𝑑𝑡 − 𝜆𝑁 𝑑𝑡
𝑑𝑁
= 𝑅 − 𝜆𝑁
𝑑𝑡
La solución de esta ecuación diferencial es:
𝑅
𝑁 𝑡 = (1 − 𝑒 −𝜆𝑡 )
𝜆
Y la actividad equivale a:
𝐴 𝑡 = 𝜆𝑁 = 𝑅(1 − 𝑒 −𝜆𝑡 )
5 Ley de Decaimiento Radioactivo – Física de Radiaciones y Dosimetría
Tecnología Médica – Universidad de Chile
Nótese que, como se espera, para t = 0, A = 0 (no hay núcleos Y presentes al inicio). Para
tiempos de irradiación grandes t >> t1/2, la expresión se aproxima al valor constante R.
Cuando t es pequeño comparado con el período de semidesintegración t1/2, la actividad
aumenta de manera lineal con respecto al tiempo:
𝐴 𝑡 = 𝑅 1 − 1 − 𝜆𝑡 + ⋯ ≅ 𝑅𝜆𝑡 (𝑡 ≪ 𝑡1/2 )
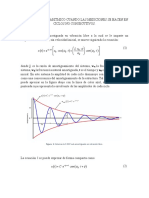
Se grafica la relación entre A(t) y t en la figura 1, y se puede observar que no se gana más
actividad cuando el tiempo de irradiación excede alrededor de dos períodos de
semidesintegración.
Figura 1. Formación de actividad en una reacción nuclear (Krane, 2012)
7. Radioactividad natural
Todos los elementos después de los más ligeros (hidrógeno y helio) fueron producidos por
reacciones nucleares en el interior de las estrellas: estas reacciones no solamente producen
elementos estables, sino que también elementos radioactivos. La mayoría de los elementos
radioactivos tienen períodos de semidesintegración mucho menores que la edad de la Tierra
(~ 4.5 x 109 años), por lo que esos elementos ya han decaído a elementos estables. Sin
embargo, algunos de estos elementos tienen períodos de semidesintegración cercanos a la
edad de la Tierra, por lo que pueden seguir siendo observados y experimentando
decaimiento radioactivo, formando parte de la radioactividad natural que nos rodea.
Estos procesos de decaimiento pueden ser de tipo alfa, cambiando el número másico A en 4
unidades, o beta o gamma, conservando A. Un proceso de decaimiento radioactivo puede
ser parte de una secuencia o series de decaimientos si un elemento radioactivo de número
másico A decae a otro elemento radioactivo de número másico A o A – 4. Esta serie de
procesos continuará hasta llegar a un elemento estable. Un esquema de una serie se muestra
en la figura 2.
6 Ley de Decaimiento Radioactivo – Física de Radiaciones y Dosimetría
Tecnología Médica – Universidad de Chile
Figura 2. Un ejemplo de una cadena de decaimiento radioactivo (Krane, 2012)
Los valores de A de los miembros de estas cadenas de decaimiento difieren por un múltiplo
de 4 (incluyendo cero como múltiplo posible), por lo que se esperan cuatro cadenas de
decaimiento posibles, con valores de A que se pueden expresar como 4n, 4n + 1, 4n + 2 y
4n + 3, donde n es un número entero.
Cada serie comienza con un elemento de vida media relativamente larga, que experimenta
muchos decaimientos α y β, los que pueden tener vidas medias muy cortas, hasta
finalmente terminar en un isótopo estable. Tres de estas series comienzan con isótopos con
períodos de semidesintegración comparables a la edad de la Tierra, por lo que siguen
siendo observados en la actualidad: por ejemplo, la serie del neptunio comienza con el
237
Np, que tiene un período se semidesintegración de 2.1 x 106 años, mucho menor que la
edad de la Tierra (4.5 x 109 años), por lo tanto, todo el 237Np que se encontraba presente
originalmente ha decaído a 209Bi. En la figura 3 se muestra la cadena de decaimiento del
235
U.
Figura 3. Cadena de decaimiento del 235U. Las líneas diagonales representan decaimientos α,
mientras que las líneas horizontales representan decaimientos β (Krane, 2012)
7 Ley de Decaimiento Radioactivo – Física de Radiaciones y Dosimetría
Tecnología Médica – Universidad de Chile
Existe cierto número de otros isótopos radioactivos que ocurren naturalmente, que no son
partes de una cadena de decaimiento de elementos pesados. Un listado se muestra en la
tabla 1.
Tabla 1. Algunos isótopos radioactivos que ocurren naturalmente, y: años (Krane, 2012)
Otros elementos radioactivos son producidos continuamente en la atmósfera terrestre como
resultado de reacciones nucleares entre moléculas de aire y partículas de alta energía
conocidas como rayos cósmicos.
El más notable es el 14C, con decaimiento beta con un período de semidesintegración de
5730 años. Cuando una planta absorbe CO2 desde la atmósfera, una pequeña fracción (~ 1
en 1012) de los átomos de carbono será 14C, el resto será el 12C estable (99%) y 13C (1%);
cuando muere, se detiene la absorción de 14C, el que comienza a decaer. Si se supone que la
composición de la atmósfera terrestre y el flujo de rayos cósmicos no ha cambiado
significativamente en los últimos miles de años, se puede determinar la edad de los
especímenes de material orgánico comparando sus razones 14C/12C con los de las plantas
vivientes, lo que se denomina fechado por radiocarbono.
8 Ley de Decaimiento Radioactivo – Física de Radiaciones y Dosimetría
Tecnología Médica – Universidad de Chile
8. Referencias
Attix, F. (1986). Radioactive Decay. En Attix F., Introduction to Radiological Physics and
Radiation Dosimetry (pp. 101-123)
Krane, K. (2012) Nuclear Structure and Radioactivity. En Krane K., Modern Physics (pp.
369-406)
Krane, K. (2012) Nuclear Reactions and Applications. En Krane K., Modern Physics (pp.
407-440)
Fernández-Varea, J. (2011) Radiactividad. En Brosed, A., Fundamentos de Física Médica
(pp. 131-164)
9 Ley de Decaimiento Radioactivo – Física de Radiaciones y Dosimetría
Tecnología Médica – Universidad de Chile
También podría gustarte
- Notas10 - Aplicaciones - Primer Orden PDFDocumento6 páginasNotas10 - Aplicaciones - Primer Orden PDFsantiagosa22Aún no hay calificaciones
- Inestabilidad NuclearDocumento13 páginasInestabilidad NuclearMaria Jose TrinidadAún no hay calificaciones
- Elementos de RadiactividadDocumento62 páginasElementos de RadiactividadSteven CadenaAún no hay calificaciones
- Desintegraciones Em2011Documento55 páginasDesintegraciones Em2011vicky8595Aún no hay calificaciones
- Problemas de AplicacionDocumento17 páginasProblemas de Aplicaciondpolaniaa0% (1)
- Decaimiento 4 ToDocumento4 páginasDecaimiento 4 TotemulentiaAún no hay calificaciones
- Radioactividad Clase 2Documento22 páginasRadioactividad Clase 2OannesAún no hay calificaciones
- Problemas Resueltos de Física Nuclear: Ley de Decaimiento Radiactivo.Documento30 páginasProblemas Resueltos de Física Nuclear: Ley de Decaimiento Radiactivo.Gabriela Alessandra Villacorta GarcíaAún no hay calificaciones
- Estudio Cuantitativo de La RadioactivadDocumento5 páginasEstudio Cuantitativo de La RadioactivadLeonardo CervantesAún no hay calificaciones
- Desintegración Radiactiva en 3 Etapas y Curva Logística - TerminadoDocumento18 páginasDesintegración Radiactiva en 3 Etapas y Curva Logística - TerminadoKatia Merlano Canoles100% (1)
- POSITRONIODocumento21 páginasPOSITRONIOtome_luqueAún no hay calificaciones
- Problemas Resueltos Modelo de DrudeDocumento13 páginasProblemas Resueltos Modelo de DrudeAntonio Navarro100% (1)
- Vida Media FormulaDocumento2 páginasVida Media FormulaHehazo Tuirhan JhosepAún no hay calificaciones
- Demostracion Decremento LogDocumento4 páginasDemostracion Decremento LogEdison TerrerosAún no hay calificaciones
- RADIOACTIVIDAD1Documento10 páginasRADIOACTIVIDAD1Romina Ticahuanca EspinalAún no hay calificaciones
- Desarrollo EcuacionesDocumento11 páginasDesarrollo EcuacionesYadir Martinez DazaAún no hay calificaciones
- 13 Isotp RadDocumento47 páginas13 Isotp RadM. MaldonadoAún no hay calificaciones
- Primeras CuantizacionesDocumento28 páginasPrimeras Cuantizacionesprofesor.sebastian.castillo.lblAún no hay calificaciones
- Ciencia de MaterialesDocumento15 páginasCiencia de MaterialesFaby Avilés NavarroAún no hay calificaciones
- ClaseS7 1Documento19 páginasClaseS7 1Milagros MorenoAún no hay calificaciones
- Supuestos o Postulados: Volumen e Interacciones Moleculares DespreciablesDocumento10 páginasSupuestos o Postulados: Volumen e Interacciones Moleculares DespreciablesFacundoo RuizAún no hay calificaciones
- Taller - Fase 2 Decaimiento Radiactivo y Desintegracion NuclearDocumento9 páginasTaller - Fase 2 Decaimiento Radiactivo y Desintegracion NuclearAndrea Niño CubillosAún no hay calificaciones
- Cap. 8Documento4 páginasCap. 8OLVER ARIEL ANCO MAMANIAún no hay calificaciones
- Física Nuclear - ApuntesDocumento5 páginasFísica Nuclear - ApuntesSandra TorralbaAún no hay calificaciones
- 06 Física Del Siglo XXDocumento32 páginas06 Física Del Siglo XXHxDavxzAún no hay calificaciones
- Decaimiento Alpha, Beta y gamma-SAVIODocumento37 páginasDecaimiento Alpha, Beta y gamma-SAVIOMiguel MejiaAún no hay calificaciones
- TEMAFQ35o NúcleoAtómicoDocumento2 páginasTEMAFQ35o NúcleoAtómicoajggAún no hay calificaciones
- Taller N°10Documento6 páginasTaller N°10David Andres Arguello BernalAún no hay calificaciones
- Ejercicios Resueltos de Física de RadiacionesDocumento11 páginasEjercicios Resueltos de Física de RadiacionesGabriela Alessandra Villacorta GarcíaAún no hay calificaciones
- Tema 3. Apuntes - Fundamentos - Cuanticos PDFDocumento23 páginasTema 3. Apuntes - Fundamentos - Cuanticos PDFRaúl López SánchezAún no hay calificaciones
- Cap 2 CF 04622 IibDocumento10 páginasCap 2 CF 04622 IibRODRIGO ALONZO VELASQUEZ FLORESAún no hay calificaciones
- Mecánica Cuántica 1Documento57 páginasMecánica Cuántica 1Jonathan ClarosAún no hay calificaciones
- Planck WeinDocumento9 páginasPlanck Weinsf9715Aún no hay calificaciones
- Ecuaciones de Johnson-Mehl y ArrheniusDocumento5 páginasEcuaciones de Johnson-Mehl y ArrheniusSebastian CedilloAún no hay calificaciones
- Ondas y CuanticaDocumento4 páginasOndas y CuanticaGabriel LeónAún no hay calificaciones
- Cinetica de La Radiactividad: CapituloDocumento11 páginasCinetica de La Radiactividad: Capitulogd6s2bpj25Aún no hay calificaciones
- Fase2 Colaborativa Elizabeth MontoyaDocumento6 páginasFase2 Colaborativa Elizabeth MontoyacarlosAún no hay calificaciones
- Ley de La Desintegracion RadiactivaDocumento3 páginasLey de La Desintegracion RadiactivaAdamAún no hay calificaciones
- Pag 61 Práctica - 8-Actividad de Un RadioelementoDocumento6 páginasPag 61 Práctica - 8-Actividad de Un RadioelementoVismel AlmonteAún no hay calificaciones
- Tarea Físca Nuclear UNAMDocumento3 páginasTarea Físca Nuclear UNAMToñooDiazVillarrealAún no hay calificaciones
- Ecuaciones Diferenciales Crecimiento y Decaimiento Ley de MalthusDocumento6 páginasEcuaciones Diferenciales Crecimiento y Decaimiento Ley de MalthusKdavid Marichal VeglianteAún no hay calificaciones
- Atractores Extraños y Geometría FractalDocumento6 páginasAtractores Extraños y Geometría FractalObitoplay UchihaAún no hay calificaciones
- Ecuaciones Diferenciales Crecimiento y Decaimiento Ley de MalthusDocumento6 páginasEcuaciones Diferenciales Crecimiento y Decaimiento Ley de MalthusMafe VergaraAún no hay calificaciones
- TallerDocumento10 páginasTallerManuel Alejandro Navas CAún no hay calificaciones
- Clases Mc1Documento37 páginasClases Mc1jimmijoelticonaAún no hay calificaciones
- Control 1Documento2 páginasControl 1julian.pinoAún no hay calificaciones
- Clase 13 - Fisica ModernaDocumento25 páginasClase 13 - Fisica ModernaRonald Alejandro Perez OrtizAún no hay calificaciones
- Ayud5 PautaDocumento6 páginasAyud5 PautaPatricio Esteban Triviño IbacacheAún no hay calificaciones
- Cuerpo NegroDocumento26 páginasCuerpo NegroLucas MalacalzaAún no hay calificaciones
- RADIACIÓNDocumento31 páginasRADIACIÓNLuis Angel Ortiz LangoAún no hay calificaciones
- Tarea Oscilaciones 3Documento5 páginasTarea Oscilaciones 3Juan Carlos Morales ParraAún no hay calificaciones
- ProyectoDocumento3 páginasProyectoAna NogueraAún no hay calificaciones
- Solucion de Problemas Tema 6 Fisica IIIDocumento5 páginasSolucion de Problemas Tema 6 Fisica IIIAlejandro Lázaro AguilarAún no hay calificaciones
- Aplicaciones en Edo Plataforma GMDocumento6 páginasAplicaciones en Edo Plataforma GMGerman MeraAún no hay calificaciones
- Fase 2 - Grupo 17.Documento12 páginasFase 2 - Grupo 17.adriana ibarra torresAún no hay calificaciones
- Curso básico de teoría de númerosDe EverandCurso básico de teoría de númerosCalificación: 5 de 5 estrellas5/5 (2)
- Ingeniería química. Soluciones a los problemas del tomo IDe EverandIngeniería química. Soluciones a los problemas del tomo IAún no hay calificaciones
- Previo3 BQDocumento3 páginasPrevio3 BQsusanaAún no hay calificaciones
- Zeolitas Estructura y AplicacionesDocumento25 páginasZeolitas Estructura y AplicacionesAaron Garcia SanchezAún no hay calificaciones
- Tema 3. El Color en La BiologiaDocumento25 páginasTema 3. El Color en La BiologiaRuben CartagenaAún no hay calificaciones
- Unidad 3 - Clasificación Del Enlace CovalenteDocumento19 páginasUnidad 3 - Clasificación Del Enlace CovalenteEdu Vallejo GaiborAún no hay calificaciones
- Ejercicios Primera Ley TermodinámicaDocumento9 páginasEjercicios Primera Ley TermodinámicabrayanfloresmerinoAún no hay calificaciones
- Tarea 7 - SólidosDocumento2 páginasTarea 7 - SólidosCuau SuarezAún no hay calificaciones
- Recibo 372191001651 JunioDocumento2 páginasRecibo 372191001651 JunioORLANDO CRUZAún no hay calificaciones
- M.O RobertDocumento25 páginasM.O RobertEmanuel CardonaAún no hay calificaciones
- Presentación Del Sr. Amadeo ArrarteDocumento24 páginasPresentación Del Sr. Amadeo Arrartejose roque mostacero ramosAún no hay calificaciones
- Ejercicios Caída LibreDocumento16 páginasEjercicios Caída LibreOlvin Steve Rosales MenjivarAún no hay calificaciones
- Ejercicios SedimentacionDocumento21 páginasEjercicios SedimentacionOlga Hernandez100% (1)
- Indicadores Serie 3000 Manual de Instrucciones: Indicador T32MEDocumento48 páginasIndicadores Serie 3000 Manual de Instrucciones: Indicador T32MElizarazojavierAún no hay calificaciones
- Campo Eléctrico y Líneas EquipotencialesDocumento11 páginasCampo Eléctrico y Líneas Equipotencialesjhonfredy araquealarcónAún no hay calificaciones
- Albert Einstein y El Síndrome de ASPERGERDocumento1 páginaAlbert Einstein y El Síndrome de ASPERGERLeon S. SchwartzmanAún no hay calificaciones
- Memoria de CalculoDocumento11 páginasMemoria de CalculoDiego Ortiz MolinaAún no hay calificaciones
- El Termometro de GalileoDocumento7 páginasEl Termometro de GalileoAAún no hay calificaciones
- CIRCUITOS NTC y PTCDocumento31 páginasCIRCUITOS NTC y PTCWilliam Manotoa100% (2)
- Módulo LED 40W Philips LUMILEDS para FarolasDocumento6 páginasMódulo LED 40W Philips LUMILEDS para FarolasIsaac Ramirez GarciaAún no hay calificaciones
- Informe 3 - Peso UnitarioDocumento33 páginasInforme 3 - Peso UnitarioAndrea Sofía Núñez VizcainoAún no hay calificaciones
- Trabajo Autonomo Grupal U2Documento47 páginasTrabajo Autonomo Grupal U2Diego OrtizAún no hay calificaciones
- DISEÑO DE VIGA TechoDocumento8 páginasDISEÑO DE VIGA Techoandres pulidoAún no hay calificaciones
- Tema 9. Enlace Químico 2000-2009 (Extra)Documento48 páginasTema 9. Enlace Químico 2000-2009 (Extra)joseluAún no hay calificaciones
- T13 Maquinas de Corriente Continua PDFDocumento11 páginasT13 Maquinas de Corriente Continua PDFOshun Graciela luna choqueAún no hay calificaciones
- Ensayo DedormaciónDocumento13 páginasEnsayo DedormaciónChristopher PozziAún no hay calificaciones
- UrielTobiasMartinez PM T2P1Documento6 páginasUrielTobiasMartinez PM T2P1URIEL TOBIAS MARTINEZAún no hay calificaciones
- Ejercicios de Teoría de Grupos Sobre Permutaciones y MorfismosDocumento6 páginasEjercicios de Teoría de Grupos Sobre Permutaciones y MorfismosMario HernándezAún no hay calificaciones
- MAnual de Mantenimiento y Reparacion KRC4 CompactDocumento72 páginasMAnual de Mantenimiento y Reparacion KRC4 CompactRuben Gaytan LealAún no hay calificaciones
- REMM Segundo Corte IndividualDocumento3 páginasREMM Segundo Corte IndividualDiego Alejandro Tello OspinaAún no hay calificaciones
- Entrega 5 - Fisica Trabajo ColaborativoDocumento14 páginasEntrega 5 - Fisica Trabajo ColaborativoYuly Paola YURGAKY VARGASAún no hay calificaciones
- Practica Iii - Tipos de MovimientosDocumento8 páginasPractica Iii - Tipos de MovimientosJacke AngelesAún no hay calificaciones