0% encontró este documento útil (0 votos)
195 vistas4 páginasPropiedades y Usos de la Acetona
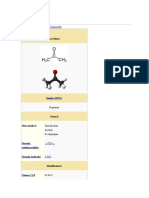
La acetona es un compuesto químico incoloro y volátil que se utiliza principalmente como disolvente industrial y en la fabricación de plásticos y fibras. Se produce a escala industrial mediante la hidrólisis del hidroperóxido de cumeno o la deshidrogenación del alcohol isopropílico. Sus principales aplicaciones son en la síntesis de metil metacrilato, bisfenol A y como disolvente.
Cargado por
EsliDavidMolerosIngunzaDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como TXT, PDF, TXT o lee en línea desde Scribd
0% encontró este documento útil (0 votos)
195 vistas4 páginasPropiedades y Usos de la Acetona
La acetona es un compuesto químico incoloro y volátil que se utiliza principalmente como disolvente industrial y en la fabricación de plásticos y fibras. Se produce a escala industrial mediante la hidrólisis del hidroperóxido de cumeno o la deshidrogenación del alcohol isopropílico. Sus principales aplicaciones son en la síntesis de metil metacrilato, bisfenol A y como disolvente.
Cargado por
EsliDavidMolerosIngunzaDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como TXT, PDF, TXT o lee en línea desde Scribd