Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Ental Pia
Cargado por
luisa fernanda0 calificaciones0% encontró este documento útil (0 votos)
7 vistas1 páginabuen documeto
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentobuen documeto
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
7 vistas1 páginaEntal Pia
Cargado por
luisa fernandabuen documeto
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 1
ENTALPIA:
La Entalpa es la cantidad de energa de un sistema termodinmico que ste puede intercambiar
con su entorno. Por ejemplo, en una reaccin quimica a presion constante, el cambio de entalpa
del sistema es el calor absorbido o desprendido en la reaccin. En un cambio de fase, por ejemplo
de lquido a gas, el cambio de entalpa del sistema es el calor latente, en este caso el de
vaporizacin. En un simple cambio de temperatura, el cambio de entalpa por cada grado de
variacin corresponde a la capacidad calorfica del sistema a presin constante. El trmino de
entalpa fue acuado por el fsico alemn Rudolf J.E. Clausius en 1850. Matemticamente, la
entalpa H es igual a U + pV, donde U es la energa interna, p es la presin y V es el volumen. H se
mide en julios.
H = U + pV
Cuando un sistema pasa desde unas condiciones iniciales hasta otras finales, se mide el cambio de
entalpa ( H).
H = Hf Hi
También podría gustarte
- Competencia de Matemáticas de 6 Hasta 11Documento3 páginasCompetencia de Matemáticas de 6 Hasta 11luisa fernandaAún no hay calificaciones
- Importancia de La TermodinamicaDocumento1 páginaImportancia de La Termodinamicaluisa fernandaAún no hay calificaciones
- Teoría de reforzamiento de SkinnerDocumento8 páginasTeoría de reforzamiento de Skinnerkalmae2wkrew100% (2)
- Biologia 1bach PDFDocumento28 páginasBiologia 1bach PDFrafagil2bAún no hay calificaciones
- Evalucion Del Curriculo en Educación Preescolar PDFDocumento132 páginasEvalucion Del Curriculo en Educación Preescolar PDFluisa fernanda100% (1)
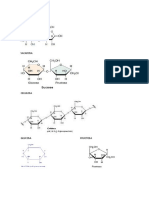
- CarbohidratosDocumento11 páginasCarbohidratosluisa fernandaAún no hay calificaciones
- Periodos o Etapas Del Desarrollo InfantilDocumento8 páginasPeriodos o Etapas Del Desarrollo Infantilluisa fernandaAún no hay calificaciones
- Sistema EconomicoDocumento16 páginasSistema EconomicoDavid SanabriaAún no hay calificaciones
- TEMA 12 1o ESODocumento5 páginasTEMA 12 1o ESOluisa fernandaAún no hay calificaciones
- Gestalt - Qué Es, Características, Leyes, Autores y Principales AplicacionesDocumento20 páginasGestalt - Qué Es, Características, Leyes, Autores y Principales Aplicacionesluisa fernandaAún no hay calificaciones
- Guía de orientación sobre términos y condiciones de uso de publicaciones del ICFESDocumento19 páginasGuía de orientación sobre términos y condiciones de uso de publicaciones del ICFESCarlosRamirezAún no hay calificaciones
- Artículo MojanaDocumento13 páginasArtículo Mojanaluisa fernandaAún no hay calificaciones
- Ensayodecurrculo 121010223456 Phpapp01Documento5 páginasEnsayodecurrculo 121010223456 Phpapp01luisa fernandaAún no hay calificaciones
- 10 ProblemasdeecuacionescuadrticasDocumento10 páginas10 ProblemasdeecuacionescuadrticasKarina PichardoAún no hay calificaciones
- EjercicioscinematicaDocumento3 páginasEjercicioscinematicaCaroLiinaa HeernaanDez100% (1)
- Trabajo 2Documento2 páginasTrabajo 2luisa fernandaAún no hay calificaciones
- Carbohidratos PDFDocumento55 páginasCarbohidratos PDFJeimmy Paola DíazAún no hay calificaciones
- Biología Celular 2012 MacromoleculasDocumento86 páginasBiología Celular 2012 MacromoleculasCarmen Nicole Monsalve EspinosaAún no hay calificaciones
- Ejercicios de Permutaciones y CombinacionesDocumento3 páginasEjercicios de Permutaciones y Combinacionesmatematicaslaunidad82% (34)
- Taller PIR 10Documento3 páginasTaller PIR 10luisa fernandaAún no hay calificaciones
- 1.5 Modelos Termodinámicos HysysDocumento12 páginas1.5 Modelos Termodinámicos HysysJorge RamirezAún no hay calificaciones
- Cinemática Directa (Robot Cilindrico)Documento23 páginasCinemática Directa (Robot Cilindrico)jared eliezer baldenegro gomezAún no hay calificaciones
- Universidad Nacional de PiuraDocumento11 páginasUniversidad Nacional de PiuraEfrain Anderson Silva SandovalAún no hay calificaciones
- DinámicaDocumento18 páginasDinámicalucy garciaAún no hay calificaciones
- Mruv Pre-U 14-03-2023Documento3 páginasMruv Pre-U 14-03-2023Alonso PumaAún no hay calificaciones
- Diseño Del Puente Peatonal Colgante FinalDocumento37 páginasDiseño Del Puente Peatonal Colgante FinalCarlos GonzalesAún no hay calificaciones
- Taller 3 A PDFDocumento2 páginasTaller 3 A PDFJoaquin A.Aún no hay calificaciones
- Apuntes Capitulo 2 de ETM 351Documento14 páginasApuntes Capitulo 2 de ETM 351Marco Antonio MamaniAún no hay calificaciones
- Ondas armónicas y su propagaciónDocumento32 páginasOndas armónicas y su propagaciónOjolo YuyiyAún no hay calificaciones
- 4 Capitulo 9Documento23 páginas4 Capitulo 9kelvis penaAún no hay calificaciones
- Tema 1 Repaso CinematicaDocumento14 páginasTema 1 Repaso CinematicaJuan José Bermejo DominguezAún no hay calificaciones
- Componentes y clasificación de eslabones y mecanismosDocumento8 páginasComponentes y clasificación de eslabones y mecanismosErick González LópezAún no hay calificaciones
- Pórticos Dúctiles de Hormigón Armado - Diseño de Vigas. Redistribución de EsfuerzosDocumento26 páginasPórticos Dúctiles de Hormigón Armado - Diseño de Vigas. Redistribución de EsfuerzosSascha ThiesfeldAún no hay calificaciones
- Tabla Ilustrada de Diagnostico de VibracionesDocumento5 páginasTabla Ilustrada de Diagnostico de VibracionesJuan GiavenoAún no hay calificaciones
- Determinacion Del Modulo de Young y Rigidez de La Papa Tomasa (Tomasa Tito Condemayta)Documento16 páginasDeterminacion Del Modulo de Young y Rigidez de La Papa Tomasa (Tomasa Tito Condemayta)Gianfranco Gzs100% (1)
- Balance de Cantidad de MovimientoDocumento11 páginasBalance de Cantidad de MovimientoBenjamín GarnicaAún no hay calificaciones
- Respuesta Del Yunque de Un Martillo de ForjaDocumento19 páginasRespuesta Del Yunque de Un Martillo de ForjaMoncayo Matute Freddy PatricioAún no hay calificaciones
- AislamientoDocumento88 páginasAislamientocrismalr3dAún no hay calificaciones
- TrabajoDocumento3 páginasTrabajoAmaury PortacioAún no hay calificaciones
- Universidad Católica de Santa María: Facultad de Ciencias E Ingenierías Físicas Y FormalesDocumento283 páginasUniversidad Católica de Santa María: Facultad de Ciencias E Ingenierías Físicas Y FormalesFlia Rincon Garcia SoyGabyAún no hay calificaciones
- Fisica Martin Soto SaldarriagaDocumento4 páginasFisica Martin Soto Saldarriagajose humberto gomez jimenezAún no hay calificaciones
- Capitulo 1Documento72 páginasCapitulo 1DianaAguilarCoroAún no hay calificaciones
- Vibraciones libres de sistemas de un grado de libertadDocumento17 páginasVibraciones libres de sistemas de un grado de libertadVickman PenagosAún no hay calificaciones
- Pendulo DobleDocumento16 páginasPendulo DobleOrlando Perez CarrilloAún no hay calificaciones
- LabMaqElectrEsta92G-Curva de Magnetizacion y Relaciones de TransformacionDocumento12 páginasLabMaqElectrEsta92G-Curva de Magnetizacion y Relaciones de TransformacionDIAZ CUBA ROGER JEANPOOLAún no hay calificaciones
- Los Potenciales ElectromagneticosDocumento38 páginasLos Potenciales ElectromagneticosOscar DiceAún no hay calificaciones
- IV FIN 111 TE Choquehuayta Eguiluz 2020Documento123 páginasIV FIN 111 TE Choquehuayta Eguiluz 2020Deisy Hurtado HuancaAún no hay calificaciones
- Deformación de La Corteza TerrestreDocumento27 páginasDeformación de La Corteza TerrestreaplicacionesAún no hay calificaciones
- Ley de HookeDocumento14 páginasLey de HookeWido Saavedra RomanAún no hay calificaciones
- Momento LinealDocumento21 páginasMomento LinealLeandro GarciaAún no hay calificaciones