Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Ejemplos de IRQ
Cargado por
Gustavo CardonaDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Ejemplos de IRQ
Cargado por
Gustavo CardonaCopyright:
Formatos disponibles
1
EJEMPLOS DE LA UNIDAD 2: MODELAJE DE LA CINETICA DE LAS REACCIONES
QUIMICAS
APLICACIN DEL METODO INTEGRAL DE ANALISIS DE DATOS CINETICOS
EJEMPLO 2.1
R.T. Dillon ha estudiado la reaccin entre el bromuro de etileno y el yoduro de potasio en
solucin de metanol al 99%:
3 4 2 2 4 2
2 3 KI KBr H C KI Br H C + + + . Dada la siguiente
tabla de datos, determinar la ecuacin de velocidad.
Temperatura: 59.72C
Concentracin inicial de KI: 0.1531kmol/m
3
Concentracin inicial de C2H4:Br2: 0.02864kmol/m
3
Tiempo, t (s) Fraccin de
dibromuro (_
A
)
29.7 0.2863
40.5 0.3630
47.7 0.4099
55.8 0.4572
62.1 0.4890
72.9 0.5396
83.7 0.5795
SOLUCION:
1. Hiptesis: segundo orden, tipo II, sistema a volumen constante:
B A A
C kC r = .
2. Datos cinticos:
2 4 2
Br H C
_ , tiempo t (s), M = C
Bo
/C
Ao
= 0.1531/0.02864 = 5.35 =
3
2 4 2
=
Br H C
KI
v
v
.
3. Procedimiento de integracin:
B A A
C kC r =
B A
A
Ao
C kC
dt
d
C =
_
Balance de moles:
) (
A Ao A
C C _ = 1 ;
A Ao A B Bo B
C C C _ v v ) / ( = ) ) / ( (
A A B Ao B
M C C _ v v =
Ecuacin:
) ) / ( ( ) (
A A B Ao A Ao
A
Ao
M C kC
dt
d
C _ v v _
_
= 1
) ) / ( )( (
A A B A Ao
A
M kC
dt
d
_ v v _
_
= 1
Separando variables:
) ) / ( )( (
A A B A Ao
A
M C
d
kdt
_ v v _
_
=
1
Integrando se tiene:
2
|
|
.
|
\
|
=
=
=
}
} }
) (
) ) ( (
ln )) / ( (
) ) / ( )( (
) ) / ( )( (
A
A B
A B Ao
A A B A Ao
A
A A B A Ao
A
t
M
M
kt M C
M C
d
kt
M C
d
dt k
A
A
_
_ v
v v
_ v v _
_
_ v v _
_
_
_
1
1
1
0
0 0
4. Variable de composicin:
|
|
.
|
\
|
) ( .
) . (
ln
A
A
_
_
1 35 5
3 35 5
, tiempo = t
5. Prueba del modelo:
TABLA E.2.1.1
Tiempo, t (s) Fraccin de
dibromuro (_
A
)
|
|
.
|
\
|
) ( .
) . (
ln
A
A
_
_
1 35 5
3 35 5
0 0 0
29.7 0.2863 0.1571
40.5 0.3630 0.2223
47.7 0.4099 0.2652
55.8 0.4572 0.3136
62.1 0.4890 0.3497
72.9 0.5396 0.4142
83.7 0.5795 0.4721
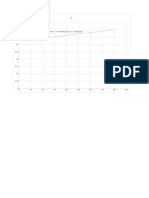
FIGURA E.2.1.1
Prueba segundo orden tipo II f(Xa) = 0.0056t
R
2
= 0.999
0
0.1
0.2
0.3
0.4
0.5
0 20 40 60 80 100
tiempo
f
u
n
c
i
n
d
e
X
a
Dado que el coeficiente de determinacin (R
2
) es 0.9996 y el valor del
intercepto es cero, puede concluirse que la correlacin lineal es buena y por
lo tanto el modelo de segundo orden tipo II es til.
6. Determinacin de los parmetros del modelo:
3
s kmol
m
k
pendiente k M C
A B Ao
*
.
)) / ( . ( .
.
. )) / ( (
3
00832 0
1 3 35 5 2864 0
0056 0
0056 0
=
=
= = v v
Ecuacin de velocidad:
B A A
C C r 00832 0. = (a T = 59.72C)
EJEMPLO 2.2
Se ha estudiado la cintica de polimerizacin de cierto vinil eter activo pticamente
usando lecturas de rotacin ptica, obtenindose los siguientes resultados:
Tiempo, t (s) Rotacin ptica
()
0 2.79
3.6 2.20
7.2 1.84
10.8 1.59
14.4 1.45
18.0 1.38
1.27
Determine el orden y la velocidad especfica de reaccin si la concentracin inicial del
monmero es M
o
.
SOLUCION:
1. Hiptesis: primer orden, sistema a volumen constante:
A A
kC r = .
2. Forma integrada de primer orden:
|
|
.
|
\
|
=
Ao
A
C
C
kt ln
3. Datos cinticos: rotacin ptica (), tiempo t (s).
4. Acondicionamiento de de datos cinticos: por tratarse de mediciones de una
propiedad fsica debe procederse a buscar la relacin entre esta propiedad y la
concentracin del reactivo, segn lo descrito en la seccin 2.4.1(a) de la unidad 2,
esta relacin viene dada por:
|
|
.
|
\
|
+ =
-
o
o
i io i
C C
o o
o o
c v
o
o
Si o = , entonces:
|
|
.
|
\
|
+ =
-
o
o
A Ao A
C C
c v
o
o
Se tiene que C
Ao
= M
o
; v
A
= -a;
a
M C
o
A
Ao
=
|
.
|
\
|
=
-
v
c
o
;
= 1.27;
o
= 2.79.
4
Entonces:
|
|
.
|
\
|
|
.
|
\
|
+ = |
.
|
\
|
= |
.
|
\
|
+ =
52 1
79 2
1
52 1
79 2
79 2 27 1
79 2
.
.
.
.
. .
.
) (
o o o
o
o A
M M M
a
M
a M C
De ello se llega a:
|
|
.
|
\
|
|
.
|
\
|
+ =
|
|
|
|
|
.
|
\
|
|
|
.
|
\
|
|
.
|
\
|
+
=
52 . 1
79 . 2
1 ln
52 . 1
79 . 2
1
ln
kt
M
M
kt
o
o
7. Prueba del modelo:
TABLA E.2.2.1
Tiempo, t (s) Rotacin ptica
()
|
|
.
|
\
|
|
.
|
\
|
+
52 1
79 2
1
.
.
ln
0 2.79 0
3.6 2.20 0.4913
7.2 1.84 0.9808
10.8 1.59 1.5581
14.4 1.45 2.1335
18.0 1.38 2.6260
1.27
FIGURA E.2.2.1
Prueba de primer orden f(Ca) = 0.1454t
R
2
= 0.9985
0
0.5
1
1.5
2
2.5
3
0 5 10 15 20
tiempo
f
u
n
c
i
n
d
e
C
a
Dado que el coeficiente de determinacin (R
2
) es 0.9990 y el valor del
intercepto es cero, puede concluirse que la correlacin lineal es buena y por
lo tanto el modelo de primer orden es til.
5
8. Y la ecuacin de velocidad para primer orden es:
A A
C r 1454 0. = (a T).
9. Sera bueno probar orden n, por el valor del coeficiente de correlacin en este
caso debe partirse de la expresin:
kt n
C C
A
n
Ao
n
A
) 1 (
1 1
1 1
=
|
|
.
|
\
|
v
que para el caso sera:
t k
kt
M
n
n n
o
' =
|
|
|
|
|
.
|
\
|
|
|
.
|
\
|
|
.
|
\
|
+
=
|
|
|
|
|
.
|
\
|
|
|
.
|
\
|
|
.
|
\
|
1
52 . 1
79 . 2
1
1
1
52 . 1
79 . 2
1
1 1
1
1 1
La determinacin del orden n debe hacerse asumiendo valores de n y analizando
el coeficiente de determinacin para cada caso.
EJEMPLO 2.3
En la figura E.2.3.1, se muestra un equipo experimental para efectuar la reaccin de
descomposicin siguiente: A R + S. El reactivo A se prepara bajo refrigeracin y se
introduce en un capilar delgado que acta como recipiente de reaccin. Este recipiente se
introduce rpidamente en un bao de agua hirviendo. Durante el manejo no hay reaccin.
Al realizar la experimentacin se tomaron lecturas de la longitud del capilar ocupada por la
mezcla reaccionante (L). Determinar el modelo cintico de reaccin de descomposicin de
A.
FIGURA E.2.3.1
SOLUCIN
Como puede observarse la reaccin en este caso es a volumen variable y la variable
indicadora de la conversin de A es L, lo que implica transformar la variable indicadora en
valores de conversin concentracin, antes de evaluar el modelo cintico de la reaccin.
Tiempo, t (min) Longitud (L, cm)
0.5 6.1
1.0 6.8
1.5 7.2
2.0 7.5
3.0 7.85
4.0 8.1
6.0 8.4
10.0 8.7
9.4
6
Para reacciones a volumen variable asumiendo comportamiento de mezcla de gases
ideales y una variacin lineal del volumen con la conversin, puede establecerse una
relacin entre el volumen y la conversin de la siguiente forma:
O
O
A A o
PT
T P
X V V ) ( e + = 1
Si P y T son constantes durante el proceso de reaccin se tiene:
) (
A A o
X V V e + = 1
Por lo tanto:
o A
o
A
V
V V
e
= _ (A)
Se sabe que: V = AL, as que sustituyendo en la ecuacin (A), se tiene:
o A
o
A
L
L L
e
= _ (B)
Desarrollar la ecuacin (B) para cada conversin implica contar con los valores de L
o
y e
A
.
Estos valores pueden determinarse como sigue:
e
A
: dado que no se introducen inertes y
Ao
= 1, por lo tanto:
A A
Ao A
n n
y
v v
= = e ; An = 1 +
1 1 = 1, y v
A
= -1, por tanto:
e
A
= 1
L
o
: Cuando la reaccin ha terminado (t = o ) con la completa conversin del reactante A
(_
A
= 1), la longitud ocupada por la sustancia en el capilar es 9.4 (L
f
), por tanto:
4.7
2
9.4
2
L
L 2L L
) X (1 L L
) X (1 V V
f
o o f
A A o
A A o
= = = =
e + =
e + =
y
7 4
7 4
.
.
=
L
A
_
En la tabla E.2.3.1 se presentan los datos de conversin correspondientes a cada
desplazamiento:
7
TABLA E.2.3.1
Tiempo,
t (min)
Longitud
(L, cm)
7 4
7 4
.
.
=
L
A
_
0.5 6.1
0.29787234
1 6.8
0.44680851
1.5 7.2
0.53191489
2 7.5
0.59574468
3 7.85
0.67021277
4 8.1
0.72340426
6 8.4
0.78723404
10 8.7
0.85106383
9.4
1
En la tabla E.2.3.2 se presentan las funciones de concentracin aplicadas para las
pruebas de orden 0, 1 y 2, as mismo se presentan los datos del coeficiente de
determinacin obtenido para cada prueba. En la figura E.2.3.2 se presenta el
comportamiento de la funcin de conversin con respecto al tiempo para las pruebas
de orden 0, 1 y 2. Como puede observarse a partir del valor del coeficiente de
determinacin y del comportamiento de la funcin de conversin, el modelo ms
adecuado es el de orden 2.
Las formas integradas de la funcin para los ordenes 0, 1 y 2 son:
n =0: t k kt
C
Ao
A
A A
' =
|
|
.
|
\
| e
= e + ) 1 ln( _ con k
C
k
Ao
A
|
|
.
|
\
| e
= '
n =1: ( ) kt
V
V
o A
A
=
|
|
.
|
\
|
|
|
.
|
\
|
e
A
= 1 ln 1 ln _
n =2:
( )
( ) t kC
Ao A A
A
A A
= e +
e +
_
_
_
1 ln
1
) 1 (
TABLA E.2.3.2
Tiempo,
t (min)
X
A
n = 0 n = 1 n = 2
0.5 0.29787234 0.260726262 0.35364004 0.494844808
1 0.446808511 0.369360103 0.592051064 1.023333552
1.5 0.531914894 0.426518517 0.759105148 1.513622124
2 0.595744681 0.467340512 0.905708623 2.041659799
3 0.670212766 0.512951023 1.109307578 2.955208551
4 0.723404255 0.544301553 1.285198244 3.945570987
6 0.787234043 0.580669197 1.547562509 5.852437491
10 0.85106383 0.615760517 1.904237453 9.524333976
R
2
0.716958432 0.920786786 0.999697607
8
FIGURA E.2.3.2
Prueba de modelos
n = 2: f(Xa) = 0.9652t
R
2
= 0.9992
0
2
4
6
8
10
12
0 2 4 6 8 10 12
tiempo(min)
f
(
X
a
)
n = 0
n = 1
n = 2
La velocidad especfica para el modelo de segundo orden vendr dada como:
Ao
Ao
C
k
kC
9652 . 0
9652 . 0
=
=
Lo que implica determinar el valor de C
Ao
, cuyo clculo se presenta a continuacin:
Durante la reaccin, la presin total (P) se mantiene constante, y es igual a la presin
atmosfrica ms la presin ejercida por el mercurio:
mmHg mmHg P P
atm
1760 1000 = + =
Como el recipiente de reaccin est sumergido en un bao de agua hirviendo la
temperatura es:
T = 100C+273.15 = 373 K
La concentracin inicial del reactivo es entonces:
l
gmol
x
K
K gmol
l mmHg
mmHg
RT
y P
RT
P
C
Ao o Ao
Ao
2
10 563 7
15 373 361 62
1 1760
=
|
|
.
|
\
|
= = = .
) . (
*
*
.
) )( (
De esta forma la velocidad especfica de reaccin es:
mol
l
x C
k
Ao
min*
.
.
. .
76 12
10 563 7
9652 0 9652 0
2
= = =
Y el modelo de velocidad:
2
76 12
A A
C mol l r min) . / . ( =
9
APLICACIN DEL METODO DIFERENCIAL AL ANALISIS DE DATOS CINTICOS
EJEMPLO 2.4
En la descomposicin del perxido de diterbutilo a acetona y etano se obtuvieron los
siguientes datos cinticos a 154.6C. Determinar el orden y la velocidad especfica de
reaccin:
6 2 2 3 3 3 3 3
2 H C CO CH CH COOC CH + ) ( ) ( ) (
Tiempo, t (min) Presin (mmHg)
0 173.5
3 193.4
6 211.3
9 228.6
12 244.4
15 259.2
18 273.9
21 286.8
SOLUCION
Para convertir los datos de presin total (P) a concentracin (C
A
) se emplear la ecuacin:
) (
o
i
io i
P P
n
P P
A
+ =
v
;
RT
P
C
i
i
=
Antes se requieren conocer los valores de An y C
Ao
:
2 1 2 1 = + + = = A
i
i
n v
l
gmol
x
K
K gmol
l mmHg
mmHg
RT
y P
RT
P
C
Ao o Ao
Ao
3
10 504 . 6
) 75 . 427 (
*
*
361 . 62
) 1 )( 5 . 173 (
=
|
|
.
|
\
|
= = =
En la tabla E.2.4.1 se presentan los valores de las presiones y concentraciones de A
correspondientes a cada valor de presin total.
TABLA E.2.4.1
Tiempo, t (min) Presin (mmHg) PA CA
0 173.5 173.5 0.00650424
3 193.4 163.55 0.00613123
6 211.3 154.6 0.00579571
9 228.6 145.95 0.00547143
12 244.4 138.05 0.00517527
15 259.2 130.65 0.00489786
18 273.9 123.3 0.00462232
21 286.8 116.85 0.00438052
10
Estos datos se analizarn con el mtodo diferencial, y el modelo de prueba ser el modelo
de orden n:
n
A A
kC r = (A)
Que para el anlisis diferencial puede expresarse como:
A A
C n k r ln ln ) ln( + = (B)
Para analizar los datos y probar el modelo, deben evaluarse los datos de velocidad
correspondientes en el seguimiento de la reaccin con el tiempo. Estos datos que en
sntesis son: -(dC
A
/dt), pueden evaluarse por mtodos numricos, grficos y de
aproximacin de polinomios (ver seccin 2.4.5(a)). En este ejemplo, por fines didcticos
se aplicarn los tres mtodos de evaluacin, ser decisin del evaluador elegir uno de
ellos para posteriores anlisis.
Mtodo de aproximacin de derivadas de -(dC
A
/dt) a (AC
A
/At)
Se calculan AC
A
y At:
l gmol C C C
A Ao A
/ 000373 . 0 006131 . 0 006504 . 0
1 1
= = = A
min 3 0 3
1 1
= = = A
o
t t t
Se evalan (AC
A
/At) y C
Ap
:
min
.
.
-
= =
= |
.
|
\
|
A
A
l
gmol
t t
C C
t
C
o
A Ao A
0001243 0
3
000373 0
1
1
1
l
gmol C C
C
A Ao
Ap
006318 . 0
2
006131 . 0 006504 . 0
2
1
=
+
=
+
=
Los resultados se resumen en el cuadro E.2.4.2. En la figura E.2.4.1 se muestra la
aplicacin de este mtodo usando la ecuacin lineal (B).
TABLA E.2.4.2
Tiempo,
t (min)
CA A CA At A CA/At CAp
0
0.00650424
3
0.00613123 0,00037301 3 0,00012434 0,00631774
6
0.00579571 0,00033552 3 0,00011184 0,00596347
9
0.00547143 0,00032428 3 0,00010809 0,00563357
12
0.00517527 0,00029616 3 9,872E-05 0,00532335
15
0.00489786 0,00027741 3 9,247E-05 0,00503657
18
0.00462232 0,00027554 3 9,1847E-05 0,00476009
21
0.00438052 0,0002418 3 8,06E-05 0,00450142
11
LN(A CA/At) LN(CAp)
-8,992518 -5,064394
-9,098441 -5,122103
-9,132516 -5,179012
-9,223223 -5,235652
-9,288626 -5,291031
-9,295390 -5,347489
-9,426012 -5,403362
FIGURA E.2.4.1
Prueba de orden n
mtodo de aproximacin de derivadas
ln (-r
A
) = 1,1716ln C
Ap
- 3,075
R
2
= 0,9707
-9.5
-9.4
-9.3
-9.2
-9.1
-9
-8.9
-5.5 -5.4 -5.3 -5.2 -5.1 -5
ln C
Ap
l
n
(
-
r
A
)
pendiente de la recta = n = 1.174
ordenada al origen = lnk = -3.075 k = 0.04619
coeficiente de correlacin = R = 0.9852
y la ecuacin de velocidad es:
17 . 1
04619 . 0
A A
C r =
Mtodo de las diferencias finitas
En la tabla E.2.4.3 y en la figura E.2.4.2 se presentan los datos obtenidos por este
mtodo, y a continuacin las ecuaciones de clculo respectivas.
TABLA E.2.4.3
Tiempo,
t (min)
CA
(dC
A
/dt) LN(dC
A
/dt)
LN(CA)
0
0.00650424 1.307x10
-4
-8,94260594 -5,03530101
3
0.00613123 1.180x10
-4
-9,04482593 -5,0943599
6
0.00579571 1.100x10
-4
-9,11503019 -5,15063729
9
0.00547143 1.035x10
-4
-9,17593895 -5,20821527
12
0.00517527 0.955x10
-4
-9,25638431 -5,26386377
15
0.00489786 0.917x10
-4
-9,29698818 -5,3189569
18
0.00462232 0.862x10
-4
-9,35884038 -5,37685854
21
0.00438052 0.745x10
-4
-9,50471143 -5,43058784
12
4
7 6 5
7
4
5 7
6
4
4 6
5
4
3 5
4
4
2 4
3
4
1 3
2
4
2
1
4
2 1
10 745 . 0 ) 3 4 (
2
1
10 862 . 0 ) (
2
1
10 917 . 0 ) (
2
1
10 955 . 0 ) (
2
1
10 035 . 1 ) (
2
1
10 10 . 1 ) (
2
1
10 18 . 1 ) (
2
1
10 307 . 1 ) 4 3 (
2
1
=
|
.
|
\
|
A
= |
.
|
\
|
= |
.
|
\
|
A
= |
.
|
\
|
= |
.
|
\
|
A
= |
.
|
\
|
=
|
.
|
\
|
A
= |
.
|
\
|
= |
.
|
\
|
A
= |
.
|
\
|
= |
.
|
\
|
A
= |
.
|
\
|
=
|
.
|
\
|
A
= |
.
|
\
|
= + |
.
|
\
|
A
= |
.
|
\
|
x C C C
t dt
dC
x C C
t dt
dC
x C C
t dt
dC
x C C
t dt
dC
x C C
t dt
dC
x C C
t dt
dC
x C C
t dt
dC
x C C C
t dt
dC
A A A
A
A A
A
A A
A
A A
A
A A
A
A A
A
Ao A
A
A A Ao
o
A
FIGURA E.2.4.2
Prueba de orden n
mtodo de diferencias finitas
ln (-r
A
) = 1,2931ln C
A
- 2,4429
R
2
= 0,9824
-9,6
-9,5
-9,4
-9,3
-9,2
-9,1
-9
-8,9
-5,5 -5,4 -5,3 -5,2 -5,1 -5
ln C
A
l
n
(
d
C
A
/
d
t
)
pendiente de la recta = n = 1.293
ordenada al origen = lnk = -2.4429 k = 0.08691
coeficiente de correlacin = R = 0.9912
y la ecuacin de velocidad es:
293 . 1
08691 . 0
A A
C r =
13
Mtodo de polinomios de orden n
Al realizar un anlisis de regresin polinomial a travs de excel empleando los datos de
concentracin (C
A
) contra tiempo (t) de la tabla E.2.4.1, se elige el polinomio grado 3, ya
que la grfica de residuos y coeficiente de regresin son los ms adecuados (ver figura
E.2.4.3)
FIGURA E.2.4.3
Polinomio grado 2 C
A
= 0,00000107980t
2
- 0,00012347067t+ 0,00649869583
R
2
= 0,99995
0
0,001
0,002
0,003
0,004
0,005
0,006
0,007
0 5 10 15 20 25
t
C
A
FIGURA E.2.4.4
Polinomio grado 3
C
A
= -0,000000013847737t
3
+ 0,000001516005291t
2
- 0,000126897989418t +
0,006502621666667
R
2
= 0,99997
0
0,001
0,002
0,003
0,004
0,005
0,006
0,007
0 5 10 15 20 25
t
C
A
C
A
= -1.385E-08t
3
+ 1.516E-06t
2
- 0,0001269t + 0,006503
) 0001269 . 0 ) 10 032 . 3 ( ) 10 155 . 4 ((
6 2 8
+ =
t x t x
dt
dC
A
De acuerdo a la ecuacin polinmica obtenida, se calculan los resultados que se
presentan en el cuadro E.2.4.4 y se representan en la figura E.2.4.5.
14
TABLA E.2.4.4
Tiempo,
t (min)
CA
(dC
A
/dt)
LN(-dC
A
/dt) LN(CA)
0 0.00650424 -0,0001 -8,97132347 -5,03530101
3 0.00613123 -0,00008827 -9,04247319 -5,0943599
6 0.00579571 -0,00007708 -9,11227218 -5,15063729
9 0.00547143 -0,00006643 -9,18002894 -5,20821527
12 0.00517527 -0,00005632 -9,2449401 -5,26386377
15 0.00489786 -0,00004675 -9,3060944 -5,3189569
18 0.00462232 -0,00003772 -9,36248739 -5,37685854
21 0.00438052 -0,00002923 -9,41304976 -5,43058784
FIGURA E.2.4.5
Prueba de orden n
mtodo de ajuste de polinomios
ln(-r
A
) = 1,1266 ln C
A
- 3,3065
R
2
= 0,9978
-9,5
-9,4
-9,3
-9,2
-9,1
-9
-8,9
-5,5 -5,4 -5,3 -5,2 -5,1 -5
ln C
A
l
n
(
-
r
A
)
pendiente de la recta = n = 1.1266
ordenada al origen = lnk = -3.3065 k = 0.03664
coeficiente de correlacin = R = 0.9989
y la ecuacin de velocidad es:
13 . 1
03664 . 0
A A
C r =
En la tabla E.2.4.5 se presenta u resumen de los resultados.
Mtodo Orden k R
Aproximacin de
derivadas
1.17 0.04619 0.9852
Diferencias finitas 1.293 0.08691 0.9912
Ajuste de polinomios 1.127 0.03664 0.9989
APLICACIONES GENERALES
EJEMPLO 2.5
Biordi ha estudiado la metanolisis del cloruro de benzilo a 25C:
15
Para la prueba se ha utilizado un exceso de metanol, rastreando el progreso de la misma
mediante lecturas de conductividad. Bajo las condiciones del experimento, la reaccin
puede considerarse irreversible. A partir de la siguiente informacin determine el orden de
la reaccin con respecto al cloruro de benzilo y la pseudo velocidad especfica de
reaccin.
Tiempo, t (s) Conductividad x10
-2
(O
-1
cm
-1
)
0 despreciable
27 0.352
48 0.646
55 0.732
62 0.813
70 0.900
79 0.969
86 1.07
93 1.12
100 1.21
105 1.26
114 1.33
120 1.40
10800 3.50
SOLUCION
Dado que se usa un vasto exceso de metanol, la concentracin de metanol permanece
esencialmente invariable, por tanto es apropiado asumir que la expresin de velocidad es
de la forma:
n
A A
kC r = .
1. Hiptesis inicial: primer orden, sistema a volumen constante:
A A
kC r = .
2. Forma integrada de primer orden:
|
|
.
|
\
|
=
Ao
A
C
C
kt ln
3. Datos cinticos: conductividad (O), tiempo t (s).
Dado que la conductividad es una funcin aditiva de las contribuciones de las especies
presentes, puede usarse la siguiente aproximacin para cuantificar las concentraciones:
|
|
.
|
\
|
+ =
-
o
o
i io i
C C
o o
o o
c v
o
o
que para el caso puede escribirse como:
C Cl + CH
3
OH C OCH
3
+ H
+
+ Cl
-
O O
16
|
|
.
|
\
|
O O
O O
+ =
-
o
o
A Ao A
C C
o
o
c v
El clculo de las variables en la ecuacin es el siguiente:
C
Ao
= C
Ao
Ao
A
Ao
A
C
C
=
=
=
v
c
v
o
*
1
O
= 3.50; O
o
= 0
Por tanto:
|
|
.
|
\
|
|
.
|
\
| O
= |
.
|
\
|
O
+ =
50 . 3
1
0 50 . 3
0
) 1 (
Ao Ao Ao A
C C C C
4. Prueba del modelo:
TABLA E.2.5.1
Tiempo,
t (s)
Conductividad
x10
-2
(O
-1
cm
-1
) |
|
.
|
\
|
|
.
|
\
| O
=
|
|
.
|
\
|
50 . 3
1 ln ln
Ao
A
C
C
0 despreciable
27 0.352 0.10599564
48 0.646 0.20404145
55 0.732 0.23463793
62 0.813 0.26433764
70 0.900 0.29725152
79 0.969 0.32414849
86 1.07 0.36487171
93 1.12 0.38566248
100 1.21 0.42421115
105 1.26 0.4462871
114 1.33 0.4780358
120 1.40 0.51082562
10800 3.50
17
GRAFICO E.2.5.1
Prueba de orden 1
f(C
A
) = 0.0043t - 0.0039
R
2
= 0.9985
0
0.1
0.2
0.3
0.4
0.5
0.6
0 20 40 60 80 100 120 140
t
f
(
C
A
)
En este caso el coeficiente de determinacin es R = 0.9992, sera recomendable probar
orden 2 para evaluar el comportamiento.
Tiempo, t (s) Conductividad
x10
-2
(O
-1
cm
-1
)
kt C
Ao
=
|
|
|
|
|
.
|
\
|
|
|
.
|
\
|
|
.
|
\
| O
1
50 . 3
1
1
0 despreciable
27 0.352 0.11181703
48 0.646 0.22634898
55 0.732 0.26445087
62 0.813 0.30256792
70 0.900 0.34615385
79 0.969 0.38285263
86 1.07 0.44032922
93 1.12 0.47058824
100 1.21 0.52838428
105 1.26 0.56250000
114 1.33 0.61290323
120 1.40 0.66666667
10800 3.50
18
GRAFICO E.2.5.2
Prueba de orden 2
f(C
A
) = 0.0059t - 0.061
R
2
= 0.9953
0
0.1
0.2
0.3
0.4
0.5
0.6
0.7
0 20 40 60 80 100 120 140
t
f
(
C
A
)
En este caso el coeficiente de determinacin es R = 0.9976, como puede observarse la
correlacin ha disminuido y el comportamiento de la serie de datos indica que el orden es
menor. La observacin anterior permite considerar que el modelo de orden 1 es
adecuado, por lo tanto:
A A
C s r ) 0043 . 0 (
1
= (T = 25C)
EJEMPLO 2.6
Helling y Hungers han reportado los siguientes datos para la reaccin entre el cido
sulfrico y el sulfato dietlico:
H SO H C SO H C SO H
4 5 2 4 2 5 2 4 2
2 = + ) (
Temperatura: 22.9C
Concentracin inicial de
4 2
SO H : 5.5 kmol/m
3
Concentracin inicial de
4 2 5 2
SO H C ) (
: 5.5kmol/m
3
Despus de 11 das la concentracin es
aproximadamente de 5.8 kmol/m
3
Tiempo, t (s) Concentracin de
H SO H C
4 5 2
(C
R
)
0 0
1680 0.69
2880 1.38
4500 2.24
5760 2.75
7620 3.31
9720 3.81
10800 4.11
12720 4.45
16020 4.86
19080 5.15
22740 5.35
24600 5.42
19
A partir de la informacin anterior evaluar la velocidades especficas para la reaccin a
22.9C, a) utilizando el anlisis integral; b) utilizando el anlisis diferencial.
SOLUCIN
Esquema de la reaccin: A + B = 2R; C
Ao
= C
Bo
= 5.5 kmol/m
3
.
a) Mtodo Integral
1. Hiptesis del comportamiento cintico: reaccin elemental reversible de segundo
orden:
2
2 1 R B A
C k C C k r = (densidad constante).
2. Acondicionamiento de los datos cinticos: Dado que se ha dado seguimiento a la
concentracin del producto, se considera conveniente expresar el balance de masa en
funcin de la fraccin de conversin de uno de los reactivos, que para el caso estn
alimentados equimolarmente. Si se expresan C
A
, C
B
y C
R
en funcin de _
A
se tiene:
( ) ( )
( )
A Ao A Ao Ro R
A Ao B
Bo A Ao Bo A Ao Bo B
A Ao A
C C C C
C C
C C C C C C
C C
_ _
_
_ _
_
2
1
2
1
1
1
1
= |
.
|
\
|
+ =
=
= = |
.
|
\
|
+ =
=
) (
C caso este en
) (
Ao
3. Sustitucin en ecuacin de la hiptesis:
2
2
2
1
2 2
2
2 2
1
4 1
4 1
A Ao A Ao
A
A Ao A Ao
A
Ao
C k C k
dt
d
C k C k
dt
d
C
_ _
_
_ _
_
=
=
) (
) (
Dividiendo entre k
1
y considerando que en este modelo K = k
1
/k
2
2 1 2
1
4 1
1
A Ao A Ao
A
K C C
dt
d
k
_ _
_
= ) ((
La constante de equilibrio en este caso vendr dada a partir de las ecuaciones de
balance de masa, con _
Ae
como la fraccin de conversin en el equilibrio a 22.9C
2
2
2
2 2
) 1 (
4
) 1 )( 1 (
) )( 4 (
Ae
Ae
Ao Ae Ae
Ao Ae
C
C
K
_
_
_ _
_
=
=
4. Obtencin de la forma integrada:
Despejando y arreglando variables:
20
t C k
do Sustituyen
t C k
K
d
dt C k
K
d
egrando
dt C k
K
d
Ao
Ae A Ae
A Ae Ae
Ao
A A
A
t
Ao
A A
A
Ao
A A
A
A
A
|
|
.
|
\
|
=
|
|
.
|
\
|
=
+
=
=
}
} }
1
1
2
) 1 2 (
ln
1 2 ) 4 1 ((
4 ) 1 ((
: int
4 ) 1 ((
1
1
0
2
0
1
0
2 2
1
2 2
_ _ _
_ _ _
_ _
_
_ _
_
_ _
_
_
_
: K
5. Prueba de Hiptesis:
TABLA E.2.6.1
Tiempo,
t (s)
Concentracin
de
H SO H C
4 5 2
(C
R
)
Ao R A
C C 2 / = _
|
|
.
|
\
|
A Ae
A Ae Ae
_ _
_ _ _ ) 1 2 (
ln
0 0 0.0000 0.0000
1680 0.69 0.0627 0.1201
2880 1.38 0.1255 0.2586
4500 2.24 0.2036 0.4668
5760 2.75 0.2500 0.6164
7620 3.31 0.3009 0.8139
9720 3.81 0.3464 1.0331
10800 4.11 0.3736 1.1935
12720 4.45 0.4045 1.4148
16020 4.86 0.4418 1.7726
19080 5.15 0.4682 2.1385
22740 5.35 0.4864 2.5041
24600 5.42 0.4927 2.6723
_
Ae
= 5.8/(2*5.5) = 0.5273
21
FIGURA E.2.6.1
Prueba reaccin reversible orden 2 elemental
mtodo Integral
f(X
A
) = 1.0972E-04t
R
2
= 9.9860E-01
0
0.5
1
1.5
2
2.5
3
0 5000 10000 15000 20000 25000 30000
t
f
(
X
A
)
Pendiente de la recta =
Ao
Ae
C k
|
|
.
|
\
|
1
1
2
1
_
= 1.0972x10
-04
Coeficiente de determinacin = 0.9993
De acuerdo a los datos la correlacin lineal es aceptable, por tanto el modelo planteado
(reaccin reversible segundo orden elemental) explica significativamente el
comportamiento de la velocidad de reaccin con la composicin. A continuacin se
presenta el clculo de los parmetros del modelo:
s kmol
m
x
C
x
k
Ao
Ae
*
.
*
.
3
5
4
1
10 1127 1
1
1
2
10 0972 1
=
|
|
.
|
\
|
=
_
dado que:
s kmol
m
x
x x
K
k
k
k
k
K
Ae
Ae
*
.
) . (
) . (
.
) (
.
3
6
2
2
5
2
2
5
1
2
2
1
10 236 2
5273 0 1
5273 0 4
10 1127 1
1
4
10 1127 1
=
|
|
.
|
\
|
=
|
|
.
|
\
|
= = =
_
_
De esta forma el modelo cintico de la reaccin a 22.9C es:
2
3
6
3
5
10 236 2 10 1127 1
R B A
C
s kmol
m
x C C
s kmol
m
x r
|
|
.
|
\
|
|
|
.
|
\
|
=
*
.
*
.
b) Mtodo diferencial
22
1. Hiptesis del comportamiento cintico: reaccin elemental reversible de segundo
orden:
2
2 1 R B A
C k C C k r = (densidad constante).
2. Acondicionamiento de los datos cinticos: El balance de masa en funcin de la
fraccin de conversin de uno de los reactivos (_
A
) contina siendo el mismo, es decir:
( ) ( )
( )
A Ao A Ao Ro R
A Ao B
Bo A Ao Bo A Ao Bo B
A Ao A
C C C C
C C
C C C C C C
C C
_ _
_
_ _
_
2
1
2
1
1
1
1
= |
.
|
\
|
+ =
=
= = |
.
|
\
|
+ =
=
) (
C caso este en
) (
Ao
Para aplicar el mtodo diferencial, se simplificar la ecuacin de velocidad
multiplicando y dividiendo entre k
1
: |
.
|
\
|
=
|
|
.
|
\
|
=
2
1
2
1
2
1
1
R B A R B A
C
K
C C k C
k
k
C C k r (A)
Al sustituir en la ecuacin (A) las concentraciones en funcin de la fraccin de
conversin de A se obtiene:
) ) ((
2 2 2
1
1
4 1
A A Ao A
K
C k r _ _
'
=
ahora, si:
dt
d
C r
A
Ao A
_
=
entonces:
(B) ) ) ((
) ) ((
2 2
1
2 2 2
1
1
4 1
1
4 1
A A Ao
A
A A Ao
A
Ao
K
C k
dt
d
K
C k
dt
d
C
_ _
_
_ _
_
'
=
'
=
3. Prueba del modelo:
En la ecuacin (B): y =
dt
d
A
_
y x = f(_
A
) = ) ) ((
2 2
1
4 1
A A
K
_ _ , aplicando el mtodo de
aproximacin de las derivadas se obtienen los datos de la tabla E.2.6.2, que se presentan
a continuacin:
23
TABLA E.2.6.2
Tiempo,
t (s)
Concentracin
de
H SO H C
4 5 2
(CR)
Ao R A
C C 2 / = _
A_A/At _Apromedio Ln (A_A/At) Ln (f(_A))
0 0 0.0000
1680 0.69 0.0627 3.73214E-05 0.03135 -10.1959429 -0.06454596
2880 1.38 0.1255 5.23333E-05 0.0941 -9.85787704 -0.20636131
4500 2.24 0.2036 4.82099E-05 0.16455 -9.93994665 -0.39123997
5760 2.75 0.2500 3.68254E-05 0.2268 -10.2093228 -0.58608367
7620 3.31 0.3009 2.73656E-05 0.27545 -10.5062241 -0.76786771
9720 3.81 0.3464 2.16667E-05 0.32365 -10.7397356 -0.98544585
10800 4.11 0.3736 2.51852E-05 0.36 -10.5892546 -1.18595792
12720 4.45 0.4045 1.60938E-05 0.38905 -11.0370796 -1.37980711
16020 4.86 0.4418 1.1303E-05 0.42315 -11.3904397 -1.66671442
19080 5.15 0.4682 8.62745E-06 0.455 -11.6605615 -2.03515897
22740 5.35 0.4864 4.97268E-06 0.4773 -12.2115521 -2.40635884
24600 5.42 0.4927 3.3871E-06 0.48955 -12.5955374 -2.68870257
FIGURA E.2.6.2
Prueba reaccin reversible orden 2 elemental
mtodo Diferencial ln(-r
A
) = 1.0098ln(f(X
A
) - 9.7023
R
2
= 0.9576
-14
-12
-10
-8
-6
-4
-2
0
-3 -2.5 -2 -1.5 -1 -0.5 0
f(X
A
)
-
r
A
Pendiente de la recta = 1.0098
Ordenada en el orgen = -9.7023
Coeficiente de determinacin = 0.9786
4. Modelo: puede considerarse que el modelo explica significativamente el
comportamiento de reaccin reversible elemental de segundo orden, y los parmetros
son los siguientes:
s kmol
m
x
x
C
x
k
x e k C
k
Ao
Ao
*
10 1117 . 1
5 . 5
10 1143 . 6 10 1143 . 6
10 1143 . 6 ) 7023 . 9 (
7023 . 9 ) ln(C intercepto
3
5
5 5
1
5
1
1 Ao
= = =
= =
= =
y
24
s kmol
m
x
x x
K
k
k
k
k
K
Ae
Ae
*
10 233 . 2
) 5273 . 0 1 (
) 5273 . 0 ( 4
10 1117 . 1
) 1 (
4
10 1127 . 1
3
6
2
2
5
2
2
5
1
2
2
1
=
|
|
.
|
\
|
=
|
|
.
|
\
|
= = =
_
_
De esta forma el modelo cintico de la reaccin a 22.9C, por el mtodo diferencial es:
2
3
6
3
5
*
10 233 . 2
*
10 1117 . 1
R B A
C
s kmol
m
x C C
s kmol
m
x r
|
|
.
|
\
|
|
|
.
|
\
|
=
APLICACIN DEL METODO DEL TIEMPO DE VIDA FRACCIONAL
EJEMPLO 2.7
En la descomposicin trmica del N
2
O a 1030 K, se obtuvieron los siguientes datos.
Presin inicial
(mmHg)
t
1/2
82.5 860
139 470
296 255
360 212
Evaluar el orden aproximado para esta descomposicin.
SOLUCION
Por tratarse de un estudio de tiempo de vida media el anlisis de datos debe partir del
planteamiento de las siguientes expresiones:
n
Ao
A
n
C
n k
t
=
1
1
2 1
1
1 2
) (
/
v
Que forma lineal se expresa como:
Ao
A
n
C n
n k
t ln ) 1 (
) 1 (
1 2
ln ln
1
2 / 1
+
|
|
.
|
\
|
=
v
Dado que se tienen lecturas de presin inicial de N
2
O, ser necesario transformarlas a
datos de concentracin inicial de A, a partir de:
25
l
gmol
x
K
K gmol
l mmHg
mmHg
C
RT
y P
RT
P
C
Ao
Ao o Ao
Ao
3
10 285 . 1
) 75 . 427 (
*
*
361 . 62
) 1 )( 5 . 82 (
: obtener permite punto primer el para que
=
|
|
.
|
\
|
=
= =
Aplicando la transformacin al resto de datos y calculando los logaritmos de C
Ao
y t
1/2
, se
obtienen la tabla E.2.7.1 y la figura E.2.7.1, que se presentan a continuacin:
TABLA E.2.7.1
Presin
inicial
(mmHg)
t
1/2
C
Ao
x10
-3
Ln t
1/2
Ln C
Ao
82.5 860 1.285 6.7569 -6.6570
139 470 2.165 6.1527 -6.1353
296 255 4.611 5.5413 -5.3793
360 212 5.608 5.3566 -5.1836
FIGURA E.2.7.1
Descomposicin del N
2
O
ln(t
1/2
) = -0.9278 ln(C
Ao
) + 0.5344
R
2
= 0.9934
0.0000
2.0000
4.0000
6.0000
8.0000
-7.0000 -6.0000 -5.0000 -4.0000 -3.0000 -2.0000 -1.0000 0.0000
ln C
Ao
l
n
t
1
/
2
De acuerdo a los datos el coeficiente de determinacin de 0.9967 representa una
correlacin lineal adecuada y por lo tanto se proceder a calcular el orden de la reaccin
como sigue:
93 1 9278 0 1 . . = = n n
EJEMPLO 2.8
La reaccin de descomposicin del N
2
O
5
se efectu a varias temperaturas en un reactor
isotrmico operado a densidad constante. La concentracin inicial de N
2
O
5
fue la misma
26
para todos los experimentos. A partir de la siguiente informacin experimental determinar
el valor de la energa de activacin.
Temperatura
(C)
t
1/2
(s)
50 780
100 4.6
150 8.8E-02
200 3.9E-03
300 3.9E-05
SOLUCION
Empleando datos de tiempo de vida media (t
1/2
) cualquier otro tiempo de vida fraccional
(t
f
), es posible determinar la energa de activacin de una reaccin si se dispone de datos
a diferentes temperaturas, en donde la ecuacin para el tiempo de vida media quedara
expresada como:
n
Ao
RT E
o A
n
C
n e k
t
=
1
1
2 1
1
1 2
) )( (
/
/
v
Que de forma lineal se expresa como:
RT
E
C n
n k
t
RT
E
C n
k
n
t
RT
E
k C n
n
t
e k C n
n
t
Ao
o A
n
Ao
o
A
n
o Ao
A
n
RT E
o Ao
A
n
+ +
|
|
.
|
\
|
|
|
.
|
\
|
=
+ +
|
|
|
|
|
.
|
\
|
|
|
.
|
\
|
=
+ +
|
|
.
|
\
|
=
+
|
|
.
|
\
|
ln ) (
) (
ln ) ln(
ln ) (
) (
) (
ln ) ln(
) ln( ln ) (
) (
ln ) ln(
) ln( ln ) (
) (
ln ) ln(
/
/
/
/
/
1
1
1 2
1
1
1 2
1
1
1 2
1
1
1 2
1
2 1
1
2 1
1
2 1
1
2 1
v
v
v
v
(A)
Para evaluar los valores de n y E es necesario contar con datos de C
Ao
, t
1/2
y T, y analizar
un modelo de regresin lineal mltiple en el que la variable a explicar sera el tiempo de
vida media y las variables explicativas seran las concentraciones iniciales del
componente A y la temperatura a la que se ha realizado cada prueba.
En este problema se explica que todos los experimentos se han efectuado usando la
misma concentracin inicial de A, de esta forma el trmino de
n
Ao
C
1
es constante y la
expresin anterior puede simplificarse como:
27
RT
E
C
n k
t
n
Ao
o A
n
+
|
|
.
|
\
|
|
|
.
|
\
|
1
1
2 1
1
1 2
) (
ln ) ln(
/
v
(B)
Empleando la ecuacin (B) con x = 1/T (en grados absolutos) y y = ln(t
1/2
), se obtienen los
datos de la tabla E.2.8.1 y de la figura E.2.8.1, donde se observa que los datos
experimentalmente se ajustan a una lnea recta.
TABLA E.2.8.1
Temperatura
(K)
t
1/2
(s)
1/T Ln(t
1/2
)
323.15 780 0.003095 6.6593
373.15 4.6 0.002680 1.5261
423.15 8.8E-02 0.002363 -2.4304
473.15 3.9E-03 0.002113 -5.5468
573.15 3.9E-05 0.001745 -10.1519
FIGURA E.2.8.1
Calculo de la Energa de Activacin (E)
ln(t
1/2
) = 12459(1/T) - 31.88
R
2
= 1
-15
-10
-5
0
5
10
0.E+00 5.E-04 1.E-03 2.E-03 2.E-03 3.E-03 3.E-03 4.E-03
1/T
l
n
(
t
1
/
2
)
Los parmetros de la lnea recta son los siguientes:
Pendiente de la recta = E/R = 12459
Ordenada en el orgen = -31.88
Coeficiente de determinacin = 1
Por lo que la energa de activacin es:
gmol cal R E / . ) . ( ) ( 8 24755 987 1 12459 12459 = = =
28
APLICACIN DEL METODO DE LAS VELOCIDADES INICIALES
EJEMPLO 2.9
Se han obtenido los siguientes datos para una reaccin homognea en fase gas: 2A + 2B
C + 2D, en un tanque rgido de 2 litros a 800C.
P
o
(kPa) y
Ao
( )
o
dt dP/
kPa/min
46 0.261 -0.8
70 0.514 -7.2
80 0150 -1.6
Asumiendo que a tiempo cero no hay C ni D presentes, obtener la ley de velocidad de
reaccin.
SOLUCION
1. Hiptesis: sistema a volumen constante:
B A
B A
C kC r
| |
= .
2. Datos cinticos: Dado que se trata de un experimento de velocidades iniciales y que
los datos obtenidos son presin total y velocidad inicial de A expresada como
variacin de la presin parcial de A con el tiempo, la ecuacin de velocidad puede
rescribirse como:
B A
B A
Ao
C kC r
| |
=
B A
Bo Ao
Ap
o
A
P P k
dt
dP
| |
=
|
|
.
|
\
|
Los valores de ( )
o
A
dt dP / , sern calculados a partir de los valores de ( )
o
dt dP/ , de
acuerdo a:
- Asumiendo conducta de gas ideal (T, V constante) entonces,
RT n V RT n PV
A t
= =
A
P y
- En cualquier instante:
D C B A t
n n n n n + + + = y
D C B A t
dn dn dn dn dn + + + =
- Por balance de moles en cualquier instante:
A A A B A t
dn dn dn dn dn dn ) 2 / 1 ( ) 2 / 1 ( = + = y a t = 0:
Ao to
dn dn ) 2 / 1 ( =
- De esta forma a partir de la ecuacin de estado y la estequiometra:
|
.
|
\
|
= |
.
|
\
|
|
.
|
\
|
= |
.
|
\
|
= |
.
|
\
|
= |
.
|
\
|
dt
dP
2
dt
dP
y
dt
dP
2
1
dt
dn
2V
RT
dt
dn
V
RT
dt
dP
A
A A t
- Estos resultados para los tres experimentos son:
29
P
Ao
(kPa) P
Bo
(kPa)
( )
o
A
dt dP /
kPa/min
12 34 -1.6
36 34 -14.4
12 68 -3.2
3. Determinacin de los parmetros del modelo:
Bo
B
Ao
A Ap
o
A
P P k
dt
dP
ln ln ln ln | | + + =
|
|
.
|
\
|
Dado que P
Bo
es constante para los dos primeros experimentos y P
Ao
para el primero y el
tercero, no ser necesario hacer una regresin mltiple, y los valores de los ordenes de
reaccin y de k
Ap
pueden determinarse a partir de:
A partir de las pruebas 1 y 2:
( )
2
3333 . 0 ln
) 1111 . 0 ln(
3
1
ln ) 1111 . 0 ln(
3
1
36
12
1111 . 0
) 34 ( ) 36 (
) 34 ( ) 12 (
4 . 14
6 . 1
= =
|
.
|
\
|
=
|
.
|
\
|
= |
.
|
\
|
=
=
A
A
Ap
Ap
A A
B A
B A
k
k
|
|
| |
| |
| |
A partir de las pruebas 1 y 3:
( )
1
5 . 0 ln
) 5 . 0 ln(
2
1
ln ) 5 . 0 ln(
2
1
68
34
5 . 0
) 68 ( ) 12 (
) 34 ( ) 12 (
2 . 3
6 . 1
= =
|
.
|
\
|
=
|
.
|
\
|
= |
.
|
\
|
=
=
B
B
Ap
Ap
B B
B A
B A
k
k
|
|
| |
| |
| |
El orden global es entonces: n = 3. Sustituyendo estos resultados en la ecuacin para
cualquiera de los experimentos se obtiene:
min / 0003268 . 0
) 34 ( ) 12 (
6 . 1
) 34 ( ) 12 ( 6 . 1
2
2
kPa k
k
Ap
Ap
= =
=
30
En unidades de concentracin se tiene:
min) * /( 68 . 26007 ) 0003268 . 0 ( ) 1073 ( ) 314 . 8 ( ) (
2 2 2 2 2
mol l k RT k
Ap
= = =
Ecuacin de velocidad:
B A A
C C
mol
l
r
2
2
2
min *
26008
|
|
.
|
\
|
= (a T = 800C)
APLICACIN DEL METODO ESTADISTICO
EJEMPLO 2.10
La hidrogenacin (H) de etileno para formar etano (EA),
6 2 4 2 2
H C H C H + , se efecta
sobre un catalizador de cobalto y molibdeno |Collect. Czech. Chem. Comn., 51,2760
(1988)|. Realice un anlisis de mnimos cuadrados no lineal con los datos que se dan en la
tabla a continuacin:
Nmero
de
prueba
Veloc. de
reaccin
(mol/kg cat. s)
PE
(atm)
PEA
(atm)
PH
(atm)
1 1.04 1 1 1
2 3.13 1 1 3
3 5.21 1 1 5
4 3.82 3 1 3
5 4.19 5 1 3
6 2.391 0.5 1 3
7 3.867 0.5 0.5 5
8 2.199 0.5 3 3
9 0.75 0.5 5 1
Determine cul de las siguientes leyes de velocidad es la que mejor describe los datos:
(a)
E E
H E
A
P k
P kP
r
+
=
1
; (b)
b
H
a
E A
P kP r =
SOLUCION
(a) MODELO:
E E
H E
A
P k
P kP
r
+
=
1
;
El modelo es un modelo no lineal, sin embargo, puede ser linealizable al
trabajar con el inverso de -r
A
, de la siguiente forma:
|
|
.
|
\
|
+
|
|
.
|
\
|
= + =
H
E
H E H E
E E
H E A
P k
k
P P k P kP
P k
P kP r
1 1 1 1 1
Los parmetros del modelo son k y k
E
. Para el anlisis de mnimos cuadrados
31
se podr trabajar con una regresin lineal mltiple sobre las variables
transformadas, en la tabla E.2.10.1 se presenta esta trasformacin de variables:
TABLA E.2.10.1
1/-r
A
1/(P
E
*P
H
) 1/P
H
0.96153846 1 1
0.31948882 0.33333333 0.33333333
0.19193858 0.2 0.2
0.2617801 0.11111111 0.33333333
0.23866348 0.06666667 0.33333333
0.41823505 0.66666667 0.33333333
0.2585984 0.4 0.2
0.45475216 0.66666667 0.33333333
1.33333333 2 1
El anlisis del modelo de regresin lineal mltiple puede realizarse tal como se
presenta en el ejercicio 2, para las variables transformadas:
(
(
(
(
(
(
(
(
(
(
(
(
+
(
(
(
(
(
(
(
(
(
(
(
(
(
=
(
(
(
(
(
(
(
(
(
(
(
(
98
8
7
6
5
4
3
2
1
/
/ 1
1 2 0
3333 . 0 6667 . 0 0
2 . 0 4 . 0 0
3333 . 0 6667 . 0 0
3333 . 0 0667 . 0 0
3333 . 0 1111 . 0 0
2 . 0 2 . 0 0
3333 . 0 3333 . 0 0
1 1 0
3333 . 1
4548 . 0
2586 . 0
4182 . 0
2387 . 0
2618 . 0
1919 . 0
3195 . 0
9615 . 0
c
c
c
c
c
c
c
c
c
k k
k
E
La estimacin de los coeficientes viene dada por
(
= ' ' =
6221 . 0
3507 . 0
) (
1
y x x x b
El coeficiente de determinacin es dado a partir de:
( )
( )
99894 . 0
1
2
1
2
1
2
2
=
= =
=
=
=
=
=
n j
j
j j
n
j
j
n j
j
j j
TOTAL
EXPLICADA
y y
y y
SC
SC
R
c
Las varianzas asociadas a cada uno de los estimadores de los parmetros
32
que son dadas a partir de
ii bi
c S S = donde c
ii
es el elemento i, i de la
diagonal principal de ( )
1
'x x , se presentan en la tabla E.2.10.2:
TABLA E.2.10.2
Parmetro estimacin S
bi
1/k
0.35069 0.01419
k
E
/k 0.62207 0.02175
La significacin global del ajuste se presenta en la E.2.10.3:
TABLA E.2.10.3
fuente SC g.l. MC F
o
explicada 1.2253 2 0.61264 3293.38
residuos 0.00130 7 0.0001857
F
o, I, (n-1-I)
=F
0.05, 2, 7
=4.74
Al comparar F
o
con el F
0.05, 2,7
puede concluirse que el modelo es
significativo, siendo la suma de cuadrados mnima de 0.0013.
En la tabla E.2.10.4 se presentan los residuos calculados y en el grafico E.2.10.1
se presenta el comportamiento de los residuos contra los valores predichos
por el modelo.
TABLA E.2.10.4 GRAFICO E.2.10.1
-0.03
-0.02
-0.01
0
0.01
0.02
0 0.5 1 1.5
VALORES PREDICHOS
R
E
S
I
D
U
O
S
Los valores de k y k
E
para el modelo son por tanto:
774 . 1 ) 852 . 2 ( * ) 6221 . 0 ( 6221 . 0
852 . 2 35069 . 0 / 1
= = =
= =
k k
k
E
Y por tanto, el modelo queda escrito como:
E
H E
A
P
P P
r
774 . 1 1
852 . 2
+
=
Este ejercicio tambin puede desarrollarse usando la funcin regresin de la opcin
anlisis de datos del men Herramientas en la hoja de clculo de Excel. En el archivo
regresin no lineal m1. xls, se presentan las salidas para dicha aplicacin:
Observacin
Pronstico
para Y
Residuos
0.961546 0.972768 -0.011221
0.319489 0.324260 -0.004767
0.191938 0.194554 -0.002615
0.261780 0.246324 0.015456
0.238663 0.230738 0.007925
0.418235 0.441153 -0.022918
0.258510 0.264692 -0.006094
0.454752 0.441153 0.013599
1.333333 1.323460 0.009873
33
(b) MODELO:
b
H
a
E A
P kP r =
Al igual que en el caso anterior el modelo no es un modelo lineal, sin
embargo, es linealizable al aplicar una transformacin logartmica, como se
presenta a continuacin:
H E A
b
H
a
E A
P b P a k r P kP r ln ln ln ) ln( + + = =
Los parmetros del modelo en este caso son lnk, a y b. Para el anlisis de
mnimos cuadrados se podr trabajar con una regresin lineal mltiple sobre
las variables transformadas. En la tabla E.2.10.5 se presenta esta
trasformacin de variables:
TABLA E.2.10.5
Ln(-r
A
) ln(P
E
) Ln(P
H
)
0.0392 0.0000 0.0000
1.1410 0.0000 1.0986
1.6506 0.0000 1.6094
1.3403 1.0986 1.0986
1.4327 1.6094 1.0986
0.8717 -0.6931 1.0986
1.3525 -0.6931 1.6094
0.7880 -0.6931 1.0986
-0.2877 -0.6931 0.0000
El anlisis del modelo de regresin lineal mltiple puede realizarse tal como se
presenta en el ejercicio 2, para las variables transformadas:
(
(
(
(
(
(
(
(
(
(
(
(
+
(
(
(
(
(
(
(
(
(
(
(
(
(
(
(
=
(
(
(
(
(
(
(
(
(
(
(
(
98
8
7
6
5
4
3
2
1
ln
0000 . 0 6931 . 0 1
0986 . 1 6931 . 0 1
6094 . 1 6931 . 0 1
0986 . 1 6931 . 0 1
0986 . 1 6094 . 1 1
0986 . 1 0986 . 1 1
6094 . 1 0000 . 0 1
0986 . 1 0000 . 0 1
0000 . 0 0000 . 0 1
2877 . 0
7880 . 0
3525 . 1
8717 . 0
4327 . 1
3403 . 1
6506 . 1
1410 . 1
0392 . 0
c
c
c
c
c
c
c
c
c
b
a
k
La estimacin de los coeficientes viene dada por
(
(
(
= ' ' =
05384 . 1
26719 . 0
10934 . 0
) (
1
y x x x b
34
El coeficiente de determinacin es dado a partir de:
( )
( )
9898 . 0
1
2
1
2
1
2
2
=
= =
=
=
=
=
=
n j
j
j j
n
j
j
n j
j
j j
TOTAL
EXPLICADA
y y
y y
SC
SC
R
c
Las varianzas asociadas a cada uno de los estimadores de los parmetros que son dadas a
partir de
ii bi
c S S = donde c
ii
es el elemento i, i de la diagonal principal de ( )
1
'x x , se
presentan en la tabla E.2.10.6:
TABLA E.2.10.6
Parmetro estimacin S
bi
ln k
-0.042239026 0.061462455
a 0.271021234 0.028559749
b 1.001607145 0.051953273
La significacin global del ajuste se presenta en la E.2.10.7:
TABLA E.2.10.7
fuente SC g.l. MC F
o
explicada 3.427844373 2 1.713922186 293.540846
residuos 0.035032716 6 0.005838786
F
o, I, (n-1-I)
=F
0.05, 2, 6
= 5.14
Al comparar F
o
con el F
0.05, 2, 6
puede concluirse que el modelo es significativo, siendo la
suma de cuadrados mnima de 0.03503.
En la tabla E.2.10.8 se presentan los residuos calculados y en el grafico E.2.10.8 se
presenta el comportamiento de los residuos contra los valores predichos por el modelo.
TABLA E.2.10.8 GRAFICO E.2.10.8
-0.1
-0.08
-0.06
-0.04
-0.02
0
0.02
0.04
0.06
0.08
0.1
-0.5 0 0.5 1 1.5 2
VALORES PREDICHOS
R
E
S
I
D
U
O
S
Los valores de k, a y b para el modelo son por tanto:
Observacin
Pronstico
para Y
Residuos
0.0392 -0.042239 0.0814597
1.1410 1.0581389 0.0828941
1.6506 1.5697855 0.0807944
1.3403 1.3558862 -0.0156357
1.4327 1.4943307 -0.0616300
0.8717 0.8702813 0.0014304
1.3525 1.3819279 -0.0294489
0.7880 0.8702813 -0.0822786
-0.2877 -0.230097 -0.0575854
35
001 . 1
271 . 0
9586 . 0 ) 04224 . 0 (
=
=
= =
b
a
e k
Y el modelo queda escrito como:
H E A
P P r
27 . 0
9586 . 0 =
Este ejercicio tambin puede desarrollarse usando la funcin regresin de la opcin
anlisis de datos del men Herramientas en la hoja de clculo de Excel. En el archivo
regresin no lineal m2. xls, se presentan las salidas para dicha aplicacin:
En funcin de la comparacin del R
2
y de la MCE (ver tabla E.2.10.9) para ambos modelos
puede concluirse que el modelo que mejor representa la ley de velocidad de los datos es
el modelo del literal a).
TABLA E.2.10.9
Modelo R
2
MCE
E
H E
A
P
P P
r
774 . 1 1
852 . 2
+
=
0.9989 0.0001857
H E A
P P r
27 . 0
9586 . 0 =
0.9898 0.005838
También podría gustarte
- Toxicologia AlacranDocumento107 páginasToxicologia AlacranFanoVSAún no hay calificaciones
- Desengrasante - Quimica IndustrialDocumento5 páginasDesengrasante - Quimica IndustrialGustavo Cardona100% (2)
- Union Simple Acero InoxDocumento1 páginaUnion Simple Acero InoxJorge VillalbaAún no hay calificaciones
- Filtros de ZeolitasDocumento28 páginasFiltros de ZeolitasGustavo Cardona100% (1)
- Trabajo Parcial - Grupo 3 - In61Documento114 páginasTrabajo Parcial - Grupo 3 - In61Margot CotrinaAún no hay calificaciones
- Practica 1 PDFDocumento18 páginasPractica 1 PDFAlinne VillegasAún no hay calificaciones
- Memoria Descriptiva de Adicional Deductivo N°01Documento30 páginasMemoria Descriptiva de Adicional Deductivo N°01Susan Ñaupa Ricaldi100% (2)
- Para Separar 96Documento1 páginaPara Separar 96Dominikq123Aún no hay calificaciones
- Traduccion Aproximada Fases y Proceso de Marisa PeerDocumento51 páginasTraduccion Aproximada Fases y Proceso de Marisa Peerjoshua lancaster100% (1)
- Capitulo 6 - MasaDocumento6 páginasCapitulo 6 - MasaPlue MilkovichAún no hay calificaciones
- اسبانية 7Documento34 páginasاسبانية 7Aljebre MohmedAún no hay calificaciones
- Discusión 9. Ley de FaradayDocumento12 páginasDiscusión 9. Ley de FaradayGustavo CardonaAún no hay calificaciones
- Problemas-Flash DestilacionDocumento14 páginasProblemas-Flash DestilacionElizabeth EscalanteAún no hay calificaciones
- Examen 1a-Sep-2016 PDFDocumento3 páginasExamen 1a-Sep-2016 PDFFrank CanalesAún no hay calificaciones
- Guia de Costo AnualDocumento5 páginasGuia de Costo AnualGustavo CardonaAún no hay calificaciones
- Problemario CompletoDocumento6 páginasProblemario CompletokeniaAún no hay calificaciones
- TALLER Ingeniería de Las Reacciones Químicas 1 PDFDocumento4 páginasTALLER Ingeniería de Las Reacciones Químicas 1 PDFAndres LlorenteAún no hay calificaciones
- Ejemplo 6.13Documento4 páginasEjemplo 6.13Jackeline Condori sanchezAún no hay calificaciones
- PRQ 3210 Escobar Miljam No LinealDocumento4 páginasPRQ 3210 Escobar Miljam No LinealMiljam Escobar100% (1)
- Ejemplo 7.3-4 Sala 6Documento16 páginasEjemplo 7.3-4 Sala 6Luis Alfredo Lozano HernandezAún no hay calificaciones
- InfluenciaDocumento7 páginasInfluenciaJose CortezAún no hay calificaciones
- Problema 7.10 KERNDocumento6 páginasProblema 7.10 KERNJurgen Corpi Gómez100% (1)
- Asignación Destilación FINALDocumento34 páginasAsignación Destilación FINALJAMIT GUZMAN MARTINEZAún no hay calificaciones
- Problema 3.25 Ocon TojoDocumento1 páginaProblema 3.25 Ocon TojoJurgen Corpi GómezAún no hay calificaciones
- ICCT Intercambiadores de Calor de Casco y TuboDocumento88 páginasICCT Intercambiadores de Calor de Casco y TuboAlbertAún no hay calificaciones
- Problemas de AbsorcionDocumento7 páginasProblemas de AbsorcionJavier SantiagoAún no hay calificaciones
- Diagrama de Equilibrio Liquido - Vapor para El Sistema N-Pentano y N-Hexano - Lizbeth Gonzalez HernandezDocumento4 páginasDiagrama de Equilibrio Liquido - Vapor para El Sistema N-Pentano y N-Hexano - Lizbeth Gonzalez HernandezLizbeth Gonzalez HernandezAún no hay calificaciones
- Kremser EjercicioDocumento9 páginasKremser EjercicioAbril AlejandraAún no hay calificaciones
- Reglas HeuristicasDocumento3 páginasReglas HeuristicasMonica AlbaAún no hay calificaciones
- Absorcion de Gases - ProblemasDocumento2 páginasAbsorcion de Gases - Problemasalexar40@hotmail.com67% (3)
- IQ.09.01 - Actividad Asincrónica 6Documento4 páginasIQ.09.01 - Actividad Asincrónica 6Adolfo LazoAún no hay calificaciones
- Problema PFRDocumento3 páginasProblema PFRMarissaAún no hay calificaciones
- MonIRQ4. Baterías CSTRDocumento2 páginasMonIRQ4. Baterías CSTRAaron CarvajalAún no hay calificaciones
- Trabajo Masa IDocumento7 páginasTrabajo Masa IRoy Caballero100% (1)
- Segundo AvanceDocumento27 páginasSegundo AvanceKEVIN DANILO ACEVEDO PEREZ ESTUDIANTE ACTIVOAún no hay calificaciones
- Problemario Solido-FluidoDocumento2 páginasProblemario Solido-FluidoAdahiAún no hay calificaciones
- SOLUCIÓN DEL EJEMPLO 5.1 SmithDocumento3 páginasSOLUCIÓN DEL EJEMPLO 5.1 SmithDavid Rodriguez100% (1)
- Ejercicio Cinética Secado Material CerámicoDocumento2 páginasEjercicio Cinética Secado Material CerámicoJazmin EsparzaAún no hay calificaciones
- SecadoDocumento3 páginasSecadoJorge MuñozAún no hay calificaciones
- Obtm Problemas Tema 4Documento28 páginasObtm Problemas Tema 4Gary Tarqui MagneAún no hay calificaciones
- Informe Práctica 1Documento8 páginasInforme Práctica 1linamendozaAún no hay calificaciones
- Lab.3 Secado Por PulverizaciónDocumento7 páginasLab.3 Secado Por PulverizaciónPaola Robles VásquezAún no hay calificaciones
- CONVERSION EN REACTOR NO IDEALL - Aux, MET-3345 #10Documento7 páginasCONVERSION EN REACTOR NO IDEALL - Aux, MET-3345 #10Víctor AguilarAún no hay calificaciones
- UntitledDocumento19 páginasUntitledFernanda MoralesAún no hay calificaciones
- PRACTICA N°2 de Reactores 3Documento2 páginasPRACTICA N°2 de Reactores 3Ale SuaznabarAún no hay calificaciones
- Practica 4 Solucion Parcialmente MisciblesDocumento19 páginasPractica 4 Solucion Parcialmente MisciblesJULIO HUMBERTO TIRADO VASQUEZAún no hay calificaciones
- Guia 1 - Metodos EspectroscopDocumento5 páginasGuia 1 - Metodos EspectroscopJULITUS10000Aún no hay calificaciones
- Problemas1,6 Equipo1 PS3.Documento36 páginasProblemas1,6 Equipo1 PS3.Karel GerardoAún no hay calificaciones
- Problemas Cap - 10 Destilacion PDFDocumento4 páginasProblemas Cap - 10 Destilacion PDFCristian GomezAún no hay calificaciones
- Tutorias Grupales Sesion 1: A0 (Mol/min)Documento2 páginasTutorias Grupales Sesion 1: A0 (Mol/min)paulaAún no hay calificaciones
- SM&MDocumento4 páginasSM&MBere GarcíaAún no hay calificaciones
- Tarea 5Documento8 páginasTarea 5juan pablo macias leonAún no hay calificaciones
- Solucionario Ocon Tojo 7-9Documento1 páginaSolucionario Ocon Tojo 7-9The RickAún no hay calificaciones
- Ejercicio Kern 7.4Documento9 páginasEjercicio Kern 7.4Ilse VillalobosAún no hay calificaciones
- Ejer Cici OsDocumento5 páginasEjer Cici OsJerry Zapana JimemezAún no hay calificaciones
- Problemario 2do Dep - LZJMDocumento36 páginasProblemario 2do Dep - LZJMLuis Alejandro Sánchez OrtegaAún no hay calificaciones
- Ejemplo7.23 Caso Sistemas InmisciblesDocumento4 páginasEjemplo7.23 Caso Sistemas InmisciblesAlvaro GustavoAún no hay calificaciones
- Determinar El Número de Etapas de Una Torre de Destilación para Mezclas BinariasDocumento11 páginasDeterminar El Número de Etapas de Una Torre de Destilación para Mezclas BinariasYemaldo Valdivia M.Aún no hay calificaciones
- Ejercicio 8.2Documento11 páginasEjercicio 8.2Evelyn PinedaAún no hay calificaciones
- Tarea5 PDFDocumento26 páginasTarea5 PDFCandy GutierrezAún no hay calificaciones
- Columna PetlyukDocumento6 páginasColumna PetlyukJaret WendolynAún no hay calificaciones
- Problemas Ponchon Savarit Metodo Grafico Equipo 6Documento19 páginasProblemas Ponchon Savarit Metodo Grafico Equipo 6Irma MartínezAún no hay calificaciones
- Operaciones Unitarias IiiDocumento9 páginasOperaciones Unitarias IiiIsabel RinconAún no hay calificaciones
- Ejercicio 7.10 KernDocumento6 páginasEjercicio 7.10 KernMirleyss PelaezAún no hay calificaciones
- Trey Bal EjerciciosDocumento7 páginasTrey Bal EjerciciosFabio Eitnar MelgarejoAún no hay calificaciones
- Estudio de Las Isotermas de Adsorcion Prq-205Documento4 páginasEstudio de Las Isotermas de Adsorcion Prq-205PaolaAún no hay calificaciones
- Ejercicios. Unidad III Cinetica de Las Reacciones Quimicas Ejercicios ResueltosDocumento6 páginasEjercicios. Unidad III Cinetica de Las Reacciones Quimicas Ejercicios ResueltosAli Ernesto100% (1)
- Tarea 4.españolDocumento16 páginasTarea 4.españolYuranny AgudeloAún no hay calificaciones
- TRABAJO ATACORI yONDER ARAYA - 0410112356 PDFDocumento11 páginasTRABAJO ATACORI yONDER ARAYA - 0410112356 PDFGustavo CardonaAún no hay calificaciones
- 08 0326 EoDocumento96 páginas08 0326 EoGustavo CardonaAún no hay calificaciones
- DESENGRASANTEDocumento2 páginasDESENGRASANTEMarcos Antonio Hernández PatiñoAún no hay calificaciones
- ACIDO BORICOfinalDocumento48 páginasACIDO BORICOfinalGustavo Cardona100% (5)
- Plantas Medicinales de Venezuela.Documento15 páginasPlantas Medicinales de Venezuela.AymericktyAún no hay calificaciones
- Métodos Numéricos Con MATLAB - John Mathews, Kurtis Fink - 3edDocumento2 páginasMétodos Numéricos Con MATLAB - John Mathews, Kurtis Fink - 3edByron Benjamin BaharasAún no hay calificaciones
- Frecan 2015 Es SPDocumento140 páginasFrecan 2015 Es SPmikel4carbajo0% (1)
- Plan APPCCDocumento10 páginasPlan APPCCMoises VillagraAún no hay calificaciones
- Mi Gato Es Un PillinDocumento45 páginasMi Gato Es Un PillinRAPHAEL LEONARDO JULCARIMA CEDILLOAún no hay calificaciones
- DerivadaDocumento13 páginasDerivadaOscarAún no hay calificaciones
- 5 Puerto Santander Documento General Tomo 5Documento38 páginas5 Puerto Santander Documento General Tomo 5Denilson Hernandez NalAún no hay calificaciones
- Ejercicios Incoterms ExportacionesDocumento2 páginasEjercicios Incoterms ExportacionesISABELA NARVAEZ ALVAREZAún no hay calificaciones
- Manual Usuario ZTE Z982Documento127 páginasManual Usuario ZTE Z982jcuc69Aún no hay calificaciones
- Caso de Guardia 01.09.22Documento71 páginasCaso de Guardia 01.09.22Javier Ariza De La HozAún no hay calificaciones
- Simulacion ComputacionalDocumento21 páginasSimulacion ComputacionalEnriqe PuentesAún no hay calificaciones
- Fundamento de La Motricidad en El Rendimientos Deportivo. Fernandez RomeroDocumento573 páginasFundamento de La Motricidad en El Rendimientos Deportivo. Fernandez RomeroJordi Cañadas LopezAún no hay calificaciones
- Ribes (2016) - La Psicologia. Que InvestigarDocumento12 páginasRibes (2016) - La Psicologia. Que InvestigarMine RHAún no hay calificaciones
- Diagnostico Integral de ArchivoDocumento36 páginasDiagnostico Integral de ArchivoUNIDAD DE ARCHIVO CENTRAL UNAMADAún no hay calificaciones
- Mapa Conceptual Proceso AdministrativoDocumento2 páginasMapa Conceptual Proceso AdministrativoFolopoAún no hay calificaciones
- Sabana Humedas de PalmerasDocumento12 páginasSabana Humedas de PalmerasErick Jonathan Hernadez RimapaAún no hay calificaciones
- Ejercicios de Propiedades Coligativas de Las SolucionesDocumento2 páginasEjercicios de Propiedades Coligativas de Las SolucionesJose MejicanoAún no hay calificaciones
- CAPÍTULO 11 - Bioenergética - La Función Del ATPDocumento14 páginasCAPÍTULO 11 - Bioenergética - La Función Del ATPMartha A HervertAún no hay calificaciones
- Volqueta T800Documento2 páginasVolqueta T800salazarAún no hay calificaciones
- Remodelacion e Implementacion de LabortorioDocumento6 páginasRemodelacion e Implementacion de LabortorioGuillermo Gutierrez50% (2)
- Fisica 2Documento5 páginasFisica 2Caty MuzoAún no hay calificaciones
- TFG L2051Documento76 páginasTFG L2051David Gómez CanabalAún no hay calificaciones
- Brochure Maquinas Desmechadora de Carnes-CleanDocumento5 páginasBrochure Maquinas Desmechadora de Carnes-Cleanjofre alexanderAún no hay calificaciones
- Guía de Actividades y Rúbrica de Evaluación - Caso 1 - ConceptualizaciónDocumento7 páginasGuía de Actividades y Rúbrica de Evaluación - Caso 1 - ConceptualizaciónLoli MonterrozaAún no hay calificaciones
- Manual de Aseguramiento de Calidad de Pollos AmanacuDocumento23 páginasManual de Aseguramiento de Calidad de Pollos AmanacuNohelia Y Rodriguez BAún no hay calificaciones