Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Conductancia de Los Electrolitos
Cargado por
John MontellanosDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Conductancia de Los Electrolitos
Cargado por
John MontellanosCopyright:
Formatos disponibles
CONDUCTANCIA DE LOS ELECTROLITOS
UNI - FIQT
Contenido
OBEJTIVOS ........................................................................................................................................... 2 FUNDAMENTO TEORICO ..................................................................................................................... 2 DATOS EXPERIMENTALES .................................................................................................................... 3 TRATAMIENTO DE DATOS ................................................................................................................... 4 DISCUSIN DE RESULTADOS ............................................................................................................. 12 CONCLUSIONES ................................................................................................................................. 12 BIBLIOGRAFA .................................................................................................................................... 13
CONDUCTANCIA DE LOS ELECTROLITOS
UNI - FIQT
CONDUCTANCIA DE LOS ELECTROLITOS
OBEJTIVOS Determinar la conductividad equivalente de los electrolitos a diferentes concentraciones. Determinar las conductividades equivalentes de los electrolitos a dilucin infinita.
FUNDAMENTO TEORICO En un conductor electroltico la conductancia depende de su concentracin, es por esto que se establece el concepto de conductividad molar, que es la conductividad que existe en 1 mol de electrolito por cada litro de solucin. Conductancia elctrica (G) est definido como la facilidad que dicho conductor presenta al movimiento de los electrones, esto es, la inversa de su resistencia elctrica (R): G=1/R La unidad de la conductancia es el siemens (S).
Conductividad La conductividad molar es una magnitud que da cuenta de la capacidad de transporte de corriente elctrica de un electrlito en una disolucin. Depende de la concentracin (n de iones en ella: cationes o aniones). Pero tambin depende de la naturaleza del soluto.
Donde K es la conductividad de la solucin y c es la concentracin molar del electrlito. Las unidades de la conductividad molar son Sm2mol-1
La conductividad de una solucin de electrolitos (fuertes o dbiles) aumenta al incrementar la concentracin de iones. En el caso de electrolitos fuertes, el nmero de iones por unidad de volumen aumenta en proporcin directa a la concentracin. No es as para electrlitos dbiles. En ellos el aumento no es tan grande debido a la ionizacin parcial del soluto. Por esta razn, la conductividad de electrolitos dbiles no aumenta tan rpido como en los electrolitos fuertes.
CONDUCTANCIA DE LOS ELECTROLITOS
UNI - FIQT
Ley de Kohlrausch
Figura N 1 Es la ecuacin de una lnea recta si se dibuja lambda vs (M)1/2 con intercepto en el eje vertical que corresponde a la conductividad molar a dilucin infinita. El valor de la conductividad molar, cuando M va a cero (dilucin infinita), representa la conductividad molar de los iones tan separados que no interaccionan entre s al migrar hacia los electrodos. La figura, a su vez, muestra electrlitos fuertes que obedecen la ley de Kohlrausch si la solucin es diluida. Para electrolitos dbiles no obtenemos una recta. El aumento en la conductividad molar de los electrolitos dbiles que ocurre al diluir, se debe principalmente a un aumento en el nmero de iones que resulta cuando se desplaza el equilibrio de disociacin hacia la derecha. Las conductividades molares en dilucin infinita de varios electrolitos fuertes diferentes, los iones migran independientemente. Esto significa que en dilucin infinita la conductividad molar es igual a la suma de las conductividades molares lmites del catin y del anin:
DATOS EXPERIMENTALES
Orden de medicin 1 2 3 4 5
C (equiv./l) 0.0003125 0.00625 0.0125 0.025 0.05
Solucin :CH3COONa Conductancia,S T(C) 48 S 608 S 1080 S 2.09 mS 3.09 mS 25.1 24.9 24.4 24.4 24.1
Solucin: NaCl Conductancia,S T(C) 39.5 S 770 S 1478 S 2.82 mS 5.66 mS 24.7 24.8 25 24.8 24.6
Solucin: HCl Concuctancia,S T(C) 53.8 S 665 S 1249 S 2.48 mS 4.83 ms 24.5 24.4 24.5 24.3 24.6
CONDUCTANCIA DE LOS ELECTROLITOS
UNI - FIQT
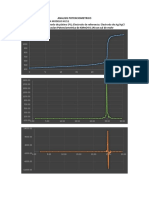
TRATAMIENTO DE DATOS 1. Calcular la conductancia especfica para cada solucin acuosa de HCl,NaCl y CH3COONa.ecuasion (1); Representar en forma grfica la conductancia especifica respecto a la concentracin para el HCl,NaCl y CH3COONa.
cocnductancia especifica(S/cm)
Conductancia medida (S/cm)
Conductancia especifica del agua destilada (S) 2.9 S/cm
Conductancia especifica de CH3COONa
CH3COONa
3500
3000
2500 2000 1500 1000 500 0 0 0.01 0.02 0.03 0.04 0.05 0.06
48 S/cm 608 S/cm 1080 S/cm 2.09 mS/cm 3.09 mS/cm
45.1 S/cm 2.9 S/cm 605.1 S/cm 2.9 S/cm 1077.1 S/cm 2.9 S/cm 2087.1 S/cm 2.9 S/cm 3087.1 S/cm
concentracion (mol/L)
conductancia especifica(S/cm)
Conductancia medida (S/cm)
Conductancia especifica del agua destilada (S) 2.9 S/cm
Conductancia especifica de NaCl
NaCl
6000 5000 4000 3000 2000 1000 0 0 0.01 0.02 0.03 0.04 0.05 0.06 concentracion (mol/L)
39.5 S 770 S 1478 S 2.82 mS 5.66 mS
36.6 S/cm 2.9 S/cm 767.1 S/cm 2.9 S/cm 1475.1 S/cm 2.9 S/cm 2817.1 S/cm 2.9 S/cm 5657.1 S/cm
CONDUCTANCIA DE LOS ELECTROLITOS
UNI - FIQT
Conductancia medida (S/cm)
conductancia especifica(S/cm)
Conductancia especifica del agua destilada (S) 2.9 S/cm
Conductancia especifica de NaCl
HCl
6000
5000 4000
53.8 S 665 S 1249 S 2.48 mS 4.83 ms
50.9 S/cm 2.9 S/cm 662.1 S/cm 2.9 S/cm 1246.1 S/cm 2.9 S/cm 2477.1 S/cm 2.9 S/cm 4827.1 S/cm
3000
2000 1000 0 0 0.01 0.02 0.03 0.04 0.05 0.06
concentracion (mol/L)
2. Calcular la conductividad equivalente para cada solucin acuosa de HCl, NaCl y CH3COONa. ecuacin (2):
Conductancia especifica de HCl 39.5 S 770 S 1478 S 2.82 mS 5.66 mS Conductancia especifica de CH3COONa 48 S/cm 608 S/cm 1080 S/cm 2.09 mS/cm 3.09 mS/cm
Concentracin(mol/L) 0.0003125 0.00625 0.0125 0.025 0.05 Concentracin(mol/L) 0.0003125 0.00625 0.0125 0.025 0.05
Conductividad especifica (=1000K/C) en Scm2/mol 11.712 12.2736 11.8008 11.2684 11.3142 Conductividad especifica (=1000K/C) en Scm2/mol 14.432 9.6816 8.6168 8.3484 6.1742
Conductancia especifica de CH3COONa. 53.8 S 665 S 1249 S 2.48 mS 4.83 ms
Concentracin(mol/L) 0.0003125 0.00625 0.0125 0.025 0.05
Conductividad especifica (=1000K/C) en Scm2/mol 16.288 10.5936 9.9688 9.9084 9.6542
CONDUCTANCIA DE LOS ELECTROLITOS
UNI - FIQT
3. Representar en forma grfica la conductividad equivalente respecto a la para el HCl, NaCl y CH3COONa. Mediante la extrapolacin determinar el valor de para el HCl, NaCl y CH3COONa cuando (dilucin infinita). La grafica de en funcion de , es casi lineal para un electrolito fuerte, use el mtodo de mnimos cuadrados. Para el Primera medicin :
Segunda medicin
Tercera medicin
Cuarta medicin
Quinta medicin
CONDUCTANCIA DE LOS ELECTROLITOS
UNI - FIQT
VS del CH3COONa
160 140 120 100 80 60 40 20 0 0 0.05 0.1 0.15 0.2 0.25 y = -296.45x + 132.74 Series1 Lineal (Series1)
De la ecuacin:
y = -296.45x + 132.74
Para el
Primera medicin
Segunda medicin
CONDUCTANCIA DE LOS ELECTROLITOS Tercera medicin
UNI - FIQT
Cuarta medicin
Quinta medicin
VS del CH3COONa
124 122 120 118 116 114 112 0 0.05 0.1 0.15 0.2 0.25 Series1
Como los puntos no muestran ninguna tendencia lineal, tomamos solo los 3 puntos del medio ya que son nicos que poseen tendencia lineal.
CONDUCTANCIA DE LOS ELECTROLITOS
UNI - FIQT
VS del CH3COONa
124 122 120 118 116 114 112 0 0.05 0.1 0.15 0.2 y = -126.34x + 132.51 Series1 Lineal (Series1)
De la ecuacin:
y = -126.34x + 132.51
Para el
Primera medicin
Segunda medicin
CONDUCTANCIA DE LOS ELECTROLITOS Tercera medicin
UNI - FIQT
Cuarta medicin
Quinta medicin
VS del CH3COONa
180 160 140 120 100 80 60 40 20 0 0 0.05 0.1 0.15 0.2 0.25
Series1 Lineal (Series1) y = -284.76x + 146.44
De la ecuacin:
y = -284.76x + 146.44
10
CONDUCTANCIA DE LOS ELECTROLITOS
UNI - FIQT
4. Puesto que la ecuacin (4) es vlida para todos los electrolitos, hallar CH3COOH a partir de:
para el
Para hallar el VALOR TEORICO de
tomaremos los datos de la tabla 11-4 del
libro Fundamentos de Fisicoqumica, Maron & Prutton
11
CONDUCTANCIA DE LOS ELECTROLITOS DISCUSIN DE RESULTADOS
UNI - FIQT
Si comparamos los valores obtenidos, as como las grficas, podemos ver que la conductividad vara con la concentracin de las soluciones. Esta aumenta a medida que la concentracin lo hace, ya que incremente tambin el nmero de iones por unidad de volumen en la solucin. Tambin, se puede observar que la conductividad del HCl es mayor a la de las dems. Esto se debe a que el in H+ presenta una gran velocidad. Cada in H+ intercambia su protn al azar con las molculas de agua que lo rodean, y as, logra avanzar ms rpido que, por ejemplo, un in Na+, que est rodeado de molculas de agua y es ms grande y, por tanto, avanza ms lento. El buen lavado del instrumento es esencial para evitar que restos de la solucin medida en la celda afecten a las siguientes mediciones. Es por esto que se lav el conductmetro varias veces con agua destilada luego de cada medicin y se comprob que la conductancia del agua est siempre entre 2.9S/cm.
CONCLUSIONES
Se comprob que la ley de Kohlrausch ( ) se cumple para soluciones diluidas de electrlitos fuertes, como es el caso del HCl, el NaCl y el CH3COONa. Adems, fue posible determinar la conductividad molar de los mismos de una manera eficiente y fcil, as como tambin, determinar la conductividad molar de un electrolito dbil a dilucin infinita. La conductividad equivalente del electrlito dbil (acetato de sodio) disminuye rpidamente al aumento de la concentracin de la solucin pues se disocia ms a mayor dilucin. La conductividad especfica (K) disminuye conforme la concentracin disminuye mientras que la conductividad equivalente (lambda) aumenta al disminuir la concentracin de la disolucin. La mayor conductividad del HCl, con respecto a los otros electrlitos, se debe a la gran velocidad que tienen los H+ para transportarse. Esto ocurre por la transferencia de los protones mediante molculas de agua del medio.
12
CONDUCTANCIA DE LOS ELECTROLITOS BIBLIOGRAFA
UNI - FIQT
LEVINE, IRA, Fsico-qumica, tercera edicin, Ed. Mc Graw Hill, Madrid, 1994, pg.: 576-590. Conductancia de electrolitos. En: http://www.scribd.com/doc/22810615/LabFiquiII-ConductanciaDeLosElectrolitosB. Bsqueda realizada el da 17 de setiembre del 2010.
CRC HANDBOOK OF CHEMISTRY AND PHYSICS 87th ed. 2006-2007. Fundamentos de Fisicoqumica, Maron & Prutton, editorial LIMUSA, pg: 422430.
13
También podría gustarte
- Astm D525Documento2 páginasAstm D525John Montellanos100% (1)
- Tecnologia SHRPDocumento5 páginasTecnologia SHRPBETOAún no hay calificaciones
- Conductimetria PDFDocumento7 páginasConductimetria PDFKariEspinozaAún no hay calificaciones
- Cuestionario 4 Orga 2Documento8 páginasCuestionario 4 Orga 2Gianpierre Rojas AgapitoAún no hay calificaciones
- Termodinamica Tecnica y Motores TermicosDocumento499 páginasTermodinamica Tecnica y Motores Termicosjose luis BerrioAún no hay calificaciones
- Segunda UnidadDocumento62 páginasSegunda UnidadMarcos OrendainAún no hay calificaciones
- Diagrama Ternario Informe LaboDocumento14 páginasDiagrama Ternario Informe LaboIz RemyAún no hay calificaciones
- Teq4p2 ConcluDocumento4 páginasTeq4p2 ConcluALEX ALEXXAún no hay calificaciones
- Practica 4.CINÉTICA QUÍMICA DE LA HIDRÓLISIS DEL CLORURO DE terc-BUTILODocumento4 páginasPractica 4.CINÉTICA QUÍMICA DE LA HIDRÓLISIS DEL CLORURO DE terc-BUTILOAlex RamosAún no hay calificaciones
- Informe 8Documento19 páginasInforme 8Giuseppe Luigi Nuñez AguilarAún no hay calificaciones
- Hidrolisis de Acetato de EtiloDocumento11 páginasHidrolisis de Acetato de EtiloEduardo Condeña CachayAún no hay calificaciones
- Capitulo III - Volumetria de Precipitacion - s2022 - IIDocumento10 páginasCapitulo III - Volumetria de Precipitacion - s2022 - IIOrson Jesús Merel RamírezAún no hay calificaciones
- Informe Computacion 1Documento13 páginasInforme Computacion 1EsliDavidMolerosIngunzaAún no hay calificaciones
- Lab 09Documento11 páginasLab 09ljsilva11Aún no hay calificaciones
- Problema 10Documento2 páginasProblema 10Dahimar Mercedes Sánchez MedinaAún no hay calificaciones
- Informe Fisico Quimica II - Volumenes Molares ParcialesDocumento14 páginasInforme Fisico Quimica II - Volumenes Molares ParcialesDaniel Villavicencio RamosAún no hay calificaciones
- Practica Torre de Enfriamiento LIQ 1Documento6 páginasPractica Torre de Enfriamiento LIQ 1AlfredoAún no hay calificaciones
- Resolución Ejercicios - Serie 7Documento17 páginasResolución Ejercicios - Serie 7eliana vegaAún no hay calificaciones
- Pract.4 Volumetria de Precipitacion Analisis de Plata en AleacionesDocumento10 páginasPract.4 Volumetria de Precipitacion Analisis de Plata en Aleacionesjuan carlosAún no hay calificaciones
- Laboratorio FQ II Guevara Bernardo ArianeDocumento13 páginasLaboratorio FQ II Guevara Bernardo ArianeAndy AlegreAún no hay calificaciones
- Ejercicios Tema7Documento9 páginasEjercicios Tema7Ximena AcAún no hay calificaciones
- 5.titulaciones ConductimetricasDocumento12 páginas5.titulaciones Conductimetricasjofre232450% (2)
- Copia de ActividadSemana5Documento6 páginasCopia de ActividadSemana5Alejandro AyalaAún no hay calificaciones
- Problemas de PH y Soluciones AqmortiguadorasDocumento7 páginasProblemas de PH y Soluciones Aqmortiguadorasdesder0% (1)
- Antecedentes Practica 8Documento9 páginasAntecedentes Practica 8Tania MorenoAún no hay calificaciones
- Grupo de Angie Salvador de La Cruz, Examen Parcial 1Documento12 páginasGrupo de Angie Salvador de La Cruz, Examen Parcial 1Angie Massiel Salvador de la cruzAún no hay calificaciones
- SZXNKJBKBKBDocumento3 páginasSZXNKJBKBKBGiovanny TorresAún no hay calificaciones
- Estandarizacion D Kmno4Documento3 páginasEstandarizacion D Kmno4Willy MelgarejoRmroAún no hay calificaciones
- Laboratorio 1 Fisico QuimicoDocumento24 páginasLaboratorio 1 Fisico QuimicoRosaAún no hay calificaciones
- Electroquímica Lab N°4 CodeposiciónDocumento9 páginasElectroquímica Lab N°4 CodeposiciónSoy un Gordo ConchatumadreAún no hay calificaciones
- Valoracion Potenciometrica de HalurosDocumento3 páginasValoracion Potenciometrica de HalurosChuck SchuldinerAún no hay calificaciones
- Cinetica Quimica-Reacciones en Serie-Simil HidraulicoDocumento10 páginasCinetica Quimica-Reacciones en Serie-Simil HidraulicoFabricio FajardoAún no hay calificaciones
- Labo de InorganicaDocumento36 páginasLabo de InorganicaAngel Ulises Reyes NAún no hay calificaciones
- Informe 1 Aldehidos y CetonasDocumento17 páginasInforme 1 Aldehidos y CetonasElizabeth EscalanteAún no hay calificaciones
- Complejos Compuestos de CoordinacionDocumento19 páginasComplejos Compuestos de CoordinacionLuis Antony Lorenzo Gonzales75% (4)
- Actividad 5Documento10 páginasActividad 5Luis Fernando Tapia RodriguezAún no hay calificaciones
- Práctica 3 LiqDocumento3 páginasPráctica 3 LiqAlexander Maus100% (1)
- Quimica de CoordinacionDocumento21 páginasQuimica de CoordinacionDenisse Alcarraz Loa0% (1)
- Pruebas para Caracterizar Compuestos OrganicosDocumento7 páginasPruebas para Caracterizar Compuestos OrganicosLAURY ESTELA VILLADIEGO SUAREZ ESTUDIANTE ACTIVOAún no hay calificaciones
- Informe No 6 Frontera MovilDocumento5 páginasInforme No 6 Frontera MovilAndrea diazAún no hay calificaciones
- INFORME PRÁCTICA 5 Sulfatos (Autoguardado)Documento8 páginasINFORME PRÁCTICA 5 Sulfatos (Autoguardado)Jeremy HernandezAún no hay calificaciones
- Alegre Guevara Andy #3Documento6 páginasAlegre Guevara Andy #3RAMOS OLLACHICA MARYORI JENNIFERAún no hay calificaciones
- Frontera MovilDocumento5 páginasFrontera MovilDuvan Pete EmbusAún no hay calificaciones
- Síntesis Del Complejo Ioduro de (Diacuo) Bis (Etilendiamino) Cobre (II) (Cu (En) 2 (H2O) 2) I2.Documento6 páginasSíntesis Del Complejo Ioduro de (Diacuo) Bis (Etilendiamino) Cobre (II) (Cu (En) 2 (H2O) 2) I2.nathaly310190Aún no hay calificaciones
- Diagrama de Fases de Un Sistema TernarioDocumento13 páginasDiagrama de Fases de Un Sistema TernarioJohn Montellanos100% (2)
- Tema 5 - Equilibrio Material de FasesDocumento2 páginasTema 5 - Equilibrio Material de Fasesdrika17Aún no hay calificaciones
- Problema 8-6Documento4 páginasProblema 8-6EduardodelAngelAún no hay calificaciones
- Problemas de EquilibrioDocumento2 páginasProblemas de EquilibrioOtZaDiazLaraAún no hay calificaciones
- 2doparcial 30-06-2015 TESADocumento17 páginas2doparcial 30-06-2015 TESAJoshua Gordillo0% (1)
- TerDocumento9 páginasTerAnonymous K75YmDxG61Aún no hay calificaciones
- Ejercicio de IR y CromatografiaDocumento13 páginasEjercicio de IR y CromatografiaKelly CamargoAún no hay calificaciones
- Manual Met Cuanti P1 y P2Documento36 páginasManual Met Cuanti P1 y P2Esteban RicoAún no hay calificaciones
- PROBELMA 2 CorregidoxpDocumento1 páginaPROBELMA 2 CorregidoxpPatriciaLlacsaLázaroAún no hay calificaciones
- MicrorreactoresDocumento1 páginaMicrorreactoresBastian Puentes NavarroAún no hay calificaciones
- Guia de Ejercicios 3 Analisis VolumetricoDocumento4 páginasGuia de Ejercicios 3 Analisis VolumetricoSamuel BoltonAún no hay calificaciones
- Volumetria de NeutralizacionDocumento46 páginasVolumetria de NeutralizacionBruno ValverdeAún no hay calificaciones
- Informe N1 de Quimica Inorgánica AIIIDocumento13 páginasInforme N1 de Quimica Inorgánica AIIIBraulio Luciano Lopez GarciaAún no hay calificaciones
- AnitaDocumento6 páginasAnitaCèsar Eduardo Vásquez VásquezAún no hay calificaciones
- Informe 16 - Descomposición CatalíticaDocumento17 páginasInforme 16 - Descomposición CatalíticaKATHERINNE LUZ CHUCO DE LA CRUZAún no hay calificaciones
- 6termoquimica 3140Documento3 páginas6termoquimica 3140german0% (1)
- Conductividad de Un ElectrolitoDocumento12 páginasConductividad de Un ElectrolitoPiero Alejandro Estrada AngelesAún no hay calificaciones
- Labo 4Documento9 páginasLabo 4Kevin FloresAún no hay calificaciones
- Problemas de Van Proyectos de InversionDocumento4 páginasProblemas de Van Proyectos de InversionJohn MontellanosAún no hay calificaciones
- Problemas de Van Proyectos de InversionDocumento4 páginasProblemas de Van Proyectos de InversionJohn MontellanosAún no hay calificaciones
- FinanzasDocumento4 páginasFinanzasJohn Montellanos0% (1)
- UCRETE CálculoDocumento6 páginasUCRETE CálculoJohn MontellanosAún no hay calificaciones
- Variables Del ProcesoDocumento7 páginasVariables Del ProcesoJohn MontellanosAún no hay calificaciones
- ANEXO Aleaciones DiagramasDocumento5 páginasANEXO Aleaciones DiagramasJohn MontellanosAún no hay calificaciones
- Cinetica ElectroquimicaDocumento66 páginasCinetica ElectroquimicaIsaac Israel Talavera BlandonAún no hay calificaciones
- Norma Coguanor NTG 41017 h11 Astm c805 PDFDocumento10 páginasNorma Coguanor NTG 41017 h11 Astm c805 PDFWilliam Montiel Cardozo100% (1)
- Modelo de La Inflación y Oferta MonetariaDocumento7 páginasModelo de La Inflación y Oferta MonetariaNery QPAún no hay calificaciones
- Curricula ELI ISTP RFADocumento1 páginaCurricula ELI ISTP RFACarlos YupanquiAún no hay calificaciones
- Trigonometría en El Triángulo RectánguloDocumento23 páginasTrigonometría en El Triángulo RectánguloLópezz Ester MaríaAún no hay calificaciones
- Catalogo Metal DesplegadoDocumento6 páginasCatalogo Metal DesplegadoLeo VillagránAún no hay calificaciones
- Taller 2 - Potencial Eléctrico y CapacitanciaDocumento6 páginasTaller 2 - Potencial Eléctrico y CapacitanciaAnibal Tobar0% (1)
- SERVOCUNA BN-100 Manual Español R 1.2Documento31 páginasSERVOCUNA BN-100 Manual Español R 1.2STEFHANIA LONGASAún no hay calificaciones
- Presentación Tesis NataliaDocumento27 páginasPresentación Tesis NataliaoscarAún no hay calificaciones
- Fisica Periodo1Documento3 páginasFisica Periodo1soporte8351Aún no hay calificaciones
- INFORME PROYECTO Cercha 5TOBDocumento14 páginasINFORME PROYECTO Cercha 5TOBAdriana Carolina Uchazara CondeAún no hay calificaciones
- Aportes de Lavoisier A La QuímicaDocumento4 páginasAportes de Lavoisier A La QuímicaIsaac SanchezAún no hay calificaciones
- Balance de Energia y Materia UntDocumento14 páginasBalance de Energia y Materia UntFernanda Nicole Miro Quezada PanaifoAún no hay calificaciones
- Formato Matriz IpevrDocumento9 páginasFormato Matriz Ipevrcarlos alberto botello rodriguezAún no hay calificaciones
- MT101 PDFDocumento3 páginasMT101 PDFRubén LoboAún no hay calificaciones
- FundicionDocumento20 páginasFundicionErick BarriaAún no hay calificaciones
- La Teoría de CuerdasDocumento2 páginasLa Teoría de CuerdasDiego CastroAún no hay calificaciones
- Contenido de Humedad Tecnologia Del ConcretoDocumento33 páginasContenido de Humedad Tecnologia Del ConcretoEdward RtzAún no hay calificaciones
- Operaciones y Montaje ElectromecánicoDocumento73 páginasOperaciones y Montaje ElectromecánicoJuan Pablo GutierrezAún no hay calificaciones
- Solucionario IngChavez PDFDocumento231 páginasSolucionario IngChavez PDFSary Sandoval SantanderAún no hay calificaciones
- Informe DiaclasasDocumento22 páginasInforme DiaclasasJahir MaguiñaAún no hay calificaciones
- Ensayo Downhole y CrossholeDocumento39 páginasEnsayo Downhole y CrossholeK'mi HernàndezAún no hay calificaciones
- Prаctica 1 - Determinaciвn de la entalpбa de descomposiciвn del perвxido de hidrвgenoDocumento6 páginasPrаctica 1 - Determinaciвn de la entalpбa de descomposiciвn del perвxido de hidrвgenoFabian HerranAún no hay calificaciones
- Analizador de InfrarrojosDocumento2 páginasAnalizador de InfrarrojosSamuel Flipperman Gutierrez MerazAún no hay calificaciones
- Taller 1 - 2023-3Documento5 páginasTaller 1 - 2023-3Estefanie CeballosAún no hay calificaciones
- Unidad 2 El Calor Como Energía CORREGIDODocumento12 páginasUnidad 2 El Calor Como Energía CORREGIDODoris Ali VelizAún no hay calificaciones
- Diferenciacion e Integracion NumericaDocumento14 páginasDiferenciacion e Integracion NumericaEdic AbundezAún no hay calificaciones
- Romero Judith Tipo de Problemas MultiplicativosDocumento1 páginaRomero Judith Tipo de Problemas Multiplicativosapi-443909133Aún no hay calificaciones