Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Tema 012
Cargado por
Luis Salinas ADescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Tema 012
Cargado por
Luis Salinas ACopyright:
Formatos disponibles
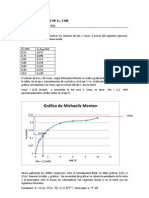
Tema: 12. Obtencin y anlisis de datos cinticos.
1. Integracin de la ecuacin de Michaelis-Menten:
1.1. Orden cero de reaccin
1.2 . Orden uno de reaccin
1.3. Orden mixto de reaccin
2. Linearizacin de la ecuacin de Michaelis-Menten:
2.1. Representacin de dobles inversos o de Linenweaver-Burk.
2.2. Representacin de Hanes
2.3. Representacin de Eadie-Hofstee.
2.4. Representacin lineal directa o representacin de Einsenthal y
Cornish-Bowden
1. Integracin de la ecuacin de Michaelis-Menten:
Estudio de acuerdo con el orden de reaccin
Dependencia de la velocidad con respecto a la [S]
| |
| | S Km
S
V v
+
= max
max max V
S
S
V
dt
dS
v = = =
t V So St
dt V dS
max
max
=
=
1.1. Orden cero de reaccin
S>>>Km
10 veces la Km
Integrando entre So y St y entre 0 y t
Permite comparar cantidades totales de enzima
Vmax1= kcat [E
01
]
Vmax2= kcat [E
02
]
| |
| | 2 max
1 max
02
01
V
V
E
E
=
La razn de las cantidades de enzima es proporcional a la razn de velocidades
mximas o de las actividades enzimticas obtenidas experimentalmente
Comparar cantidades de una misma enzima de un tejido o en
circunstancias metablicas diversas, diferenciacin, patologas, etc
1.2. Orden uno de reaccin
S<<<<Km
A concentraciones 1/10 Km
| |
| | S Km
S
V v
+
= max
Km
S
V
dt
dS
v max = =
| |
t
Km
V
t St
So
e So St
t
Km
V
St
So
t
Km
V
So St
dt
Km
V
S
dS
max
0
max
ln
max
ln ln
max
- =
=
=
=
} }
Integrando entre S
0
y S
t
Conociendo cantidad incial de
enzima [Eo] puede obtenerse la
constante de especificidad (kcat/Km)
Obtener el valor de Vmax/Km
1.3. Orden mixto de reaccin
| |
| | S Km
S
V v
+
= max
( )
t
S S
Km Km
V
St
So
t
t V St So
So
St
Km
dt V ds
dt
dS
Km
dt V
S
S Km
dS
S Km
S
V
dt
dS
v
t o
St
So
t St
So
) ( 1 max
ln
1
max ln
max
max
max
0
=
= +
=
=
+
+
= =
} } }
Km
m
1
=
S Km
Dividiendo los dos trminos por Km y por t
Vmax
St
So
t
ln
1
t
S S t o ) (
Linearizacin de la ecuacin
integrada de M-M a S Km
Estudiando el avance de una sola reaccin cuando
estamos en orden mixto se pueden obtener:
Vmax y Km
Para obtener los parmetros cinticos de una enzima lo que solemos hacer
es obtener la velocidad inicial, v, a diferentes concentraciones de S.
v frente a [S]
Lo primero es obtener los correspondientes parmetros cinticos.
2. Linearizacin de la ecuacin de Michaelis-Menten
v
[S]
V
max
| |
| | S Km
S
V v
+
= max
H Imaginemos que estamos estudiando una reaccin S P
catalizada por una enzima E, y que obtenemos los siguientes
resultados:
[S] (mmol L
-1
) v
o
(mol L
-1
min
-1
)
0,30 0,57
0,50 0,85
0,75 1,18
1,50 1,82
3,00 2,50
7,50 3,23
A partir de estos datos calcular Vmax y Km mediante la
representacin V [S].
Calclenlo ahora y escriban sus resultados en la
pizarra.
* Estas dificultades, fueron ya tenidas en cuenta por Michaelis y
Menten, quienes intentaron representar v frente a log[S]. Esta
representacin tiene ciertas ventajas, aparte de su valor histrico,
pero debido a su poco xito, en la bioqumica moderna, no
comentaremos nada ms sobre ella.
Como acabamos de ver la representacin de v frente a
[S] es poco til para estos fines, debido a:
- la dificultad para dibujar con precisin una hiprbola
rectangular
- la dificultad para encontrar las asntotas (Vmax), de
manera correcta, y consecuentemente para calcular Km
Analicen los datos.
Alguna conclusin?
Para resolver este problema, y poder calcular Vmax y Km con
mayor fiabilidad, se han propuesto varios procedimientos o
mtodos. La mayora de ellos basados en la linealizacin de la
ecuacin de Michaelis-Menten
Quizs las tres representaciones ms usadas sean:
- Representacin de Linenweaver-Burk o de dobles inversos
(1/v 1/[S])
- Representacin de Hanes ([S]/v [S])
- Representacin de Eadie-Hofstee (v v/[S])
Adems de estas tres representaciones, basadas en la
linealizacin de la ec. de M&M, existe una curta basada en la
representacin directa v [S], o representacin de Einsenthal y
Cornish-Bowden.
- Si escribimos la ecuacin de Michaelis-Menten en su forma inversa,
obtenemos:
1 1 Km 1
---- = ------------- + ------------- ---------
v Vmax Vmax [S]
y = b + m x
( )
S V
Km
S V
S
v
S V
Km S
v
max max
1
max
1
+ =
+
=
2.1.Representacin de dobles inversos o de Linenweaver-Burk
1/v
1/[S]
1/Vmax
- 1/Km
m =Km/Vmax
o
-Pendiente Km/Vmax
-Corte en el eje-x 1/v =0 -1/Km
-Corte en el eje-y 1/[S] =0 1/Vmax
1/v
1/[S])
La representacin ms utilizada, no es la ms recomendable ya que da
impresiones extremadamente engaosas de los errores experimentales: as para
pequeos valores de v, pequeos errores en la medida de v, conducen a grandes
errores en 1/v, mientras que para valores grandes de v los mismo pequeos
errores en la medida de v conducen a errores apenas apreciables en 1/v.
Si multiplicamos ambos miembros de la ec. de dobles inversos, por [S], obtendremos,
La representacin de [S]/v frente a [S], da una recta:
y = b + m x
- Esta representacin se conoce como representacin de
Hanes, representacin de Woolf o de Hanes-Woolf.
2.2. Representacin de Hanes
| |
| | S
V V
Km
v
S
|
.
|
\
|
+
|
.
|
\
|
=
max
1
max
| |
| | S
S V
Km
V v
|
|
.
|
\
|
+ =
1
max max
1 1
| | | |
max max V
S
V
Km
v
S
+ =
[S]/v
[S]
Km/Vmax
- Km
m = tgo = 1/Vmax
o
Pendiente = 1/Vmax
corta en el eje [S]/v en un punto = Km/Vmax,
corta en el eje [S] en un punto = - Km
* En esta representacin, como puede verse en la siguiente figura, los errores en [S]/v
son un reflejo mucho ms fiel de los errores cometidos al medir el valor de v. Por este
motivo, la representacin de Hanes es preferible a otras linealizaciones de la ecuacin
de Michaelis-Menten.
[S]/v
[S]
Cmo afectarn los errores de medida de la velocidad de
reaccin en esta representacin?
Tarea 1 Imaginemos que estamos estudiando una reaccin S
P catalizada por una enzima E, y que obtenemos los siguientes
resultados:
[S] (mmol L
-1
) v
o
(mol L
-1
min
-1
)
0,30 0,57
0,50 0,85
0,75 1,18
1,50 1,82
3,00 2,50
7,50 3,23
A partir de estos datos calcular Vmax y Km mediante la
representacin de Hanes.
Si multiplicamos ambos miembros de la ecuacin de inversos por v * Vmax
obtenemos,
Vmax = v + (Km v)/[S]
y reordenando
y = b - m x
Esta representacin se conoce como representacin
de Eadie-Hofstee
2.3.Representacin de Eadie-Hofstee.
| | S
v
Km V v = max
| |
max
1
max max
1 1
vV
S V
Km
V v
|
|
.
|
\
|
+ =
La representacin de v frente a v/[S] nos da una recta de:
- pendiente = -Km
- corte en el eje v = Vmax
- corte en el eje v/[S] = Vmax/Km
v
v/[S]
Vmax
Vmax/Km
m = tgo = -Km
o
Esta representacin en general proporciona resultados
realmente buenos, ya que v aparece en ambas coordenadas
como factor multiplicativo, por lo que los errores cometidos en la
medida de v, harn que la curva se acerque o aleje del origen en
lugar de hacerlo paralelamente al eje de ordenadas.
v/[S]
v
Esta representacin, contrariamente a la
de dobles inversos que hace aparecer
como buenos malos resultados, hace
aparecer como malos, buenos resultados,
dificultando grandemente el ocultamiento
de puntos que se desven de la recta.
Aspectos Positivos
Aspectos Negativos
Por lo que esta representacin es la ms
adecuada para el estudio de comportamientos
que se desven del modelo de Michaelis-Menten.
Tarea 2 Imaginemos que estamos estudiando una reaccin S
P catalizada por una enzima E, y que obtenemos los siguientes
resultados:
[S] (mmol L
-1
) v
o
(mol L
-1
min
-1
)
0,30 0,57
0,50 0,85
0,75 1,18
1,50 1,82
3,00 2,50
7,50 3,23
A partir de estos datos calcular Vmax y Km mediante la
representacin de Eadie-Hofstee.
Independientemente, en 1974:
- J. Jimnez Vargas y J.M. Macarulla. Fisicoqumica Fisiolgica,
Interamericana (4 Edicin), Madrid, (1974)
- R. Eisenthal y A. Cornish-Bowden. Biochem J., 139, 715-720,
(1974)
* Publicaron un procedimiento, totalmente diferente a los
anteriores, para la obtencin de Vmax y Km, conocido como
representacin lineal directa.
2.4.Representacin lineal directa o representacin de Einsenthal
y Cornish-Bowden
- La ecuacin de M y M podemos transformarla en la ecuacin
cannica de una recta en la que tratamos a Vmax y Km como
variables, y a [S] y v como constantes,
Dividiendo por v(S)
Reordenando,
1
max
=
+
S
Km
v
V
Si r es la recta que pasa por los puntos (a, 0) y (0,b), la ecuacin la podemos escribir
| |
| |
| | ( ) | |
| | v
V
S
Km
S V S Km v
S Km
S V
v
max
1
max
max
= +
= +
+
=
Si el primer par de valores observados de v y [S] son v
1
y [S
1
] y
representamos la recta que definen:
Km
Vmax
v1
-S1
Si tomamos ahora un segundo par de valores observados:
v2 y (S2), ....
Km
Vmax
v1
-S1 -S2
v2
Y luego un tercer par: v3 y (S3), ....
- Como podemos observar, las distintas rectas se cortan,
intersecan, en un punto, comn a todas ellas, de coordenadas
(Km, Vmax).
Km
Vmax
v1
-S1 -S2
v2
-S3
v3
(Km, Vmax)
NOTA: Experimentalmente, de manera general, no obtendremos
un punto, si no un entorno de puntos, y la media de las
coordenadas de estos puntos nos dar el valor medio de Km y
Vmax con sus correspondientes desviaciones estndar.
Km
Vmax
v1
-S1 -S2
v2
-S3
v3
(Km, Vmax)
- El nmero mximo de puntos de corte vendr dado por: [n(n-1)]/2,
donde n es el nmero de rectas.
Tarea 3. Suponga que estamos estudiando una enzima E que
cataliza la reaccin S P, y que obtenemos los siguientes datos
experimentales:
Concentracin inicial Concentracin de producto (mol L
-1
)
de sustrato (mmol L
-1
) a distintos tiempos (t = min)
t=0 t=1 t=2 t=3 t=4
5,0 0 150 300 450 600
6,5 0 180 360 540 720
10,0 0 235 470 705 940
20,0 0 325 650 975 1300
40,0 0 410 820 1230 1640
Calcular Km y Vmax utilizando todos los procedimientos
estudiados.
Resumen
Estudiada la ecuacin de Michelis-Menten de acuerdo con el orden de reaccin podemos
encontrar las siguientes circunstancias-
a) A concentraciones saturantes de substrato nos encontramos en el orden cero de reaccin
La comparacin de actividades enzimticas en ordn cero de reaccin puede servir para
comparar cantidades de una misma enzima en diferentes circunstancias metablicas.
b) A concentraciones de substrato menores que un dcimo de la constante de Michaelis, nos
encontramos en orden uno de reaccin.
c) A concentraciones de substrato del orden de la constante de Michaelis es posible obtener una
ecuacin a partir de la ecuacin integrada de Michaelis-Menten permite determinar
graficamente los parmetros dinticos Vmax y Km estudiando la curva del avance de una
reaccin con respecto al tiempo
La ecuacin de Michaelis-Menten es una cnica, hiprbola que pasa por el centro de coordenadas
v:S, cuya asintota paralela al eje de las abcisas representa la velocidad mxima.
Diferentes transformaciones algebricas permiten la linealizacin de la ecuacin de M-M para
una determinacin ms fcil de los parmetros Vmax y Km.
Entre estas se encuentran:
Representacin de dobles inversos o de Linenweaver-Burk.
Representacin de Hanes
Representacin de Eadie-Hofstee
Representacin lineal directa o representacin de Einsenthal y Cornish-Bowden
También podría gustarte
- Problemas resueltos de electromagnetismo. Volumen I: ElectrostáticaDe EverandProblemas resueltos de electromagnetismo. Volumen I: ElectrostáticaAún no hay calificaciones
- Tema 012Documento27 páginasTema 012Franz Tucta HuillcaAún no hay calificaciones
- 1CLAE ENzimas 16 AbrilDocumento30 páginas1CLAE ENzimas 16 AbrilKelletCadilloBarruetoAún no hay calificaciones
- Transformación lineal directa: Aplicaciones prácticas y técnicas en visión por computadora.De EverandTransformación lineal directa: Aplicaciones prácticas y técnicas en visión por computadora.Aún no hay calificaciones
- Diapositivas de Métodos Matemáticos para Calcular Parámetros CinéticosDocumento30 páginasDiapositivas de Métodos Matemáticos para Calcular Parámetros CinéticosMirella Corina Vargas GòmezAún no hay calificaciones
- Modelos Cinetica EnzimaticaDocumento4 páginasModelos Cinetica EnzimaticaDui Dui Dui DuiAún no hay calificaciones
- Ec MichaelisDocumento10 páginasEc MichaelisJeka JekatronikAún no hay calificaciones
- Cinética de Las Reacciones para Sistemas BiológicosDocumento41 páginasCinética de Las Reacciones para Sistemas BiológicosJessy HernándezAún no hay calificaciones
- Representacion Eadie-HofsteeDocumento11 páginasRepresentacion Eadie-HofsteeMarifer RiveraAún no hay calificaciones
- Ingenieria de Reacciones Enzimàticas: Desarrollo de Expresiones Cinèticas.Documento21 páginasIngenieria de Reacciones Enzimàticas: Desarrollo de Expresiones Cinèticas.Balam ToscanoAún no hay calificaciones
- Clase 10Documento37 páginasClase 10Kade CadeAún no hay calificaciones
- Ecuaciones de Michaelis PDFDocumento2 páginasEcuaciones de Michaelis PDFAmaury Daniel CortesAún no hay calificaciones
- 2da Practica Bioingeniería 2. Cinetica Enzimatica II-2018Documento5 páginas2da Practica Bioingeniería 2. Cinetica Enzimatica II-2018Andrés Felipe Aristizabal MonterrozaAún no hay calificaciones
- Las Enzimas Clase-1Documento37 páginasLas Enzimas Clase-1Kate ́s FilmAún no hay calificaciones
- Bioquimica WordDocumento3 páginasBioquimica WordDaniela Valencia LópezAún no hay calificaciones
- Clase 2 Gráficos de Control EnzimáticoDocumento31 páginasClase 2 Gráficos de Control EnzimáticoHarold Jose100% (1)
- Guia de Vectores 1ro MedioDocumento6 páginasGuia de Vectores 1ro MedioMauro GiaveriniAún no hay calificaciones
- Determinaciòn de Los Parámetros Cinéticos de La EnzimaDocumento30 páginasDeterminaciòn de Los Parámetros Cinéticos de La EnzimaLeon VásquezAún no hay calificaciones
- Apuntesparte5 10178Documento38 páginasApuntesparte5 10178Josimar Pasquel100% (1)
- Ejercicios de Vectores, Mru, MruaDocumento13 páginasEjercicios de Vectores, Mru, MruaBayron Leandro Rosero Huertas100% (1)
- Tutorial Calculos de KM y VmaxDocumento3 páginasTutorial Calculos de KM y VmaxFrancisca Fuentes100% (1)
- Met de Separacion de Variables EDPDocumento90 páginasMet de Separacion de Variables EDPbleizherAún no hay calificaciones
- Reporte 3 Campos y OndasDocumento16 páginasReporte 3 Campos y OndasFabricio LopezAún no hay calificaciones
- EDocumento1 páginaEGuadalupe GAún no hay calificaciones
- Cinetica EnzimáticaDocumento38 páginasCinetica EnzimáticaFernanda Castillo ÜAún no hay calificaciones
- Modelo Cinético de MichaelisDocumento7 páginasModelo Cinético de MichaelisEdward Jorge Matias AtenciaAún no hay calificaciones
- Práctica Métodos Experimentales de Parámetros CinéticosDocumento4 páginasPráctica Métodos Experimentales de Parámetros CinéticosMarianAún no hay calificaciones
- Reporte Conservación de La Energía MecánicaDocumento7 páginasReporte Conservación de La Energía MecánicaSara Quijano BustamanteAún no hay calificaciones
- Metodos Graficos para La Determinacion DDocumento2 páginasMetodos Graficos para La Determinacion DRosario SaldivarAún no hay calificaciones
- Ecuación Diferencial de LegendreDocumento16 páginasEcuación Diferencial de LegendreJuan M. Soubran100% (1)
- Reduccion Al Eje Mayor.Documento2 páginasReduccion Al Eje Mayor.Edgar Alfredo Salazar CrucesAún no hay calificaciones
- Algoritmo de Bellman-FordDocumento3 páginasAlgoritmo de Bellman-FordDavid MurilloAún no hay calificaciones
- CAPITULO - 5 - Cinètica EnziODocumento125 páginasCAPITULO - 5 - Cinètica EnziOcamilo calizayaAún no hay calificaciones
- Guia VECTORES 2do MedDocumento7 páginasGuia VECTORES 2do MedMauro GiaveriniAún no hay calificaciones
- Clase06 MAT MED Funciones Polinomicas2 Ajuste de Curvas 28 03 2019 2Documento31 páginasClase06 MAT MED Funciones Polinomicas2 Ajuste de Curvas 28 03 2019 2Cristóbal Arenas ZuñigaAún no hay calificaciones
- Algoritmo de Bellman-FordDocumento3 páginasAlgoritmo de Bellman-FordRobertico35Aún no hay calificaciones
- Modelo Matematico Cable CorrugadoDocumento15 páginasModelo Matematico Cable CorrugadoCarlos ruaAún no hay calificaciones
- infomeLINEAS EQUIPOTENCIALESDocumento9 páginasinfomeLINEAS EQUIPOTENCIALESdaniel santosAún no hay calificaciones
- Informe de Lineas de CorrienteDocumento19 páginasInforme de Lineas de CorrienteAntony More VillegasAún no hay calificaciones
- Espacio Vectorial ACTUALIZADO (Autoguardado)Documento45 páginasEspacio Vectorial ACTUALIZADO (Autoguardado)Leonardo CamposAún no hay calificaciones
- Deducción Ecuación Michaelis MentenDocumento11 páginasDeducción Ecuación Michaelis Mententere ramirezAún no hay calificaciones
- Informe #3Documento14 páginasInforme #3Sebastian GuarinAún no hay calificaciones
- Ecuacion de La RectaDocumento20 páginasEcuacion de La Rectapesito_100Aún no hay calificaciones
- Vector EsDocumento39 páginasVector Esjhanuni24Aún no hay calificaciones
- Lectura 2 Cinética Enzimática Michaellis-Menten y Alostérico.Documento8 páginasLectura 2 Cinética Enzimática Michaellis-Menten y Alostérico.Chucho chuAún no hay calificaciones
- P3 S KM VmaxDocumento2 páginasP3 S KM VmaxEdson DiazAún no hay calificaciones
- Fisica EisbergDocumento682 páginasFisica EisbergMateo Annavalaina100% (1)
- Regresion Sesgada.Documento30 páginasRegresion Sesgada.AmIn20122Aún no hay calificaciones
- Mate Matic AsDocumento10 páginasMate Matic AsJEISON AMILKAR SOLANO LOPEZAún no hay calificaciones
- CinemáticaDocumento46 páginasCinemáticaJosé AntonioAún no hay calificaciones
- Operaciones Con VectoresDocumento12 páginasOperaciones Con VectoresRichard BuitronAún no hay calificaciones
- Método GraficoDocumento14 páginasMétodo GraficogregorioAún no hay calificaciones
- Resolución de La Ecuación de Laplace Por Medio de Iteración Numérica en MatlabDocumento10 páginasResolución de La Ecuación de Laplace Por Medio de Iteración Numérica en MatlabGerardoDuranAún no hay calificaciones
- Vectores en R2 y R3Documento42 páginasVectores en R2 y R3PrimitivaAún no hay calificaciones
- NM4 VectoresDocumento24 páginasNM4 VectoresEdicson VelasquezAún no hay calificaciones
- 34 ClotoideDocumento10 páginas34 ClotoidefgaloppoAún no hay calificaciones
- Método GraficojjjjjjjjjjDocumento13 páginasMétodo GraficojjjjjjjjjjgregorioAún no hay calificaciones
- Informe Minimos CuadradosDocumento11 páginasInforme Minimos CuadradosSvetllana DuranAún no hay calificaciones
- Trigonometria IntegralDocumento103 páginasTrigonometria IntegralAnonymous 7za15o00% (1)
- Tarea U333.fullDocumento10 páginasTarea U333.fullGeorge Contreras HernandezAún no hay calificaciones
- Parábola, Elipse e HipérbolaDocumento10 páginasParábola, Elipse e HipérbolaShodanAún no hay calificaciones
- CoordenadasDocumento21 páginasCoordenadasPavel Vilca HuaripaucarAún no hay calificaciones
- Evaluación Tres REPETIDA MAT315-SOLUCIONDocumento4 páginasEvaluación Tres REPETIDA MAT315-SOLUCIONIwjshsAún no hay calificaciones
- Informe de Caminos 004 y 005 Perfil Longitudinal y Los Cálculos de Cotas en Curvas Verticales, Con Corrección de PendientesDocumento13 páginasInforme de Caminos 004 y 005 Perfil Longitudinal y Los Cálculos de Cotas en Curvas Verticales, Con Corrección de PendientesLenin Monago TarazonaAún no hay calificaciones
- Principios de Geometría Analítica y Algebra LinealDocumento45 páginasPrincipios de Geometría Analítica y Algebra LinealAna Maria QuinteroAún no hay calificaciones
- Act 1 - 9.3.1Documento1 páginaAct 1 - 9.3.1felixAún no hay calificaciones
- Solucionario Calculo de Varias Variables 5Documento2 páginasSolucionario Calculo de Varias Variables 5miguel carlosAún no hay calificaciones
- Clase4. Alineamiento Horizontal3Documento18 páginasClase4. Alineamiento Horizontal3Arles Alejandro Panza RamosAún no hay calificaciones
- Geodesia-Semana 3 - Elementos de La Esfera Celeste-2023Documento27 páginasGeodesia-Semana 3 - Elementos de La Esfera Celeste-2023JEAN PIERRE STEVEN HERNAN FLORES CHIPANAAún no hay calificaciones
- Monografia Topografia CoordenadasDocumento32 páginasMonografia Topografia CoordenadasYeltsito DeriamAún no hay calificaciones
- CI1, Aplicaciones de La Derivada 1, CORREGIDO PDFDocumento5 páginasCI1, Aplicaciones de La Derivada 1, CORREGIDO PDFJulio Fernando García VicenteAún no hay calificaciones
- Historia de La ElipseDocumento17 páginasHistoria de La ElipseHenry Jhoel Suero Ureña100% (2)
- Mgan1 U3 A1 MalgDocumento7 páginasMgan1 U3 A1 MalgMayra Lugo GarciaAún no hay calificaciones
- S12.s2 - Resolver EjerciciosDocumento2 páginasS12.s2 - Resolver EjerciciosiBwave UserAún no hay calificaciones
- Modulo 1. Geometria Analitica NEW 1 PDFDocumento12 páginasModulo 1. Geometria Analitica NEW 1 PDFchristopher jimenezAún no hay calificaciones
- EJERCICIOS DE LONGITUD DE ARCO Y SECTOR CIRCULAR 2da ClaseDocumento3 páginasEJERCICIOS DE LONGITUD DE ARCO Y SECTOR CIRCULAR 2da Clasejavier cordova floresAún no hay calificaciones
- Plano CartesianoDocumento4 páginasPlano CartesianoNovoa Photoshop TutorialAún no hay calificaciones
- Guía Funcion Cuadratica N°3Documento5 páginasGuía Funcion Cuadratica N°3Loreto Rojas OvalleAún no hay calificaciones
- Universidad Nacional Mayor de San Marcos: Curso: CDocumento4 páginasUniversidad Nacional Mayor de San Marcos: Curso: CAndric Adriano Apaza MartinezAún no hay calificaciones
- Interpretación Géometrica de Las Derivadas Parciales de Una Funcion de Dos VariablesDocumento2 páginasInterpretación Géometrica de Las Derivadas Parciales de Una Funcion de Dos VariablesMiguelito Pa Q MasAún no hay calificaciones
- Planos TridimensionalesDocumento18 páginasPlanos TridimensionalesMartin Aranda TorresAún no hay calificaciones
- S09.s1 - Longitud de Arco - PPT UTPDocumento19 páginasS09.s1 - Longitud de Arco - PPT UTPJuan Pablo Ramos UcharicoAún no hay calificaciones
- Teoria Electromegnetica Juan Carlos GranadaDocumento323 páginasTeoria Electromegnetica Juan Carlos GranadaErika ErikaAún no hay calificaciones
- Informe N°02Documento18 páginasInforme N°02SC IngenierosAún no hay calificaciones
- Informe T4Documento16 páginasInforme T4Emi Carito Ugaz SuarezAún no hay calificaciones
- Guia 4 - Angulos Trigonométricos. 10° Grado. 2021.Documento7 páginasGuia 4 - Angulos Trigonométricos. 10° Grado. 2021.Andres UrregoAún no hay calificaciones
- S14.s1 HipérbolaDocumento28 páginasS14.s1 HipérbolaGiancarlo BendezuAún no hay calificaciones
- Módulo Teórico Práctico 6to Matemática AplicadaDocumento48 páginasMódulo Teórico Práctico 6to Matemática AplicadaAriadna ForigoAún no hay calificaciones