Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Informe 2 Oxigeno y Peroxido
Cargado por
Franz CaliDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Informe 2 Oxigeno y Peroxido
Cargado por
Franz CaliCopyright:
Formatos disponibles
UNVERSIDAD NACIONAL DEL CALLAO
FACULTAD: Ingeniera Qumica
LABORATORIO DE QUIMICA INORGANICA
TEMA: Oxigeno y Peroxidos Obtencion y Propiedades
Quimica
PROFESORA: BENIGNO HILARIO ROMEO
INTEGRANTES:
o Acua Huyhua, Gerson
o Rimarachin Lpez Adriana
o Calisaya Choque, Franz
CICLO
2014 - B
Bellavista - Callao
Universidad Nacional del Callao
Facultad de Ingeniera Qumica
I.-INTRODUCCN
PEROXIDO Y
OXIGENO
El OXIGENO, es un elemento qumico de nmero atmico 8 y smbolo O. En su forma
molecular ms frecuente, O2, es un gas a temperatura ambiente. Representa
aproximadamente el 20,9% en volumen de la composicin de la atmsfera terrestre.
Es uno de los elementos ms importantes de la qumica orgnica y participa de forma
muy importante en el ciclo energtico de los seres vivos, esencial en la respiracin
celular de los organismos aerbicos. Es un gas incoloro, inodoro (sin olor) e inspido.
Existe una forma molecular formada por tres tomos de oxgeno, O3, denominada
ozono cuya presencia en la atmsfera protege la Tierra de la incidencia de radiacin
ultravioleta procedente del Sol.Un tomo de oxgeno combinado con dos de hidrgeno
forman una molcula de agua.
El PEROXIDO DE HIDROGENO, (H2O2), tambin conocido como agua oxigenada,
dioxogen o dioxidano, es un compuesto qumico con caractersticas de un lquido
altamente polar, fuertemente enlazado con el hidrgeno tal como el agua, que por lo
general se presenta como un lquido ligeramente ms viscoso que sta. Es conocido
por ser un poderoso oxidante.
II.-OBJETIVOS
Objetivo general:
Reconocer las propiedades qumicas de perxidos y oxigeno asi
como su obtencin
Objetivo especfico:
Reconocer si tanto el perxido de sodio como el xido de sodio pueden formar
una base
Obtener la correcta formacin del Perxido de hidrgeno (H2O2) sometido a una
mezcla frigorfica ya que a partir de esta obtencin realizaremos las reacciones
de identificacin, oxidacin y reduccin posteriormente.
Aprender a diferenciar el comportamiento del Perxido de hidrgeno (H2O2) ya
sea cuando actu como medio o como agente oxidante
III.- ESQUEMA TEORICO
~2~
Universidad Nacional del Callao
Facultad de Ingeniera Qumica
PEROXIDO Y
OXIGENO
IV.-MATERIALES Y REACTIVOS
~3~
Universidad Nacional del Callao
Facultad de Ingeniera Qumica
INSTRUMENTOS Y MATERIALES
Pipeta
PEROXIDO Y
OXIGENO
gradilla
Tubos de ensayo
Piseta
01 Pinza
Vaso precipitado
mechero
REACTIVOS :
~4~
Universidad Nacional del Callao
Facultad de Ingeniera Qumica
KClO3 y Mn O2 (dixido de manganeso)
(cloruro de manganeso)
K 2 Cr 2 O7
H 2 S O4
sulfrico)
azufre(S)
V.-PROCEDIMIENTO EXPERIMENTAL
1. OBTENCION DEL OXIGENO
En un tubo de ensayo colocar
PEROXIDO
Y
Cl2
Mn
OXIGENO
KCl O3(s)
~5~
Mn O2(s)
(Acido
Universidad Nacional del Callao
Facultad de Ingeniera Qumica
PEROXIDO Y
Calentar el tubo de ensayo
OXIGENO
En otro tubo de ensayo con agua conectar con una manguera en
un recipiente
con agua hasta desocupar todo el agua
Quedando en el tubo oxgeno y proceder a tapar
KC lO3 (s) + Mn O 2(s) O2 (g) + KC l(s )
2. PROPIEDADES DEL OXIGENO
2.1
Se calienta azufre hasta que empieza a arder.
Luego se agrega al envase que contiene oxgeno y se vuelve a tapar con
el tapn, formndose el
S O2(g)
Luego agregamos agua destilada y se forma
H 2 S O3(ac )
Para demostrar que se forma ese acido ponemos un papel tornasol
~6~
Universidad Nacional del Callao
Facultad de Ingeniera Qumica
PEROXIDO Y
OXIGENO
O2 (g )+ S(S ) S O2(g)
S O2(g) + H 2 O(l ) H 2 S O3(ac)
OBSERVACIONES:
Se observa que al aadirle papel tornasol al acido sulfuroso toma un color naranja
2.2
Se agrega a un tubo de ensayo cloruro de manganeso II
Luego se aade al tubo de ensayo que contiene oxigeno
Luego se agrega oxgeno, formndose el bixido de manganeso.
MnC l 2 (ac ) +O2 ( g) Mn O(s) +Cl 2
OBSERVACIONES:
El precipitado de bixido de manganeso es de color marrn.
Pero en el experimento realizado tomo un color blanco que pudo haber sucedido
MnC l 2 (ac )
probablemente por el
estaba pasado
~7~
Universidad Nacional del Callao
Facultad de Ingeniera Qumica
PEROXIDO Y
OXIGENO
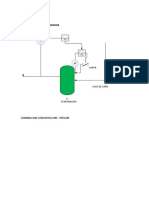
3. OBTENCION DE PEROXIDO DE HIDROGENO (H2O2)
3.1 En un vaso de precipitado colocamos una pequea cantidad de cido sulfrico
(H2SO4 ) y adems oxido de bario (BaO2 ) luego disolvemos.
3.2 Posteriormente introducimos por 20 minutos dicho vaso a un depsito que contiene
una especie de mezcla frigorfica.
Reaccin:
BaO2 + H2SO4 --------- BaSO4 + H2O2
Observacin:
Al realizar el proceso de obtencin del perxido de hidrogeno observamos la formacin
de precipitado color blanco que evidenciara la presencia del sulfato de bario(BaSO4) y
tambin la formacin de una solucin transparente por encima que vendra a ser el
producto requerido(H2O2).
La reaccin de formacin del perxido de hidrogeno es exotrmica por ende
necesitamos someterla a una mezcla frigorfica; mezcla que puede ser de hielo o un
conjunto de sales.
~8~
Universidad Nacional del Callao
Facultad de Ingeniera Qumica
PEROXIDO Y
OXIGENO
H 2 O2
BaSO 4
4. IDENTIFICACION DEL PEROXIDO DE HIDROGENO.
1. En tubo de ensayo preparamos una solucin mezclando los siguientes
reactantes:
1ml H2O2 a un 3%,
1ml de H2SO4 de concentracin 2 N
Gotas de ter.
Gotas de K2Cr2O7
Reaccin:
K2Cr2O7 (ac) + H2
O2
(l) + H2SO4 (ac) K2SO4 (ac + 2CrO2 (ac) + 2 H2O (ac) +
3/2O2 (ac)
Observacin:
Al realizar el procedimiento indicado observamos inmediatamente la formacin de un
anillo color azul que evidencia la formacin de perxido de cromo, notamos tambin
que debido a esta formacin el cromo inicialmente se reduce actuando el perxido
como reductor.
~9~
Universidad Nacional del Callao
Facultad de Ingeniera Qumica
PEROXIDO
Al final de la reaccin el perxido de cromo queda como cido crmico
tornndose Y
la
OXIGENO
solucin un color verduzco.
5. PROPIEDADES OXIDANTES DE PEROXIDO DE HIDROGENO.
1. Aadir 1 ml. de la solucin de KI al y 1 ml. de H2SO4, 1 ml de solucin de
H2O2 al 3%.
Reaccin:
KI (ac) + H2SO4 (ac) + H2O2 (l) K2SO4 (ac) + I2 (ac) + H2O (ac)
Observacin:
Al mezclar inicialmente solucin de KI, de color caracterstico amarillo
transparente, con H2SO4, observamos que ste cido acta como medio y no
debe oxidar al KI,es decir al juntar estas dos soluciones el KI no debe cambiar
de color considerablemente ,en nuestra practica de laboratorio el H2SO4 se
hallaba muy concentrado por lo que oxidaba al yoduro para ello tuvimos que
diluir el cido con una cantidad considerable de agua destilada. Debido a que el
cido acta como medio el perxido de hidrogeno acta como agente oxidante
as tambin el yoduro pasa a ser el agente reductor.
~ 10 ~
Universidad Nacional del Callao
Facultad de Ingeniera Qumica
PEROXIDO Y
OXIGENO
Efectuada la reaccin con todos los solventes observamos finalmente la
formacin de dos fases en el tubo de ensayo, por el color caracterstico del yodo
afirmamos la presencia de l en la capa inferior.
6. PROPIEDADES REDUCTORA DEL H2O2
6.1
En un tubo de ensayo colocamos permanganato de potasio KMnO 4 (ac) (color
violeta) con una concentracin moderada y lo combinamos con cido sulfrico
diluido (H2SO4 (dil)).
A esa mezcla le echamos el perxido de hidrogeno (H 2O2 (l)).
2 KMn O4 + H 2 O2+ H 2 S O4 5 O2 +8 H 2 O+ K 2 S O4 +2 MnS O4
~ 11 ~
Universidad Nacional del Callao
Facultad de Ingeniera Qumica
PEROXIDO Y
OXIGENO
OBSERVACION:
observamos la decoloracin que sufre el color violeta por la reduccin de
manganeso +7(Mn+7) a manganeso +2 (Mn+2).
6.2
En un tubo de ensayo colocamos perxido de hidrogeno (H 2O2 (l)) y le adicionamos
el medio el cual es hidrxido de amonio (NH 4OH (dil)).
Despus le adicionamos aproximadamente 0.1g de xido de mercurio (HgO).
HgO+ H 2 O2 Hg+ H 2 O+O2
OBSERVACION:
Observamos que la reaccin libera un gas el cual es
Hg (g).
7. DESCOMPOSICION DEL Na2O2
7.1
En un tubo colocamos Na2O2 y le adicionamos agua.
A esa mezcla le adicionamos fenolftalena con el cual la mezcla tomo una
coloracin
N a2 O 2 (s) +2 H 2 O (l ) 2 NaOH + H 2 O2
~ 12 ~
Universidad Nacional del Callao
Facultad de Ingeniera Qumica
PEROXIDO Y
OXIGENO
OBSERVACION:
Observamos que al adicionamos
fenolftalena con el cual la mezcla
tomo una
coloracin rojo
grosella(rosado oscuro) el cual es
el color caracterstico de una base.
Como pudimos observar en medio
acuoso el perxido de sodio
tambin forma una base
7.2
En un tubo colocamos Na2O2 y seguido lo calentamos con el mechero
Para notar el desprendimiento de O 2 (g) acercamos a la boca del tubo una astilla
incandescente.
Despus de obtendr oxido de sodio y despus de unos minutos de que enfri
echamos agua seguidamente le adicionamos 2 gotas de fenolftalena con el cual
toma una coloracin rojo grosella(rosado oscuro) que es color caracterstico de
una base
2 N a 2 O2(s ) 2 N a 2 O(s) +O2
N a2 O(s) +2 H 2 O(l) 2 NaOH + H 2 O
~ 13 ~
Universidad Nacional del Callao
Facultad de Ingeniera Qumica
OBSERVACION:
PEROXIDO Y
OXIGENO
Observamos
que
mientras el fuego en la
astilla se intensifique
seguir saliendo O2 (g)
cuando
culmine
la
emisin de O2 (g) el tubo
de ensayo se deja
enfriar por un tiempo
prolongado.
VI.-CONCLUSIONES
En efecto se concluy que al tomar una muestra de Na 2O2 y al agregarle agua
nos da una base y esto comprueba agregndole a la solucin la fenolftalena
que nos brinda un color rojo grosella caracterstico de una base. Los mismo
sucede cuando se toma una muestra de Na 2O2 y lo calentamos y se notara un
desprendimiento de Oxigeno con un palito de fsforo y nos quedara Na 2O que
al agregarle agua efectivamente tambin nos dar una base y se con prueba con
la fenolftalena por lo tanto ambos forman base en solucin acuosa.
Es necesario someter a una mezcla frigorfica ya sea de hielo o un conjunto de
sales la reaccin que da lugar a la formacin del Perxido de hidrgeno (H2O2)
debido a que esta reaccin es exotrmica.
Es necesario utilizar cido Sulfrico (H2SO4) poco concentrado para que el
proceso de oxidacin del Perxido de hidrgeno (H2O2) se lleve a cabo o de lo
contrario ste acido actuara como agente reductor desplazando al perxido
~ 14 ~
Universidad Nacional del Callao
Facultad de Ingeniera Qumica
PEROXIDO Y
OXIGENO
VII.-RECOMENDACIONES
En el caso de reaccin y oxidacin del Perxido de hidrgeno (H2O2) no es
necesario utilizar las cantidades exactas que nos indica la gua del laboratorio,
ya que con una mnima cantidad de ellas es suficiente para que se lleven a
cabo.
Mantener tapado el tubo de ensayo que contiene oxigeno
Al realizar la reaccin de identificacin del Perxido de hidrgeno (H2O2) al
momento de aadir ter, utilizar con suma precaucin debido a que si llega a
darse una exposicin muy prolongada de este compuesto puede ocasionar
daos severos a la piel, al sistema respiratorio u otros.
Es recomendable que el medio no sea tan concentrado sino diluido para que as
el medio no participe en la reaccin como por ejemplo e la experiencia que se
utiliza al cido sulfrico si est muy concentrado va a ser muy oxidante y nos
dar un color rojo, esto es porque participara el medio, caso que no debe ser
as. El color que debe ser es amarillo claro esto nos indicara que es menos
concentrado
VIII.-BIBLIOGRAFIA
QUIMICA ELEMENTAL MODERNA INORGANICA
Celsi Iacobucci
Editorial Kapelusz
QUIMICA ANALITICA CUALITATIVA
Vogel Arthur
~ 15 ~
Universidad Nacional del Callao
Facultad de Ingeniera Qumica
James huheey Quimca inorgnica
~ 16 ~
PEROXIDO Y
OXIGENO
También podría gustarte
- Inorganica Informe N6Documento10 páginasInorganica Informe N6erichescobar1230% (2)
- Compuestos Oxigenados Del Nitrógeno (Parte Ii)Documento8 páginasCompuestos Oxigenados Del Nitrógeno (Parte Ii)Sol RubíAún no hay calificaciones
- Compuestos Oxigenados Del NitrogenoDocumento10 páginasCompuestos Oxigenados Del Nitrogenooasismania100% (1)
- Practica N°2 OxigenoDocumento20 páginasPractica N°2 OxigenoRayluz De la cruzAún no hay calificaciones
- Informe Práctica 10 Elementos Del Grupo IA y IIADocumento12 páginasInforme Práctica 10 Elementos Del Grupo IA y IIABrian Williams0% (1)
- Informe Practica 3 Oxigeno Peroxidos Oxidos AguaDocumento12 páginasInforme Practica 3 Oxigeno Peroxidos Oxidos AguaWashington Quisperima Galdós0% (3)
- G1-Informe N°2 Lab. InorganicaDocumento19 páginasG1-Informe N°2 Lab. InorganicaCAICAY OTOYA LUIS EDUARDOAún no hay calificaciones
- Inorganica Informe N10Documento11 páginasInorganica Informe N10erichescobar123Aún no hay calificaciones
- Informe Practica 5 Compuestos Oxigenados Del AzufreDocumento13 páginasInforme Practica 5 Compuestos Oxigenados Del AzufreWashington Quisperima Galdós100% (2)
- Analisis Elemental II Organica 1Documento22 páginasAnalisis Elemental II Organica 1Meliza Rosi Bravo Castillo0% (1)
- Compuestos Oxigenados Del NitrogenoDocumento12 páginasCompuestos Oxigenados Del Nitrogenoyacqueline huamanAún no hay calificaciones
- Inorg 4Documento9 páginasInorg 4Kevin VizcarraAún no hay calificaciones
- Informe Lab4Documento14 páginasInforme Lab4David Francisco Benites MillanAún no hay calificaciones
- Informe Práctica 10 Elementos Del Grupo IA y IIADocumento12 páginasInforme Práctica 10 Elementos Del Grupo IA y IIApooolcito0% (1)
- Informe 7 Labo InorganicaDocumento4 páginasInforme 7 Labo InorganicaDiego Montenegro100% (1)
- Informe Inorganica Práctica N - 9 Boro y AluminioDocumento11 páginasInforme Inorganica Práctica N - 9 Boro y AluminioPool Icanaque Espinal100% (4)
- # 6 # Quimica Del Metal de Transicion Del CobaltoDocumento11 páginas# 6 # Quimica Del Metal de Transicion Del CobaltoAydee100% (2)
- Compuestos Oxigenados de NitrogenoDocumento5 páginasCompuestos Oxigenados de NitrogenoRut Gutíerrez100% (1)
- Informe de Laboratorio 1 de Química Inorganica UNMSMDocumento8 páginasInforme de Laboratorio 1 de Química Inorganica UNMSMwaldir marcelino100% (1)
- Fosforo Arsenico Antimonio y BismutoDocumento8 páginasFosforo Arsenico Antimonio y BismutoMaria Del CarmenAún no hay calificaciones
- Informe Del Peroxido de HidrogenoDocumento32 páginasInforme Del Peroxido de HidrogenoWill Bermejo100% (1)
- Labo de InorganicaDocumento36 páginasLabo de InorganicaAngel Ulises Reyes NAún no hay calificaciones
- Compuestos Oxigenados Del NitrógenoDocumento4 páginasCompuestos Oxigenados Del NitrógenoDiego MontenegroAún no hay calificaciones
- Informe de Laboratorio N6 Gurpo 8Documento3 páginasInforme de Laboratorio N6 Gurpo 8jaime perezAún no hay calificaciones
- Compuestos Oxigenados de AzufreDocumento6 páginasCompuestos Oxigenados de AzufreLuz Angelica Vera ChavezAún no hay calificaciones
- Informe 6 Compuestos Oxigenados Del AzufreDocumento5 páginasInforme 6 Compuestos Oxigenados Del AzufreRAMOS OLLACHICA MARYORI JENNIFERAún no hay calificaciones
- +hno Cu (NO) + No + H ODocumento3 páginas+hno Cu (NO) + No + H OC'Denisse PalominoAún no hay calificaciones
- Informe Práctica 8 Carbono y SilicioDocumento13 páginasInforme Práctica 8 Carbono y Siliciopooolcito0% (1)
- Informe 12Documento27 páginasInforme 12AnelizAún no hay calificaciones
- Examen Final de Inorganica 2020b Ss Quispe LuyoDocumento6 páginasExamen Final de Inorganica 2020b Ss Quispe LuyoQUISPE LUYO ROSALINDAAún no hay calificaciones
- Quimica Inorganica II: Fosforo, Arsenico, Antimonio y BismutoDocumento9 páginasQuimica Inorganica II: Fosforo, Arsenico, Antimonio y BismutoAngel Bryan Ñahuis OrtizAún no hay calificaciones
- Informe de Ino 5Documento12 páginasInforme de Ino 5Isaac Vilchez CAún no hay calificaciones
- Lab 4 AZUFRE Y SULFUROSDocumento6 páginasLab 4 AZUFRE Y SULFUROSLilibethEspinoza100% (2)
- 10Documento2 páginas10Abi C. AlanyaAún no hay calificaciones
- Reporte N5Documento6 páginasReporte N5Nilton Jesus Curi100% (1)
- Segundo Grupo de CationesDocumento23 páginasSegundo Grupo de CationesAmaro Andres Caso Lloclla38% (8)
- Analisis Elemental 2Documento19 páginasAnalisis Elemental 2Sandra Hilario QAún no hay calificaciones
- Informe Inorganica Practica N 9 Boro y AluminioDocumento10 páginasInforme Inorganica Practica N 9 Boro y Aluminioluis romeroAún no hay calificaciones
- Compuestos Oxigenados Del Azufre - Informe 4Documento11 páginasCompuestos Oxigenados Del Azufre - Informe 4renzo6tello6cribilleAún no hay calificaciones
- 1er Informe de Orga 2Documento18 páginas1er Informe de Orga 2Luz C-HzAún no hay calificaciones
- Informe Práctica 10 Elementos Del Grupo IA y IIADocumento12 páginasInforme Práctica 10 Elementos Del Grupo IA y IIABrian WilliamsAún no hay calificaciones
- Sulfato Sulfito y TiosulfatoDocumento12 páginasSulfato Sulfito y TiosulfatoDavis BernardoAún no hay calificaciones
- Informe 7Documento22 páginasInforme 7Felix Lopez MurgaAún no hay calificaciones
- Lab # 11 CromatografiaDocumento17 páginasLab # 11 CromatografiaJackie AmaoAún no hay calificaciones
- INFORME 7 - Oxigenados Del Nitrogeno 1Documento12 páginasINFORME 7 - Oxigenados Del Nitrogeno 1David Francisco Benites MillanAún no hay calificaciones
- Labo InorganicaDocumento10 páginasLabo InorganicaMaria Del CarmenAún no hay calificaciones
- Informe 2 Química InorgánicaDocumento7 páginasInforme 2 Química InorgánicaClaudiaPalominoZelayaAún no hay calificaciones
- Informe 4 Inorganica Azufre y SulfurosDocumento25 páginasInforme 4 Inorganica Azufre y SulfurosElMaharaja0% (1)
- Precipitacion de SulfurosDocumento4 páginasPrecipitacion de SulfurosBruno Valverde100% (1)
- INFORME 8 - Oxigenados Del Nitrogeno 2Documento12 páginasINFORME 8 - Oxigenados Del Nitrogeno 2David Francisco Benites MillanAún no hay calificaciones
- Marcha Analitica Grupo IIADocumento19 páginasMarcha Analitica Grupo IIAHans Castro VillanoAún no hay calificaciones
- Grupo IIIA de CationesDocumento51 páginasGrupo IIIA de CationesBilly CordovaAún no hay calificaciones
- Historia Quimica OrganometalicaDocumento12 páginasHistoria Quimica OrganometalicaCamila MolanoAún no hay calificaciones
- Vdocuments - MX Compuestos Oxigenados Del AzufreDocumento5 páginasVdocuments - MX Compuestos Oxigenados Del AzufreAngélica MontalvoAún no hay calificaciones
- Reporte #9 Fosforo Arsenico Bismuto y AntimonioDocumento9 páginasReporte #9 Fosforo Arsenico Bismuto y AntimonioALEJANDRA LUCERO MEJ�A CRUZAún no hay calificaciones
- Informe 2 Obtencion Del Oxigeno 2016Documento12 páginasInforme 2 Obtencion Del Oxigeno 2016Felipe Valencia100% (1)
- Informe 3-Oxígeno-Peroxidos-Oxidos-AguaDocumento11 páginasInforme 3-Oxígeno-Peroxidos-Oxidos-AguaNICOL ELIZABETH MILLA CRUZAún no hay calificaciones
- Informe Lab3Documento7 páginasInforme Lab3David Francisco Benites MillanAún no hay calificaciones
- Tiosulfatos TerminadoDocumento17 páginasTiosulfatos TerminadoFranz CaliAún no hay calificaciones
- Laboratorio 8Documento13 páginasLaboratorio 8Ana Cristal Galvez EspinoAún no hay calificaciones
- Clase 1 Labo3Documento9 páginasClase 1 Labo3Franz CaliAún no hay calificaciones
- Elaboracion de FideosDocumento6 páginasElaboracion de FideosYanina AliagaAún no hay calificaciones
- Final MASA I 04vDocumento3 páginasFinal MASA I 04vFranz CaliAún no hay calificaciones
- 2Documento1 página2Franz CaliAún no hay calificaciones
- Laboratorio 3 Reactor TubularDocumento20 páginasLaboratorio 3 Reactor TubularFranz CaliAún no hay calificaciones
- Jabon y MelazaDocumento2 páginasJabon y MelazaFranz CaliAún no hay calificaciones
- Imperio y FactoresDocumento3 páginasImperio y FactoresFranz CaliAún no hay calificaciones
- AlimentosDocumento16 páginasAlimentosFranz CaliAún no hay calificaciones
- BiodieselDocumento16 páginasBiodieselFranz CaliAún no hay calificaciones
- Control Cascada EvaporadorDocumento1 páginaControl Cascada EvaporadorFranz CaliAún no hay calificaciones
- Expo Procesos 2 LopezDocumento5 páginasExpo Procesos 2 LopezFranz CaliAún no hay calificaciones
- Examen Final AutomatizacionDocumento8 páginasExamen Final AutomatizacionFranz CaliAún no hay calificaciones
- Caída de PresiónDocumento3 páginasCaída de PresiónFranz CaliAún no hay calificaciones
- Panificacion TrabajoDocumento25 páginasPanificacion TrabajoFranz CaliAún no hay calificaciones
- BiodieselDocumento16 páginasBiodieselPilar YsabelAún no hay calificaciones
- Fruta ConfitadaDocumento9 páginasFruta ConfitadaFranz CaliAún no hay calificaciones
- Masa Area VariableDocumento17 páginasMasa Area VariableFranz CaliAún no hay calificaciones
- Caracteristicas Del FiaDocumento9 páginasCaracteristicas Del FiaFranz CaliAún no hay calificaciones
- BiodieselDocumento16 páginasBiodieselPilar YsabelAún no hay calificaciones
- Panificacion TrabajoDocumento25 páginasPanificacion TrabajoFranz CaliAún no hay calificaciones
- Problemas de La Unidad I de Sistemas HidraulicosDocumento45 páginasProblemas de La Unidad I de Sistemas HidraulicosPako Chato59% (17)
- CORRIENTEDocumento2 páginasCORRIENTEFranz CaliAún no hay calificaciones
- Tabla Datos Obtenidos en El LaboratorioDocumento1 páginaTabla Datos Obtenidos en El LaboratorioFranz CaliAún no hay calificaciones
- Conserva de PiñaDocumento8 páginasConserva de PiñaFranz CaliAún no hay calificaciones
- Tema 13Documento19 páginasTema 13Franz CaliAún no hay calificaciones
- PROBLMADocumento1 páginaPROBLMAFranz CaliAún no hay calificaciones
- Tarea Académica #1 Manejo de Residuos SólidosDocumento8 páginasTarea Académica #1 Manejo de Residuos SólidosFranz CaliAún no hay calificaciones
- Empresa de Yogurt y FrugosDocumento7 páginasEmpresa de Yogurt y FrugosFranz CaliAún no hay calificaciones
- Volumen MolarDocumento9 páginasVolumen MolarFranz CaliAún no hay calificaciones
- Clase 4 Principios Generales Procesamiento2Documento47 páginasClase 4 Principios Generales Procesamiento2Franz CaliAún no hay calificaciones
- Práctica 2Documento4 páginasPráctica 2Joseph FigueroaAún no hay calificaciones
- Fisica Cuarto ParcialDocumento3 páginasFisica Cuarto ParcialMariví Alvarez0% (1)
- Elementos de ClasificaciónDocumento16 páginasElementos de Clasificaciónkblo2006Aún no hay calificaciones
- Manual Civil 3D 2012Documento92 páginasManual Civil 3D 2012Marvin Jairo López Larrea100% (3)
- Gamas de Reles de Proteccion MiCom PDFDocumento16 páginasGamas de Reles de Proteccion MiCom PDFRicardo Hernandez MoralesAún no hay calificaciones
- Anteproyecto de Metodologia - Tejada Arbildo Daniel AgustinDocumento38 páginasAnteproyecto de Metodologia - Tejada Arbildo Daniel AgustinDaniel A. TejadaAún no hay calificaciones
- Ciclo de RankineDocumento3 páginasCiclo de RankineCarlos R GtzAún no hay calificaciones
- Contenido Del Código ASME y de La Normas Del TEMADocumento2 páginasContenido Del Código ASME y de La Normas Del TEMAFrancisco LarioAún no hay calificaciones
- WARTEGGDocumento8 páginasWARTEGGYohana Carolina GCAún no hay calificaciones
- Metodologia, Instrumentos y Tecnucas de La Geografia 234Documento27 páginasMetodologia, Instrumentos y Tecnucas de La Geografia 234paula foreroAún no hay calificaciones
- AntiderivadaDocumento8 páginasAntiderivadaAlejandro CarrasqueroAún no hay calificaciones
- TERMOMETRIADocumento12 páginasTERMOMETRIAAnonymous LNHGiVz8Aún no hay calificaciones
- 7 Fases de La EntrevistaDocumento6 páginas7 Fases de La EntrevistaEsteban Peralta CalzadillaAún no hay calificaciones
- Jornada HTF Centrales TermosolaresDocumento4 páginasJornada HTF Centrales TermosolaresquetransaAún no hay calificaciones
- Tesis de Relacion de Humedad Con Propiedades Mecanicas de Madera PDFDocumento165 páginasTesis de Relacion de Humedad Con Propiedades Mecanicas de Madera PDFJaime ValdiviaAún no hay calificaciones
- 4c.medidas de Potencia y EnergíaDocumento5 páginas4c.medidas de Potencia y EnergíaroxyAún no hay calificaciones
- Manual de Nomenclatura de Compuestos Organicos de AlcanosDocumento21 páginasManual de Nomenclatura de Compuestos Organicos de AlcanosCristian Cueva SotoAún no hay calificaciones
- La Pelota Saltarina de Meg PDFDocumento2 páginasLa Pelota Saltarina de Meg PDFLaura Gomez AnzaldoAún no hay calificaciones
- Manual Ondas RusasDocumento57 páginasManual Ondas RusasJoel Lopez100% (2)
- 4-Elctri RepasoDocumento15 páginas4-Elctri RepasoCarlos Ignacio Reyes AcostaAún no hay calificaciones
- Práctica 1 - Etapa 1Documento5 páginasPráctica 1 - Etapa 1Isabel LópezAún no hay calificaciones
- Nat 2Documento6 páginasNat 2Anonymous odGJGkiCAún no hay calificaciones
- Volumen MolarDocumento6 páginasVolumen MolarGerard Pajita100% (1)
- Falla Por DesgasteDocumento22 páginasFalla Por DesgasteGiorgio Giacomo Crose GuzmánAún no hay calificaciones
- El Uso de Los Rayos X en La MedicinaDocumento4 páginasEl Uso de Los Rayos X en La MedicinaAdriana Floreano MiñanoAún no hay calificaciones
- ASTROLOGIADocumento19 páginasASTROLOGIAManuela NazAún no hay calificaciones
- Manual Sonda Cloro Etap Ecl3 NDocumento6 páginasManual Sonda Cloro Etap Ecl3 NsdfAún no hay calificaciones
- Contaminación Del Río Pataqueña Por Parte de La Mina ArasiDocumento8 páginasContaminación Del Río Pataqueña Por Parte de La Mina ArasiKevin Alcantara GuaniloAún no hay calificaciones
- PP Modulo 1 (Sabater)Documento93 páginasPP Modulo 1 (Sabater)Osvaldo Esteban MoradoAún no hay calificaciones