Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Propiedades Coligativas
Propiedades Coligativas
Cargado por
russowebmasterDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Propiedades Coligativas
Propiedades Coligativas
Cargado por
russowebmasterCopyright:
Formatos disponibles
UNIVERSIDAD DE PUERTO RICO EN HUMACAO
DEPARTAMENTO DE QU MICA
(http://www.uprh.edu/~quimgen)
QUIM 3004
PROBLEMAS RESUELTOS - PROPIEDADES COLIGATIVAS
Ejemplo #1
PRESIN DE VAPOR DE UNA DISOLUCIN DE COMPONENTES VOLTILES
A 40/C, la presin de vapor del heptano puro es de 92.0 torr y la presin de vapor del octano puro es de
31.0 torr. Considera una disolucin que contiene 1.00 mol de heptano y 4.00 moles de octano. Calcula
la presin de vapor de cada componente y la presin de vapor total sobre la disolucin.
Planteamiento
Primero calculamos la fraccin molar de cada componente en la disolucin lquida. Despus aplicamos
la Ley de Raoult a cada uno de los componentes voltiles. La presin de vapor total es la suma de las
presiones de vapor de los componentes.
Solucin
Primero calculamos la fraccin molar de cada componente en la disolucin lquida.
Aplicando la Ley de Raoult para los componentes voltiles en la solucin:
QUIM 3004 - Propiedades Coligativas
Pgina -2-
Aplicando la Ley de Dalton para los componentes voltiles sobre la solucin:
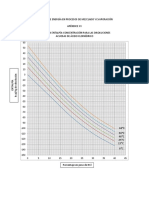
Grfica # 1: Equilibrio Lquido - Vapor para una solucin ideal
Ejemplo #2
COMPOSICIN DEL VAPOR
Calcula las fracciones molares de heptano y de octano en el vapor que estn en equilibrio con
la disolucin en el ejemplo anterior.
Planteamiento
La fraccin molar de un componente en una mezcla gaseosa es igual a la relacin entre su
presin parcial y la presin total. En el ejemplo anterior calculamos la presin parcial de
cada componente en el vapor y el de la presin de vapor total.
QUIM 3004 - Propiedades Coligativas
Pgina -3-
Solucin :
Usando la Ley de Dalton , en el vapor
Ejemplo #3
MASA MOLAR A PARTIR DE UNA PROPIEDAD COLIGATIVA
Una muestra de 1.20 gramos de un compuesto covalente desconocido se disuelve en 50.0
gramos de benceno. La disolucin se congela a 4.92/C. Calcule la masa molar del compuesto.
Planteamiento
Para calcular la masa molar de un compuesto desconocido, hallamos el nmero de moles
representados por 1.20 gramos del compuesto desconocido. Usamos primero los datos de punto
de congelacin para determinar la molalidad de la disolucin. La molalidad relaciona el nmero
de moles de soluto y la masa de disolvente (conocida), de modo que esto nos permite calcular
el nmero de moles del desconocido.
Solucin
El punto de congelacin del benceno puro es de 5.48/C y Kf vale 5.12/C/m.
)Tf = 5.48/C - 4.92/C = 0.56/C
m = molal
M = masa molar
QUIM 3004 - Propiedades Coligativas
Pgina -4-
M soluto
M soluto
M soluto
Ejemplo # 4
Determinacin de una frmula molecular a partir de datos de puntos de congelacin. La
nicotina, extrada a partir de las hojas de tabaco, es un lquido completamente miscible con agua
a temperaturas inferiores a 60/C (a) cul es la molalidad de la disolucin acuosa si comienza
a congelarse a 0.450/C, (b) si la disolucin se obtiene disolviendo 1.921 g de nicotina en 48.92
g de H O, cul debe ser la masa molar de la nicotina? los productos de la combustin indican
que la nicotina contiene 74.03 por ciento de C; 8.70 por ciento de H; 17.27 por ciento de N, por
masa. Cul es la frmula molecular de la nicotina?
2
Solucin:
a)
Se puede calcular la molalidad de la nicotina. Observe que Tf = -0.450/ C y que
)Tf = 0.00/C - [-(0.45/C) = 0.45/C]
b)
Ahora puede utilizarse la definicin de molalidad, pero con una molalidad conocida
(0.242m) y una masa molar del soluto desconocida (M). El nmero de moles de soluto es
simplemente 1.921 g/M.
molalidad =
(1.921 g/M )
(0.04892 Kg agua )
= 0.242 mol
Kg agua
QUIM 3004 - Propiedades Coligativas
Pgina -5-
M=
1.921 g
= 162 g / mol
(0.04892 Kg )(0.242 mol / Kg)
c) Determine la frmula emprica. El resultado que debe obtener es C5H7N. La masa de la
frmula emprica es de 82 u. La masa es exactamente dos veces este valor, 162 u.La
frmula molecular es dos veces C5H7N , es decir C10H14N2. Puede determinar M (la masa
molar exacta utilizando una tabla de pesos atmicos).
Ejemplo # 5
Determinacin de la masa molar a partir de medidas de presin
osmtica
Se prepara una muestra de 50.00 mL de una solucin acuosa que contiene 1.08 g de una
protena del plasma sanguneo, seroalbmina humana. La disolucin tiene una presin
osmtica de 5.85 mmHg a 298 K. Cul es la masa molar de la albmina?
Solucin
Primero es necesario expresar la presin osmtica en atmsferas
Ahora se puede despejar la ecuacin, esto es con el nmero de moles de soluto (n)
representado por la masa del soluto (m) dividida por la masa molar (M) y se obtiene M.
También podría gustarte
- Sedimentación Discontinua - Informe de LabDocumento52 páginasSedimentación Discontinua - Informe de LabValeriaMuñoz100% (1)
- EJERCICIOS UNIDADES DE CONVERSIÓN de BalanceDocumento1 páginaEJERCICIOS UNIDADES DE CONVERSIÓN de BalanceLenin Rojas PerezAún no hay calificaciones
- Informe Técnico: Gestión de PH en El Vino de CalidadDocumento112 páginasInforme Técnico: Gestión de PH en El Vino de CalidadManu San Clemente100% (2)
- Actividades de Repaso de Física y QuímicaDocumento15 páginasActividades de Repaso de Física y QuímicaCarmen María López MartínezAún no hay calificaciones
- Cálculo de DosisDocumento22 páginasCálculo de DosisEdgar Toledo Cáceres100% (7)
- Determinación de Cloruros y CianurosDocumento29 páginasDeterminación de Cloruros y CianurosJorman Iván Barrera VergaraAún no hay calificaciones
- PRACTICA N°1 QMC-131 Carlos Sebastian Rea CallisayaDocumento26 páginasPRACTICA N°1 QMC-131 Carlos Sebastian Rea CallisayaCarlos Sebas Rea CallisayaAún no hay calificaciones
- Guia 2 Pet 120 GrealesDocumento3 páginasGuia 2 Pet 120 GrealesAndres Guisberth ApazaAún no hay calificaciones
- EntropiaDocumento39 páginasEntropiaUbeiden CifuentesAún no hay calificaciones
- Lab 1 de TermodianmicaDocumento8 páginasLab 1 de TermodianmicaMarcos YaviAún no hay calificaciones
- Crioscopia FiquiDocumento14 páginasCrioscopia FiquiElion Vicente Fuentes RuizAún no hay calificaciones
- Informe #2-Dterminaciòn de La Constante de Un Calorímetro - GonzalezDocumento12 páginasInforme #2-Dterminaciòn de La Constante de Un Calorímetro - GonzalezalexandraAún no hay calificaciones
- Balances de Materia y Energía Usando MatlabDocumento4 páginasBalances de Materia y Energía Usando MatlabManuela ArenasAún no hay calificaciones
- Tarea 2 Balance Con Reacción QuímicaDocumento13 páginasTarea 2 Balance Con Reacción QuímicaKevin Borbor SalazarAún no hay calificaciones
- Físico QuímicaDocumento4 páginasFísico QuímicaValeria DelgadoAún no hay calificaciones
- Lab - 3-Analisisdealimentos (1) CENIZAS CORREGIDODocumento8 páginasLab - 3-Analisisdealimentos (1) CENIZAS CORREGIDOCarlita TorricoAún no hay calificaciones
- Cuestionario Física LabDocumento3 páginasCuestionario Física LabLoida Ulpana almazanAún no hay calificaciones
- Trabajo Proyecto TermodinamicaDocumento9 páginasTrabajo Proyecto TermodinamicamarcelaAún no hay calificaciones
- Elaboracion de ManjarDocumento12 páginasElaboracion de ManjarJoselyne ParraAún no hay calificaciones
- Problema 6Documento2 páginasProblema 6yossymarAún no hay calificaciones
- Cuestionario Practica 4Documento2 páginasCuestionario Practica 4Oriana RamosAún no hay calificaciones
- Equilibrio Quimico y Velocidad de Reaccio1 2Documento5 páginasEquilibrio Quimico y Velocidad de Reaccio1 2erwinAún no hay calificaciones
- Ejercicios de La Primera Ley de Termodinamica Unidad 1Documento2 páginasEjercicios de La Primera Ley de Termodinamica Unidad 1Dayer Carrasco UrbinaAún no hay calificaciones
- Ejercicios Castellan Fisicoquimica 2 ResueltosDocumento2 páginasEjercicios Castellan Fisicoquimica 2 Resueltosbraulio moises gutierrez mozombite0% (2)
- Elaboración de Mermelada - Quispe Velarde GuadalupeDocumento12 páginasElaboración de Mermelada - Quispe Velarde GuadalupeGuadalupe QAún no hay calificaciones
- Calor AbsorbidoDocumento11 páginasCalor AbsorbidoMaria Del CarmenAún no hay calificaciones
- Lab 4. Balances TérmicosDocumento11 páginasLab 4. Balances TérmicosArmando Ibarra FernandezAún no hay calificaciones
- Laboratorio de Analisis Instrumental 4 - DETERMINACION DE HIERRODocumento10 páginasLaboratorio de Analisis Instrumental 4 - DETERMINACION DE HIERROAntony Ramirez CamposAún no hay calificaciones
- Relaciones TermodinamicasDocumento21 páginasRelaciones TermodinamicasVirginia Otero YusteAún no hay calificaciones
- Informe de Balance de MateriaDocumento13 páginasInforme de Balance de MateriaCeleste CondoriAún no hay calificaciones
- Practica PHDocumento2 páginasPractica PHMesha RockefellerAún no hay calificaciones
- Problemas Resueltos 3Documento5 páginasProblemas Resueltos 3ivanAún no hay calificaciones
- Informe 4 BioquimicaDocumento4 páginasInforme 4 BioquimicaAndresArevaloCortes50% (2)
- PRACTICA #03-Mate3Documento4 páginasPRACTICA #03-Mate3Angel CondoriAún no hay calificaciones
- Informe de Laboratorio SolubilidadDocumento6 páginasInforme de Laboratorio SolubilidadVlado ManriqueAún no hay calificaciones
- Elaboracion de Yogurt Con ProvioticosDocumento4 páginasElaboracion de Yogurt Con Provioticosruben ramos quintanaAún no hay calificaciones
- Ejercicios de GasesDocumento3 páginasEjercicios de GasesJuan Andres Velez CalderónAún no hay calificaciones
- Balance de Materia en Sistemas Con Operaciones Unitarias-XiomyDocumento4 páginasBalance de Materia en Sistemas Con Operaciones Unitarias-XiomybiotechdogoAún no hay calificaciones
- Metodo de Enumeracion Implicita Cero UnoDocumento5 páginasMetodo de Enumeracion Implicita Cero UnoccggmmuuAún no hay calificaciones
- Informe de Laboratorio de BioquimicaDocumento9 páginasInforme de Laboratorio de BioquimicaGreysiʚïɞGironAún no hay calificaciones
- Harina Centeno PDFDocumento9 páginasHarina Centeno PDFJesús Miguel Jacinto NavaAún no hay calificaciones
- Practica PRQ 3250Documento10 páginasPractica PRQ 3250Harold Cesar Gabriel HerreraAún no hay calificaciones
- Entalpía Concentración HCLDocumento1 páginaEntalpía Concentración HCLRaulAún no hay calificaciones
- Calor de ReacciónDocumento5 páginasCalor de ReacciónannyAún no hay calificaciones
- Informe de EntalpiaDocumento15 páginasInforme de EntalpiaJoselin España100% (1)
- Guia Lab. QmcaDocumento56 páginasGuia Lab. QmcaHector Valdes Rojas100% (1)
- Etapas de La Conservación Del Pescado y DerivadosDocumento6 páginasEtapas de La Conservación Del Pescado y DerivadosHilder Aranda CastroAún no hay calificaciones
- Balance de MateriaDocumento31 páginasBalance de MateriajoaquinAún no hay calificaciones
- PDF 218840724 Balance de Energia y Materia Ejercicios Resueltospdf - CompressDocumento56 páginasPDF 218840724 Balance de Energia y Materia Ejercicios Resueltospdf - CompressAlejandra QuintinAún no hay calificaciones
- Fracción Molar PDFDocumento2 páginasFracción Molar PDFXicoténcatl Martínez ManzanoAún no hay calificaciones
- Balance de Materia - DestilaciónDocumento8 páginasBalance de Materia - DestilaciónJavier MoralesAún no hay calificaciones
- Laboratorio Tratamiento Estadistico de DatosDocumento13 páginasLaboratorio Tratamiento Estadistico de DatosJoseph Silva OrdonezAún no hay calificaciones
- Articulo Dilatacion Termica de LiquidosDocumento15 páginasArticulo Dilatacion Termica de LiquidosGisellaPuentesAún no hay calificaciones
- Quimica ProblemasDocumento4 páginasQuimica Problemashpdam2Aún no hay calificaciones
- Problemas de Leyes y Estequiometrc3ada de GasesDocumento1 páginaProblemas de Leyes y Estequiometrc3ada de GasesXela ScAún no hay calificaciones
- Guia de Problemas de Introduccion Al Analisis de Datos de Velocidad-1Documento22 páginasGuia de Problemas de Introduccion Al Analisis de Datos de Velocidad-1rodry zuritaAún no hay calificaciones
- Equilibrio de Reparto de YodoDocumento6 páginasEquilibrio de Reparto de YodoCamila LluscoAún no hay calificaciones
- Capitulo 4 Termodinamica Resuelto PDFDocumento13 páginasCapitulo 4 Termodinamica Resuelto PDFJesus Alejandro Salas SanchezAún no hay calificaciones
- Ejercicios de ComplejosDocumento1 páginaEjercicios de Complejoschupetintrujillo123Aún no hay calificaciones
- 4 Propied ColigaDocumento5 páginas4 Propied ColigaLorena QuilesAún no hay calificaciones
- Trabajo de Soluciones I y IIDocumento12 páginasTrabajo de Soluciones I y IIAllenAún no hay calificaciones
- Propiedades ColigativasDocumento9 páginasPropiedades ColigativasJuan V RamirezAún no hay calificaciones
- Ejercicios Gases y DisolucionesDocumento3 páginasEjercicios Gases y DisolucionesDiego FelicianoAún no hay calificaciones
- La Fracción MolarDocumento5 páginasLa Fracción Molarcfabrizzio90Aún no hay calificaciones
- Informe de Química Analítica II. No. 4. RefractometríaDocumento9 páginasInforme de Química Analítica II. No. 4. RefractometríaDamian NauqueAún no hay calificaciones
- Estabilidad MedicamentosDocumento10 páginasEstabilidad MedicamentosOskar LazaroAún no hay calificaciones
- Monografia Osmosis InversaDocumento54 páginasMonografia Osmosis InversaClaudia Quenta100% (4)
- Blender Maxtec - SpanishDocumento26 páginasBlender Maxtec - SpanishNorberto MartinezAún no hay calificaciones
- Información Agrícola - Difusión, Ósmosis, Imbibición, Potencial de Agua PDFDocumento16 páginasInformación Agrícola - Difusión, Ósmosis, Imbibición, Potencial de Agua PDFPedro Monteza Chamaya100% (1)
- Curso Traducciel Uso de Lippia Alba (Mill.) N. E. Br. Ex Britt. & Wills. / Verbenaceae (Falso Melissa) en La Medicina Popular Brasileña Se Debe, Principalmente, A Las Propiedades SedantesonDocumento5 páginasCurso Traducciel Uso de Lippia Alba (Mill.) N. E. Br. Ex Britt. & Wills. / Verbenaceae (Falso Melissa) en La Medicina Popular Brasileña Se Debe, Principalmente, A Las Propiedades SedantesonDiana IlerAún no hay calificaciones
- Soluciones Titulacion Ácido BaseDocumento11 páginasSoluciones Titulacion Ácido BaseSam CAún no hay calificaciones
- Método CIATEXDocumento4 páginasMétodo CIATEXJonnatan Victor Bañon AriasAún no hay calificaciones
- Practica 3 Reaccion de UreasaDocumento3 páginasPractica 3 Reaccion de UreasaGerardoMendozaDorado29% (7)
- Determinacion Potenciometrica de Cloruros 1Documento10 páginasDeterminacion Potenciometrica de Cloruros 1Amarië FelagundAún no hay calificaciones
- Qué Hacer Con El Suero Del QuesoDocumento9 páginasQué Hacer Con El Suero Del QuesoIngenieriaAlimentosAún no hay calificaciones
- Proyecto de BioenergeticaDocumento4 páginasProyecto de BioenergeticaMinchola Ipanaque BryamAún no hay calificaciones
- Metodos PotenciometricosDocumento7 páginasMetodos PotenciometricosIvanMardoqueoMonrroyLopezAún no hay calificaciones
- Teoria de Acidos y Bases Segun Bronsted Curso en LineaDocumento64 páginasTeoria de Acidos y Bases Segun Bronsted Curso en Lineamafalda_quino1985Aún no hay calificaciones
- Clase Metodos Densimetricos y Grav.Documento18 páginasClase Metodos Densimetricos y Grav.Evelyn Cespedes100% (1)
- Nmx-Aa-084 Determinacion de SulfurosDocumento14 páginasNmx-Aa-084 Determinacion de SulfurosYuri Jesus V.Aún no hay calificaciones
- Fósforo Asimilable.Documento2 páginasFósforo Asimilable.carlos_wa_3100% (1)
- Propiedades Coligativas EjerciciosDocumento3 páginasPropiedades Coligativas Ejerciciosoturaleni09olAún no hay calificaciones
- Principios TeoricosDocumento6 páginasPrincipios TeoricosMarcos QpAún no hay calificaciones
- Tulas Libro Vi Anexo 3Documento31 páginasTulas Libro Vi Anexo 3Coastman Ecuador100% (1)
- NMX Aa 127 Scfi 2006Documento18 páginasNMX Aa 127 Scfi 2006Gabriela Ruiz OrantesAún no hay calificaciones
- Titulación de Anilina e Hidroxido de SodioDocumento11 páginasTitulación de Anilina e Hidroxido de SodioBetelgeuse Yad Al-jawzaAún no hay calificaciones
- Albion ProcessDocumento2 páginasAlbion ProcessSteven DziobaAún no hay calificaciones
- Soluciones - 2010 - 2010 09 28 290Documento13 páginasSoluciones - 2010 - 2010 09 28 290Gabriel BecerraAún no hay calificaciones
- Calibracion de Un Cromatografo e HPLCDocumento48 páginasCalibracion de Un Cromatografo e HPLCJessica Mendoza Tarazona100% (2)