Documentos de Académico
Documentos de Profesional
Documentos de Cultura
01 El Átomo y Su Estructura
Cargado por
John Alberto Vasquez Hurtado0 calificaciones0% encontró este documento útil (0 votos)
52 vistas15 páginasDerechos de autor
© © All Rights Reserved
Formatos disponibles
PPT, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPT, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
52 vistas15 páginas01 El Átomo y Su Estructura
Cargado por
John Alberto Vasquez HurtadoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPT, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 15
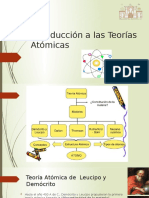
El tomo y su estructura
Esp. Luis Eduardo Olmos
Desde la Antigedad, el ser humano se ha
cuestionado de qu estaba hecha la materia.
Unos 400 aos antes de Cristo, el filsofo
griego Demcrito consider que la materia estaba
constituida por pequesimas partculas que no
podan ser divididas en otras ms pequeas.
Por ello, llam a estas partculas tomos, que en
griego quiere decir "indivisible".
Demcrito atribuy a los tomos las cualidades de
ser eternos, inmutables e indivisibles.
El tomo
El tomo esta formado por 2 partes
bsicas, ellas son:
El ncleo
La corteza
El ncleo: Es la parte central del tomo y
contiene partculas con carga positiva,
los protones, y partculas que no poseen
carga elctrica, es decir son neutras, los
neutrones.
Todos los tomos de un elemento qumico
tienen en el ncleo el mismo nmero de
protones. Este nmero, que caracteriza a
cada elemento y lo distingue de los dems, es
el nmero atmico y se representa con la
letra Z.
La corteza: Es la parte exterior del tomo. En
ella se encuentran los electrones, con carga
negativa. stos, ordenados en distintos
niveles, giran alrededor del ncleo. La masa
de un electrn es unas 2000 veces menor que
la de un protn.
Los tomos son elctricamente neutros,
debido a que tienen igual nmero de protones
que de electrones. As, el nmero atmico
tambin coincide con el nmero de electrones.
Modelos atmicos
Son representaciones graficas de los tomos,
entre estos tenemos:
Modelo de Dalton
Modelo de Thompson
Modelo de Rutherford
Modelo de Bohr
Modelo de Dalton
En 1808, Dalton public sus ideas sobre el modelo
atmico de la materia las cuales han servido de base
a la qumica moderna.
1. La materia est formada por minsculas partculas
indivisibles llamadas tomos.
2. Hay distintas clases de tomos que se distinguen
por su masa y sus propiedades. Todos los tomos
de un elemento poseen las mismas propiedades
qumicas.
3. Los compuestos se forman al combinarse los
tomos de dos o ms elementos en proporciones
fijas y sencillas. De modo que en un compuesto los
de tomos de cada tipo estn en una relacin de
nmeros enteros o fracciones sencillas.
4. En las reacciones qumicas, los tomos se
intercambian de una a otra sustancia, pero ningn
tomo de un elemento desaparece ni se transforma
en un tomo de otro elemento.
John Dalton
Modelo de Thompson
Demostr que dentro de los tomos hay unas
partculas diminutas, con carga elctrica negativa, a
las que se llam electrones.
El modelo conocido informalmente como el pudn de
ciruelas, segn el cual los electrones eran como
'ciruelas' negativas incrustadas en un 'pudn' de
materia positiva.
De este descubrimiento dedujo que el tomo deba de
ser una esfera de materia cargada positivamente, en
cuyo interior estaban incrustados los electrones.
Joseph John
Thomson
Modelo de Rutherford
Demostr que los tomos no eran macizos, como
se crea, sino que estn vacos en su mayor parte
y en su centro hay un diminuto ncleo.
Dedujo que el tomo deba estar formado por
una corteza con los electrones girando alrededor
de un ncleo central cargado positivamente.
Ernest Rutherford
Modelo de Bohr
Propuso un nuevo modelo atmico, segn el cual
los electrones giran alrededor del ncleo en unos
niveles bien definidos.
Bohr supuso que el tomo solo puede tener
ciertos niveles de energa definidos.
Bohr establece as, que los electrones solo
pueden girar en ciertas rbitas de radios
determinados.
Niels Bohr
Isotopos
Aunque todos los tomos de un mismo elemento se
caracterizan por tener el mismo nmero atmico, pueden
tener distinto nmero de neutrones.
Llamamos istopos a las formas atmicas de un mismo
elemento que se diferencian en su nmero msico.
La suma del nmero de protones y el nmero de
neutrones de un tomo recibe el nombre de nmero
msico y se representa con la letra A.
A= Z + n
Para representar un istopo, hay que indicar el nmero
msico (A) propio del istopo y el nmero atmico (Z),
colocados como ndice y subndice, respectivamente, a la
izquierda del smbolo del elemento.
Isotopos
También podría gustarte
- Problemario para El Segundo Examen Parcial (2019-2)Documento18 páginasProblemario para El Segundo Examen Parcial (2019-2)Yiovanni De Vicente50% (2)
- Escrito de Inicio de Ejecucion ForzadaDocumento2 páginasEscrito de Inicio de Ejecucion ForzadaMarleni Flores Caballero100% (1)
- Modelos Atomicos y Problemas.Documento22 páginasModelos Atomicos y Problemas.Patty VasquezAún no hay calificaciones
- Modelo Atómico de ThompsonDocumento11 páginasModelo Atómico de ThompsonFrancisco Javier ShagñayAún no hay calificaciones
- La Estructura de Los ÁtomosDocumento21 páginasLa Estructura de Los ÁtomosEduardo CastilloAún no hay calificaciones
- Teorias AtomicasDocumento24 páginasTeorias AtomicasfrankssereAún no hay calificaciones
- Estructura Del ÁtomoDocumento33 páginasEstructura Del ÁtomopabloAún no hay calificaciones
- Estructura Basica Del Atomo y Sus InteraccionesDocumento13 páginasEstructura Basica Del Atomo y Sus InteraccionesMarion AlvarezAún no hay calificaciones
- La Historia de La Ingeniería ElectrónicaDocumento5 páginasLa Historia de La Ingeniería ElectrónicaCarlos Adrian García Jr.Aún no hay calificaciones
- HIDRATOSDocumento21 páginasHIDRATOSmonica arpe100% (1)
- Teorias AtomicasDocumento1 páginaTeorias AtomicasAngelCochaAún no hay calificaciones
- Modelos Atomicos para Grado Decimo 4 Mayo de 2020Documento20 páginasModelos Atomicos para Grado Decimo 4 Mayo de 2020Johana De La HozAún no hay calificaciones
- Contaminacion Del Aire Por Los VolcanesDocumento4 páginasContaminacion Del Aire Por Los VolcanesErick Manosalvas100% (4)
- Experimento 6 GasesDocumento17 páginasExperimento 6 GasesRicardo Calderon100% (1)
- Modelo atómico de SchrödingerDocumento2 páginasModelo atómico de SchrödingerDEINERAún no hay calificaciones
- Tabla PeriodicaDocumento10 páginasTabla Periodicaapi-294786513Aún no hay calificaciones
- Collins La Mirada Sociológica y Sus AnteojerasDocumento7 páginasCollins La Mirada Sociológica y Sus AnteojerasGazpChiconiAún no hay calificaciones
- Efecto Zeeman y espín electrónicoDocumento9 páginasEfecto Zeeman y espín electrónicoGregorio MendezAún no hay calificaciones
- Modelo Atómico ActualDocumento7 páginasModelo Atómico ActualLala PalaAún no hay calificaciones
- Estructura Del AtomoDocumento25 páginasEstructura Del AtomoKeny Witney Chipana AnglesAún no hay calificaciones
- Modelos atómicos de Thomson y RutherfordDocumento14 páginasModelos atómicos de Thomson y Rutherfordjoseluis251168Aún no hay calificaciones
- Clase Números CuanticosDocumento22 páginasClase Números CuanticosConstanza Rojos AlmunaAún no hay calificaciones
- Unidad 2. Enlace Quimico PDFDocumento60 páginasUnidad 2. Enlace Quimico PDFCisli didi Aguilar Martínez100% (1)
- Modelos AtomicosDocumento10 páginasModelos AtomicosNico GonzaAún no hay calificaciones
- Números Cuánticos 2022Documento25 páginasNúmeros Cuánticos 2022ANGIE ANDREA ALFARO ANDRADEAún no hay calificaciones
- Espectros atómicos y radiación electromagnéticaDocumento11 páginasEspectros atómicos y radiación electromagnéticaRubenAún no hay calificaciones
- Taller Configuracion Electronica y T.P PDFDocumento6 páginasTaller Configuracion Electronica y T.P PDFKiara Mosquera RodriguezAún no hay calificaciones
- Teoría atómica de Dalton y sus contribuciones a la químicaDocumento4 páginasTeoría atómica de Dalton y sus contribuciones a la químicaNilber Martinez100% (1)
- EFECTO-FOTOELECTRICO Margi DiaposDocumento21 páginasEFECTO-FOTOELECTRICO Margi DiaposAnonymous gxbo46MAún no hay calificaciones
- Revista de QuimicaDocumento50 páginasRevista de QuimicaFernando Angel GORDILLO RUIZAún no hay calificaciones
- Folleto CuanticaDocumento39 páginasFolleto CuanticaCliffor Jerry Herrera CastrilloAún no hay calificaciones
- Qué Es EstequiometríaDocumento3 páginasQué Es EstequiometríaNorkis Mejias100% (1)
- Los Sofistas y Socrates L Jose GajateDocumento8 páginasLos Sofistas y Socrates L Jose GajateSr. LeonardoAún no hay calificaciones
- Espín Del ElectrónDocumento13 páginasEspín Del ElectrónAndyAún no hay calificaciones
- Espectroscopía atómica y modelosDocumento20 páginasEspectroscopía atómica y modelosCristian TovarAún no hay calificaciones
- Profesoras Nombre Del Estudiante: Curso y División:: Instituto Nuestra Señora de La MercedDocumento27 páginasProfesoras Nombre Del Estudiante: Curso y División:: Instituto Nuestra Señora de La MercedCele ZárateAún no hay calificaciones
- Modelo Atómico ActualDocumento77 páginasModelo Atómico ActualNeyibe Neried Gutierrez HerradaAún no hay calificaciones
- UNIONES QUÍMICAS Nomenclatura y FormuleoDocumento19 páginasUNIONES QUÍMICAS Nomenclatura y Formuleolilip100% (3)
- Números cuánticos principalesDocumento47 páginasNúmeros cuánticos principalesCarolina Andrea Parra QuijadaAún no hay calificaciones
- El Átomo y Sus Partículas Subatómicas (Autoguardado)Documento12 páginasEl Átomo y Sus Partículas Subatómicas (Autoguardado)Hugo ValAún no hay calificaciones
- Modelo Atómico de BohrDocumento22 páginasModelo Atómico de BohrValentina CarpioAún no hay calificaciones
- UNIDAD 2 Estructura AtómicaDocumento18 páginasUNIDAD 2 Estructura AtómicaJavier J SalazarAún no hay calificaciones
- UNIDAD IV Quimica ResumenDocumento5 páginasUNIDAD IV Quimica ResumenDanny BarreraAún no hay calificaciones
- Ley Periodica: Elementos Del Grupo 1, Periodo 3 y Elementos Del Grupo 12Documento13 páginasLey Periodica: Elementos Del Grupo 1, Periodo 3 y Elementos Del Grupo 12Miguel Betancourt G100% (1)
- Clase 10 Modelos AtomicosDocumento19 páginasClase 10 Modelos AtomicosSandy Torres carhuallanquiAún no hay calificaciones
- Historia de La Tabla PeriodicaDocumento4 páginasHistoria de La Tabla PeriodicaDenisse Sosa OrtizAún no hay calificaciones
- Estructura Electrónica de Los SolidosDocumento5 páginasEstructura Electrónica de Los SolidosAlejandro BejaranoAún no hay calificaciones
- Estructura átomo radiactividadDocumento46 páginasEstructura átomo radiactividadDiego AmarisAún no hay calificaciones
- Material de Estudio 1. Revisión de Estructura Atómica v3Documento8 páginasMaterial de Estudio 1. Revisión de Estructura Atómica v3maga_azulAún no hay calificaciones
- Capítulo 3 Espectroscopía de Absorción MolecularDocumento41 páginasCapítulo 3 Espectroscopía de Absorción MolecularLorena SilvaAún no hay calificaciones
- Modelos atómicos a través de la historiaDocumento35 páginasModelos atómicos a través de la historiaJuan K MarroquinAún no hay calificaciones
- Introducción A Las Teorías AtómicasDocumento20 páginasIntroducción A Las Teorías AtómicaslauraAún no hay calificaciones
- Guía Simulador Modelo Atómico de RutherfordDocumento4 páginasGuía Simulador Modelo Atómico de RutherfordSebastian Matheus Londono MoralesAún no hay calificaciones
- TRPECV geometríasDocumento33 páginasTRPECV geometríasChristian SumanoAún no hay calificaciones
- Metales, No Metales y Gases NoblesDocumento7 páginasMetales, No Metales y Gases NoblesVivi Reca GAún no hay calificaciones
- Radio IonicoDocumento1 páginaRadio IonicoAnonymous ZAuWf2Aún no hay calificaciones
- Isotopos QuímicosDocumento18 páginasIsotopos QuímicosAnonymous 24gbDOp3Aún no hay calificaciones
- Estructura Atómica y Clasificación Periódica de Los ElementosDocumento10 páginasEstructura Atómica y Clasificación Periódica de Los ElementosBegoña García AcevedoAún no hay calificaciones
- QUIMICADocumento18 páginasQUIMICAKenjo VasquezAún no hay calificaciones
- Unidad #1 Atomo Moleculas IonesDocumento32 páginasUnidad #1 Atomo Moleculas IonesPedro BarreraAún no hay calificaciones
- El Atomo y La Teoria AtomicaDocumento8 páginasEl Atomo y La Teoria Atomicaabenitezmendez2307Aún no hay calificaciones
- El At0m0 y Su EstructuraDocumento5 páginasEl At0m0 y Su EstructuraTUTORIALES GAMERSAún no hay calificaciones
- Investigacion PreparatoriaDocumento14 páginasInvestigacion PreparatoriaJohn Alberto Vasquez HurtadoAún no hay calificaciones
- Subasta de Vehiculos 002-2021-Jus - Pronabi (Triptico)Documento2 páginasSubasta de Vehiculos 002-2021-Jus - Pronabi (Triptico)julinhoAún no hay calificaciones
- Plazos D.P. según casosDocumento11 páginasPlazos D.P. según casosJohn Alberto Vasquez HurtadoAún no hay calificaciones
- Codigo Del Niño y AdolescenteDocumento93 páginasCodigo Del Niño y AdolescenteJohn Alberto Vasquez HurtadoAún no hay calificaciones
- Fidel Rojas NCPPDocumento37 páginasFidel Rojas NCPPAmaliaAún no hay calificaciones
- Personas Naturales - Victor Guevara PezoDocumento260 páginasPersonas Naturales - Victor Guevara PezoAnonymous erxJ9wHa100% (7)
- 4e1e6e - Flujograma 1 PDFDocumento5 páginas4e1e6e - Flujograma 1 PDFJohn Alberto Vasquez HurtadoAún no hay calificaciones
- Registro de Entrega de EppsDocumento1 páginaRegistro de Entrega de EppsJohn Alberto Vasquez HurtadoAún no hay calificaciones
- Atencion CemDocumento2 páginasAtencion CemJohn Alberto Vasquez HurtadoAún no hay calificaciones
- Solicitud de Pase Personal Laboral PDFDocumento2 páginasSolicitud de Pase Personal Laboral PDFJohn Alberto Vasquez HurtadoAún no hay calificaciones
- Interdicto de RecobrarDocumento3 páginasInterdicto de RecobrarAnonymous kpCltzY5100% (2)
- Modelo de Registro FotográficoDocumento11 páginasModelo de Registro FotográficoJohn Alberto Vasquez HurtadoAún no hay calificaciones
- Como Hacer Una Tesis de Derecho y No Envejecer en El Intento - Carlos Ramos Nuñez PDFDocumento444 páginasComo Hacer Una Tesis de Derecho y No Envejecer en El Intento - Carlos Ramos Nuñez PDFJohn Alberto Vasquez HurtadoAún no hay calificaciones
- Modelo de Carta de Renuncia Con Exoneracion de PreavisoDocumento1 páginaModelo de Carta de Renuncia Con Exoneracion de PreavisoJuan Miguel Flores CastroAún no hay calificaciones
- Cuáles Son Los Derechos Del Adulto MayorDocumento1 páginaCuáles Son Los Derechos Del Adulto MayorJohn Alberto Vasquez HurtadoAún no hay calificaciones
- Ley #30490 - Ley de La PersonaDocumento6 páginasLey #30490 - Ley de La PersonaJohn Alberto Vasquez HurtadoAún no hay calificaciones
- Casación 4516 2016 Lambayeque Legis - PeDocumento14 páginasCasación 4516 2016 Lambayeque Legis - PeJohn Alberto Vasquez HurtadoAún no hay calificaciones
- CongresoDocumento344 páginasCongresoJohn Alberto Vasquez HurtadoAún no hay calificaciones
- Modelo de EscritoDocumento3 páginasModelo de EscritoJohn Alberto Vasquez HurtadoAún no hay calificaciones
- Ley AdultoDocumento16 páginasLey AdultoJohn Alberto Vasquez HurtadoAún no hay calificaciones
- Ley 28803 Ley Del Adulto MayorDocumento6 páginasLey 28803 Ley Del Adulto MayorJuan Francisco Bejarano FloresAún no hay calificaciones
- MedicionDocumento1 páginaMedicionJohn Alberto Vasquez HurtadoAún no hay calificaciones
- Teoria Del DelitoDocumento21 páginasTeoria Del DelitoSlevin KelevraAún no hay calificaciones
- BIOFARMACIA Presentación de Microsoft PowerPointDocumento37 páginasBIOFARMACIA Presentación de Microsoft PowerPointJohn Alberto Vasquez HurtadoAún no hay calificaciones
- Titis Media Aguda OMA: EfinicionesDocumento7 páginasTitis Media Aguda OMA: EfinicionesJohn Alberto Vasquez HurtadoAún no hay calificaciones
- Cuadro de Aranceles Judiciales - Ejercicio Gravable 2019Documento1 páginaCuadro de Aranceles Judiciales - Ejercicio Gravable 2019Walter Nieto100% (1)
- Antirretrovirales y AntineoplasicosDocumento70 páginasAntirretrovirales y AntineoplasicosJohn Alberto Vasquez HurtadoAún no hay calificaciones
- DisenosDocumento12 páginasDisenosHanccoTrellesWenmerJairoAún no hay calificaciones
- Farmacologia OcularDocumento49 páginasFarmacologia OcularJohn Alberto Vasquez Hurtado100% (2)
- Vision - Moderna Del AtomoDocumento2 páginasVision - Moderna Del Atomoake_motoAún no hay calificaciones
- Tema 1. Estructura de La Materia (Apuntes y Actividades)Documento28 páginasTema 1. Estructura de La Materia (Apuntes y Actividades)Gloria GarciaAún no hay calificaciones
- Partículas elementales y sus interaccionesDocumento12 páginasPartículas elementales y sus interaccionesDiego ReyesAún no hay calificaciones
- Proyectos Integrado Ala CienciaDocumento10 páginasProyectos Integrado Ala CienciaYonathan RoqueAún no hay calificaciones
- Cruadro Comparativo - Modelos AtomicosDocumento5 páginasCruadro Comparativo - Modelos AtomicosEleAún no hay calificaciones
- Evolución Atómica Hasta La ActualidadDocumento11 páginasEvolución Atómica Hasta La ActualidadDanIel Carbonell AcuñaAún no hay calificaciones
- Tabla Periódica 2020Documento5 páginasTabla Periódica 2020hskv20025525Aún no hay calificaciones
- Caracterización Petrofísica A Partir de Núcleos de Perforación y Registros de Pozo para Las Areniscas de La Formación Mugrosa Del Campo Colorado Bloques I y IiDocumento116 páginasCaracterización Petrofísica A Partir de Núcleos de Perforación y Registros de Pozo para Las Areniscas de La Formación Mugrosa Del Campo Colorado Bloques I y IiEfer Cuadros BAún no hay calificaciones
- Resúmen Herramientas MDW y LWDDocumento10 páginasResúmen Herramientas MDW y LWDCristhian Soliz100% (1)
- Trabajo Átomo de Borh y Elementos QuímicosDocumento2 páginasTrabajo Átomo de Borh y Elementos QuímicosFausto Teodoro Ramirez FranchiAún no hay calificaciones
- Clei 3 Taller2 Ciencia Naturales Avtiv 2 HechoDocumento4 páginasClei 3 Taller2 Ciencia Naturales Avtiv 2 HechoArlinson Mosquera LambrañoAún no hay calificaciones
- Qué Es La Materia DayersonDocumento7 páginasQué Es La Materia DayersonManuel De Jesus Briceño SuarezAún no hay calificaciones
- Teoría InflacionariaDocumento13 páginasTeoría InflacionariaJorge Bautista SuarezAún no hay calificaciones
- Bases Conceptuales de Anatomía y Fisiología HumanaDocumento3 páginasBases Conceptuales de Anatomía y Fisiología HumanaKahelAún no hay calificaciones
- Semana 03 - Tarea Academica 1 - Teorias AtomicasDocumento12 páginasSemana 03 - Tarea Academica 1 - Teorias AtomicasAlanis Ortiz TenorioAún no hay calificaciones
- Modelos AtomicosDocumento1 páginaModelos AtomicosIsabel Gonzales100% (1)
- Preguntas Tipo para El Examen de Modelos AtómicosDocumento2 páginasPreguntas Tipo para El Examen de Modelos Atómicosdcurie100% (10)
- Isótopos radiactivos y componentes dañinosDocumento5 páginasIsótopos radiactivos y componentes dañinoscaleAún no hay calificaciones
- Reseña Histórica Del KickingballDocumento15 páginasReseña Histórica Del KickingballGilmer Rosendo Sanan SantayAún no hay calificaciones
- QuimicaDocumento8 páginasQuimicaRamsay Lagher100% (1)
- Sesion N°7Documento36 páginasSesion N°7GUIRIA00Aún no hay calificaciones
- Modelo AtómicoDocumento6 páginasModelo AtómicoVing LGAún no hay calificaciones
- Estructura de La Materia 2018Documento82 páginasEstructura de La Materia 2018samioAún no hay calificaciones
- Evolución del pensamiento científico a través de los siglosDocumento4 páginasEvolución del pensamiento científico a través de los siglosPaula AlmadaAún no hay calificaciones
- Introducción a la Química y Física BiológicasDocumento203 páginasIntroducción a la Química y Física BiológicasGimena GarecaAún no hay calificaciones
- 99469460-620-Preguntas-resueltas-De-Quimica-01 PreguntasDocumento98 páginas99469460-620-Preguntas-resueltas-De-Quimica-01 PreguntasElgieDavidHernandezHernandez100% (1)
- Prueba de Estructura AtómicaDocumento3 páginasPrueba de Estructura Atómicaerik villarAún no hay calificaciones
- Warden El Enemigo Como Un SistemaDocumento15 páginasWarden El Enemigo Como Un SistematempestadAún no hay calificaciones
- Ex Fq02 Sem21Documento4 páginasEx Fq02 Sem21sinon ukatoAún no hay calificaciones