Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Term Odin A Mica
Cargado por
Wilder Mita0 calificaciones0% encontró este documento útil (0 votos)
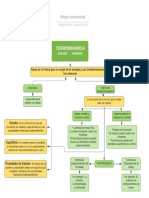
6 vistas10 páginasEste documento define la termodinámica como la rama de la física que estudia la relación entre el calor, la fuerza aplicada y la transferencia de energía. Explica que un proceso termodinámico es la evolución de las propiedades de un sistema termodinámico y puede ser reversible o irreversible. Finalmente, describe los diferentes tipos de procesos termodinámicos, incluyendo procesos isobáricos, isocóricos, isotérmicos, adiabáticos, isentrópicos y politrópicos
Descripción original:
Título original
Term Odin a Mica
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PPTX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoEste documento define la termodinámica como la rama de la física que estudia la relación entre el calor, la fuerza aplicada y la transferencia de energía. Explica que un proceso termodinámico es la evolución de las propiedades de un sistema termodinámico y puede ser reversible o irreversible. Finalmente, describe los diferentes tipos de procesos termodinámicos, incluyendo procesos isobáricos, isocóricos, isotérmicos, adiabáticos, isentrópicos y politrópicos
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPTX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
6 vistas10 páginasTerm Odin A Mica
Cargado por
Wilder MitaEste documento define la termodinámica como la rama de la física que estudia la relación entre el calor, la fuerza aplicada y la transferencia de energía. Explica que un proceso termodinámico es la evolución de las propiedades de un sistema termodinámico y puede ser reversible o irreversible. Finalmente, describe los diferentes tipos de procesos termodinámicos, incluyendo procesos isobáricos, isocóricos, isotérmicos, adiabáticos, isentrópicos y politrópicos
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPTX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 10
TERMODINAMICA
Nombre: Wilder Mita Equilea
Lic. : Efrain Villca
Año: 300 M.A.
¿Qué es termodinámica?
La termodinámica es la rama de la física que estudia la relación entre el calor, la
fuerza aplicada (también conocida como trabajo) y la transferencia de energía.
¿Qué es un proceso termodinámico?
Se denomina proceso termodinámico a la evolución de unas determinadas
magnitudes o propiedades en relación a un determinado sistema termodinámico.
Estas propiedades se denominan propiedades termodinámicas.
Para poder estudiar un proceso termodinámico se requiere que el sistema esté en
equilibrio termodinámico en el punto inicial y final del proceso. Es decir, que las
magnitudes que sufren una variación al pasar de un estado a otro deben estar
completamente definidas en sus estados inicial y final.
Un proceso termodinámico también puede ser visto como los cambios de un
sistema, desde unas condiciones iniciales hasta otras condiciones finales.
Un proceso termodinámico puede ser reversible o irreversible. Todas las
transformaciones reales son irreversibles, ya que las fricciones no se pueden eliminar
por completo, por lo que la condición de reversibilidad es solo una aproximación
teórica.
La teoría de los procesos térmicos se aplica al diseño de motores, unidades de
refrigeración, industria química y meteorología.
Tipos de procesos termodinámicos:
Proceso isobárico:
Un proceso isobárico es un cambio en el estado de una cierta cantidad
de materia en la que la presión permanece constante. Lo que sí cambia
es una o más de sus variables de estado. Si se transfiere calor al sistema
se realiza trabajo y también cambia la energía interna del sistema.
Proceso isocórico:
El volumen permanece constante. Por lo tanto, si el sistema está a volumen
constante, el trabajo hecho por el sistema será cero. Esto implica que el
proceso no realiza trabajo presión-volumen. De ello se desprende que,
cualquier energía térmica transferida al sistema externamente, éste lo
absorbe en forma de energía interna.
proceso isotérmico:
Es una transformación termodinámica a temperatura constante. Es decir, una
variación del estado de un sistema físico durante el cual la temperatura del sistema
permanece constante.
Proceso adiabático:
Es un proceso en el que no hay transferencia de calor. Para un proceso
reversible, esto es idéntico a un proceso isentrópico. Se puede decir que
el sistema está térmicamente aislado de su entorno y que no puede
intercambiar calor con el entorno.
Proceso isentrópico:
Es un proceso termodinámico, en el cual la entropía del fluido o gas permanece
constante. También se llama un proceso de entropía constante.
Proceso politrópico:
Un proceso politrópico es un proceso termodinámico durante el cual la capacidad
calorífica de un gas permanece sin cambios, es decir, no existen intercambios de calor.
También podría gustarte
- Resumen Teoria General de Los SistemasDocumento5 páginasResumen Teoria General de Los SistemasingrcAún no hay calificaciones
- UF1026 - Caracterización de procesos e instalaciones frigoríficasDe EverandUF1026 - Caracterización de procesos e instalaciones frigoríficasCalificación: 4 de 5 estrellas4/5 (1)
- Las Constelaciones FamiliaresDocumento10 páginasLas Constelaciones FamiliaresfelixperezvAún no hay calificaciones
- PRACTICA 3 Quimica Aplicada Esime ZacatencoDocumento16 páginasPRACTICA 3 Quimica Aplicada Esime ZacatencoErika EscalanteAún no hay calificaciones
- Procesos Termodinamicos.Documento12 páginasProcesos Termodinamicos.Miré Caya Ruiz100% (2)
- Ciclo Inverso de CarnotDocumento13 páginasCiclo Inverso de CarnotFelipe Valenzuela Yepez100% (3)
- Glosario de TermodinámicaDocumento5 páginasGlosario de TermodinámicaEriikaDiaz67% (3)
- Examen Parcial 2018A-CD SolucionarioDocumento3 páginasExamen Parcial 2018A-CD SolucionarioYosimar Enoki RojasAún no hay calificaciones
- Procesos TermodinámicosDocumento3 páginasProcesos Termodinámicosrodrigo vargasAún no hay calificaciones
- Procesos Termodinamico.Documento4 páginasProcesos Termodinamico.Nicol Ortiz VillarAún no hay calificaciones
- Proceso Termodinámico: Procesos IsoDocumento2 páginasProceso Termodinámico: Procesos IsoAlexis MendezAún no hay calificaciones
- Procesos ISODocumento22 páginasProcesos ISOCesar OrtegaAún no hay calificaciones
- Trabajo de Investigacion MamitaDocumento5 páginasTrabajo de Investigacion MamitaBoulevard De Los Sueños RotosAún no hay calificaciones
- TermodinamicaDocumento66 páginasTermodinamicaNicol Yamilet Cordova AliagaAún no hay calificaciones
- Proceso TermodinámicoDocumento6 páginasProceso TermodinámicoKelvin GarciaAún no hay calificaciones
- Semana 2-Operaciones Unitarias - 2020 - IIDocumento66 páginasSemana 2-Operaciones Unitarias - 2020 - IILIZET KARINA AZA�ERO HUAYNACARIAún no hay calificaciones
- Procesos de Bombeo y Compresion de HidrocarburosDocumento7 páginasProcesos de Bombeo y Compresion de HidrocarburosGonzalo TellesAún no hay calificaciones
- Procesos TermodinamicosDocumento5 páginasProcesos TermodinamicosCesar FloresAún no hay calificaciones
- Termodinamica 6to Año.Documento16 páginasTermodinamica 6to Año.Lucas EstecheAún no hay calificaciones
- Unidad 3 de Termodinámica, Leandro Barrios, Ci - 29660642Documento7 páginasUnidad 3 de Termodinámica, Leandro Barrios, Ci - 29660642Leandro BarriosAún no hay calificaciones
- Procesos Reversibles e IrreversiblesDocumento10 páginasProcesos Reversibles e IrreversiblesSony KenpachiAún no hay calificaciones
- Ejemplos de Propiedades Termodinámicas IntensivasDocumento2 páginasEjemplos de Propiedades Termodinámicas IntensivasAide F. GarcíaAún no hay calificaciones
- Estados Procesos y CiclosDocumento8 páginasEstados Procesos y CiclosRichard PinosAún no hay calificaciones
- La Ley Cero de La TermodinámicaDocumento3 páginasLa Ley Cero de La TermodinámicaYubelgxAún no hay calificaciones
- FisicaDocumento18 páginasFisicaDuvan PerezAún no hay calificaciones
- Eter2 U1 A1 EdmsDocumento7 páginasEter2 U1 A1 EdmsLalo MartiAún no hay calificaciones
- TermodinamicaDocumento9 páginasTermodinamicaFREDERICKESCOBARAún no hay calificaciones
- Previo Práctica 7 VICTOR PEREZ LOPEZ 8022Documento4 páginasPrevio Práctica 7 VICTOR PEREZ LOPEZ 8022VICTOR PEREZ LOPEZAún no hay calificaciones
- Ejercicio 3 Fisica Dave RinconDocumento8 páginasEjercicio 3 Fisica Dave RinconDave RinconAún no hay calificaciones
- Estados Procesos y CiclosDocumento8 páginasEstados Procesos y CiclosRichard PinosAún no hay calificaciones
- Guia 01 ConceptosDocumento5 páginasGuia 01 ConceptosAlexander SosaAún no hay calificaciones
- Cuestionario de Procesos TermodinámicosDocumento6 páginasCuestionario de Procesos TermodinámicosSantiago Xavier0% (1)
- Trabajo TermodinamicoDocumento7 páginasTrabajo TermodinamicoLopez MelizaAún no hay calificaciones
- Procesos y CiclosDocumento7 páginasProcesos y CiclosMichelleAún no hay calificaciones
- Equilibrio Térmico y Procesos TermodinámicosDocumento12 páginasEquilibrio Térmico y Procesos Termodinámicossantiago100% (2)
- Procesos TermodinamicosDocumento7 páginasProcesos TermodinamicosJorge Alberto Bustos ZamoraAún no hay calificaciones
- Expo FisiicaDocumento4 páginasExpo FisiicaMIRIAM ELIZABETH PADILLA RIVERAAún no hay calificaciones
- Introducción A La TermodinamicaDocumento15 páginasIntroducción A La TermodinamicaRicardo Felix Diaz LopezAún no hay calificaciones
- La Termodinamica 1 Sesion 7 y 8Documento88 páginasLa Termodinamica 1 Sesion 7 y 8gustavo_castro_17Aún no hay calificaciones
- Ejemplos de Los Diferentes Tipos de Procesos TermodinamicosDocumento2 páginasEjemplos de Los Diferentes Tipos de Procesos TermodinamicosNeider OrtizAún no hay calificaciones
- Tipos de Procesos Termodinámicos.Documento5 páginasTipos de Procesos Termodinámicos.AARON VAZQUEZ MARTINEZAún no hay calificaciones
- Primera Ley de La Termodinamica.Documento12 páginasPrimera Ley de La Termodinamica.Rufo C MtzAún no hay calificaciones
- Baez 2Documento15 páginasBaez 2NoElia CaBreraAún no hay calificaciones
- Trabajo de Investigación de TermodinámicaDocumento20 páginasTrabajo de Investigación de TermodinámicaMarcosAún no hay calificaciones
- Procesos TermodinámicosDocumento15 páginasProcesos TermodinámicosJorge LujanAún no hay calificaciones
- Glosario UNIDAD 1Documento8 páginasGlosario UNIDAD 1Mariana Michel Castro HerediaAún no hay calificaciones
- Practica Termo QuimicaDocumento11 páginasPractica Termo QuimicasamuelAún no hay calificaciones
- Tipos de Procesos TermodinámicosDocumento6 páginasTipos de Procesos TermodinámicosJUAN ANTONIO DE LA CRUZ GOMEZAún no hay calificaciones
- Tarea de Termodinamica de # 2Documento10 páginasTarea de Termodinamica de # 2Jhonny Wladimir Peñaloza Cabello0% (2)
- Termodinámica Aplicada A La IngenieríaDocumento19 páginasTermodinámica Aplicada A La Ingenieríaluisangel CharrisAún no hay calificaciones
- Tipos y Procesos TermodinamicaDocumento1 páginaTipos y Procesos TermodinamicaNavarro José LuisAún no hay calificaciones
- Termodinamica GeneraldiadesDocumento26 páginasTermodinamica GeneraldiadesSaul Fernando SandovalAún no hay calificaciones
- Práctica No5 Quimica AplicadaDocumento5 páginasPráctica No5 Quimica AplicadaSebastian PatricioAún no hay calificaciones
- Segundo Avance Grupo 9 - Proyecto Procesos TermodinamicosDocumento17 páginasSegundo Avance Grupo 9 - Proyecto Procesos Termodinamicosprivt vateAún no hay calificaciones
- Presentación Termodinámica ClaseDocumento34 páginasPresentación Termodinámica ClaseLuis GuevaraAún no hay calificaciones
- LaboratorioDocumento11 páginasLaboratorioclientes KoneAún no hay calificaciones
- 1.7 Procesos y Ciclos y 1.8 DensidadDocumento12 páginas1.7 Procesos y Ciclos y 1.8 DensidadangelAún no hay calificaciones
- U3 BME Actividad 1Documento5 páginasU3 BME Actividad 1Diego GerardoloAún no hay calificaciones
- Ucci - Termo 02 - 2018-22Documento57 páginasUcci - Termo 02 - 2018-22Kukin Erik Usquiano Uscuvilca100% (1)
- Ciclos TermodinamicosDocumento15 páginasCiclos TermodinamicosRaquel Jrz SvAún no hay calificaciones
- Informe S..Documento9 páginasInforme S..Luigi Andre Depaz RamirezAún no hay calificaciones
- TermofluidosDocumento40 páginasTermofluidosAguzz Campuzano100% (3)
- Preparar y acondicionar elementos y máquinas de la planta química. QUIE0108De EverandPreparar y acondicionar elementos y máquinas de la planta química. QUIE0108Aún no hay calificaciones
- Modelo Matemático Whiten para Harneros VibratoriosDocumento15 páginasModelo Matemático Whiten para Harneros VibratoriosElder Fabian Chapilla CastilloAún no hay calificaciones
- Informe Química 2 Calor EspecíficoDocumento2 páginasInforme Química 2 Calor EspecíficonilsonAún no hay calificaciones
- Microcurriculos Snna-SenescytDocumento70 páginasMicrocurriculos Snna-SenescytTodo Juegos ProgramasAún no hay calificaciones
- Estrategias (1.1)Documento5 páginasEstrategias (1.1)jhassadi mincholaAún no hay calificaciones
- La Estrategia para La Construcción de Un Modelo de Juego en El FútbolDocumento21 páginasLa Estrategia para La Construcción de Un Modelo de Juego en El FútbolDavid GpAún no hay calificaciones
- Estudio Analisis Dinamico No Lineal y Discreto y Desarrollo de Un SistemaDocumento285 páginasEstudio Analisis Dinamico No Lineal y Discreto y Desarrollo de Un SistemaEdwin Zamudio TiconaAún no hay calificaciones
- Taller 1 Normas - Roxana Esther Mamani VilcaDocumento3 páginasTaller 1 Normas - Roxana Esther Mamani Vilcakatherine espinoza neiraAún no hay calificaciones
- Taller 15% Segundo Corte Diseño Mecatronico Ii - 2Documento55 páginasTaller 15% Segundo Corte Diseño Mecatronico Ii - 2roxanaAún no hay calificaciones
- Nivel de ServicioDocumento27 páginasNivel de ServicioSolange TC100% (1)
- Termodinamica - Clase 1 PDFDocumento23 páginasTermodinamica - Clase 1 PDFJonathan Alexis Jony CTAún no hay calificaciones
- Planeación de ProyectosDocumento17 páginasPlaneación de ProyectosMaRkMitchellAún no hay calificaciones
- Costos Paramétricos Por Sistema HVACDocumento4 páginasCostos Paramétricos Por Sistema HVACMiguel HerediaAún no hay calificaciones
- PLC Actividad InicialDocumento4 páginasPLC Actividad InicialROBINSON NUEZ FERNANDEZAún no hay calificaciones
- Calor y Primera LeyDocumento59 páginasCalor y Primera LeyClases virtuales con Miss KarinaAún no hay calificaciones
- TermodinámicaDocumento5 páginasTermodinámicaReyes EsmeraldaAún no hay calificaciones
- 15 Resumen - PROBLEMOLOGIADocumento6 páginas15 Resumen - PROBLEMOLOGIAAngel Joshua PaytanAún no hay calificaciones
- Formato SÍLABO Termodinámica Química I - 2P-2020Documento4 páginasFormato SÍLABO Termodinámica Química I - 2P-2020estebanAún no hay calificaciones
- Pensamiento Sistémico - Resumen 7,8Documento9 páginasPensamiento Sistémico - Resumen 7,8Fabian100% (2)
- Lectura ExplicativaDocumento6 páginasLectura ExplicativaMa Antonieta GalindoAún no hay calificaciones
- Practica #06 CalorDocumento22 páginasPractica #06 CalorGabriela Quichua AronesAún no hay calificaciones
- 2º Bach Tec Industrial IIDocumento10 páginas2º Bach Tec Industrial IIAnaAún no hay calificaciones
- Silabo - Del - Curso ADocumento6 páginasSilabo - Del - Curso ATara KnightAún no hay calificaciones
- Eter2 U1 A1 EdmsDocumento7 páginasEter2 U1 A1 EdmsLalo MartiAún no hay calificaciones
- Mapa ConceptualDocumento1 páginaMapa ConceptualjabedoyagAún no hay calificaciones
- Informe Pràctica CalorimetriaDocumento4 páginasInforme Pràctica Calorimetriak. Cristina RuizAún no hay calificaciones
- Examen de La Teoría de Sistemas y Teoría Del CaosDocumento3 páginasExamen de La Teoría de Sistemas y Teoría Del CaosGiadranca Nuñez100% (1)
- BTC 8100 ManualDocumento4 páginasBTC 8100 ManualAlvaro FloresAún no hay calificaciones