Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Infografía Línea Del Tiempo Historia Ilustrado Beige
Infografía Línea Del Tiempo Historia Ilustrado Beige
Cargado por
Emma PeraltaDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Infografía Línea Del Tiempo Historia Ilustrado Beige
Infografía Línea Del Tiempo Historia Ilustrado Beige
Cargado por
Emma PeraltaCopyright:
Formatos disponibles
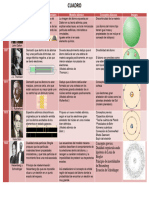
COMPOSICIONES DEL ÁTOMO
Contribuciones para determinar la composición
del átomo
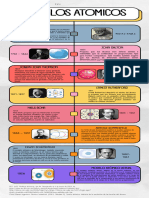
460 a. C.
Demócrito
“Todas las cosas están compuestas de
partículas diminutas indivisibles e
indestructibles”.
· Propiedades de la materia cambiantes.
· Atomos de diferente forma y tamaño.
· Teoría atómica del universo.
1808
John Dalton
· Primera formulación moderna de la teoría
atómica
· Minúsculas partículas esféricas, indivisibles
e inmutables, iguales entre si en cada
elemento químico.
1907
J.J. Thomson
· Supuso que el átomo no era la partícula
más pequeña.
· Descubrió que dentro de los átomos
habían unas partículas diminutas con carga
negativas a las cual se les llamo electrones.
1911
E. Rutherford
· Dedujo que podía haber una corteza en los
átomos con los electrones alrededor del
núcleo.
· Sugiere que la carga positiva esta
concentrada en un núcleo, mientras que los
electrones se mueven en órbitas alrededor
del núcleo
1913
Niels Bohr
· Modelos atómico de Bohr: nuevo modelo
atómico en el cual los elementos giran
alrededor del núcleo en unos niveles bien
definidos.
1916
Sommerfeld
· Modelo atómico de Sommerfeld: versión
mejorada del modelo atómico de Bohr.
· Explica el comportamiento de los electrones
mediante la existencia de diferentes niveles
energéticos en el átomo.
1925
Heisenberg
· Principio de incertidumbre en los orbitales
de electrones que rodean el núcleo atómico.
· Instauro los cimientos de la mecánica
cuántica para estimar el comportamiento de
las partículas subatómicas.
1926
Schrodinger
· Modelo atómico de Schrodinger: conocido
como el modelo mecánico cuántico del
átomo y describe el comportamiento
ondulatorio del electrón.
También podría gustarte
- Contrato de Franquicia ModeloDocumento3 páginasContrato de Franquicia Modelodoris50% (2)
- Tríptico - Tipos de Modelos AtómicosDocumento2 páginasTríptico - Tipos de Modelos AtómicosDenisse100% (4)
- Charlas 5 Minutos PrevencionistasDocumento219 páginasCharlas 5 Minutos Prevencionistasmarlene fuentesAún no hay calificaciones
- Taller Modelos AtomicosDocumento2 páginasTaller Modelos AtomicosJenny Patricia Mina Balanta0% (1)
- Q10° Teoría Atómica 1Documento18 páginasQ10° Teoría Atómica 1Luis Hernando López LozanoAún no hay calificaciones
- Modelo AtomicosDocumento29 páginasModelo AtomicosCATALINA JOSELYN VERA PERALTAAún no hay calificaciones
- El Censo, Emilio Carballido.Documento8 páginasEl Censo, Emilio Carballido.Ana100% (1)
- Anexo No 2 Modelos AtómicosDocumento4 páginasAnexo No 2 Modelos AtómicosLuz Nelly Maya OrtizAún no hay calificaciones
- Modelos AtomicosDocumento15 páginasModelos Atomicosángel Medrano100% (1)
- El Glucocálix o Cubierta CelularDocumento3 páginasEl Glucocálix o Cubierta CelularAna Isabel Andrade Cedeño100% (1)
- (D) 2019. Guía de Anfibios, Reptiles y Aves de La Provincia de El Oro. Segunda EdiciónDocumento430 páginas(D) 2019. Guía de Anfibios, Reptiles y Aves de La Provincia de El Oro. Segunda EdiciónJuan Carlos SánchezAún no hay calificaciones
- Rectificación de Altas CorrientesDocumento109 páginasRectificación de Altas CorrientescamiloAún no hay calificaciones
- Teoría Atómica y Estructura de La Materia Equipo 3Documento23 páginasTeoría Atómica y Estructura de La Materia Equipo 3lesliemartinezAún no hay calificaciones
- Quimica BasicaDocumento2 páginasQuimica BasicaGuillermo Montero HerreraAún no hay calificaciones
- Tabla Periódica de Los Elementos y Modelos AtómicosDocumento13 páginasTabla Periódica de Los Elementos y Modelos AtómicosEmy CasadoAún no hay calificaciones
- TEORIA ATÓMICA (Victor Adrian Perez Hernandez)Documento9 páginasTEORIA ATÓMICA (Victor Adrian Perez Hernandez)adrian perezAún no hay calificaciones
- Modelos AtómicosDocumento19 páginasModelos AtómicosLarissa VerásteguiAún no hay calificaciones
- SalinasCarmona Yoselin M14S1 ElatomoDocumento3 páginasSalinasCarmona Yoselin M14S1 ElatomoYoselin Salinas CarmonaAún no hay calificaciones
- Estructura Atomica II - QuimicaDocumento4 páginasEstructura Atomica II - QuimicaBrinny VelazcoAún no hay calificaciones
- Los Modelos Atomicos y Su HistoriaDocumento5 páginasLos Modelos Atomicos y Su HistoriaKennia Rivera GuapulemaAún no hay calificaciones
- Cuadro Comparativo de Los Modelos AtomicosDocumento1 páginaCuadro Comparativo de Los Modelos Atomicoslautarobre10Aún no hay calificaciones
- F12ee9734e1edf70 20230708 140930rCEsIDocumento12 páginasF12ee9734e1edf70 20230708 140930rCEsI670EAún no hay calificaciones
- Presentacion Power Point Episodio 4 IIDocumento24 páginasPresentacion Power Point Episodio 4 IIMaría Eugenia García CarralAún no hay calificaciones
- Tema n1. Teorias AtomicasDocumento21 páginasTema n1. Teorias AtomicasYovana SaavedraAún no hay calificaciones
- Taipe Chachayma Edith Sesión 5Documento14 páginasTaipe Chachayma Edith Sesión 5Edith Rosmery Taipe ChachaymaAún no hay calificaciones
- InfografíaDocumento1 páginaInfografíaLorena CastroAún no hay calificaciones
- Linea de TiempoDocumento2 páginasLinea de TiempoAlbamarina MarinAún no hay calificaciones
- Unidad 2. Estructura AtómicaDocumento33 páginasUnidad 2. Estructura AtómicaPhoenix Juegos y masAún no hay calificaciones
- Tarea Evidencias de Estructura AtómicaDocumento5 páginasTarea Evidencias de Estructura Atómicaalanntorres09ctrlAún no hay calificaciones
- DocumentoDocumento16 páginasDocumentoGénesis sari Marcial mazaAún no hay calificaciones
- Evolucion de Las TeoriasDocumento17 páginasEvolucion de Las TeoriasMANUEL EDUARDO ANGULO DOMINGUEZAún no hay calificaciones
- ÁtomosDocumento10 páginasÁtomosYabil LopezAún no hay calificaciones
- CUADRODocumento1 páginaCUADROPerez AlhanAún no hay calificaciones
- Cuadro Comparativo Modelos Atomicos.Documento3 páginasCuadro Comparativo Modelos Atomicos.Andres CanoAún no hay calificaciones
- Taller Modelos AtomicosDocumento3 páginasTaller Modelos AtomicosAleja DiazAún no hay calificaciones
- Modélo Atómico-1ro QuímicaDocumento13 páginasModélo Atómico-1ro QuímicaThe worldAún no hay calificaciones
- Modelos AtómicosDocumento27 páginasModelos AtómicosMiryam Aguilar Velásquez100% (1)
- Modelos AtomicosDocumento4 páginasModelos AtomicosAlo Peralta100% (1)
- Los Modelos AtómicosDocumento16 páginasLos Modelos AtómicosBrigite Veronica Sonco GonzaloAún no hay calificaciones
- Linea Del Tiempo PDFDocumento1 páginaLinea Del Tiempo PDFFranklin Enmanuel Cordero BobadillaAún no hay calificaciones
- Linea de Tiempo Modelos AtomicosDocumento1 páginaLinea de Tiempo Modelos AtomicosMARCO ANTONIO RAMIREZ REYESAún no hay calificaciones
- Modelo AtomicoDocumento2 páginasModelo AtomicoJustiber Ibarra100% (1)
- Modelos AtomicosDocumento4 páginasModelos AtomicosCitlali MezaAún no hay calificaciones
- Linea Del TiempoDocumento3 páginasLinea Del TiempoZaidy HAún no hay calificaciones
- Ciencia Del Futuro Basada en Los Modelos AtómicosDocumento2 páginasCiencia Del Futuro Basada en Los Modelos AtómicosCarolina AvilaAún no hay calificaciones
- Infografía Línea Del Tiempo Timeline Historia Moderno Creativo MulticolorDocumento3 páginasInfografía Línea Del Tiempo Timeline Historia Moderno Creativo MulticolorRosannksAún no hay calificaciones
- Modelos AtómicosDocumento18 páginasModelos AtómicosCarlos RamirezAún no hay calificaciones
- Modelo de Esfera SolidaDocumento4 páginasModelo de Esfera Solidaamezcuasantiago2006Aún no hay calificaciones
- Teoría AtómicaDocumento26 páginasTeoría Atómicaalcatraso perezAún no hay calificaciones
- Modelo AtomicoDocumento4 páginasModelo AtomicoAlan BuenoAún no hay calificaciones
- Que Es Un Modelo AtomicoDocumento8 páginasQue Es Un Modelo AtomicoKatheryn ZárateAún no hay calificaciones
- Teorías AtómicasDocumento17 páginasTeorías AtómicasAnaAún no hay calificaciones
- 6 Modelos de Átomos Aportes y AñosDocumento3 páginas6 Modelos de Átomos Aportes y AñosDany SolanoAún no hay calificaciones
- Atomos y Modelos AtomicosDocumento4 páginasAtomos y Modelos AtomicosIgnacio Nuñez FuentesAún no hay calificaciones
- Portafolio de Evidencias 1Documento76 páginasPortafolio de Evidencias 1garciasanchezsergio2021370177Aún no hay calificaciones
- Modelo de Carta Derecho CivilDocumento8 páginasModelo de Carta Derecho CivilWilliam castilloAún no hay calificaciones
- Infografía Línea Del Tiempo Modelos AtómicosDocumento2 páginasInfografía Línea Del Tiempo Modelos AtómicosRosannksAún no hay calificaciones
- Fusión NuclearDocumento30 páginasFusión NuclearTrapGameAún no hay calificaciones
- Modelos AtómicosDocumento5 páginasModelos AtómicosTrapGameAún no hay calificaciones
- Infografia Informativa Bellas Artes Cuadros Simple Llamativa AzulDocumento2 páginasInfografia Informativa Bellas Artes Cuadros Simple Llamativa Azulwtgw4nw66gAún no hay calificaciones
- Tema 3 Estructura AtomicaDocumento44 páginasTema 3 Estructura AtomicaCARLOS GONZALO MAMANI QUISPEAún no hay calificaciones
- El ÁtomoDocumento4 páginasEl ÁtomoDamely Olivo AvilesAún no hay calificaciones
- Estructura Atómica 2Documento29 páginasEstructura Atómica 2u20231212683Aún no hay calificaciones
- Bono DemográficoDocumento59 páginasBono DemográficoGustavo Garabito BallesterosAún no hay calificaciones
- Escuela Superior Politécnica Del Litoral: Previo A La Obtención Del Título deDocumento134 páginasEscuela Superior Politécnica Del Litoral: Previo A La Obtención Del Título dewpacheco.rhelecAún no hay calificaciones
- Patente Ep2853801a1Documento10 páginasPatente Ep2853801a1Santiiago VEAún no hay calificaciones
- D T MDocumento38 páginasD T MPedro Reynaldo Marin DominguezAún no hay calificaciones
- Sociedad Anonima CerradaDocumento4 páginasSociedad Anonima CerradaPriscila Fernandez Reyes100% (2)
- Tabla de ConversionDocumento2 páginasTabla de ConversionDulce Mariah MárquezAún no hay calificaciones
- Taller Liderazgo Transformador ParacompartirDocumento13 páginasTaller Liderazgo Transformador ParacompartirCeciliaGallegosAún no hay calificaciones
- U6 Electricidad ActividadesDocumento19 páginasU6 Electricidad ActividadesjavicarpsAún no hay calificaciones
- Curso Aire Acondicionado 1parteDocumento11 páginasCurso Aire Acondicionado 1parteYerith Villarreal CuentasAún no hay calificaciones
- El Auditor Interno en La Gestión de Riesgos CorporativosDocumento16 páginasEl Auditor Interno en La Gestión de Riesgos CorporativosHSE TRANSNAVALAún no hay calificaciones
- Estructura de Un Sistema Servo Controlado Imi91Documento21 páginasEstructura de Un Sistema Servo Controlado Imi91Javier Pat33% (6)
- 2° Abril - Educación FisicaDocumento11 páginas2° Abril - Educación FisicaSHIRLEYAún no hay calificaciones
- 3.5 Esquemas de Instalaciones y Diagramas de Conexiones EléctricasDocumento25 páginas3.5 Esquemas de Instalaciones y Diagramas de Conexiones EléctricasArq Noe Miguel67% (3)
- 1.5 Calculo de Perdidas de PresionDocumento11 páginas1.5 Calculo de Perdidas de Presionfrancisco0% (1)
- Selectividad Economía y Organización de EmpresasDocumento32 páginasSelectividad Economía y Organización de EmpresasJosé Luis100% (9)
- 6°? S9 Plan Juan PabloDocumento16 páginas6°? S9 Plan Juan Pablocortes bogarinAún no hay calificaciones
- Taller 5 Prorrateo Iva PDFDocumento14 páginasTaller 5 Prorrateo Iva PDFEdisson VARGAS RUBIO0% (1)
- Sesgo y CurtosisDocumento2 páginasSesgo y CurtosismarcelomchapaAún no hay calificaciones
- Adam SandlerDocumento2 páginasAdam SandlerMiguel Angel Aguilar EstanislaoAún no hay calificaciones
- Python MicroPythonDocumento2 páginasPython MicroPythonMiguel CastañedaAún no hay calificaciones
- Triptico RacsDocumento2 páginasTriptico Racsgreina24Aún no hay calificaciones
- Seminario Transferencia de Calor Por Conducción y ConvecciónDocumento4 páginasSeminario Transferencia de Calor Por Conducción y ConvecciónbbleanAún no hay calificaciones
- Conta Bili DadDocumento14 páginasConta Bili DadZianiAún no hay calificaciones
- Formato Guardias Enfermeras Periodo 2023Documento1 páginaFormato Guardias Enfermeras Periodo 2023JielAún no hay calificaciones