Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Postulados de Niels Bohr
Cargado por
Koko Pnc GuzmánDescripción original:
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Postulados de Niels Bohr
Cargado por
Koko Pnc GuzmánCopyright:
Formatos disponibles
POSTULADOS DE NIELS BOHR
Los diferentes á tomos está n formados por distintos á tomos
Los á tomos son indivisibles y conservan sus características cuando ocurre una reacció n quimica
El electró n solo podrá girar en ciertas ó rbitas circulares de energía y radios determinados, y al
moverse en ellas el electró n no radiará energía. En ellas la energía del electró n será constante.
En estas ó rbitas se cumplirá que el momento angular del electró n será mú ltiplo entero de h/2∏.
Estas será n las ú nicas ó rbitas posibles.
El electró n solo emitirá energía cuando estando en una de estas ó rbitas pase a otra de menor
energía.
ACTIVIDAD: Investiga en tu tabla perió dica los siguientes datos para completar la tabla
Nombre del elemento Símbolo Numero atómico Masa atómica
Sodio
Hierro
Bario
Niobio
Oxigeno
Silicio
Aluminio
Azufre
Boro
Cobre
Potasio
Plata
Un ENLACE QUÍMICO es el proceso químico responsable de las interacciones atractivas entre
átomos y moléculas, que confiere estabilidad a los compuestos químicos diatómicas y poli atómicos.
Los enlaces químicos son fuerzas intramoleculares, que mantienen a los átomos unidos en las
moléculas.
Un enlace se refiere a la cantidad de pares de electrones que interactúan en un enlace entre 2
átomos.
- En un ENLACE SENCILLO intervienen 2 electrones. Pueden ser aportados uno por cada átomo, o
ambos por el mismo átomo
- En un ENLACE DOBLE intervienen 4 electrones (2 pares)
- En un ENLACE TRIPLE intervienen 6 electrones (3 pares)
Un enlace triple es más fuerte que uno doble y uno doble es más fuerte que uno sencillo
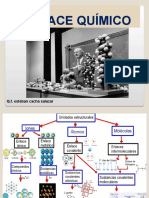
EL ENLACE QUIMICO
Es la unión entre átomos
Puede ser
IONICO COVALENTE METALICO
Se une un METAL y un Se unen dos NO METALES Se unen dos
NO METAL METALES
También podría gustarte
- Enlace Quimico IonicoDocumento16 páginasEnlace Quimico IonicoEdu SllAún no hay calificaciones
- Clase 2 Ciencia de MaterialesDocumento20 páginasClase 2 Ciencia de MaterialesAna Maria PerezAún no hay calificaciones
- Enlace QuímicoDocumento23 páginasEnlace QuímicoALEXANDER ROBIN ALIAGA EGUSQUIZAAún no hay calificaciones
- U2 Enlace QuimicoDocumento12 páginasU2 Enlace QuimicoEndhir Garcia PerezAún no hay calificaciones
- 2da. Parte de Quimica)Documento16 páginas2da. Parte de Quimica)marggv82Aún no hay calificaciones
- Enlaces QuímicosDocumento26 páginasEnlaces Químicoserick tixiAún no hay calificaciones
- Unidad 04 Enlace QuímicopptxDocumento40 páginasUnidad 04 Enlace QuímicopptxjoelquimicoAún no hay calificaciones
- RESUMENDocumento5 páginasRESUMENzairaibarra2005Aún no hay calificaciones
- Trabajo Fisica y Quimica IntermolecularDocumento27 páginasTrabajo Fisica y Quimica IntermolecularFernando M. TorresAún no hay calificaciones
- Quimica EzDocumento86 páginasQuimica Ezangela zariagaAún no hay calificaciones
- Enlace QuímicoDocumento22 páginasEnlace QuímicoMiChaelEspinozaRiveraAún no hay calificaciones
- CLASE 7-Enlace QuímicoDocumento59 páginasCLASE 7-Enlace Químicojhonnatan loyolaAún no hay calificaciones
- Clase 3 - Enlace Quimico 2024Documento87 páginasClase 3 - Enlace Quimico 2024sylvana maguiñaAún no hay calificaciones
- Tipos de Enlaces QuímicosDocumento1 páginaTipos de Enlaces QuímicosxdAún no hay calificaciones
- Enlaces Quimicos e Interacciones IntermolecularesDocumento5 páginasEnlaces Quimicos e Interacciones Intermolecularesfelipedejesus.2508Aún no hay calificaciones
- Tema 1 Introduccion A La Quimica OrganicaDocumento59 páginasTema 1 Introduccion A La Quimica OrganicaBRANI ARANCIBIA TARDIOAún no hay calificaciones
- QUI1MUNI2N1MAC Estr - Lewis EnlacesDocumento30 páginasQUI1MUNI2N1MAC Estr - Lewis EnlacesjuniorinnovadorAún no hay calificaciones
- Enlace Atómico 2021 BDocumento75 páginasEnlace Atómico 2021 BPEDRO HORACIO VILLANUEVA CARLOAún no hay calificaciones
- Enlaces AtomicosDocumento20 páginasEnlaces AtomicosAnonymous HGEL832Aún no hay calificaciones
- Distribucion ElecrtronicaDocumento12 páginasDistribucion ElecrtronicaJENNIFER DANIELA TOAPANTA CAMACHOAún no hay calificaciones
- Enlaces Quimicos 2010-1Documento82 páginasEnlaces Quimicos 2010-1Juan Diaz ValdezAún no hay calificaciones
- Propiedades Fisicas de Las Sustancias Ionicas, Covalentes, y Metalicas.Documento38 páginasPropiedades Fisicas de Las Sustancias Ionicas, Covalentes, y Metalicas.Bryan Fernando MurilloAún no hay calificaciones
- Ordenamiento Atómico 2021Documento28 páginasOrdenamiento Atómico 2021Federico MarengoAún no hay calificaciones
- Uniones QumicasDocumento7 páginasUniones QumicasCarina CremaschiAún no hay calificaciones
- Qui MicaDocumento20 páginasQui MicaCatalina Rivas MoralesAún no hay calificaciones
- Tipos de Enlaces QuímicaDocumento15 páginasTipos de Enlaces QuímicaGamejorchi Retro GamesAún no hay calificaciones
- UNIDAD 2 - Química MECDocumento26 páginasUNIDAD 2 - Química MECJonathan Ramiro Grijalva herreraAún no hay calificaciones
- Quimica 2Documento34 páginasQuimica 2mrjuegosAún no hay calificaciones
- Reporte de Laboratorio de Enlaces Quimico. Enlace IónicoDocumento4 páginasReporte de Laboratorio de Enlaces Quimico. Enlace IónicoNeighbors BandAún no hay calificaciones
- Enlaces QuímicosDocumento14 páginasEnlaces QuímicosPapelería ChayoAún no hay calificaciones
- Enlaces Químicos y FísicosDocumento80 páginasEnlaces Químicos y FísicosFrank Silva Fonseca0% (1)
- J. Enlace QuimicoDocumento47 páginasJ. Enlace QuimicoAngelica RubioAún no hay calificaciones
- Enlace QuímicoDocumento23 páginasEnlace Químicomorenoluja690Aún no hay calificaciones
- Resumo BioquímicaDocumento2 páginasResumo BioquímicaCamila DiniAún no hay calificaciones
- Los Covalentes, Enlaces Iónicos, Enlace Metálico, Electronegatividad y ElectropositividadDocumento11 páginasLos Covalentes, Enlaces Iónicos, Enlace Metálico, Electronegatividad y ElectropositividadCristina PerezAún no hay calificaciones
- Tipos de Enlaces Quimicos (Cuadro Comparativo)Documento3 páginasTipos de Enlaces Quimicos (Cuadro Comparativo)Jesus Armando Martinez100% (1)
- Teoría de Orbital Molecular PDFDocumento63 páginasTeoría de Orbital Molecular PDFcesar2fernando2floreAún no hay calificaciones
- Propiedades Periódicas y Uniones QuimicasDocumento14 páginasPropiedades Periódicas y Uniones QuimicasTécnicos QuímicosAún no hay calificaciones
- Capítulo 4Documento2 páginasCapítulo 4Carlos Jiménez RomeroAún no hay calificaciones
- Clase 6 Unidad 3 Enlace Quimico (2.)Documento15 páginasClase 6 Unidad 3 Enlace Quimico (2.)JHORMAN JOFFRE ZAMBRANO SANTANAAún no hay calificaciones
- Enlace QuímicoDocumento180 páginasEnlace QuímicoJose Ignacio Flores GonzalesAún no hay calificaciones
- Informe 8Documento2 páginasInforme 8Yoselin Eliana Espinoza LeónAún no hay calificaciones
- Complemento Teórico y Actividades III. Química 6ADocumento5 páginasComplemento Teórico y Actividades III. Química 6Alalavienr-Aún no hay calificaciones
- 1AM1. Equipo 4 - EnlacesDocumento20 páginas1AM1. Equipo 4 - EnlacesGarcía Martínez VictorAún no hay calificaciones
- Diapositivas - Introduccion A Los Enlaces InteratomicosDocumento28 páginasDiapositivas - Introduccion A Los Enlaces InteratomicosJose Carlos Villanueva VidalAún no hay calificaciones
- Unidad 2 QuimicaDocumento33 páginasUnidad 2 QuimicaJose ManuelAún no hay calificaciones
- Quimica TOMDocumento61 páginasQuimica TOMAronAlexisGomezMirandaAún no hay calificaciones
- Tema 4Documento18 páginasTema 4alejasp1708Aún no hay calificaciones
- El Enlace MetálicoDocumento4 páginasEl Enlace MetálicoindiraAún no hay calificaciones
- Enlaces QuimicosDocumento15 páginasEnlaces QuimicosMoisesito EspinozaAún no hay calificaciones
- 2023-6-26 - Instituto Monseñor Roubineau - Físico - Química - Teoría - Uniones Qcas 2023 3FDocumento16 páginas2023-6-26 - Instituto Monseñor Roubineau - Físico - Química - Teoría - Uniones Qcas 2023 3FGaelChillAún no hay calificaciones
- Enlace QuímicoDocumento20 páginasEnlace QuímicoBelen Alessandra Jayo HernandezAún no hay calificaciones
- Semana 3 - Tabla Periódica - Enlace Químico - Enlace IónicoDocumento35 páginasSemana 3 - Tabla Periódica - Enlace Químico - Enlace IónicoALVARO LUIS PASQUEL MEZAAún no hay calificaciones
- Enlaces Químicos P II 2020Documento30 páginasEnlaces Químicos P II 2020LilithAún no hay calificaciones
- Enlaces Atomicos y Estructturas CristalinasDocumento13 páginasEnlaces Atomicos y Estructturas CristalinasMarcial GonzalezAún no hay calificaciones
- Enlace QuimicoDocumento2 páginasEnlace QuimicoChristian Malagón100% (1)
- PROFUNDIZACION (Reacciones y Enlaces Químicos)Documento8 páginasPROFUNDIZACION (Reacciones y Enlaces Químicos)Benjamín Mir EstAún no hay calificaciones
- Objetivo 3 EnlacesDocumento11 páginasObjetivo 3 EnlacesIbeth Henao de AponteAún no hay calificaciones
- Teoría electromagnética para estudiantes de ingeniería: Notas de claseDe EverandTeoría electromagnética para estudiantes de ingeniería: Notas de claseCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Ejerc NeutralizacionDocumento1 páginaEjerc NeutralizacionKoko Pnc GuzmánAún no hay calificaciones
- Encuesta General de Intereses Primaria y SecundariaDocumento3 páginasEncuesta General de Intereses Primaria y SecundariaKoko Pnc GuzmánAún no hay calificaciones
- Test Relaciones AfectivasDocumento2 páginasTest Relaciones AfectivasKoko Pnc GuzmánAún no hay calificaciones
- Autoevaluación Propuesta DidácticaDocumento1 páginaAutoevaluación Propuesta DidácticaKoko Pnc GuzmánAún no hay calificaciones
- Oxidación Del AguacateDocumento2 páginasOxidación Del AguacateKoko Pnc GuzmánAún no hay calificaciones
- 10 Rasgos de Perfil de EgresoDocumento1 página10 Rasgos de Perfil de EgresoKoko Pnc GuzmánAún no hay calificaciones
- Proyectos ComunitariosDocumento14 páginasProyectos ComunitariosKoko Pnc GuzmánAún no hay calificaciones
- Dosificación Química 2011Documento6 páginasDosificación Química 2011Koko Pnc GuzmánAún no hay calificaciones
- Infraestructura y EquipamientoDocumento2 páginasInfraestructura y EquipamientoKoko Pnc GuzmánAún no hay calificaciones
- Técnicas e Instrumentos de Evaluación.Documento39 páginasTécnicas e Instrumentos de Evaluación.Koko Pnc GuzmánAún no hay calificaciones