Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Odontoblastos
Cargado por
Daniela Ruiz OrtuñoTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Odontoblastos
Cargado por
Daniela Ruiz OrtuñoCopyright:
Formatos disponibles
S.
a, b a,c b a
Rajan *, A. Ljunggren , D.J. Manton , A.E Björkner , M. McCullough
2020 ODONTOBLASTOS POSTMITÓTICOS EN LA SALUD, LA ENFERMEDAD Y LA
REGENERACIÓN
Archives of Oral Biology, volume 109, No. 104591.
Revisión Bibliográfica
RESUMEN
Descripción del ciclo de vida de los odontoblastos, una visión general de las complejas
interacciones moleculares conocidas que ocurren cuando la salud de la pulpa dental es desafiada y
las estrategias de manejo actuales y futuras en dientes vitales y no vitales. Métodos: Se realizó una
búsqueda bibliográfica en las bases de datos electrónicas que incluyen MEDLINE (1966-abril 2019),
CINAHL (1982-abril 2019), EMBASE y EMBASE Classic (1947-abril 2019), y se realizaron búsquedas
manuales de las referencias recuperadas utilizando los siguientes términos MESH 'odontoblast*',
'inflammation', 'dental pulp*', 'wound healing' y 'regenerative medicine'. Resultados: Los
odontoblastos tienen una función sensorial y de mecano-transducción para detectar los estímulos
externos que desafían a la pulpa dental. Al detectarlos, los odontoblastos estimulan la inmunidad
innata activando mecanismos de defensa clave en los mecanismos de curación y reparación del
diente. Una mejor comprensión del papel de los odontoblastos dentro del complejo de la pulpa
dental permitirá una oportunidad de gestión biológica para eliminar la causa de la agresión a la
pulpa dental, modular el proceso inflamatorio y promover las capacidades de curación y
reparación del diente. Las estrategias actuales incluyen el uso de medicamentos convencionales
para la pulpa dental, mientras que los métodos más nuevos incluyen moléculas bioactivas,
modificaciones epigenéticas e ingeniería de tejidos. Conclusión: Los métodos de medicina
regenerativa están en su fase inicial y experimental en el mejor de los casos. Esta revisión pone de
relieve la dirección futura de la gestión de la caries dental y, en consecuencia, de la investigación.
Introducción El Instituto Nacional de Investigación Dental y Craneofacial define que la medicina
regenerativa aprovecha las propiedades de crecimiento y curación del cuerpo para reparar o
sustituir células, tejidos u órganos dañados. Los investigadores recurren a los campos de la
biología de las células madre y del desarrollo, la bioingeniería, la ciencia de los materiales y la
edición de genes, entre otros, para desarrollar terapias regenerativas seguras y eficaces (NIDCR,
2018). Actualmente en odontología, las principales células a las que se dirige la medicina dental
regenerativa son los odontoblastos y las células madre de la pulpa dental. El crecimiento y las
propiedades de curación del complejo pulpar dental vital son asistidos por la aplicación de
materiales bioactivos. La sustitución del complejo pulpar dental dañado es la investigación
relacionada con la ingeniería de tejidos. La endodoncia regenerativa es "un procedimiento de base
biológica diseñado para sustituir la estructura dental dañada, incluida la dentina y la estructura
radicular, así como las células del complejo pulpar-dentinario" (Murray, Garcia-Godoy, &
Hargreaves, 2007). Los odontoblastos son células postmitóticas que se mantienen durante toda la
vida del diente hasta que se produce la muerte celular, ya sea por traumatismo, enfermedad o
apoptosis. Su función principal es la de depositar la dentina primaria, secundaria y terciaria en los
dientes. Sin embargo, también desempeñan un papel fundamental en el mantenimiento
Ricardo Mora Torres pág. 1
fisiológico de la pulpa y, en caso de lesión, tienen la capacidad de desencadenar una respuesta
inmunitaria defensiva que ayuda al diente a curarse y repararse (dentina terciaria). Esta oportuna
revisión ofrece una visión general de los conocimientos actuales sobre el ciclo de vida de los
odontoblastos y su papel en la inmunidad innata, que ayudará a los clínicos e investigadores a
desarrollar métodos reproducibles en la consulta para diagnosticar con precisión las
enfermedades de la pulpa dental. Posteriormente, utilizar este conocimiento para la aplicación de
los enfoques actuales de la medicina regenerativa para ayudar a los odontoblastos en la curación y
reparación tras la eliminación del factor causante de la enfermedad. Se revisarán las tendencias y
los posibles métodos que utilizan moléculas bioactivas, modificaciones epigenéticas e ingeniería
de tejidos.
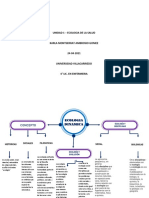
El ciclo de vida original fue introducido por Couve (Couve, 1986), que describió cuatro fenotipos
funcionales: preodontoblasto, secretor, transicional y envejecido. Sin embargo, esto se actualizó
recientemente a fenotipos de odontoblasto preodonto, secretor, maduro y viejo (Couve, Osorio, &
Schmachtenberg, 2013)(Fig. 1). En el estadio de preodontoblasto las células son cortas, cilíndricas
y de 15 μmin de altura (Couve, 1986). Las células carecen de polaridad en este estadio. Los
centríolos se localizan cerca del aparato de Golgi poco definido, formando el cilio primario. El
retículo endoplásmico rugoso (RER) se observa en toda la célula a medida que se desarrolla el
mecanismo intracelular para la producción de proteínas. La célula sigue alargándose a medida que
pasa del estadio de preodontoblasto al estadio de secreción. Los odontoblastos en fase secretora
(Fig. 1A) forman la clásica capa única de células columnares de 50μm de altura que están
altamente polarizadas y conectadas entre sí mediante gap junctions y complejos de unión (Couve,
1986). Las uniones gap conectan los odontoblastos entre sí y con los fibroblastos de la pulpa
dental en la región subodontoblástica en la base de los odontoblastos. Estas uniones gap facilitan
el movimiento de iones y moléculas, y permiten la "comunicación" entre las células, mientras que
los complejos gap se encuentran en el polo apical entre el cuerpo celular del odontoblasto y los
procesos del odontoblasto que progresan hacia la zona predentinaria donde se descarga el
transporte activo de moléculas secretoras durante la etapa secretora (Sasaki & Garant, 1996). El
RER se observa en el extremo terminal de la célula, cerca del núcleo, donde se sintetizan las
proteínas y se envían al aparato de Golgi para su empaquetamiento y distribución. Las
mitocondrias están dispersas por toda la célula para ayudar suministrando energía para el
transporte de las moléculas secretoras dentro y hacia el polo apical del proceso odontoblástico.
Durante la etapa secretora, se ha informado de que los odontoblastos producen activamente
dentina primaria a un ritmo de 4μm por día (Farges et al., 2015)o de 4-8μm por día (Bleicher,
2014; Couve, 1986; Simon et al., 2009) durante 2-3 años de forma continua. Durante la
dentinogénesis primaria (antes de la erupción del diente), se ha observado una alta expresión de
fosfoproteínas y, en particular, de la fosfoproteína ácida de la matriz dentinaria (DMP)-1 (Balic y
Mina, 2011). La predentina es rica en matriz extracelular (ECM), como el colágeno de tipo 1 (90%),
proteínas-glicoproteínas no colágenas, proteoglicanos y fosfoproteínas dentinarias DMP-1 y
sialofosfoproteína dentinaria (DSPP) (Kawasaki & Weiss, 2008). La DMP-1 y la DSPP son los
biomarcadores de la producción activa de dentina (Goldberg, Kulkarni, Young y Boskey, 2011), lo
que indica que el odontoblasto se encuentra en la fase de secreción.
El odontoblasto se transforma de la etapa secretora (dentinogénesis primaria) a la madura (Fig.
1B) (dentinogénesis secundaria) cuando se completa la formación de la corona y el diente
Ricardo Mora Torres pág. 2
erupciona. Los cambios se observan en el fenotipo celular y en la reducción de la tasa de secreción
de dentina a 0,4-0,5 μm por día (Bleicher, 2014; Couve, 1986; Farges et al., 2015; Simon et al.,
2009). Las células del odontoblasto se vuelven más estrechas y menos polarizadas. La autofagia
está implicada en la homeostasis celular, donde se reciclan los patógenos, los orgánulos dañados y
las proteínas (Couve et al., 2013; Pei, Wang, Chen y Zhang, 2016; Qian, Fang y Wang, 2017; Zhang
y Chen, 2018). Este es un proceso esencial que afecta al desarrollo, la diferenciación, la inmunidad
y el envejecimiento en las células postmitóticas y que está mediado por el lisosoma. Debido al
aumento de la actividad autofágica, se observa una reducción de orgánulos (RER, aparato de Golgi
y mitocondrias) con aumento de vacuolas autofágicas (Couve, 1986). Del mismo modo, hay una
regulación a la baja de la producción de DMP-1 (Balic y Mina, 2011). Este proceso continúa a
medida que los odontoblastos envejecen. Durante el estadio de odontoblasto viejo (Fig. 1C), las
células son más cortas (45μm de altura), están apiñadas y tienen un aspecto pseudoestratificado.
El citoplasma tiene una reducción significativa de orgánulos, no hay gránulos de secreción y tiene
grandes vacuolas llenas de lípidos (acumulación de lipofuscina) debido a la disminución de la
actividad lisosomal. Los depósitos de lipofuscina tienden a acumularse debido a la disminución de
la eficiencia del sistema autofágico-lisosomal en el odontoblasto viejo (Couve, 1986) y pueden ser
utilizados como un marcador de edad (Rubinsztein, Marino, & Kroemer, 2011). En condiciones
patológicas, un odontoblasto maduro puede aumentar la producción de dentina volviendo a la
fase secretora (Couve, 1986). El aumento de la deposición de dentina puede producirse en las
zonas intratubulares, peritubulares y en la dentina terciaria en un intento de disminuir la
permeabilidad de la dentina y reducir la agresión a la pulpa dental (Mjor, 2009). La dentina
terciaria producida tiene dos tipos distintos: dentina reactiva y reparadora (Farges et al., 2015;
Smith et al., 1995). La vía de las proteínas quinasas activadas por el mitógeno p38 (MAPKs),
responsable de funciones celulares básicas como la proliferación, la diferenciación, la motilidad, la
respuesta al estrés, la apoptosis y la supervivencia, puede estar implicada en la transición de la
actividad de la dentinogénesis secundaria a la terciaria a través de la liberación de la superfamilia
del factor de crecimiento transformante (TGF) (Simon, Smith, Berdal, Lumley y Cooper, 2010). El
TGF-β1 y el TGF-β3 promueven activamente la diferenciación de los odontoblastos y la
dentinogénesis terciaria (condiciones de reparación/curación) (Simon et al., 2010). Por lo tanto, los
miembros de la superfamilia TGF son marcadores de la diferenciación de los odontoblastos (Simon
et al., 2010; Smith, Smith, Shelton y Cooper, 2012). La dentina reactiva es producida por las células
odontoblásticas existentes expuestas a estímulos externos leves. La dentina tubular secretada
tiene características similares a la dentina primaria y secundaria. Sin embargo, si los estímulos se
prolongan con mayor intensidad, los subproductos bacterianos pueden causar daños irreversibles
en las células del odontoblasto. La región perivascular es rica en células madre de la pulpa dental
(DPSC) que desempeñan un papel en la homeostasis y la reparación postnatal (Shi y Gronthos,
2003). El sistema del complemento activado proporciona fragmentos de C5a (consta de 74
aminoácidos) que ayudan a aumentar el reclutamiento de DPSC (Chmilewsky, Jeanneau, Laurent,
Kirschfink y About, 2013), mientras que los fragmentos de C3a (consta de 77 aminoácidos)
aumentan la proliferación de DPSC y guían su migración al lugar de la infección (Rufas, Jeanneau,
Rombouts, Laurent y About, 2016). Las DPSC se someten a una compleja cascada de respuestas
celulares que implica la diferenciación en células similares a los odontoblastos que secretan
dentina reparadora en un intento de bloquear los estímulos ofensivos para que no lleguen a la
pulpa dental (Farges et al., 2015). Hay una falta de estructura organizada en la dentina reparadora,
Ricardo Mora Torres pág. 3
se pierde la característica de la dentina tubular y se deposita un material calcificado más amorfo o
similar a un puente calcificado para evitar la invasión bacteriana en el espacio de la pulpa dental.
La progresión de la caries es una interacción compleja dentro de la biopelícula dental en la que el
equilibrio neto de las bacterias acidógenas, acidogénicas y neutralizadoras afecta al cambio de
actividad de la caries hacia la desmineralización, la estabilidad o la remineralización (Marsh, 2016
específica. Un aumento de los leucocitos, NK (natural killer) y células dendríticas (DC), tanto del
sistema local como del circulatorio, migran al lugar de la infección. Los neutrófilos son reclutados
para engullir y destruir los patógenos. Los patógenos que no son destruidos son neutralizados o
desactivados por los neutrófilos, continuando el proceso infeccioso. Para ayudar a la afluencia de
células al lugar de la lesión, la angiogénesis se produce junto con la detección del patógeno en las
primeras fases de la inmunidad innata (Farges et al., 2015). La angiogénesis y la neurogénesis son
componentes críticos en el proceso de curación y reparación en cualquier parte del cuerpo,
incluido el complejo pulpar dental. La dentina desmineralizada libera factores de crecimiento
proangiogénicos que contribuyen a aumentar la vascularidad en el lugar de la lesión (Smith,
Duncan, Diogenes, Simon y Cooper, 2016). Los vasos sanguíneos también liberan mediadores
inflamatorios, como histamina, neuropéptidos, prostaglandinas y NO, que aumentan la
permeabilidad y la vascularidad de la pulpa afectada permitiendo el reclutamiento de células
inmunitarias (Farges et al., 2015). La pulpa dental está ricamente inervada y cuando es estimulada
expresa potentes neuropéptidos como el péptido relacionado con el gen de la calcitonina, la
sustancia P y el neuropéptido Y (Byers y Narhi, 1999) que estimulan el brote de terminaciones
nerviosas en el lugar de la lesión y la reparación (Byers, Suzuki y Maeda, 2003; Rajan y otros,
2014). El espacio intersticial se expande y se vuelve rico en citoquinas, leucotrienos, proteasas y
factores del complemento. Se cree que el sistema del complemento se activa por primera vez en
las células de fibroblastos de la pulpa a través de las vías clásica, alternativa y de la lectina para
promover la inmunidad adaptativa principalmente mediante los fragmentos de anafilatoxinas C3a
y C5a (Ehrengruber, Geiser y Deranleau, 1994; Hartmann et al., 1997; Nataf, Davoust, Ames y
Barnum, 1999). Estos fragmentos inician cambios vasculares y celulares. A medida que el proceso
inflamatorio avanza, los macrófagos, las CD y las células NK desencadenan la activación de la
inmunidad adaptativa, compuesta por células T y B que se dirigen específicamente al patógeno
invasor (Farges et al., 2015).. La persistencia de los estímulos nocivos da lugar a que el sistema
inmunitario se active por completo y provoque un daño importante tanto al huésped como al
patógeno. La inflamación de bajo grado de la pulpa dental tiene un papel importante en la
estimulación de la reparación. La autofagia se activa para proteger las células del daño. La
diferenciación de los odontoblastos se regula mediante la supresión de la vía de señalización
NF(factor nuclear)-kappaB (Couve et al., 2013; Pei et al., 2016; Zhang & Chen, 2018). Sin embargo,
como la pulpa dental se encuentra en un espacio cerrado, la inflamación incontrolada puede
contribuir a la necrosis de la pulpa dental (Cooper, Holder, & Smith, 2014; Goldberg, Njeh, &
Uzunoglu, 2015). Por lo tanto, la producción de reguladores inmunitarios es fundamental para
lograr un equilibrio entre la señalización inmunitaria o la inhibición de la reparación y la
regeneración (dentinogénesis terciaria). Los reguladores inflamatorios como la IL-10, IL-4, IL-13,
iTreg y adrenomedullina (ADM) son críticos ya que ayudan a regular y controlar la respuesta
inmune excesiva dentro del tejido de la pulpa dental, limitando el daño al huésped. La rica
inervación también coordina la nocicepción protectora y regula la inflamación y la función de los
odontoblastos (Smith et al., 2016). Cuando los odontoblastos están sometidos a un estrés
Ricardo Mora Torres pág. 4
continuo (inflamación en fase tardía), la autofagia ayuda a controlar la inflamación induciendo la
apoptosis celular y promoviendo la supervivencia de los odontoblastos restantes (Pei et al., 2015).
Existe una relación interdependiente entre la inflamación, la angiogénesis y la regeneración (Smith
et al., 2016) en la reparación del tejido mineralizado y el proceso de curación. Cada vez hay más
pruebas de que el mecanismo epigenético también puede contribuir a la regulación del proceso
inflamatorio en la pulpa dental (Cardoso et al., 2010; Hui et al., 2014, 2017). La infección
bacteriana es el principal factor etiológico que influye en la inflamación de la pulpa dental
(Kakehashi, Stanley y Fitzgerald, 1965; Trope, 2008), por lo que puede tener un efecto ambiental
en la estimulación de los genes inflamatorios (Hui et al., 2017; Lindroth y Park, 2013). Los genes
regulan la inflamación a través de las citocinas IL-1, IL-2, IL-6, IL-8, IL-10 e IL-12 (Fitzpatrick &
Wilson, 2003; Wen, Schaller, Dou, Hogaboam, & Kunkel, 2008), interferón gamma (IFN- γ)(White,
Watt, Holt, & Holt, 2002), TLR-2 y TLR4(Shuto et al., 2006; Takahashi, Sugi, Hosono, &
Kaminogawa, 2009). 2.3. Papel de los marcadores biológicos en la enfermedad y curación de la
pulpa dental El diagnóstico clínico basado en la historia del dolor, los signos y síntomas clínicos, las
pruebas radiográficas y de sensibilidad, ha sido considerado poco fiable por algunos investigadores
(Dummer, Hicks, & Huws, 1980; Garfunkel, Sela, & Ulmansky, 1973; Seltzer, Bender, & Ziontz,
1963) y preciso por otros (Pigg, Nixdorf, Nguyen, Law, National Dental Practice-Based Research
Network Collaborative, & G., 2016; Ricucci, Loghin, & Siqueira, 2014). Por lo tanto, los
investigadores han intentado utilizar marcadores biológicos de inflamación pulpar para ayudar a
mejorar el diagnóstico del estado de la pulpa, ya que un diagnóstico preciso guiará el manejo de la
pulpa y el posterior pronóstico del tratamiento. Una reciente revisión sistemática analizó los
biomarcadores disponibles en relación con la inflamación pulpar (Rechenberg, Galicia, & Peters,
2016). Basándose en 57 de 847 estudios que cumplían los criterios para el análisis cualitativo,
informaron de 64 marcadores biológicos en pulpas irreversiblemente inflamadas que eran
estadísticamente diferentes de las pulpas sanas, mientras que 19 marcadores biológicos no lo
eran. Los marcadores biológicos asociados al estado de la pulpa pueden agruparse en los
siguientes: 1) Citocinas (IL-1alfa, IL-1ralfa, IL-1beta,IL-2, IL-4, IL-6, IL-7, IL-8, IL-12p40, IL-13, IL-15,
IL-18, TNF-alfa, TNF-beta, MIP1alfa, MIP-1beta, MIP-3alfa, CCR6, TGF-alfa, TGF-beta1, CXCL10,
SDF-1, Oncostatina M, GM-CSF, GFO, MCP-1, MCP-3, MDC, INF-alfa, G-CSF, Eotaxina, flt3ligando,
Fractalkina, CD40L, sIL-2ralpha, IP-10, PDGF-AA, PDGF-AB/BB, RANTES, Osteocalcina); 2) Proteasas
y otras enzimas (MMP-1, MMP-2, pro-MMP-2, MMP-3, MMP-9, t-PA, SOD, Cu, Zn-SOD, Mn-SOD,
MDA, Elastasa, Capthesin-G, Fosfatasa alcalina, Aspartato aminotransferasa, Catalasa, NADPH-
diaforasa, eNOS, iNOS, cGMP PDE, cAMP PDE, TIMP-2, MPO); 3) Mediadores inflamatorios (AMPc,
GMPc, PGE2, PGF2alfa, alfa-2M, 6-K-PGF1alfa, TXB2, endotoxinas, COX-2, sustancia P,
neuroquinina A, CGRP, neuropéptido Y, VIP, NOD2, VEGF, FGF); 4) Péptidos antimicrobianos (hBD-
1. hBD-2, hBD-3, hBD-4); 5) Otros (receptor de la sustancia P, AAMØ CD163 +expresando CGRPr,
NaV1.8, NaV1.9, miRNAs, EphA7) (Rechenberg et al., 2016). En el 42% (21/50) de los estudios se
utilizó la histología con tinción de hematoxilina y eosina para confirmar ⁵el diagnóstico.
Otros métodos utilizados en el estudio incluían la investigación de la detección de antígenos y
anticuerpos (mediante i. e ensayo multiplex, microarray, western blot, citometría de flujo,
radioinmunoensayo, inmunohistoquímica), expresión de ARN (mediante reacción en cadena de la
polimerasa de transcripción inversa (RT-PCR)), detección de enzimas (mediante ensayo
inmunoenzimático, zimografía, ensayos enzimáticos específicos) y detección y cuantificación de
endotoxinas bacterianas (mediante ensayo de amebocitos de limulus) (Rechenberg et al, 2016).
Ricardo Mora Torres pág. 5
Las opciones experimentales actuales para el diagnóstico molecular pulpar en la consulta incluyen
métodos no invasivos e invasivos (Rechenberg et al., 2016). La mayoría de estos estudios están
relacionados con la enfermedad periodontal y la inflamación. La dificultad con el diagnóstico
pulpar es la obtención de una muestra (es decir, tejido pulpar o sangre pulpar) para el análisis que
implicará procedimientos invasivos para acceder a la pulpa. El método utilizado en el
procedimiento no invasivo es a través de la toma de muestras de fluido crevicular gingival o fluido
dentinal (preparación post-cavidad) mientras que los métodos invasivos implican el acceso a la
cámara pulpar mediante la obtención de fluido periapical a través del conducto radicular
utilizando puntas de papel estériles o sangre pulpar coronal con bolitas de algodón estériles
(Rechenberg et al., 2016). La contaminación, lo invasivo del procedimiento y la cantidad de la
muestra obtenida son las principales dificultades a las que se enfrenta el diagnóstico pulpar
preciso. Se espera que en el futuro se pueda disponer de un método de diagnóstico preciso y no
invasivo en la consulta, ya que esto ayudará a los clínicos a determinar el tratamiento con el mejor
pronóstico (Kearney, Cooper, Smith y Duncan, 2018). La formación de tejido duro en los seres
humanos está regulada genéticamente. Los genes de la fosfoproteína secretora de unión al calcio
(SCPP) participan en la mineralización del esmalte y la dentina. El gen de la SCPP tiene cinco genes
de la SCPP ácida y dos subfamilias (Kawasaki & Weiss, 2008). Los genes que codifican cinco
proteínas SCPP ácidas son DSPP, DMP-1, IBSP (sialoproteína de unión a integrinas), MEPE
(fosfoglicoproteína extracelular de la matriz) y SPP1 (fosfoproteína secretada 1). La primera
subfamilia codifica la SCPP rica en Pro y Gln (P/Q) depositada por los ameloblastos que producen
el esmalte (George & Veis, 2008). La segunda subfamilia codifica proteínas SCPP ácidas (también
conocidas como SIBLINGs-Small Integrin Binding Ligand N-linked Glycoproteins) que son
secretadas por células derivadas del mesénquima, osteoblastos, osteocitos y odontoblastos. La
familia de genes SCPP se encuentra en el cromosoma 4 que forma dos grupos de genes que
consisten en cinco genes SCPP ácidos y proteínas SCPP ricas en 16P/Q separadas por una región
intergénica de 17 megabases. El gen de la amelogenina (AMEL) se encuentra en el cromosoma
sexual. Los genes SCPP ricos en 16P/Q codifican el esmalte, la caseína de la leche y las proteínas
salivales, a saber, la caseína alfa S1 (CSN1S1), la caseína beta (CSN2), la estaterina (STATH), la
histatina 3 (HTN3), la histatina 1 (HTN1), la LOC401137, la odontogénica asociada a los
ameloblastos (ODAM), Péptido secretado por células dendríticas foliculares (FDCSP), Caseína
kappa (CSN3), Prolinerich 5 (PROL5), Proline-rich 1 (PROL1), Mucin 7 (MUC7), Amelotina (AMTN),
Ameloblastina (AMBN) y Enamelina (ENAM) (Kawasaki & Weiss, 2008). Hay otros dos genes
relacionados con el SCPP: la proteína secreta rica en cisteína ácida (SPARC) y el SPARC-like 1
(SPARCL1) que codifican proteínas de la matriz extracelular (ECM) (Yan & Sage, 1999).
Los genes SPARCL1 y SCPP-Pro-Gln-rich 1 (SCPPQ1) regulan la expresión de DSPP que estimula la
producción de matriz dentinaria en las células de los odontoblastos y de matriz ósea en los
osteoblastos y osteocitos (Kawasaki, 2011). En el complejo pulpar de la dentina, la DSPP es
secretada por los odontoblastos durante la fase secretora activa (Simon et al., 2009). La DMP-1 es
una proteína de la matriz extracelular altamente fosforilada, de la familia SIBLINGs que tiene un
papel en la mineralización de la dentina y en la regulación de la diferenciación de los
odontoblastos (Martini et al., 2013). Los investigadores han identificado la DMP-1 como un
marcador fenotípico de la diferenciación de los odontoblastos (Butler, 1995; Unterbrink,
O'Sullivan, Chen y MacDougall, 2002) y de la madurez (Simon et al., 2009). Por lo tanto, tanto
DMP-1 (Goldberg et al., 2011; Narayanan, Gajjeraman, Ramachandran, Hao, & George, 2006;
Ricardo Mora Torres pág. 6
Simon et al., 2009) como DSPP (Begue-Kirn, Krebsbach, Bartlett, & Butler, 1998; Narayanan et al:
Goldberg et al., 2011) podrían, por tanto, utilizarse como marcadores específicos de
odontoblastos. Hay varias vías implicadas en la dentinogénesis terciaria. La vía de señalización Wnt
regula muchos procesos de desarrollo y puede estimular la señal pro-supervivencia/anti-
apoptótica en las células madre para promover la curación (Hunter et al., 2015). Esta vía
desempeña un papel importante en el desarrollo de muchos órganos autorrenovables, como el
hueso, el intestino y la piel, y es necesaria para el mantenimiento de la homeostasis en estos
órganos (Yoshioka et al., 2013). La β-Catenina es el principal componente de la vía Wnt/-β
Catenina y se expresa en los odontoblastos, las células similares a los odontoblastos y las células
de la pulpa dental (Han et al., 2011). Es una proteína de doble función que controla la
coordinación de la adhesión entre células y la transcripción de genes. Es una subunidad del
complejo proteico cadherina y actúa como transductor de señales intracelulares en la vía de
señalización Wnt (Yoshioka et al., 2013). Los odontoblastos responden a Wnt y tienen la capacidad
de mejorar la regeneración de la dentina (Hunter et al., 2015). Tanto los odontoblastos
postmitóticos como las células similares a los odontoblastos se activan a través de la vía de
señalización β-Catenina/Wnt (Han et al., 2011). Por lo tanto, la actividad de los odontoblastos
puede evaluarse a través del marcador β-Catenina que indica la activación de la vía de señalización
β-Catenina/Wnt. El factor nuclear (NF)-kappaB es otra vía que se activa, tiene funciones tanto pro
como antiinflamatorias que ayudan a iniciar la inflamación, y tiene la capacidad de modular la
inflamación a través de la regulación de la apoptosis de los leucocitos en un mecanismo de
retroalimentación para controlar la intensidad y la duración de la respuesta inflamatoria
(Lawrence, 2009). Cuando se inicia, se liberan citoquinas proinflamatorias como la IL-1 y el TNF α.
La familia MAPK (proteína quinasa activada por mitógenos) y las vías PI3K/ AKT/mTOR
(fosfatidilinositol 3 quinasa/proteína quinasa B/objetivo mecanístico de la rapamicina) están
implicadas en la proliferación celular, la apoptosis, la adhesión y la migración. La familia MAPK
consta de tres subfamilias, a saber, p38 MAPK, ERK (quinasa regulada por señales extracelulares) y
JNK (quinasa N-terminal c-Jun), responsables de la diferenciación y la proliferación celular, la
actividad secretora de los odontoblastos y las respuestas inflamatorias. Las vías de señalización del
TGF-β/Smad (Factor de Crecimiento Transformante β/pequeña madre contra la decapitación) son
desencadenadas por las células de la pulpa dental expuestas a moléculas bioactivas y al TGF-β1.
Una revisión detallada de las vías ha sido proporcionada por da Rosa, Piva y da Silva (2018).
Los odontoblastos también son capaces de responder a estímulos ambientales como los térmicos,
mecánicos y químicos, ya que expresan la familia de receptores transitorios (TRP) (da Rosa et al.,
2018). Las bajas temperaturas en la superficie de la dentina son detectadas por la expresión de
TRPM8 (TRP subfamilia de melastatina 8) y TRPA1 (TRP subfamilia de anquirina 1) (Tsumura et al.,
2013). TRPA1 también se activa en entornos alcalinos (Kimura et al., 2016), mientras que TRPV1
(canal de cationes TRP subfamilia V1), TRPV2 y TRPV4 se activan para mediar en la dentinogénesis
reactiva (Tsumura et al., 2013).
En la actualidad no existen métodos reproducibles en la consulta para evaluar la inflamación de la
pulpa dental; sin embargo, con el conocimiento de los diversos biomarcadores y las vías
implicadas, podrían desarrollarse métodos reproducibles que ayuden a los clínicos a evaluar la
fase del proceso inflamatorio, a diagnosticar con precisión la salud de la pulpa dental y a
administrar los tratamientos bioactivos adecuados en la medicina dental regenerativa que
Ricardo Mora Torres pág. 7
modulen la inflamación para promover la curación y la reparación. 2.4. Una visión general de la
medicina dental regenerativa Los materiales bioactivos utilizados con éxito para la pulpotomía
vital tanto en dientes primarios como permanentes con "pulpitis reversible" a través de materiales
de recubrimiento pulpar directos o indirectos son el hidróxido de calcio (Ca(OH)2), el agregado de
trióxido mineral (MTA) de mezcla de silicato de calcio y los materiales derivados del MTA
(cementos hidráulicos de silicato de calcio) (Prati y Gandolfi, 2015). Algunos ejemplos de cementos
hidráulicos de silicato de calcio son Biodentine™ (Septodont, Saint-Maur-des-Fossés, Francia),
Harvard MTA Caps® (Harvard Dental International GmbH, Hoppegarten, Alemania), Ledermix®
MTA (Riemser, Riems, Alemania), MM-MTA™ (Micromega, Besancon, Francia), MTA Angelus
(Angelus Dental Solutions, Londrina, PR, Brasil), MTA Plus™(Prevest Detpro Limited, Jamnu, India),
ProRoot® MTA (Dentsply Tulsa, Johnson City, TN, USA), Tech Biosealer capping (Isasan Sr, Rovello
Porro, Co, Italia), TheraCal® (Bisco Inc, Schaumburg, IL, USA). La aplicación de biomateriales a base
de hidróxido de calcio induce la dentinogénesis terciaria a través de una serie de eventos
(Sangwan, Sangwan, Duhan, & Rohilla, 2013). La aplicación inicial de Ca (OH)2, que tiene un pH
elevado y propiedades antibacterianas, provoca una zona de necrosis al entrar en contacto con los
tejidos pulpares (Schroder y Granath, 1971). Curiosamente, estudios más recientes han
demostrado que la actividad antibacteriana se limita a las capas superficiales y es eficaz con una
mínima infección bacteriana (Goldberg et al., 2008). La acción antiinflamatoria del Ca(OH)2 se
debe a la desnaturalización de las citoquinas proinflamatorias que confieren al biomaterial un
efecto inmunomodulador que reduce la intensidad de la inflamación (Khan, Sun y Hargreaves,
2008). La resolución de la inflamación inicial causada por el material se prevé en la primera
semana (Sangwan et al., 2013). El elevado pH del Ca(OH)2 desnaturaliza los túbulos dentinarios
locales liberando las moléculas bioactivas solubilizadas atrapadas en los túbulos dentinarios (Smith
et al., 2012). Además, el pH elevado es capaz de neutralizar el entorno ácido creado por los
subproductos bacterianos, la inflamación correspondiente (Heithersay, 1975) y desnaturalizar los
mediadores proinflamatorios (Khan et al., 2008), lo que contribuye a los efectos
inmunomoduladores e inclina la balanza desde la actividad de los dentinoclastos hacia
mecanismos odontogénicos favorables (Segura et al., 1997). El límite óptimo de pH fisiológico de
los odontoblastos está en torno al rango de pH 10 (Heithersay, 1975), por encima de éste, puede
producirse la muerte celular y los odontoblastos son sustituidos por células similares a los
odontoblastos
Las moléculas bioactivas liberadas, estimulan la reparación y curación observada a través de la
activación de la inmunidad innata produce dentina terciaria (Farges et al., 2015). La formación de
la dentina terciaria se produce en cuatro semanas (Yoshiba, Yoshiba, Nakamura, Iwaku, & Ozawa,
1996). El proceso de reparación es incontrolado con resultados imprevisibles, quizá debido al
estado de la pulpa en cuanto al grado de inflamación y la presencia de microorganismos y
productos metabólicos, células pluripotentes indiferenciadas viables, la presencia de
biomoléculas, factores de crecimiento, genes y el entorno local para sostener y apoyar la curación.
Los materiales bioactivos a base de silicato de calcio, como el MTA (Giraud et al., 2018) y los
cementos hidráulicos de silicato de calcio (Prati y Gandolfi, 2015), actúan de forma similar. La
formación de puentes calcificados (dentina reparadora) es el producto de células similares a los
odontoblastos.
Ricardo Mora Torres pág. 8
Stefanska y MacEwan, 2015). El mecanismo implica la metilación del ADN, la modificación de las
histonas y los ARN no codificantes (ARNnc). Kearney y sus colegas han proporcionado una revisión
en profundidad del tema, el desarrollo potencial de diagnósticos precisos y aplicaciones de
biomateriales dentales dirigidos (Kearney et al., 2018). Sin embargo, con cualquier manipulación
genética, existen preocupaciones potenciales sobre los posibles efectos secundarios y la
aprobación clínica necesaria para utilizar estos métodos de forma segura. En la actualidad, no
existe ninguna aprobación para ningún fármaco basado en la epigenética en Estados Unidos (FDA)
para uso médico y dental, aunque en el Reino Unido existen fármacos basados en la epigenética,
especialmente para pacientes oncológicos (Kearney et al., 2018).
Conclusión La medicina dental regenerativa ha proporcionado muchas nuevas posibilidades para
el futuro manejo de la caries dental y sus secuelas. La comprensión de las interacciones
moleculares y genéticas dentro del complejo de la pulpa dental en la salud y la enfermedad
ayudará a los investigadores a afinar los métodos disponibles en materiales bioactivos, moléculas,
modificaciones epigenéticas y bioingeniería. Esperamos que en un futuro próximo podamos curar
o regenerar la pulpa dental para ayudar a conservar los dientes estructuralmente sanos
Ricardo Mora Torres pág. 9
También podría gustarte
- Lira AsmaDocumento58 páginasLira AsmaJosehp LiraAún no hay calificaciones
- Monografia DengueDocumento9 páginasMonografia DengueMax TorresAún no hay calificaciones
- FitoterapiaDocumento29 páginasFitoterapiaClaudio Malermo SalinasAún no hay calificaciones
- Asma BronquialDocumento88 páginasAsma BronquialManuel MendozaAún no hay calificaciones
- Leptospirosis SeminarioDocumento23 páginasLeptospirosis SeminarioMirian Verdes100% (1)
- Libro de Resumenes VPUBLICACION 3Documento383 páginasLibro de Resumenes VPUBLICACION 3Luis Castro MilanoAún no hay calificaciones
- Wuolah-Examen Parcial de Inmunología BásicaDocumento9 páginasWuolah-Examen Parcial de Inmunología BásicaWillMonasHuertasAún no hay calificaciones
- Coagulacion Intravascular DiseminadaDocumento7 páginasCoagulacion Intravascular Diseminadamariano villavicencioAún no hay calificaciones
- Cuestionario de InmunologíaDocumento59 páginasCuestionario de InmunologíaLeandro Miguel BidondoAún no hay calificaciones
- Nutrientes e InmunidadDocumento8 páginasNutrientes e Inmunidadpablitss27Aún no hay calificaciones
- Examen Patologia Parcial 2022-IiDocumento23 páginasExamen Patologia Parcial 2022-IiCamila SigueñasAún no hay calificaciones
- Gastroenterologia PediatricaDocumento27 páginasGastroenterologia PediatricaKarina Jácome RuizAún no hay calificaciones
- RETROALIMENTACIÓN Ensayo de Filosofia. RisoterapiaDocumento6 páginasRETROALIMENTACIÓN Ensayo de Filosofia. RisoterapiaConstanza MoralesAún no hay calificaciones
- Sistema HematicoDocumento39 páginasSistema HematicoGabriel CantoAún no hay calificaciones
- Gel ReductorDocumento107 páginasGel ReductorRUTH MARINA ANDRADE PORTILLAAún no hay calificaciones
- Propiedades Antigénicas e InmunogénicasDocumento2 páginasPropiedades Antigénicas e InmunogénicasFrancisco Rivera Avelar100% (2)
- Artritis ReumatoideDocumento62 páginasArtritis ReumatoideSELENE BEATRIZ OSORIO CRUZAún no hay calificaciones
- Unidad 1 - Ecologia de La SaludDocumento31 páginasUnidad 1 - Ecologia de La SaludJonathan DamianAún no hay calificaciones
- InmunomicologíaDocumento15 páginasInmunomicologíaJaime Jara AlvaradoAún no hay calificaciones
- INMUNOLOGIADocumento55 páginasINMUNOLOGIAdnfb9hsmb4Aún no hay calificaciones
- Inflamación PatologíaDocumento74 páginasInflamación PatologíaChiara PereiraAún no hay calificaciones
- Aspectos Inmunológicos de La Enfermedad PeriodontalDocumento8 páginasAspectos Inmunológicos de La Enfermedad PeriodontalSara OdonnellAún no hay calificaciones
- AO TEJIODOS BLANDOS INGLES - Compressed (1) .En - EsDocumento28 páginasAO TEJIODOS BLANDOS INGLES - Compressed (1) .En - EsHarlis HernandezAún no hay calificaciones
- Fisiopatologia de Amenaza de Parto Prematuro AppDocumento10 páginasFisiopatologia de Amenaza de Parto Prematuro AppJose Jose Balladares BancesAún no hay calificaciones
- Citocinas de La Inmunidad Innata PDFDocumento28 páginasCitocinas de La Inmunidad Innata PDFJose Daniel Becerra GonzalezAún no hay calificaciones
- Resúmenes CortosDocumento85 páginasResúmenes Cortosmaicrauwu16Aún no hay calificaciones
- Formacion PNIE I Modulo 3 SemanaDocumento30 páginasFormacion PNIE I Modulo 3 SemanaLeandro Quito100% (1)
- Vías Inflamatorias en La Resistencia A La InsulinaDocumento4 páginasVías Inflamatorias en La Resistencia A La InsulinaRuth Vargas ChaAún no hay calificaciones
- Actualización de Peritonitis Infecciosa Felina (75-82)Documento8 páginasActualización de Peritonitis Infecciosa Felina (75-82)Guillermo MartínezAún no hay calificaciones
- Fisiopatologia Cardiovascular CompendioDocumento47 páginasFisiopatologia Cardiovascular CompendioAlexandra AraujoAún no hay calificaciones