Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Robert M. Silverstein
Robert M. Silverstein
Cargado por
Linda Flor De Maria Cuevas Palencia100%(1)100% encontró este documento útil (1 voto)
535 vistas86 páginasDerechos de autor
© © All Rights Reserved
Formatos disponibles
PDF o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF o lea en línea desde Scribd
100%(1)100% encontró este documento útil (1 voto)
535 vistas86 páginasRobert M. Silverstein
Robert M. Silverstein
Cargado por
Linda Flor De Maria Cuevas PalenciaCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF o lea en línea desde Scribd
Está en la página 1de 86
obert M. Silverstein, G. Clayton aa
y Terence C. Morrill
eel
AAT
PTS
HH
@ 6 «ey © @)
i
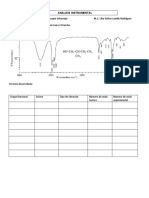
(CH) .NCH.CHLOCCH, ND,CH,CH,COOD CICH.CH,OH
acetato de Bealanina 2-cloroetanol €)-ccncnon
2-dimetilaminoetilo fe |
2-fenoxietanol,
Espectrometria infrarroja
1. Introduccién
La radiacién infrarroja se refiere generalmente 2
la parte del espectro electromagnético comprendida
entre las regiones visible y de las microndas. De enor.
me uso prictico para el quimico orginico es Ja por-
ién limitada entre 4000 cm y 666 cmr* (2.5-15.0
um). Recientemente ha existido un interés creciente
en la region del infrarrojo cercano, 14 2904000 cm*
(07-25 mm) y Ta tegién de infrarrojo Iejano, 700-
200 cm (143-50 ym).
Una vez que se haya considerado la breve descrip-
cién teérica que sigue, sera evidente que aun una
molécula sumamente simple puede dar lugar a un
‘spectro extremadamente complejo. El quimico orga-
nico se beneficia con esta complejidad cuando iguala
el espectro de un compuesto desconocido en contra
del correspondiente a una muestra auténtica. La corre-
lacién pico a pico constituye una excelente prueba
para la identificacién. Es poco probable que dos com-
puestos cualesquiera, excepto en el caso de los enan-
_tiomorfos, proporcionen ¢l mismo espectro infrarrojo.
‘Aun cuando el espectro infrarrojo es caracteristico
de toda Ia molécula, resulta que ciertos grupos de
tomos originan bandas a la misma frecuencia o aproxi-
madamente, en forma independiente de la estructura,
del resto de la molécula, Es la persistencia de estas
bandas caracteristicas la que permite al quimico ob
tener una informacién estructural itil mediante la
simple inspeccidn y referencia con tablas generalizadas
de frecuencias de grupo caracteristicas. Confiaremos,
nosotros, bastante en estas frecuencias de grupo carac-
teristicas.
Ya que no dependemos exclusivamente del espec-
tto infrarrojo para la identificacién, no se requiere el
andlisis detallado del espectro. Siguiendo nuestro plan
general, solarnente presentaremos la teoria suficiente
para lograr nuestro propésito: la utilizacién del espec
to infrarrojo en conjunto con otros datos espectrales
para determinar la estructura molecular.
Casi todos los laboratorios académicos e indus-
triales disponen de espectrofotémetros infrarrojos como
tna herramienta de laboratorio para el quimico or-
ginico. Un espectrofotémetzo infrartojo simplificado
tiene un costo de aproximadamente 5000 dolares. Se
dispone de instrumentos de precisién cuyo costo es
de 12000 a 17000 dolares. Los espectrofot6metros
infrartojos que cubren la gama de 667-33 cm (15:
300 xm) cuestan aproximadamente 35 000 délares. Ya
que el quimico orgénico con bastante frecuencia ob-
tiene sus propios espectros infrarrojos, describiremos
la instrumentacién y preparacion de muestras con algo
més de detalle que el proporcionado en los capitulos
de la espectrometria de masas y la espectrometria de
RMN.
E] creciente interés en. la espectrometria infrarroja
como herramienta para el quimico orginico practico
es bastante evidente considerando el ndmero de libros
que se han publicado y dedicado total o parcialmente
a la descripcién de las aplicaciones de la espectrome-
tria infrarroja. No existe una carencia de material de
referencia que cubra todos los aspectos de la espec-
trometria infrarroja.’* El texto de Colthup, Daly y
Wiberly* presenta un estudio completo de la teorfa,
prictica y correlaciones de espectro-estructura, Los
manuales compactos de Cross,* Flett,"* Szymanski y
Nakanishi" constituyen fuentes de referencia’ adecua-
das para lograr una informacién concisa, Los voliiie-
nes de Potts y Miller?” representan referencias va-
liosas para la operaciGn instrumental y las técnicas de
manipulacién de muestras. Existen recopilaciones de es-
pectros infrarrojos que incluyen indices de colecciones
de espectros y de la literatura.*~* El libro de Con-
ley*** es una introduccién a nivel elemental de la teo-
tia, determinacién ¢ interpretacién. El libro de Be-
lamy y su suplemento inclayen revisiones amplias de
la literatura
Ml. Teoria
Una molécula orginica absorbe 1a radiacién infra:
rroja con frecuencias menores de aproximadamente
100 em (longitudes de onda mayores de 100 um) y
la convierte en energia de rotacién molecular. La
absorcién es cuantificada; siendo asi, un espectro de
rotacién molecular consiste en lineas discretas,
85
Una molécula orginica absorbe la radiacién infra
rroja en la gama de aproximadamente 10 000-100 cm
(1-100 jm) y la convierte en encrgia de vibracién
molecular. sa absorcién tambien se cuantifica, pero
el espectro de vibracién aparece como bandas y no
como lineas, debido a que un cambio de energia vi
bracional simple va acompaiiado de varios cambios
de energia rotacional. Son estas bandas de energia vi
bracional-rotacional, particularmente las que se presen-
tan entre 4000 cm? y 666 cm! (2.5-15 pm), las que
son de nuestro interés. La frecuencia o la longitud de
onda de la absorcién depende de las inasas relativas
de los atomos, las constantes de fuerza de los enlaces
v la geometria de los dtomos.
Las posiciones de banda en los espectros infrarro-
jos se presentan ya sea como longitudes de onda
como nitmeros de onda. La micra (= 10 metros)
se ha utilizado comiinmente desde hace mucho tiem-
po como unidad para la longitud de onda A en la
espectrometria infrattoja, pero recientemente el tér-
nino micra ha sido sustituido por el de micrdmetio
(um = 10-* metros). Actualmente se utiliza la unidad
de niimero de onda (cnr, reciproca de centimetro),
pues es directamente proporcional a Ta energia v por-
que muchos de los nuevos espectrdmetros sofisticados
son Tineales en la escala de cnr, Las unidades se en-
cuentran relacionadas como sigue:
1
cm = —— x 10!
roy
Las absorciones especificas y' los intervalos de absor-
cién se indicarn en cm, adjuntando los datos de
um’ cortespondientes (normalmente entre paréntesis)..
En’ el apéndice E se proporciona una tabla til que
relaciona los em" y jm.
Observe que los ntimeros de onda (7) frecuente-
thente se denominan “frecuencias”; esto no es riguro-
samente correcto .ya que los mimeros de onda son
1/a y Ia frecuencia (») es ¢/A. Tal “frecuencia” para
la terminologia # es bastante comtin y probablemente
no canstituye un error serio mientras se tenga en nen-
te elitérinino faltante’ de la velocidad de-la luz (c).
En este libro se utilizan los espectros lineales en ym y
en em. Un espectro lineal en niimeros de onda tiene
una apariencia bastante distinta de uno que es lineal
en la longitud de onda, tal como se muestra poste-
riormente (figura 7, pgina 96).
Las intensidades de banda se expresan ya sea como
trasmitancia (T) 0 como absorbancia (A). La tras-
mitancia es la relacién entre la potencia radiante tras-
mitida por una muestra y la potencia radiante inci-
dente en la muestra. La absorbancia es el logaritmo, de
base 10, de la reciproca de la trasmitancia; A = login
(1/T). Periédicamente. se publica una recopilacién
concisa de la nomenclatura de espectrometria apro-
ada.
Existen dos tipos de vibraciones molecularcs: alar
gamiento \ flexion. Una vibracién de alargamicnto
representa un movimiento ritmico a to largo del ce
de enlace de tal modo que la distancia interatomica
aumenta o disminuye. La vibracién de flexion puede
consistir en un cambio en Ios dngulos de enlace entre
Jos enlaces con un atomo comiin, 0 el movimiento
de un grupo de fitomos con respecto al restante de la
molécula sin que se tenga cl miovimiento de los sito
mos en el grupo con respecto al otro. Por ejemplo, las
vibraciones de torsidn, torcimiento y oscilacién impli
can un cambio en los angulos de enlace con referencia
a un conjunto de coordenadas establecidas arbitratia
mente dentro dela molécula.
Las vibraciones que se observan en el infrarrojo son
solo las que dan por resultado un cambio ritmico del
momento dipolar de la molécula. El campo eléctrico
alternante, producido por la distribucién de carga cam,
biante que acompafia.a una vibracién, acopla la vibra-
cién molecular con el campo eléctrico oscilante de la
radiacién electromagnética.
Una molécula tiene grados de libertad en la misma
cantidad que el total de grados de libertad de sus dto-
imos individuales. Cada atomo tiene 3 grados de liber-
tad que corresponden a las coordenadas cartesianas (X,
Y, Z) necesatias para definir su posicién relativa a
los otros atomos en la molécula. Una molécula de n
4tomos consecuentemente tiene 32 grados de liber-
tad. Para las moléculas no lineales, tres de los grados
de libertad definen la rotacién, y tres, la traslacién; el
restante de 31-6 grados de libertad son los grados de
libertad vibracionales o vibraciones fundamentales, Las
moléculas lineales tienen 3n-5 grados de libertad vi
bracionales, ya que solamente se requiere dos grados
de libertad para definir la rotacién.
Las vibraciones fundamentales no implican un cant
bio en el centro de gravedad de la molécula.
Las tres vibraciones fundamentales de la molécula
de agua triatémica no lineal pueden representarse como
sigue:
Alargomiento Alargamiento
simétrico (40H). oximético (¥as08),
3652 em™!(2.74 yim) 3756 cm! (2.66 ym)
En tijera
(HOE),
31596 cm! (627 9m)
Observe e] espaciamiento bastante cercano del alar-
gamiento simétrico y asimétrico interaccionante (“azo
plado”) anterior comparado con Ia forma en tir
alejada. Posteriormente, esto demostrara ser de utili
dad para la clasificacién de las absorciones y su apli
cacién en la determinacién de estructuras.
86 IDENTIFICACION ESPECTROMETRICA DE COMPUESTOS ORGANICOS
La molécula de CO, es lineal y contiene tres. ato
mos; consecuentemente, tiene cuatro vibraciones fun-
damentales ((3 X 3) — 5)
~—@—-
(D Atergamiento
suméttico (4 CO),
1340 em™!(46 um)
~-—__
@) Alergomieato
osimiteico as CO).
2350 cm™"(4:26um)
2 @ 8
2) Ep tijera iflexién)s
(6, C02), 666 em=!(15.0 umn) (4) Ee era (flexién}
(6, C02), 666 m= (15.0um)
@ and © indicate movement perpendicular to the plane of the page
La vibracién de alargamiento simétrico (1) ¢s in-
activa en el infrarrojo ya que no produce cambio en
el momento dipolo de la molécula. Las vibraciones
de flexion (3) y (4) son equivalentes, y constituy
Jos componentes resueltos del movimiento de flexi
orientado a cualquier angulo del eje internuclear; tie-
nen la misma frecuencia y se dice que son doblemen-
te degeneradas.
Los diversos modos de alargamiento y flexién de
tun grupo AX; que aparece como una porcién de mo-
\écula, por ejemplo el grupo CH, en una molécula
de hidrocarburo, se muestran en la figura 1. La regla
3n-6 no se aplica debido a que el CH; solamente re-
presenta una porcién de la°molécula.
hae
Alargamiento Alergomiento
ee CHa) @, CH)
VIBRACIONES DE ALARGAMIENTO
y ¥
En tera 0 flexién En abonico 0 flexiga
en el plano fuera de plano
(6, Cla) (CH)
Toreimiento 0 flexién Ostilecién 0 Hlexién
fuere de plone en el plano
(r CH) @ CH)
VIBRACIONES DE FLEXION
Fioura 1. Modos vibracionales para el grupo CH,. (®
y © indican el movimiento perpendicular con respecto
al plano de la pagina).
El nimero tedrico de vibraciones fundamentales
(frecuencias de absorcién) raramente se puede obser-
var debido a que los sobretonos (multipletes de. una
frecuencia dada) y los tonos de combinacién (suma de
otras dos vibraciones) aumentan el nimero de ban-
das, mientras que otros fenémenos reducen el niimero
de ‘bandas. Los siguientes reducen el némero teéri-
co de bandas:
1. Las frecuencias fundamentales que se encuentran
fuera de la regién de 2.5.1.5 am.
2. Las bandas fundamentales que son demasiado
débiles para ser observadas
3. Las vibraciones fundamentales que tienen tal cer-
canfa que llegan a juntarse.
4. La presencia de una banda degenerada derivada
de varias absorciones de la misma frecuencia en
moléculas sumamente simétricas.
5, La falla de ciertas vibraciones fundamentales en
cuanto a aparecer en el infrarrojo debido a la
falta del cambio requerido en el cardcter dipolar
de la molécala.
Las asignaciones de las frecuencias de alargamiento
pueden aproximarse mediante la aplicacién de la ley
de Hooke. En la aplicacién de esta ley, dos atomos
y su enlace de conexién se tratan como un oscilador
arménico simple formado de dos masas unidas” por
medio de un muelle. La ecuacién 1, derivada de la
ley de Hooke, establece la relacién entre’ la frecuen-
cia de la oscilacién, las masas atémicas y la constante
de fuerza del enlace.
frecuencia vibracional (cm~*)
velocidad de la luz. (cm/seg)
f = constante de fuerza del enlace (dinas/em)
Mx y My = masas del dtomo x y y, respectivamente (g)
El valor de f es de aproximadamente 5 X 10° dinas
por centimetro para el caso de los enlaces simples y
ESPECTROMETRIA INFRARROJA 87
de aproximadamente dos a tres veces este valor para
los enlaces dobles + triples, respectivamente.
La aplicacién de a formula al alargamiento C-H,
utilizando 19.8 xX 107'g v 1.64 x 10-*'g como valo-
res de masa para C y H, respectivamente, sitita a la
frecuencia de vibracion del enlace C-H en 3040 cm
(3.30 um). En realidad, las vibraciones de alargamien:
to C-II asociadas con los grupos metilo » metileno
generalmente se observan en la region comprendida
entre 2960-2850 cm (3.38-3.51 nm). El cilculo no
es preciso debido a que se han ignorado los efectos
que se derivan del medio que rodea al C-H dentro de
la molécula. La frecuencia de la absorcién infrarroja
normalmente se utiliza para calcular la constante de
fuerza de los enlaces.
El desplazamiento en la frecuencia de absorcién
que sigue a la deuteracién frecuentemente se utiliza
en la asignacién de las frecuencias de alargamiento
C-H. Si el hidrégeno en el grupo X-H se
por deuterio, Ia ecuacién 1 indica que la relacio
Jas frecuencias de alargamiento C-H y C-D debe ser
igual a 2. Si la relacién de frecuencias posterior.
mente a la deuteracién es bastante menor de V2, no
podemos suponer que la vibracién representa simple-
mente una vibracién de alargamiento C-H, sino mas
bien una vibracién mezclada que implica la interac-
cién (acoplamiento) con otro tipo de vibracién. La
forma verdadera de la vibracién es una combinacién
de ambas.
El calculo sitta a las frecuencias de alargamiento
de los siguientes enlaces en las regiones de absorcién
general que se indican a continuacién.
1300-800 cm-* (7.7-12:5 ym)
2300-2000 cmt (4
3800-2700 em-* (2.
0 ym)
7 pm)
Para aproximar las frecuencias vibracionales del
alargamiento de enlace mediante la ley de Hooke, se
debe considerar las contribuciones relativas de las re-
sistencias de enlace y las masas atémicas: Por ejem-
plo, la comparacién superficial del grupo C-H con
el grupo F-H, con base en Jas masas atomicas, podria
Nevar a la conclusién de que la frecuencia de alarga-
miento del enlace F-H debe presentarse a una fre-
cuencia inferior que la del enlace C-H. Sin embargo,
el aumento en la constante de fuerza de izquierda a
derecha a través de las dos primeras hileras de la tabla
periédica tiene un efecto mayor que el aumento de
Ta masa. Siendo asf, el grupo F-H absorbe a una fre-
cuencia mayor (4138 cm, 242 wm) que el grupo
C-H (3040 cm, 3.30 pm).
En términos generales, los grupos funcionales que
tienen un dipolo intenso originan absorciones fuertes
en el infrarrojo.
Cuando dos osciladores de culace
Interaccid
comparten um itomo comin, es Taro que se compor
ten como osciladores individuales, a menos que las
frecuencias de oscilaciin sean bastante distintas. Esto
se debe a que existe una interaccién de acoplamiento
mecanico entre los osciladores. Por cjemplo, la mo:
lécula de bidxido de carbono, la cual consiste en dos
enlaces C = O con un atomo de carbono comin, tie-
ne dos vibraciones de alargamiento fundamentales
una forma de alargamiento simétrico v una asimétrica.
La forma de alargamiento simétrico consiste en un
alargamiento 0 contraccién en fase de los enlaces C
a O, y la absorcidn se presenta a una longitud de
onda mayor que la observada para el grupo carbonilo
en una cetona alifitica. La forma de’ alargamicnto
simétrico no prodtice cambio en el momento dipolar
de la molécula y consecuentemente ¢s “inactiva” en
el infrartoju, pero se observa con facilidad en el es
pectro Raman cerca de 1340 cm (7.46 wm). En la
forma de alargamiento asimétrico, los dos. enlaces
C a O se alargan fuera de fase; uno de los enla-
ces C-O se alarga mientras que el otro se contrac. La
forma de alargamiento asimétrico, debido a que pro-
duce un cambio en el momento dipolar, es activa en
el infrartojo; la absorcién (2350 cm, 4.26 pm) se
encuentra a una longitud de onda mas corta (mayor
frecuencia) que la observada para el grupo carbonilo
en las cetonas alifaticas.
Esta diferencia en las frecuencias de absorcién del
carbonilo manifestada por la molécula del bidxido de
carbono resulta del fuerte acoplamiento mecanico o
interaccién. En contraste, dos grupos carbonilo ceté:
nicos que se encuentran separados por uno jo més to-
mos de carbono muestran una absorcién dé carbonilo
normal cerca de 1715 cnr* (5.83 pam) debido a que
el acoplamiento de grado considerable se evita apa-
rentemente por el (los) atomo(s) de carbono que in-
terviene(n).
El acoplamiento explica las dos bandas de alarge-
miento N-H en Ia regién 3497-3077 cm! (2.86-3.25
nim) en los espectros de amina primaria y amida pti
maria, asi como las dos bandas de alargamiento C = 0
en la regién de 1818-1720 cmr* (5.50-5.81 wm) de los
espectros correspondientes a los anhidridos carboxtlicos
y de imida, y las dos bandas de alargamiento C — H
fen la regién de 3000-2760 cm (3.33-3.62 ym) tanto
para el grupo metileno como metilo.
Las bandas de frecuencia de grupo caracteristicas
frecuentemente implican las vibraciones acopladas, Los
espectros de los alcoholes tienen una banda fuerte en
la region dentro del intervalo de 1212 y 1000 cm*
(8.25-10.00 pm) que generalmente se define como la
“banda de alargamiento C-O”. En el espectro del
metanol, esta banda se encuentra 1034 cm* (9.67 xm)
y en el espectro del etanol se encuentra en 1053 cm?
(9.50 ym). La ramificacién y la insaturacién produ-
cen una absorcién caracteristica de estas estructuras®
88 |DENTIFICACION ESPECTROMETRICA DE COMPUESTOS ORGANICOS
(véase la parte correspondiente a los alcoholes). Es
exidente que no estamos tratando con una vibracién
de alargamiento C-O aislada, sino mis bien con una
vibracion asimétrica acoplada que implica el alarga
mento C-C-O.
Las vibraciones que resultan de la flexién angular
del enlace frecuentemente se acoplan de modo similar
2 las vibraciones de alargamiento. Siendo asi, las fre:
cuencias de flexién fuera de plano del C-H anular
correspondiente a las moléculas aromiticas dependen
del niimero de dtomos de hidrégeno advacentes en el
anillo; el acoplamiento entre los atomos de hidrogeno
se altera por la flexién del enlace C-C en el anillo
al cual se encuentran unidos los atomos de hidrégeno.
La interaccién que se deriva del acoplamiento de
las vibraciones de alargamiento y flexién se ilustra por
mnedio de la absorcién de las amidas aciclicas secun-
darias. Este tipo de amidas, que existen predominan-
temente en la conformacién trans, muestran una
absorcién intensa en la regién 1563-1515 cm (6.40-
6.60 wm); esta absorcién implica el acoplamiento de
has vibraciones de flexién N-H y alargamiento C-N.
Los requisitos para una efectiva interaccién de
acoplamiento pueden resumirse de la siguiente manera
1. Las vibraciones deben ser de las mismas especies
simétricas en caso de que se presente la inter.
accién,
2. El acoplamiento intenso entre Ihs vibraciones de
alargamiento requieren un tomo comin entre
Jos grupos.
3. La interaccién es méxima cuando los grupos aco-
plados absorben individualmente casi la misma
frecuencia,
4. El acoplamiento entre las vibraciones de flexién
y_alargamiento puede presentarse si el enlace de
alargamiento forma un lado del Angulo cambiante.
5. Se requiere un enlace comiin para el acoplamien-
to de las vibraciones de flexién.
6. El acoplamiento es despreciable cuando los gru-
pos se encuentran separados por uno o més 4tomos
de carbona y en caso de que las vibraciones sean
perpendiculares mutuamente.
Frexi6n ex nuorbceNo. E] enlazamiento del hidré-
geno puede ocurrir en cualquier sistema que contenga
tin grupo dador de protones (X-H) y un aceptador
de protones, Y, cuando el orbital s del protén puede
traslapar efectivamente el orbital p o = del grupo acep
tador. Los atomos X y ¥ son electronegativos mien
tras que Y posee un par solitario de electrones. Los
grupos comunes dadores de protones en las moléculas
organicas son los grupos carboxilo, hidroxilo, aniina o
amida, Los dtomos comunes aceptadores de protones
son el oxigeno, nitrdgeno y los haldgenos. Los grupos
insaturados, tal como el enlace etilénico, también pue
den actuar como accntadores de protones.
La resistencia del entace hidrégeno es maxima cuan-
do el grupo dador de protones y el eje del orbital de
par solitario son colineales. La resistencia del enlace
s inversamente proporcional a la distancia entre X
vy
El enlazamiento de hidrégeno altera la constante
de fuerza de ambos grupos; asi, las frecuencias de las
vibraciones de alargamiento y de flexién se alteran.
Las bandas de alargamiento X-H se mueven a longi
tudes de onda mavores (frecuencias menores), nor-
malmente con el aumento de la intensidad vy la
amplitud de banda, La frecuencia de alargamiento del
po aceptador (por ejemplo, C = O) también se
reduce, pero en menor grado que el grupo dador de
protones. La vibracién de flexién H-X_normalmen-
te se desplaza a una longitud de onda mis corta cuan-
do se presenta la flexidn; este desplazamiento es menos
pronunciado que el correspondiente a la frecuencia
de alargamiento.
El enlazamiento de hidrégeno intermolecular im-
plica la asociacién de dos o mas moléculas de com-
puestos iguales o diferentes. El enlazamiento inter-
molecular puede resultar en moléculas de dimero (tal
como se observa en los acidos carboxilicos) 0 en mo-
léculas de polimetro, las cuales existen en muestras
puras o en soluciones concentradas de alcoholes mo-
nohidricos. Los enlaces de hidrégeno intramoleculares
se forman cuando dador v aceptador de protones estén
presentes en una molécula simple bajo condiciones
espaciales que permiten el traslape requerido de los
orbitales; por ejemplo, Ia formacién del anillo de 5
0 6 miembros. El grado de proporcién del enlazamien-
to inter ¢ intramolecular depende de la temperatura.
El efecto de la concentracién en el enlazamiento de
hidrégeno intermolecular ¢ intramolecular es notable-
mente distinto. Las bandas que resultan del enlaza-
miento intermolecular generalmente desaparecen a
concentraciones bajas (menos de aproximadamente
0.01 M en los solventes no polares). El enlazamiento
de hidrégeno intramolecular representa un efecto in-
temo y persiste a concentraciones sumamente bajas.
El cambio de frecuencia entre la absorcién de OH
“libre” y Ia absorcién de OH enlazado es una medida
de la resistencia del enlace de hidrégeno. La tensién
anular, la geometria molecular y la acidez y basicidad
relativa de los grupos dador y aceptador de protones
alteran la resistencia del enlazamiento. El enlazamiert-
to intramolecular que implica los mismos grupos de
enlazamiento ¢s mas resistente cuando se forma un
anillo de 6 miembros a diferencia del caso en que
resulta un anillo menor del enlazamiento. El enla-
zamiento de hidrogeno ¢s mas resistente cuando la
estructura enlazada queda estabilizada por resonancia.
En la tabla 1 se resumen los efectos del enlaza-
miento de hidrégeno en las frecuencias de alargamiento
de los grupos hidroxilo y carbonilo.
Un aspecto importante del enlazamiento de hidrd-
geno implica la interaccién entre los grupos funciona-
les del solvente y el soluto. Cuando el soluto es po-
ESPECTROMETRIA INFRARROJA 89
‘Tanta 1. Frecuencias de alargainiento en ef entazamiento de hidrogeno
ENLAZAMIENTO INTERMOLECULAR ENLAZAMIENTO INTRAMOLECULAR
esis. Reduccién de freeuen. Reduccién de frecuen %
tencia cia (cin)® Clase de cia (om-)= Clase de
XY yOH sC=08 compuesto vOH C=O? compuesto
Dail 300 15 Alcoholes, fenoles y Dioles 1,2; cetonas
entlzzamiento inter. droxilo y la mayoria de
molecular hidroxilo las fi; fenokes ocloro y
a catbonilo <100 10 o-alcoxidioles
Media 100-300 50 1,3; algunas cetonas i
droxi; compuestos
B-hidroxi_ amino; com.
puestos Bhidioxi nitro
Eclonas
Fuerte >500 50. —-dimeros de RCOOH >300 100 ohidroxi arilo; 4cidos
o-+hidroxi arilo; ésteres
ohidroxi arilo;
A-dicetonas; tropolonas.
* Desplazamiento de frecuencia referido a las frecuencias de alargamiento “libre”.
> Alargamiento carbonilo solamente cuando es aplicable.
lat, es necesario especificar el solvente utilizado y la
coticentracién del soluto.
ResowaNcia DE FeaMt. Como hemos visto en
nuestra, descripcién de la interaccién, el acoplamiento
de dos formas de vibraciones fundamentales produce
das, modos nuevos de vibracién,. teniéndose frecuen-
cia’ mayores y menores que las observadas cuando la
‘inteticgién no se presenta. La interaccién también
‘puede:“ocurrir entre. las vibraciones fundamentales y
‘las. vibiaciones de sobretonos y tonos de combinacién.
“Tal interaccién se conoce como resonancia de Fermi
(un ejemplo es el modelo de absorcién del biéxido de
carbono). En nuestra descripcién de la interaccién,
indicamos que la banda de alargamiento simétrico del
CO, aparece en el espectro Raman cerca de 1340 cm
(746 ym): En realidad se observan dos bandas; una
a 1286 cm (7.78 nm) y otra a 1388 cm* (7.20 um).
La separacign resulta del acoplamiento entre la vibra-
cién C=O fundamental cerca de 1340 em (7.46
xm) y el primer sobretono de la vibraciényde flexién.
La vibracién de flexién fundamental ocurre cerca de
666 cm (15.00 ym) y el primer sobretono cerca
de 1334 em" (7.55 um).
La resonancia de Fermi es un fenémeno comin en
los espectros infrarrojo y Raman. Requiere que los
niveles vibracionales scan de las mismas especies simé-
tricas y que los grupos.de interaccién se encuentren
localizados en: la moléeula de modo que el acopla-
miento mecénico sea notable.
Un ejemplo de la resonancia de Fermi en una es-
tructura organica es la apariencia de “doblete” del
alargamiento C = O de la ciclopentanona bajo con.
diciones de resolucién suficientes. La figura 2 mues-
tra la apariencia del espectro de Ia ciclopentanona
bajo las condiciones usuales. Bajo condiciones espe-
ciales (figura 3), la resonancia de Fermi con una ban-
da de sobretono 0 de combinacién de un grupo «me
tileno da como resultado dos absorciones en la regién
de alargamiento carbonilo*
fll. Instrumentacién
El espectrofotémetro infrarrojo modemio de doble
haz consta de cinco secciones principales: fuente (ra
diacién), area de muestra, fotdmetro, graticula (mo-
nocromador) y detector (termopar). En la figura 4 se
muestra un diagrama del sistema Optico de tn espec
trofotémetro infrarrojo de doble haz.
Fuente pe rapiaci6n. La radiacién infrarroja se
produce mediante el calentamiento elécttico de una
fuente, normalmente un filimento de Nernst o un Glo
bar, hasta 1000-1800 °C. El filamento de Nemst se
fabrica a partir de un aglutinante y éxidos de circo
nio, torio y cerio. El Globar es una pequeita varilla
de carburo de silicio. La imagen de la fuente debe
tener mayor amplitud que la amplitud maxima de las
rendijas (véase la referencia 28d). La radiacién méxi-
ma para el Globar se presenta en la regién de 5500-
5000 cm (1.8-2.0 pm) y decrece en un factor mis
(© menos de 600 al aproximarse a la regién de 600
cm (167 ym). El filamento de Nernst proporciona
90 IDENTIFICACION ESPECTROMETRICA DE COMPUESTOS ORGANICOS
2000
TRASMMITANCIA [i
1000 900
oe ee ee
LONGITUD OF ONDA
Fioura 2,
NOMERO DE ONDA (cxt-")
1740 17801740 1780 1740 1780_1740_1780
z TITY ttt yt tty rt
$
8 sok 4
eg
&
5 st 4
8 fa 8 c °
Sa Pe i
Ficura 3. Espectro infrarrojo de la ciclopentanona en
diversos medios. A. Solucién en tetracloruro de carbono
(0.015 molar). B. Solucién en bisulfuro de earbono (0.023
molar). C. Solucién en cloroformo (0.025 molar). D. Es-
tado liquido (pelicula fina). (Amplitud de rendija espec-
tral computada, 2 cmt),
Ciclopentanona, pelicula liquida
su méxima energia de radiacién cerca de 7100 em
(14 wm) y disminuye en un factor de aproximada-
mente 1000 al aproximarse a la regién de frecuencia
inferior.
La radiacién de la fuente se divide en dos haces
por medio de los espejos M1 y M2. Los dos haces, es
decir, el de referencia y el de muestra, se enfocan al
drea de muestra por medio de los espejos M3 y M4.
‘AREA DE MUESTRA. Los haces de-teferencia-y de
muestra entran al area de muestra y pasan 3 trav‘
de la celda de referencia y la celda de muestra, Yespep-
tivamente. Los obtufadores opacos, montados en “el
alojamiento de la fuente, permiten el bloqueo deicual-
quiera de los haces ‘en forma independiente.,E¥¥4
de muestra de un espectrofotémetro preciso. iticlaye
una amplia variedad de accesorios de muestra’ que
varian-desde las celdas de gas de 40 m de trayectoria
efectiva hasta las microceldas. 2
MONOCROMADOR
(oraricua)
f HAZ OE
REFERENCIA
Ficura 4. Sistema dptico del espectrofotdmetro infrarrojo de doble har.
ESPECTROMETRIA INFRARROJA 91
Forbwero, Fi haz de referencia pasa a través
del atenuador (véase mis adelante) y se tefleja por
parte de los espejos M6 5 MB hacia el espejo de see-
tor rotatorio M7, que altemativamente refleja el haz
fuera del sistema y que trasmite el haz hacia el espejo
M9. V1 haz de referencia esta formado ahora por un
haz intermitente con una “frecuencia” desde 8 hasta
13 ciclos por segundo dependiendo del instumento
particular. Este haz, se enfoca por medio del espejo
M10 sobre la rendija Sl. El haz de muestra pasa a
través del peine (véase mas adelante) ¥ se refleja por
medi del espejo MS hacia cl espejo de sector rota
torio M7, el cual trasmite alternativamente el haz
fuera del sistema éptico v lo refleja hacia el espejo
M9 \ posteriormente al espejo MIO y la rendija SI.
En cualquier momento dado, el haz enfocado so:
bre la rendija Sl representa el haz de referencia que
ha sido trasmitido por el espejo de sector rotatorio
M7, 0 el haz de muestra que ha sido reflejado por M7.
Es decir, el haz de referencia y el de muestra se han
combinado en un haz simple de segmentos altemnan-
tes; esto establece una frecuencia conmutante en el
detector que equivale a la velocidad de rotacién de
M7.
Cuando los haces son de la misma intensidad, el
instrumento se encuentra en una condicién dptica
nula. El peine en el haz de muestra permite el balan-
ceo de los haces. La plumilla de registro se encon-
traré entonces en 100% de trasmitancia cuando no
esté presente la muestra.
El atenuador se hace entrar y salir del haz de re-
ferencia en respuesta a la sefial originada en el detec-
tor por el haz de muestra. Asi, cuando la muestra
absorbe el haz de muestra, el atenuador se hace entrar
al haz de referencia hasta que su intensidad se iguale
con el haz de muestra.
Monocromavor. El haz combinado pasa a través
de la rendija de admisién S1 hacia el espejo M11, el
cual refleja hacia la graticula de difraccién Gl. Este
haz se dispersa en varias frecuencias; se refleja nueva-
mente hacia el espejo M11 y posteriormente al espejo
M12. El espejo M12 lo enfoca el haz hacia la rendija
de salida S2. La amplitud del intervalo de frecuencias
enfocado sobre la rendija S2 se determina por la am-
plitud de la rendija de admisin S1_y por le potencia
de dispersién de la graticula. La banda de frecuen-
cia de un haz dispersado y enfocado sobre la rendija
S2. en cualquier momento esté determinada por el
Angulo de la graticula GI en dicho momento. La 10-
tacién de la graticula Gl produce un rastreo de ban-
das de frecuencia en la rendija de salida S2 conse
cuentemente en el detector. Los filtros se insertan
automaticamente en la trayectoria de radiacién en la
rendija de salida en cierta secuencia pare eliminar
la radiacién indeseable; esta radiacién indeseable co-
rresponde a los miiltiples arménicos de la frecuencia
por medir.
La resalucion avixima se loger mediante el uso de
agraticulas solamente en el intervalo de ht nxiinna ef
tividad de dispersion. Fu consecuencia, para el caso
de un instrumento moderno de alta resolucion, sc
hace uso de dos o mis graticuls (Cl y G2 de la
figura 4).
Cuanto mis estrecha sea la amplitud de la rendija
mayor ¢s la resolucion. Ln este caso, nucvamente, tal
compromiso se hace necesario debido a lt reduccion
en Iz salida de energia de Ja fuente a las frecucncias
inferiores (longitudes de onda mavores). Fin la_ma
voria de los instrumentos, la amiplitud de rendija se
programa para aumentar conforine disminuye la ener
gia trasmitida por la fuente, con To cual la cne
del haz de referencia que entra al monocromador ¢s
constante.
Detector (TerMorar). Después de abandonar la
rendija de salida del monocromador, el haz se refleja
por medio del espejo aplanado M13 hacia el espejo
clipsoide M14, Ei foco del espejo elipsoide se encuen
tra en la rendija de salida $2 y en el detector.
El detector consiste en tm dispositive que mide la
energia radiante por medio de su efecto de calenta
miento. Dos tipos comunes de detectores son el ter
mopar y el bolémetro. En el detector de termopar, la
energia radiante calienta una de dos juntas bimetili-
cas ¥ se produce una fem entre las dos juntas que
€s proporcional al grado de calentamiento. EI bolé-
metro cambia de resistencia a causa del calentamien-
to. Sirve como un brazo de un puente, de modo que)
el cambio de temperatura origina una seal desbalan-
ceada a través del circuito. La seftal desbalanceada
puede amplificarse y registrarse 0 utilizarse pars acti-
var un servomecanismo fon objeto de volver a esta
blecer el balance.
Ya que el detector percibe alternativamente el haz
de referencia y el de muestra a una frecuencia de
conmutacién determinada por la rotacién del espcjo
de sector, cualquier cambio en ha intensidad de radia
cién debido a la absorcién se detecta como sefial fucra
de nulo.
La sefial fuera de nulo amplificada del detector se
utiliza para’ situar el atenuador éptico de modo que
la radiacién del haz de referencia y del de muestra
se conserven en la misma intensidad. La proporcién
de atenuacién requerida constituye una medida di
recta de la absorcién por parte de la muestra, E] mo-
vimiento’ del atenuador se registra por medio de a
plumilla de carta del registrador.
IV. Manejo de la muestra
Los espectros infrarrojos se pueden obtener para gs
8€5, liquidos 0 sdlidos.
1. El espectro de gases 0 liquidos de bajo punto
de ebullicién puede lograrse mediante la expansién de
92 ADENTIFICACION ESPECTROMETRICA DE COMPUESTOS ORGANICOS
ta muestra en el interior de una celda al vacio. Las
celdas cquupadas con puntas cle expulsion por conge
lacion s¢ utilizan para la concentracion de la muestra
y esacuacidn de la celda antes de la expansién de la
inestra en el interior de ta celda. Se dispone de cel-
das de gases con longitudes desde algunos centimetros
hasta 40 metros. El area de muestra de un espectro:
fotdmetto infrarrojo cstindar no permite el acomodo
de celdas mucho mayores de 10 cm; las trayectorias
luigas se logran mediante un sistema dptico de re
fleidn maltiple
La técnica en fase vapor es de caricter limitado
debido al porcentaje relativamente alto de compo:
nentes que no tienen la suficiente presién de vapor
para producir un espectro de absorciin itil. Sin em
hargo, la utilidad de la técnica puede aumentarse
mediante el calentamiento de la celda.
La determinacién de los espectros infrarrojos de
compuestos volatiles, tal como se obtienen de la cro
matografia de gas, ¢s posible ahora mediante el uso
del espectrofotdmetzo infrarrojo de rastreo rapido.
Se ha informado que este instrumento puede lograr
tun rastreo completo desde 2.5 hasta 14.5 am en 4
segundos. Los espectros se obtienen con 30 microgra:
mos de efluente volitil.
2. Los liquidos pueden examinarse en forma pura
0 en solucién. Los liquidos puros se examinan entre
placas de sal y normalmente sin un separador. El pren-
sado de una muestra liquida entre placas planas pro-
duce una pelicula de 0.01 mm 0 menos de espesor;
las placas se mantienen unidas por capilaridad. Se
requiere de muestras de 1-10 mg. Las muestras espe-
s35 de liquidos puros generalmente absorben demasia
. do intensamente produciendo espectros satisfactorios.
Los liquidos volitiles se examinan en celdas selladas,
con separadores sumamente delgados. Las placas KRS-5
o de cloruro de‘plata se utilizan para las muestras que
disuelven las placas de cloruro de sodio. Recientemen-
te se han puesto a la disposicfén las ventanas de clo-
muro de plata de bajo costo,t las cuales permiten
realizar el andlisis infrarrojo a través de pelicula fina,
siendo las longitudes de traycctoria de 0.025 0 0.050
mm (figura 5).
Las soluciones se manejan en celdas de 0.1-1 mm
de espesor. Se requiere de voltimenes de 0.1-1 ml de
soluciones de 0.05-10% para el caso de las celdas des:
montables que pueden conseguirse con facilidad. Una
zelda de compensacién, que contenga el solvente puro,
se coloca en el haz de referencia. El espectro resul-
tante corresponde al soluto excepto en las regiones
donde el solvente tiene una absorcién intensa. Por
Gemplo, las muestras concentradas de tetracloruro de
arbono absorben intensamente cerca de 800 cm*
(12.50 wm); la compensacién de esta banda es inefee-
* Beckman Instruments, Inc., Fullerton, Calif, Modelo 1R-102.
‘ Wilks Sciemtfic Corp., Norwalk del Sur, Conn
Ventanas colocedas pora: el pulido
Ventanas celecodes para une longitud
de trayectoria de 0.025 mm
| (ZI)
Ventonas colocedas pore una lengitud de wayectoria de 0.05 mm
Voricciones de longitud de trayectotia de lazventanas de minicelda
Ficura 5. Equipo para el anélisis'espectral IR de pe-
licula fina (muestra pura) y en solucién.
tiva ya que la abgorcién intensa evita que cualquier
radiacién Hegue al detector.
El solvente seleccionado debe ser seco y razona-
blemente trasparente en la regidn de interés. Cuando
todo el espectro es de interés, se puede hacer uso de
varios solventes. Un par comiin de solventes ¢s el te-
tracloruro de carbono y el disulfuro de carbono. El
tetracloruro de carbono se encuentra relativamente
exento de absorcién a frecuencias superiores a 1333
cn (menos de 7.50 nm) mientras que el disulfyro
de carbono muestra poca absorcién menor de 1383
cm (mayor de 7.50 zm). Deben evitarse las comb
naciones de solvente y soluta de que reaccionan. Pi
ejemplo, el disulfuro de carbono no puede emplearse
como solvente para las aminas primarias 0 secunda-
rias. Los amino alcoholes reaccionan lentamente con
el disulfuro de carbono y el tetracloruro de carbono.
‘Cuando solamente se dispone de muestras suma-
mente pequefias, se utilizan las celdas de cavidad ul-
tramicro en conjunto con un condensador de haz. La
celda mis pequeita de disponibilidad comercial tiene
una longitud de trayectoria de mas 0 menos 0.05 mm
ESPECTROMETRIA INFRARROJA 93
Ficuna 6. Miniprensa y operacién. (a) Soporte de celda.
(b) Tuerea = celda. (c) Pertos.
y una capacidad cercana a 0.8 microlitros.* De este
modo puede lograrse un espectro con algunos micro:
gramos de muestra en solucién. Cuando la volati
lidad lo permite, el soluto puede recuperatse para su
examen mediante otras técnicas espectrométricas.
El modelo de absorcién de los salventes scleccio
nados ¢ los aceites de molienda se presentan ene)
apéndice A.
3. Los sdlidos se examinan generalmente en forma
de una pasta untable, un disco. prensado 0 como pe
licula vidriada depositada
Las pastas o stspensiones untables se preparan me
diante la molienda uniforme de 2-5 mg del sdlido en
un mortero de Agata liso. La molienda se continéa
después de la adicién de una o dos gotas del aceite de
molienda. Las particulas suspendidas deben ser me
nores de 2 xm para evitar la dispersion excesiva de la
radiacién, La suspensién untable se examina en Ia for-
ma de una pelicula fina entre placas de sal planas. El
nujol (un aceite de petréleo de alto punto de ebulli
cién) cominmente se utiliza como agente de molien-
da, Cuando las bandas de hidrocarburo interfieren con
el espectro, se puede hacer uso del fluorolube (un
polimero completamente halogenado que contiene F
y Cl) 0 el hexaciorobutadieno. El uso de las suspen-
siones untables de nujol y fluorolube hace posible el
rastreo, esencialnente libre de bandas de interferencia,
cen la regién de 4000 cm~ a 250 cm (2.5-40.0 wm)
La técnica del disco prensado depende del hecho
de que el bromuro de potasio pulverizado y seco (u
atros haluros de metal alcalino) se pueda prensar bajo
presién al vacfo para formar discos trasparentes. La
muestra (0.5.1.0 mg) se mezcla intimamente con una
cantidad de aproximadamente 100 mg de bromuro de
potasio pulverizado y seco. El mezclado puede reali
zarse mediante la molienda cuidadosa en un mortero
de Agata liso 0, mis eficientemente, con un pequeiio
moling de bolas vibratorio, o-por medio de Ia liofili-
zacién. La mezcla se prensa para formar un disco
trasparente, utilizando matrices especiales, a una pre-
siém de 704-1056 kg/em*. La calidad del espectro de-
pende de la intimidad del mezclado y de la reduccién
de las particulas suspendidas hasta 2 jam o menos. Los
microdiscos (su didmetro es de 0.5 a 1.5 mm) pueden
utilizarse conjuntamente con un condensador de haz.
La técnica del microdisco permite el examen de mues-
tras tan pequefias como un microgramo. Las bandas
cerca de 3448 cm y 1639 em (2.9 y 6.1 pm) debi
das a la humedad frecuentemente aparecen en los
espectros obtenidos mediante la técnica del disco pren
sado (véase el espectro del HzO en el apéndice A)
Frecuentemente se ha evitado el uso de los discos
© grinulos de KBr, debido a la pericia requerida
]a formacién de grinulos satisfactorios. Tales técni
del KBr pueden ser més accesibles mediante el uso di
Ja miniprensa (figura 6) en que se usa un procedi
miento simple; la’ mezcla de K8rmuestra se coloca
en la porcién de tuerca del dispositivo con un tor
nillo en su lugar. Se introduce el segundo tomillo o
pemo y se aplica presién por medio del apriete de los
pemos. La remocién de los pernos deja un grénulo
en la tuerca que ahora sirve como celda.
* Barnes Engineering Co, Instrument Division, Stamford,
Conn,
94 IDENTIFICACION ESPECTROMETRICA DE COMPUESTOS ORGANICOS
Las peliculas depositadas son de utilidad solamente
cuando el mate:ial puede depositarse a partir de una
solucién 0 enfriarse 2 partir de una masa fundida en
forma de mictocristales o en la forma de una pelicula
vidriosa. Las peliculas cristalinas generalmente origi-
nan una gran dispersin de la luz. La orientacién es-
pecifica del cristal puede dar lugar a espectros que
difieren de los observados para particulas orientadas
al azar, tal como existen en un amasijo o disco de
haluro. La técnica de la pelicula depositada es de par-
ticular efectividad para la obtencién de los espectros
de resinas y plasticos. Se debe tener cuidado en cuanto
a liberar a la muestra del solvente por medio del tra-
tamiento al vacio o el calentamiento moderado.
La técnica conocida como espectroscopia de te:
flexién intema o de reflexién total atenuada se puede
utilizar actualmente para obtener los espectros cuali
tativos de sélidos independientemente del espesor. La
téenica depende de que el haz de luz reflejado inter
namente desde la superficie de un medio de trasmi-
sién pase a una corta distancia del limite de reflexién
y tegrese al medio de trasmisién como parte del pro-
ceso de reflexién, Cuando un material (por ejemplo,
la muestra) de menor fndice de refraccién que el
medio de trasmisién se lleva al contacto con la super-
ficie reflectora, la luz pasa através del material hasta
una profundidad de algunas’ micras, produciendo un
espectro de absorcién. Una ampliacién de la técnica
considera las reflexiones interna multiples a lo largo
de la superficie de la muestra. La técnica de reflexio-
nes interna miltiple da como resultado espectros de
intensidades comparables con las espectros de tras-
misién.*
En términos generales, la solucién diluida en un
solvente_no polar proporciona el mejor espectro (es
decir, ei menos distorsionado). Los compuestos “no
polates proporcionan esencialmente el mismo espectro
én la fase condensada (0 sea, el iquido puro, un ama-
sijo, un disco de KBr o una pelicula) que el corres-
pondiente al obtenido en solventes no polares. Sin
embargo, los compuestos no polares frecuentemente
manifiestan efectos de enlazamiento de hidrégeno en
la fase condensada. Desafortunadamente, los compues-
tos polares a menudo son insolubles en los solventes
no polares y el espectro debe obtenerse ya sea en fase
condensada o en un solvente polar; este iltimo intro
duce la posibilidad del enlazamiento de hidrégeno del
solvente-soluto.
Se debe tener un cuidado razonable en el manejo
de las celdas y placas de sal, y emplear muestras li-
‘bres de humedad. Los dedos no deben quedar en con-
tacto con las superficies dpticas. Asimismo, hay que
tener cuidado de evitar la contaminacién con silico-
nes, los cuales resultan dificiles de remover ademas de
que tienen modelos de absorcién intensa.
* Wilks Scientific Corp,, Norwalk del Sur, Conn,
V. Interpretacién de datos
No existen reglas rigidas para la interpretacidn de
tun espectto infrarrojo. Sin embargo, hay cierto’Ne-
quisitos que deben satisfacerse antes de intentar la
interpretacién de un espectro.
1. El espectro debe cstar resuelto adecuadamente y
tener una intensidad apropiada.
2. El espectio debe corresponder a un compuesto
razonablemente puco.
3. El espectrofotdmetro debe calibrarse de modo que
las bandas se observen a las frecuencias o longi.
tudes de onda adecuadas. La calibracién apropiada
puede realizarse mediante estindares confiables
tal como una pelicula de poliestireno.
4. Debe especificarse el método de manejo de la
muestra. Cuando se usa un solvente, debe indi-
carse el solvente, la concentracién y el espesor
de la celda.
No ¢3 posible el tratamiento preciso de las vibra-
ciones de una molécula compleja; siendo asi, el espec-
tro infrarrojo debe interpretarse mediante la compa-
racién empirica de los espectros, y la extrapolacién de
estudios de moléculas mis simples, Muchas de las in-
terrogantes en la interpretacién de un espectro infra-
rojo pueden responderse a partir de los datos obtenidos
de los espectros de masas, ultravioleta y RMN,
La absorcién infrarroja de las moléculas orginicas
se ha resumido en una tabla de frecuencias de grupo
caracteristicas que se incluye en el apéndice B. Muchas
de las frecuencias de grupo varian dentro de un in-
tervalo amplio debido a que las bandas se originan a
partir de vibraciones de interaccién complejas dentro
de la molécula. Sin embargo, las bandas de absorcién
representan fundamentalmente a una forma vibracio-
nal simple. Por ejemplo, las bandas de absorcién que
se derivan de las formas de alargamiento C-H, O-H.
y C=O permanecen dentro de regiones relativamente
estrechas del espectro. Algunos detalles importantes
de la estructura pueden determinarse al conocer la
posicién exacta de una banda de absorcién dentro de
estas regiones estrechas. Los desplazamientos en la po-
sicién de absorcién y los cambios en los contornos
de la banda, lo cuales acompafian a los cambios del
medio molecular, también pueden sugerir detalles es-
tructurales de importancia.
Las dos dreas de importancia para el examen pre:
liminar de un espectro corresponden a las regiones de
4000-1300 cm (2.5-7.7 wm) y 909-650 em (11.0-
154 zm). La porcién de longitud de onda corta (ener-
gia alta) del espectro se denomina regién de grupo
funcional. Las frecuencias de alargamiento caracteris-
ticas para los grupos funcionales de importancia tales
como el OH, NH y C 4 O se presentan en esta por-
cién del espectro. La afsencia de absorcién en los
intervalos definidos para Jos diversos grupos funciona-
les generalmente pueden{emplearse como prucbas de
ESPECTROMETRIA INFRARROJA 95
Longitd de ond wm
Por cent de trosmiancia
2000
i800
Numero de onda, emt
@
Numero de ondo, ent!
1500
1000 900,
haa]
15
9
13 14
Longitud de endo, ym
Ficuna 7. Rotiestireno:
‘ia ausencia de tales grupos en la moléeula. Sin em-
bargo, debe fenerse cuidado en las interpretaciones
de este tipo ya que ciertas caracteristicas estructurales
pueden originar que una banda se debilite v se vuelva
extremadamente amplia como para no ser notada. Pot
ejemplo, el enlazamiento de hidrégeno intramolecu-
Jar en la forma enélica de acetilacetona da por resul
tado una banda de OH amplia y débil, la cual puede
pasar desapercibida, La ausencia de absorcién en la
regién de 1850-1540 emt (5.40-6.50 xm) excluye a
9%
@®
la muestra es igual para (a) y (b). (a) lineal en numero de onda (emt); (b) lineal en
ongitud de onda (xm).
la estructura que contenga un grupo carbonilo. Las
bandas débiles en la regin de longitud de onda corta,
que resultan de la absorcién fundamental de grupos
funcionales como el S-H y el C=C, son sumamente
valiosas en la determinacién de la estructura. Tales
bandas débiles serian de pqco valor en las regiones
mis complicadas del espectlo. Los sobretonos y los
tonos de combinacién de barflas con longitud de onda
mayor aparecen frecuentemepite en de én de lon:
gitud de onda corta del espectro. Las oe Klas de sobre
IDENTIFICACION ESPECTROMETRICA DE COMPUESTOS ORGANICOS
tono } combinacién de tonos son caracteristicamente
debiles excepto cuando se presenta la resonancia de
Fermi. Las bandas esqueletales intensas para los aro
miticos v los heteroaromaticos quedan en la region
de 1600-1300 cm-* (6.25-7.70 wm) del espectro.
La falta de bandas de absorcién intensa en la re
gion de 909-650 cm (11.0-15.4 um) generalmente
mndica una estructura no aromitica. Los compuestos
aiomaticos v heteroaromaticos manifiestan bandas de
absorcién de flexién anular vy flexién C-H_ fuera
de plano en esta region que frecuentemente pueden
correlacionarse con el modelo de sustitueién. La absor
cién_moderadamente intensa y amplia en la region
de longitud de onda larga sugiere la presencia de di.
meros de acido carboxilico, aminas o amidas, todos los
cuales manifiestan flexién fuera del plano en esta
regién. Cuando la regién se extiende hasta 1000 em-*
(10.0 wm), quedan incluidas bandas de absorciém ca-
racteristicas de las estructuras olefinicas.
+ La porcién intermedia del espectro, 1300-909 em-*
(7.7-11.0 um), generalmente se denomina regién de la
“huella digital”. El modelo de absorcidn en esta regién
fecuentemente es complejo, y las bandas se originan
en formas de vibracién interaccionante. Esta porcién
del espectro es de suma utilidad cuando se examina
con referencia a otras regiones./Por ejemplo, si la ab-
sorcién de alargamiento O-H alcohélico 0 fendlico
aparece en le regin de longitud de onda corta del
‘spectro, la posicidn de la banda de absorcién C-C-O
en Jz region de 1260-1000 cm (7.93-10.00 pm) fre:
cuentemente hace posible asignar la absorcién OH a
los alcoholes y fenoles con estructuras altamente es
pecificas. La absorcién en esta regién intermedia
probablemente resulta Gnica para cada especie mo-
lecular.
Cualquier conclusién a ls que se Iegue después
dei examen de una banda particular deberd confir
marse cuando sea posible mediante el examen de otras
porciones del espectro. Por ejemplo, la asignacién de
una banda de carbonilo a un aldehido debe confimar.
se por la aparicién de una banda o un par de bandas
en la region de 2900-2695 cm-* (345-371 um) del
perio, To. cual se origina de la vibracién de alarga.
miento C-H del grupo aldehido. De modo similar, la
asignacién de una banda de carbonilo a un éster debe
confirmarse mediante la observacién de una banda
intensa en la regién de alargamiento C-O, 1300-1100
car? (7.69.1 pm).
Finalmente, en una comparacién de “huella digi-
tal” de espectros,'0 en cualquiera otra situacién en
que las formas de los picos sean de importancia, se
debe considerar por anticipado el cambio considerable
de ls apariencia general del espectro al pasar dé un
‘spectro que es lineal en la escala de mimero de onda
2 uno que sea lipeal en la longitud de onda (fi
zu 7)
VI. Freeuencias de grupo caracteristicas
de las moléculas orgénicas
En el apéndice B se presenta una tabla de frecuen
cias de grupo caracteristicas. Los intervalos presentados
para las frecuencias de grupo se han definido despues
del examen de muchos compuestos en que se encuen:
tra presente el grupo. Aun cuando los intervalos estan
bastante bien definidos, la frecuencia o longitud de
onda precisa a la que absorbe un grupo especifico
cepende de su medio ambiental dentro de la molécala
y de su estado fisieo.
Esta seccién del capitulo se, relaciona con la re
Vision comprensiva de estas frecuencias de grupo ca-
racteristicas y con su correlacién con la estructura
molecular. Los libros que deben consultarse como su-
plemento de esta segeién son los de Bellamy? Con
ley" y Colthup, Daly y Wiberley."*
‘A medida que se introduce cada nuevo tipo o clase
de molécula o grupo funcional en las secciones pos-
teriores, se proporcionari un ejemplo de espectro in-
frarrojo con las asignaciones de pico importantes. En
el apéndice A se hard referencia 2 los ejemplos de es-
pectios infrarrojos, que constituyen miembros de diver-
sas clases de estas moléculas orginicas; los espectros
de ee apéndice no disponen de asignaciones de ab-
sorcién detalladas.
PARAFINAS (ALCANOS) NORMALES
El expectro de las parafinas normales puede inter-
pretarse en términos de cuatro vibraciones, es decir,
el alargamiento y flexién de los enlaces C-H y C-C.
EI andlisis detallado de los espectros correspondientes
a los miembros inferiores de la serie de los alcanos ha
hecho posible establecer las asignaciones detalladas
de las posiciones espectrales de los modos de vibracién
especificos.
No todas las frecuencias de absorcién posibles de
la molécula de parafina tienen el mismo valor en la
asignacién de la estructura. Las vibraciones de flexi6n.
C-€ ocurren a frecuencias bastante bajas (inferiores
2500 cm", mayores de 20 um) y consecueatemente
no apareceén en nuestros espectros. Las bandas asigna-
das ales vibraciones de alargamiento Q-C son débiles
y aparecen en la region amplia de 1200-800_cm™ (8.3
12.5 ym); por lo general, son de poca utilidad para la
identificacién. *
Las. vibraciones mds catacteristicas son las que se
derivan del alargamiento y-flexién C-H. De estas vi-
braciones, las que se derivan del torcimiento y en
abanico metilénico normalmente tienen un valor de
diagnéstico limitado debido a su debilidad e inesta-
bilidad, siendo esta Gltima el resultado de un fuerte
acoplamiento con el resto de la molécula.
x
ESPECTROMETRIA INFRARROJA 97
s 1
Peso Expeciogiome
ODECANO inolecel pees
evn Inleorrox0
=. Ac ane
A: alargamiento ©-11; CH, 2962 can-* (3.38 jxm), vagCH,
“2872 em! (3.48 ym), »,CH,
CH, 2926 cm! (343 pm), eye
2953 cu! (3.51 jm), ve
B: flexién C-H CH, 1375 cm (7.28 pm), 8 ‘
1450 cm (6.90 pin), Bae
CHy L465 cm? (6.83 wm), 8,CH,
Cr oscilaciin CH, CH, 720 m+ (13.9 pm)
Fioura 8,
Los modos de vibracién de las parafinas son comu-
nes a muchas de las moléculas orginicas. Aun cuando
las posiciones de las frecuencias de flexién y alarga
miento C-H de los grupos metilo y metileno perma
necen_pricticamente-constantes en los hidrocarbutos,
Ja unién del CH, 0 CH, a Atomos:distintos del car-
bono, o a un grupo carbonilo 0 anillo aromitico, pue-
‘den dar como resultado desplazamientos notables de
‘las frecuencias de flexién y alargamiento C-H. Estos
dcsplazamientos se resumen en las tablas Ty IT del
apéndice C.
El espectro del dodecano, figura 8, es tipico de ur
hidrocarburo de cadena recta 0 lineal.
“._ Vibraciones de alargamiento C-H, =
‘La absorcién que se origina del alargamiento cH
en los alcanos ocurre en la region general de 3000-2840
em (3.33.5 um). La posicién de las vibractones de
~alargamiento C-H pueden considerarse como dentro
de las mas estables del espectro. Cuando el espectro
se obtiene con un instrumento que dispone de un
\ prisma de cloruro de sodio, las bandas de esta regién
frecyentemente quedan sin resolucién (como en la
figura "8). La resolucién se logra mediante e) uso de
un prisma de fluoruro o un instrumento de graticula.
Gaupos aesito. El examen de iuna gran cantidad
de Fidrorarburos saturados que contienen grupos me-
tilo, en todos los casos ha demostrado que se presen:
tan dos bandas definidas en,2962 cm" (3.38 um) y a
2872 cor (3.48 ym). La primerarde estas resulta del
“tnodo de alargamiento asimétrico en que dos enlaces
C-H del grupo metilo se extienden mientras que el
tercero se ‘contrae (r,CH,), Laseaunda se deriva
del_alargamiento_simétrico (v.CH,) en que Ios tres
enlaces se extienden o se contracn en fase. La
presencia de varios grupos metilo en la molécula re-
sulta de una absorcién intensa en estas posiciones.
Gropos METILENO. El alargamiento asimétrico (vs.
CH,) y el alargamiento simétrico (v,CH.) ocurre,
-sespectivamente, cerca de 2926-cmr* (3.43 um) y 2853
cm (3.51 zm). Las posiciones de estas bandas no
varian mis de +10 cm** en los hidrocarburos aliféticos
y ciclicos sin tensién. La frecuencia del alargamieuto
metileno se incrementa cuando el gnipo metileno for-
ma parte del anillo sometido a tension.
Vibraciones de flexién C-H
Grupos mento. Dentro de un grupo metilo ocu
ren dos vibraciones de flexién. La primera de estas,
la vibracién de flexién simétricag implica la flexién’ en.
fase de los enlaces C-HI (1). La segunda, es decir,
vibracién de flexién asimétrica, implica la flexién fue
ra de fase de los enlaces C-H (11).
En los diagramas anteriores, el centro del Atome
de carbono se encuentra en el plano de la pigina cor
Jos Atomos de hidrégeno localizados y moviéndose
esencialmente atriba y abajo del plano de la pigina
La vibracién de'flexién simétrica.(8,CH) ocurre cére:
de 1375 emr* (7.28 am) y la vibracién de flesién asi
miétrica (8,,CH,) cerca de 1450 em (6:90 am).
[398 -WDENTIFICACION ESPECTROMETRICA DE COMPUESTOS ORGANICOS
La vibracién asimétrica generalmente se_traslapa
con la vibracién de tipo tijera del grupo metileno (véa-
se mas adelante). Sin embargo, se obscrvan dos bandas
definidas en los compuestos tal como la dietilcetona,
donde la banda de tijera del metileno ha sido despla-
zada hacia una frecuencia menor, 1439-1399 em? (6.95.
7.15 am) y ha aumentado de intensidad debido a su
proximidad al grupo carbonilo
La banda de absorcién cerca de 1375 om (7.28
um), que se origina en la flexién simétrica de los enla
ces C-H metilgne, es bastante estable en cuanto a su
posieién cuando el grupo metilo se encuentra unido
2 otto atomo de carbono. La intensidad de esta banda
es mayor por cada grupo metilo en el compuesto en
comparacion con la vibracién de flexién de metilo
asimétrica o la vibracién tipo tijera del ietileno.
Grupos meviteno. Las vibraciones de flexién de
los enlaces C-H en el grupo metileno ya se han
mostrado esquemiticamente en la figura 1. Las cua-
tyo vibraciones de flexién se denominan vibracién de
tijera, vibracién de oscilacién, vibracién de abanico
y vibracién de torcimiento.
La_banda.de vibracién en tijera (8,CH) en el
expectio de los hidrocarburos se presenta a una. posi-
ciGn_casi constante, cerca de 1465 em (6.83 nm).
La banda que resulta de la vibracién de oscilacién
del metileno (eCH:), donde todos los grupos metileno Ww.
oscilan en fase, aparece cerca de 720 cm (13.9 xm)
para el caso de las parafinas de cadena recta de siete
o més 4tomos de carbono. Esta banda puede apare
cer en la forma de un doblete en el espectro de las
muestras sélidas. En los miembros inferiores de la se
tie de n-parafinas, la banda aparece 2 frecuencias algo
mayores.
La absorciém. de los hidrocarburos, debida a las
vibraciones de torcimiento y en abanico del metile-
no, se observa en la region de 1350-1150 cm (7.4
2A-DIMETILPENTAHO Peso
* procedentia
Ficura
A: alargamiento C-H (véase la figura 8).
B. flexion C-H (véase la figura 8).
Observe el doblete (C) de gem-dimetilo, 1385 cm? (7.22 wm)
8.7 yin), Estas bandas generalmente son bastante mas
débiles que las resultantes de la vibracién en. tijera
del metileno. Una serie de bandas en esta region, de
rivadas del grupo metileno, es caracteristica de los es-
pectros de mucstras sOlidas comespondientes a ésteres,
amidas y dcidos de cadena larga.
HIDROCARBUROS DE CADENA RAMIFICADA
En términos generales, los cambios originados en
el espectio de un hidrocarburo por la ramificacién re-
sultan de los cambios en las vibraciones de alargamien-
to esqueléticas y en las vibraciones de flexién del me
tilo; esto se presenta abajo de 1500 cm (mavor de
6.7 nm). El espectro de la figura 9 corresponde @ un
hidrocarburo ramificado tipico
Vibraciones de alargamiento C-H
Grupos c-it TeRcrAnids. La absorcién resultante de
este modo de vibracién es bastante débil y general-
mente se pierde en otra absorcidn C-H alifatica. La
absorcién en los hidrocarburos se presenta cerca de
2890 cm (3.46 um). 5
Vibraciones de flexién C-H
Grupos cem-prmento. Las configuraciones donde
dos grupos metilo se encuentran unidos al mismo dto-
mo de carbono manifiestan una absorcién distintiva
en Ja regién de flexién C-H. El grupo isopropilo ma-
nifiesta un doblete intenso, con picos casi dé la misma |
intensidad, a 1385-1380 emt (7.27.25 wm) y a 13705
1365 cm (7.30-7.33 um). El grtpo butilo terciario.
origina dos bandas de flexién C-H,, una en Ia regién
1395-1385 em (7.17-7.22 um) y otra cerca de 1370
,
som Expectrograma infrorojo!™
9.
1368 cm (7.31 am).
ESPECTROMETRIA INFRARROJA .99.
em (730 ym). En el doblete del thutilo, fa banda
con Tongitud de onda larga es mas intensa, Cuando los
grupos genvdimetilo se encuentran en una posicién
intema, el doblete se observa pricticamente en la mis
ma region donde ocurte la absorcién de los grupos
isopropilo y t-butilo. Los dobletes de los grupos gem:
dimetilo se observan debido 2 la interaccién entre la
flexin simétrica en fase v fuera de fase de CH, co-
espondiente a los dos grupos metilo unidos a un
tomo de carbono comin
n los grupos isopropilo y tbutilo resultan bandas
debiles derivadas de las vibraciones ce oscilacién del
metilo. Estas vibraciones son sensibles a la masa y
Ja interaccién con los modos de alargamiento esque
letal_y por lo general son menos confiables que las
vibraciones de flexion C-H. Se han establecido las si
guientes asignaciones: grupo isopropilo, 922-919 cm
(10.85-10.88 zm) y grupo t-butilo, 932-926 em (10.73
10.80 pm)
CICLOPARAFINAS (ALCANOS CICLICOS)
Vibraciones de alargamiento C-H
Las vibraciones de alargamiento metileno de las
estructuras de polimetileno ciclicas son bastante pa-
recidas a las observaciones en las parafinas acielicas
EI incremento dll esfuerzo anular desplaza las bandas
de alergamiento C-H progresivamente hacia frecuen
ccias superiores. Los grupos CH y CH, anulares en cl
‘ciclopropano monoalquilico absorben en la regién de
3100-2990 curt (3.23.2 3.34 pm)
Vibraciones de flexién C-H
La ciclizacién disminuye a frecuencia de la
cién en tijera del CH,. El ciclohexano absorbe f 1452
cm (6.89 pm), mientras que el mhexano absor
1468 cm-* (6.81 jan). El ciclopentanio absorbe a 1455
“em (6.87 ym) y el ciclopropano a 1442 cm (6.94
pin). Este desplazamiento frecuentemente hace posi-
ble observar bandas definidas para la absorcién del
metileno en esta regidn, Los espectros de otros hidro:
carburos saturados aparecen en el apéndice A: hexa
no, 0. 1; nujol, no. 2, y ciclohexano, no. 3.
HIDROCARBUROS OLEFINICOS v
(ALQUENOS)
La estructura olefinica introduce varios niodos nue-
vos de vibracién en la molécula de hidrocarburo: una
vibracién de alargamiento C = C, vibraciones de alar-
gamiento C-H donde el dtomo de carbono se encuen-
tra presente en el enlace olefinico, y la flexién en
plano y fuera de plano del enlace C-H olefinico. El
espectto de la figura 10 corresponde a una olefina ter-
minal tipica.
100
Vibraciones de alargamiento C = C
Onerias Laneaues six conyucar, El modo de
alargamiento C = C de las olefinas.sin conjugar usual
mente se manifiegta en la forma de una absorcion
débil en 1667-1640 cm (6.00-6.10 nim), Las olefinas
monosustituidas (por ejemplo, los grupos vinilo) ab
sorben cerca de 1640 cm (6.10 xm) con intensidad
moderada, Las olefinas trans disustituidlas asi como las,
olefinas tri_v tetralquilo sustituidas absorben en 0
cerca de 1670 cm (5.99 pin); las olefinas cis disus
tituidas y las olefinas de tipo vinilideno absorben cerca
de 1650 cur* (6.06 wm)
La absorcién de las olefinas trans disustituidas 0
de las olefinas tetrasustituidas puede ser extremada
mente débil o ausente, Las olefinas cis, que adolecen
de la simetria de la estructura trans, absorben mi
intensamente que las olefinas trans. Los dobles nla
ces internos generalmente absorben con mayor debi
lidad que los dobles enlaces terminales debido a lt
seudosimetria,
La absorcién a una frecuencia anormalmente alta
se observa en el caso de los grupos ~ CH = CF, y
= CF = CF, El primero’ absorbe cerca de 1754 cn"
(5.70 pm) y el ltimo cerca de 1786 cm” (5.60 -.m)
En contraste, la frecuencia de absorcién se reduce por
1 acoplamiento del cloro, bromo o vodo.
Cicouermas, La absorcién del doble entace in:
temo en cl sistema de ciclohexeno sin esfuerzo es pric
ticamente la misma que la del isémero cis en el siste
ma aciclico, La vibracién del alargamiento C = C se
acopla con el alargamiento C-C de los enlaces adya
Jc
centes. A medida que el angulo « (c 2S
se vuelve menor, la interaccién es inferior hasta Hegar
aun minimo a 90° en el ciclobuteno (1566 cm,
639 jan). En la estructura del ciclopropeno, la inter-
accién_nuevamente se vuelve notable y" le frecuencia
de absorcién aumenta (1641 cnr, 6.09 jm).
La sustitucién de grupos alquilo por un atomo de
hhidrdgeno en los sistemas anularés sometidos a ten:
sign sitve para inerementar la frecuencia de la absor
cién C= C. El ciclobuteno absorbe a 1566 em (6.39
um) y el I-metileiclobuteno a 1641 em (6.09 xm).
La frecuencia de absorcién de los enlaces olefini
cos externos (exociclico) aumenta al disminuir cl
tamaiio del anillo, El metilenciclohiexano absorbe a
1650 cm-* (6.6 um) v el metilenciclopropatio a 178)
em" (5,62 am)
Sistemas Conjucavos. Las vibraciones de alarge
miento de enlace olefinico en los dienos conjugados
sin centro de simetria interaccionan_ para producir dos
bandas de alargamiento C=C. El espectro de un
dieno conjugado asimétrico, tal como el I,3:pentadie
no, muestra absorcién cerca de 1650 em (6.06 wm)
y cerca de 1600 cm (6.25 ym). La molécula simé.
trica, 1,3-butadieno, muestra solamente una banda
IDENTIFICACION ESPECTROMETRICA DE COMPUESTOS ORGANICOS
Povo
1-BECENO
malzculor PE
Procedencio:
ESPECTROGRAMA
INFRARROIO 5909
= Celda: do 0.025 mm” Rostreo en Perkin-Elmer 21
Ficura 10
alargamiento C-H (véase la figura 8)
alargamiento C = C, 1645 cm-t (6.08
flexion C-H fuera de plano: 986 a (it 14 ym)
(olefinico) 907 em-* (11.03 jm)
oscilacién metilénica: 720 cm (13.88 jm).
= 99 PF
cerca de 1600 cm" (6.25 um), que resulta del alar
gamiento asimétrico; la banda de alargamiento simé
trico es inactiva en el infrarrojo.
La conjugacién de un doble enlace olefinico con
un anillo aromatico produce una mejor absorcién ole-
finica cerca de 1625 cm~ (6.15 um),
La frecuencia de absorcién del gnlace olefinico en
la conjugacién con un grupo catbonilo se reduce
aproximadamente en 30 cm (ca, 0.11 xm); Ta in-
tensidad de la absorcién aumenta, En las estracturas
s-cis, la absorcién olefinica puede ser tan intensa como
Ja del grupo carbonilo. La estructura s-trans absorbe
mis débilmente que las estructuras s-cis,
Oxerinas acumutabas. Un sistema de doble en-
lace acumulado, tal como ocurre en los alenos
N\
( C=Ce ctu) » absorbe cerca de 2000-1900 cm-*
fo
(5.00-5.26 nm). La absorcién resulta del alargamiento
simétrico C = C = C., La absorcién puede. conside-
rarse como un caso extremoso de la absorcién C = C
exociclica,
Vibraciones de alargamiento C-H olefinico
En general, cualquier banda de alargamiento’ C-H
arriba de 3000 cm (abajo de 3.33 um) resulta del
alargamiento C-H oletinico, acetilénico, heteroaromé-
tico 0 aromético. También se encuentra dentro de la
misma regién el alargamiento C-H en los anillos pe-
quefios, tal como el ciclopropano, y el C-H en los
grupos alquilo halogenados, La frecuencia y la inten-
sidad de la absorcién del alargamiento C-H olefinico
esta influida por el modelo de la sustitucién, Median-
te la resolucién apropiads, se observan bandas mil-
tiples para las estructuras en donde la interaccién de
Observe el alargumiento C-H olefinico %) a 3049 cmt (3.28 ym).
|, véase la tabla III del apéndice C.
alargamiento puede presentarse. Por ejemplo, el grupo
vinilo produce tres bandas de alargamiento C-H se-
paradas cercanamente, Dos de estas resultan del alar-
gamiento simétrico y asimétrico de los grupos C-H
terminales y la tercera del alargamiento del C-H res-
tante simple.
Vibraciones de flexién C-H olefinica
Los enlaces C-H olefinicos pueden quedar someti-
dos a la flexiém, ya sea en el mismo plano que el ¢n-
lace C = C 0 perpendicular al mismo; las vibraciones
de flexién pueden ser en fase 0 fuera de fase con res
pecta a si mismas.
Se han establecido asignaciones para algunas de
las vibraciones de flexién en el plano que son notables
y confiables. El grupo vinilo absorbe cerca de 1416
emt (7.06 wm) debido a la vibracién en tijera_del
metileno terminal. La vibracién de’ oscilacién C-H
de una olefina cisdisustituida ocurre en la misma re-
gidn general.
Los modos vibracionales mis caracterfsticas de las
olefinas son las vibraciones de flexién C-H fuera de
plano entre 1000 y 650 cm (10.0 y 15.4 um). Estas
bandas generalmente son intensas en el espectro de
las olefinas. Las bandas de mayor confiabilidad co-
mesponden a las del grupo: vinilo, el grupo vinilideno
y las olefinas trans sustituidas. La absorcién olefinica
se resume en las tablas III a V del apéndice C.
En las estructuras de aleno se observa una absor-
cin intensa cerca de 850 cm (11.26 um), que se
deriva de la vibracién de abanico H;. El primer
sobretono de esta banda también se puede observar.
Algunos espectros que muestran caracteristicas olefi-
nicas se incluyen en el apéndice A: tricloroetileno,
no. 12, y tetracloroetileno, no. 13.
ESBRCTROMETRIA INFRARROJA- 101
HIDROCARBUROS ACETILENICOS
(ALQUINOS)
Las dos vibraciones de alargamiento en las molécu
las acetilénicas implican el alargamiento C=C y
CHL. La absorcién debida a la flexién C-H es carac
teristica de los acetilenos monosustituides y del ace
tileno. El espectro de la figura 11 corresponden a un
alquino terminal tipico.
Vibraciones de alargamiento C = C
La banda de alargamiento C = C débil de las mo-
éculas acetilénicas ocurre en la region de 2260-2100
cm (4.43-4.76 xm). Debido a la simetria, no se ob-
serva ninguna banda C=C en el espectro infrarrojo
del acetileno y los acetilenos sustituidos simétrica-
mente. En el espectro infrarrojo de los acetilenos mo-
nosustituidos, la banda aparece a 2140-2100 cm-*
(4.67-4.76 4am). Los acetilenos disustituidos, donde los
sustituyentes son distintos, absorben cerca de 2260-
2190 cm (4434.57 pm). Cuando los sustituyentes
son similares en masz, 0 cuando producen efectos in-
ductivos 0 mesoméricos similares, la banda puede ser
tan débil que puede pasar desapercibida en el espec-
tro infrarrojo. Por razones de.simetria, un C=C ter-
minal produce una banda més intensa que el C=C
intemo (seudosimetria). La intensidad de la banda
de alarganiento C =C se incrementa por la conju-
gacién con el grupo carbonilo.
Vibraciones de alargamiento C-II
“La banda de alagamiento C-H de los acetilenos
monosustituidos ocurre en Ja regién general de 3333-
3267 em! (3.00-306 pm). Esta es una banda intensa
y més estrecha que las bandas de OH y NH enlazado
que se presentan en lz misma regi
1-HEXINO Peso
sow molecular an
en Procedenciay
Vibraciones de flexion C-H
La vibracién de flexién C-H del acetileno y los
acetilenos monosustituidos origina una absorcion am
plia e intensa en la regién de 700-610 em (14.29.
1639 pi). El primer sobretono de Ia vibracién de
flexién C-II se presenta en la forma de una banda
amplia y débil en la region de 1370-1220 em (7.30.
8.20 ym)
HIDROCARBUROS AROMATICOS
MONONUCLEARES
Las bandas mas notables y de mayor informacién
en el espectto de los compuestos aromaticos se pre-
sentan en el. intervalo de baja frecuencia entel Wy
675 km (11.11 y 14.82 wm). Estas bandas de absor
\Sorintdrea resultan de fe flexién fuera _de_planogde
los enlaces (C-HyLas bandas de fTexién en_ el” plano
aparecen en Ja regin ge 1300-1009 cm (7.70-10.00
#m). Las vibraciones eléticas;1 que implican el
«alargamiento carbono a carbono dentro del anillo,
absorben en la region de 1600-1585 cmt (6.25-6.31
(ae y en la regién de 1500.1400-em-* (6.67.7 14 am)
Las bandas esqueléticas frecuentemente aparecen como
“dobletes, dependiendo de Ja naturaleza de los sustitu:
yentes en el anillo.
~“Las bandas de alargamiento C-IL/aromitico ocu-
rren entre 3100 y. 3000 m=? (3.23 y 3.33 em)
Las bandas de sobretono y combinacién débiles
aparecen en la regién de 2000-1650 curt ,(5.00-6.06
um). El modelo de las bandas dé sobretono es carac-
teristico del modelo de sustitucién-del anillo, Debido
a que son débiles, las bandas de sobretono y combi-
nacién pueden observarse con mayor facilidad en Jos
espectros obtenidos a partir de muestras de gran es-
pesor. Los espectros de las figuras 12 y 13 correspon-
den a compuestos aromiticos (benzenoides) tipicos.
ESPECTROGRAMA,
INFRARROJO 2775
Por ciento de
Celdo: 0.02 mm Rostreo en
Beckman IR-&
Ficura 11
Alargamiento = C ~ 11, 3268 em? (3.06 ym)
Alargamiento C= C, 2110 m=" (4.74 ym).
Sobretono de flexion =C~H, 1247 cmt
Flexién fandamenta
(8.02 um
moOOR>
“402
C~H, < 667 em (> 1.50 ym
Alargamiento C-H_ normal (véase la figura 8), 2857-2941 em" (3.4.3.5 jm)
IDENTIFICACION ESPECTROMETRICA DE COMPUESTOS ORGANICOS
= om
Caltng PM.
ongited de onde, yam
1600
14g5-1445%¢ NBO 1.4998 (lit. Colde copilor: puro
106.17 Pe
7 8 9 a as 20
300
i
woo 12001000
Rostreo en Perkin-Elmer 521
FRECUENCIA, ex
sclencio: The Matheron Co., Inc. E. Rutherford, Nt
Figura 12
Alargamieato C-H aromitico, 3008 cm-* (3.32 um).
Fledén C-H fuera de plang, 742 om (13-48 xm).
Las posiciones de sustitucién en los anillos de ben-
‘ceno frecuentemente pueden determinarse tomando
como referencia la figura. 4, Este procedimiento se
encuentra limitado a la absorcién débil de tales ban-
hs de sobretono (0 combinacién). Cuando se tiene
tuna absorcién intensa en tal regidn (tal como el alat
gamiento de carbonilo, véase més adelante), las ban-
Gas de sobretono débiles se extinguen.
Vibraciones de flexién C-H fuera de plano
La flexién en fase y fuera de fase de un dtomo de
hidrégeno anular se acopfa intensamente con los ato
mos de hidrégeno adyacentes. La posicién de la absor
cién de la banda de flexién fuera de plano es conse-
Cuentemente caracteristica del niimero de atomos de
hhidzégeno adyacentes en el anillo. Las bandas a me
nudo resultan ser intensas y pueden utilizarse para
|e determinacién cuantitativa de las concentraciones
relativas de los isomeros en mezclas.
Las asignaciones para las bandas de flexién C-H
fuera de plano en el espectro de los bencenos sustitui-
dos aparecen en Ja grifica de frecuencias de grupo
caracteristicas (apéndice B). Normalmente estas asig-
aciones son confiables para los bencenos sustituidos
con alquilo, pero debe tenerse cuidado en la interpre-
[ .
Aeeimients CAH metlco, 2965, 2938, 2918, 2875 em (3373.40, 3.43, 348 wm) (vase la figura 8)
Bande de sobretono o combinaciOn, 2000-1667 cm: (906-6.0 qm) (véase la figura 14)
: Alargamiento C-C 1605, 1495, 1466 em (6.23, 6.69, 6.82 pm).
Flenén C-H en el plano, 1052, 1022 cm (9.51, 9.78 pm).
; Glexién C-C anular. fuera de plano, 438 em (22.83 .m).
tacién de los espectros cuando se tienen grupos polares
unidos directamente al anillo; por ejemplo, los nitro-
bencenos, dcidos aromiticos y &teres o amidas de los.
cidos aromaticos.
La banda de absorcién que frecuentemente aparece
en el espectro de los bencenos sustituidos cerca “de
710.675 cm-* (14.08-14.81 pm) se atribuye a 4a flexi6n
jaular fuera de plano, En el apéndice A se inchiyen
any eNO A GPE Fue Muestran absorciones aromaticas
tipicas: benceno, no. 4; indeno, no. 8; dietilftalato, no.
21, y maileno, no. 6.
COMPUESTOS AROMATICOS
POLINUCLEARES
Las compuestos arométicos polinucleares, igual que
los aromaticos mononucleares, tienen absorcién carac-
teristica en tres regiones del espectro.
Bl alargamiento C-H aromético y las vibraciones
esqueléticas absorben en las mismas regiones observa-
das para los arométicos. mononucleares. La absorcién
mds caracteristica de los arométicos polinucleares re-
sulta de la flexion C-H fuera de plano en la regién
de 900-675 cm (11.11-14.81 xm). Estas bandas pue-
den conelacionarse con el nimero de étomos de
ESPECTROMETRIA INERARROJA 103.
a
vionvadosey
vee}
600 400200
También podría gustarte
- Capital Cost Reduction by The Use of Divided WallDocumento6 páginasCapital Cost Reduction by The Use of Divided WallLinda Flor De Maria Cuevas PalenciaAún no hay calificaciones
- Técnicas Extracción de Proteína y PepetidosDocumento7 páginasTécnicas Extracción de Proteína y PepetidosLinda Flor De Maria Cuevas PalenciaAún no hay calificaciones
- Tarea 5 - Análisis de MezclasDocumento1 páginaTarea 5 - Análisis de MezclasLinda Flor De Maria Cuevas PalenciaAún no hay calificaciones
- Export PDFDocumento1 páginaExport PDFLinda Flor De Maria Cuevas PalenciaAún no hay calificaciones
- s0308 81462900307 7Documento8 páginass0308 81462900307 7Linda Flor De Maria Cuevas PalenciaAún no hay calificaciones
- Tablas de AromáticosDocumento1 páginaTablas de AromáticosLinda Flor De Maria Cuevas PalenciaAún no hay calificaciones
- 4.3.4 Fotoluminiscencia AlumnosDocumento14 páginas4.3.4 Fotoluminiscencia AlumnosLinda Flor De Maria Cuevas PalenciaAún no hay calificaciones
- 4.2.6. - Tarea Cuantitativo IRDocumento4 páginas4.2.6. - Tarea Cuantitativo IRLinda Flor De Maria Cuevas PalenciaAún no hay calificaciones
- Teoria Molecular de La Viscosidad de Gases A Baja DensidadDocumento1 páginaTeoria Molecular de La Viscosidad de Gases A Baja DensidadLinda Flor De Maria Cuevas PalenciaAún no hay calificaciones
- 4.2.6.1 Ejercicio Espectro IR 2Documento1 página4.2.6.1 Ejercicio Espectro IR 2Linda Flor De Maria Cuevas PalenciaAún no hay calificaciones
- Flujo A Través de Tubos ConcéntricosDocumento3 páginasFlujo A Través de Tubos ConcéntricosLinda Flor De Maria Cuevas PalenciaAún no hay calificaciones
- Cuarto Examen Parcial de Electroquímica-Sem1-2022-6 PMDocumento2 páginasCuarto Examen Parcial de Electroquímica-Sem1-2022-6 PMLinda Flor De Maria Cuevas PalenciaAún no hay calificaciones
- Teoria Cientifica y Gerencial de McgregorDocumento1 páginaTeoria Cientifica y Gerencial de McgregorLinda Flor De Maria Cuevas PalenciaAún no hay calificaciones