Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Clase 5
Cargado por
Jose HumeresTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Clase 5
Cargado por
Jose HumeresCopyright:
Formatos disponibles
[FISICOQUIMICA II] Aux.
Rodrigo Rene Aguayo Torrez
CLASE : 5
CAPITULO : 2
TEMA : ESTADO SOLIDO
INDICES DE MILLER
Los índices de Miller se utilizan en cristografia, son un juego de tres números que permiten identificar
unívocamente un sistema de puntos, vectores y planos cristalográficos. Entonces en un sistema cbico unitario
podemos ubicar puntos (coordenadas), direcciones o vectores (líneas) y planos. Para ello en la siguiente tabla
se muestra la nomenclatura.
COORDENADA DE LOS PUNTOS DIRECCIONES PLANOS
En paréntesis En corchetes En paréntesis
Se utiliza coma “,” No se utiliza coma No se utiliza coma
Pueden ser fracciones Son números enteros Son números enteros
(1,1,0) ; (1,0,0) [100]; [112] (101) ; (221)
EJEMPLOS DE INDICES DE MILLER
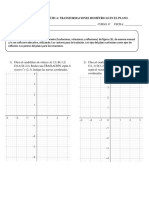
EJEMPLO 1. (Coordenadas de los puntos) En el siguiente Sistema cubico unitario indicar las coordenadas
de los puntos.
a: (0,0,0)
b: (0,0,1)
c: (1,1,1)
d: (1/2,1,0)
e: (1,1,0)
f: (1,0,0)
QMC – 1300 “A” | 1
[FISICOQUIMICA II] Aux. Rodrigo Rene Aguayo Torrez
EJEMPLO 2. (DIRECCIONES) Determine los índices del vector de dirección cubico que se muestra en las
siguiente figura
Pasos:
1ro. Identificas las coordenadas del punto de inicio y
final
Final: (0,1,1/3)
Inicio: (1,0,1/2)
2do. Restar el: final-inicial, respetando los ejes de
coordenadas, es decir, xf-xi, yf-yi, zf-zi
Final - Inicio: (0,1,1/3) - (1,0,1/2) = (-1,1,-1/6)
3ro. No debe existir fracción, entonces multiplicamos:
IM=(-1,1,-1/6)*6
IM = [ ̅ ̅]
EJEMPLO 3. Determine el Indice de Miller del vector de dirección cubico entre las coordenadas de posición
(3/4,0,1/4) y (1/4,1/2,1/2)
Pasos:
1ro. Identificas las coordenadas del punto de inicio y final
Final: (3/4,0,1/4)
Inicio: (1/4,1/2,1/2)
2do. Restar el: final-inicial, respetando los ejes de coordenadas, es decir, x f-xi, yf-yi, zf-zi
Final - Inicio: (3/4,0,1/4) - (1/4,1/2,1/2)= (1/2,-1/2,-1/4)
3ro. No debe existir fracción, entonces multiplicamos:
IM=(1/2,-1/2,-1/4)*4
IM =[ ̅ ̅]
EJEMPLO 4. Determine los siguientes vectores dirección en una celdilla unitaria cubica
a) [100]
b) [110]
c) [112]
La aclaración del inciso c, como es una
celda cubica unitaria no puede existir el
dos dentro de la celda, por lo tanto para
encontrar el vector hay que convertirlo
en fracción, en este caso dividir entre
dos. Lo que sería: ½ en x ½ en y y 1 en z
QMC – 1300 “A” | 2
[FISICOQUIMICA II] Aux. Rodrigo Rene Aguayo Torrez
EJEMPLO 5. (PLANOS) Dibujar los siguientes planos critalograficos:
a) (101)
b) (221)
c) (111)
Para encontrar los planos se siguen los siguientes pasos, para el a)
(101)
1ro. Encontrar las intersecciones del Índice
de Miller en los ejes de coordenadas. En
este caso 1 en x, 0 en y, 1 en z. Como indica
el plano solo corta en x,z pero no corta el
eje y
2do. Unir los puntos dibujados en el paso
anterior
3ro. Levantar un plano a partir de las líneas
dibujadas.
NOTA: Cuando el plano no corta un eje (en
esta caso el y), el plano es hasta el infinito
QMC – 1300 “A” | 3
[FISICOQUIMICA II] Aux. Rodrigo Rene Aguayo Torrez
Para el b)
(221)
Cuando en el Índice de Miller nos muestra números mayores a la unidad, en este
ejemplo 2. Entonces se saca el reciproco del índice de Miller, es decir, la inversa. Por lo
que se tiene ( ½ ½ 1) y es estos puntos los que ubicamos en el sistema cubico unitario
1ro. Encontrar las intersecciones del Índice
de Miller en los ejes de coordenadas. En
este caso 1 en x, 0 en y, 1 en z. Como indica
el plano solo corta en x,z pero no corta el
eje y anterior
2do. Unir los puntos dibujados en el paso
3ro. Levantar un plano a partir de las líneas
dibujadas.
NOTA: El plano corta en todos los ejes,
entonces no se eleva hasta el infinito
QMC – 1300 “A” | 4
[FISICOQUIMICA II] Aux. Rodrigo Rene Aguayo Torrez
Para el c) exactamente los mismos pasos.
(111)
QMC – 1300 “A” | 5
[FISICOQUIMICA II] Aux. Rodrigo Rene Aguayo Torrez
FORMULARIO DE LOS SISTEMAS CRISTALINOS
Tabla 1. Diferentes parámetros para los diferentes sistemas de cristalización
Estructura Figura ( ) #átomos/celda F.A.A. N.C.
Cubica Simple
(CS)
1 átomo 0.52 6
Abreviatura
en ingles
Cubico de
“Body CC”
Cuerpo
2 átomos 0.68 8
Centrado √
(BCC)
Cubico de
Cara
Centrada
(FCC) 4 átomos 0.74 12
Abreviatura √
en ingles
“Face CC”
Hexagonal
3 átomos 0.64
Simple
Hexagonal
6 átomos 0.74 12
Compacto
En el sistema Hexagonal, ambos casos “𝑎 " es el parámetro de arista, los diferentes triángulos que se
forman en la base del polígono son triángulos equiláteros (6 triángulos). La única diferencia
geométrica entre el Simple y Compacto es que en el SIMPLE la altura del polígono es igual a su
arista “𝑐 𝑎 ”, en cambio en el COMPACTO, la altura del polígono es mayor “𝑐 𝑎 ”
QMC – 1300 “A” | 6
[FISICOQUIMICA II] Aux. Rodrigo Rene Aguayo Torrez
EXPLIACION
En la tabla 1 se describe todos los parametros de los tipos de los cinco tipos de cristalización
En la segunda columna se muestra la representación grafica de las estructuras cristalinas
En la tercera columna, se muestra la relación que existe entre el parámetro de celda ( ) y el radio del
átomo que se analiza (r). En esta relación tanto el parámetro de celda y el radio del átomo dependen de la
naturaleza del cristal, es decir, del Cobre serán diferentes al del Oro y de otro cristal aunque tengan
la misma estructura cristalina
En la cuarta columna, se indica la cantidad de átomos que caben dentro de un sistema cubico unitario. Por
ejemplo, en el Sistema Cubico Simple, hay 8 átomos en las 8 aristas del cubo, pero de cada uno de los 8
átomos tan solo la octava parte se encuentra dentro del cubo. Por lo tanto:
De la misma manera se determina de los otros sistemas cristalinos
F.A.A. es el FACTOR DE ACOMODAMIENTO ATOMICO o FACTOR DE EMPAQUETAMIENTO, es la fracción
en volumen del espacio que ocupan los átomos dentro de un celda cubica unitaria. Su relación es
“volumen de átomos/volumen total de la celda unitaria”. Para el mismo ejemplo del Sistema Cubico
Simple, seria, el “volumen de 1atomo/volumen del cubo”
N.C. es número de coordinación y es el número de átomos mas próximos
EJEMPLOS
EJEMPLO 1. El hierro a temperatura ambiente presenta una estructura cubica centrada en el cuerpo con un
parámetro de red de 𝑎𝑜 7 Å. Sabiendo que su peso molecular es 55.847 gr/mol, determinar:
a) La masa de un átomo
b) La densidad del hierro
c) El radio atómico del hierro
d) El volumen atómico
e) El número de átomos por m3
f) El número de átomos por gramo
g) El número de moles por m3
h) La masa de una celda unitaria
i) El número de celdas unitarias existentes en 1gr de hierro
j) El volumen de una celda unitaria
k) La densidad atómica lineal en la dirección [111]
l) La densidad atómica superficial en el plano (110)
QMC – 1300 “A” | 7
[FISICOQUIMICA II] Aux. Rodrigo Rene Aguayo Torrez
SOLUCIÓN:
a) Se utiliza el peso molecular y el número de Avogadro
7 7
b) Utilizamos como información la estructura cristalina del hierro, Cubica de Cuerpo Centrado, entonces en la
tabla del formulario se tiene información sobre este tipo de estructura cristalina
Cubico de Cuerpo Centrado
2 átomos
(BCC) √
Entonces, calculamos el volumen de una celda unitaria (un cubo)
( 7Å )
Å
Calculo de la masa de una celda unitaria de hierro, que tiene 2 átomos por celda.
( 7 ) ( )
Mismo Dato extraído del Conversión
cálculo del formulario de unidades
inciso a)
Entonces, la densidad:
c) Para el radio atómico del hierro, se utiliza la ecuación de parámetro de red, para el sistema cubico indicado
√
√ √
7Å
QMC – 1300 “A” | 8
[FISICOQUIMICA II] Aux. Rodrigo Rene Aguayo Torrez
Å
d) El volumen atómico
( ) 7
e) El número de átomos por m3, se conoce que hay 2 átomos por celda unitaria, entonces:
f) Numero de átomos por gramo, con el número de Avogadro y peso atómico:
g) Numero de moles por metro cubico, utilizamos la densidad
Resultado
b) 7
7
h) La masa de una celda unitaria
Resultado f),
(la inversa)
i) Número de celdas unitarias en un gramos de hierro, es la inversa del inciso h)
j) Volumen de una celda unitaria, ya calculamos para el inciso a)
( 7Å )
Å
k) La densidad atómica lineal en la dirección [111]
QMC – 1300 “A” | 9
[FISICOQUIMICA II] Aux. Rodrigo Rene Aguayo Torrez
En la 1ra figura se muestra la estructura Cubica de Cuerpo Centrado
En la 2da figura, el vector dirección [111]
En la 3ra figura, se muestra en verde el vector dirección y de color azul y amarillo los átomos por los cuales
pasa el vector dirección. El vector dirección debe pasar justo por el núcleo de los átomos, si no es asi, no se
toma en cuenta el átomo
Continuando con el ejercicio, el vector pasa por ½ de átomo (azul que son 2) y por todo 1 atomo (amarillo),
entonces en total.
Por otro lado, utilizando trigonometría y cálculos algebraicos se calcula la distancia o tamaño que tiene el
vector, sabiendo que el parámetro de red es 7 Å. Entonces la distancia es (por cuestión de no hacer
mas largo el ejercicio, se dara directamente el resultado de esta distancia, usted puede realizar los calculos):
[ ] √ √ ( 7 ) 7
Finalmente:
l) La densidad atómica superficial en el plano (110)
QMC – 1300 “A” | 10
[FISICOQUIMICA II] Aux. Rodrigo Rene Aguayo Torrez
En la 1ra figura está el plano (110)
En la 2da figura, se muestra el plano (110) y los átomos a los cuales atraviesa, en los vértices, solo ¼ de atomo
se encuentra dentro del plano
Entonces para el número de átomos:
Por trigonometría se calcula el área del plano:
√ √ ( 7 )
Finalmente, la densidad:
QMC – 1300 “A” | 11
[FISICOQUIMICA II] Aux. Rodrigo Rene Aguayo Torrez
EJEMPLO 2. La celda elemental del aluminio es cubica centrada en las caras. Su masa atómica es 26.982
gr/mol y el parámetro de red 𝑎𝑜 𝑛𝑚. Calcular:
a) La densidad teórica
b) La densidad atómica lineal en la dirección [110]
c) La densidad atómica superficial en el plano (111)
d) El radio atómico
e) El factor de empaquetamiento
SOLUCIÓN:
Cubico de Cara Centrada
4 átomos 0.74 12
(FCC) √
a) Densidad teórica, entonces calculamos la densidad dentro de una celda unitaria, con los datos de la
tabla:
( )
b) Densidad lineal en la dirección [110]
QMC – 1300 “A” | 12
[FISICOQUIMICA II] Aux. Rodrigo Rene Aguayo Torrez
En la 1ra figura, el sistema cubico de cuerpo centrado
En la 2da figura, el vector dirección [110]
En la 3ra figura, los átomos de aluminio por los cuales atraviesa el vector dirección, son dos átomos de ½ y un átomo
entero.
La distancia o tamaño del vector dirección es:
[ ] √ √ ( ) 7
Entonces la densidad lineal:
c) Densidad atómica en el plano (111)
En la 1ra figura, se
muestra el plano (111)
En la 2da figura, los
átomos por los cuales
corta el plano (111).
Son 3 (anaranjado) de ½
de átomo y 3 (azules)
de 1/6 de átomo
La suma de ángulos interiores en un triángulo es igual a 180°. Al ser en este
caso el plano un triángulo equilátero, todos los ángulos internos son iguales
entonces (180°/3) los ángulos interiores son 60°.
Para saber la fracción de átomo que corta el plano, se divide 60°/360° . (360°
son los grados de una circunferencia). Entonces este cálculo es 1/6
QMC – 1300 “A” | 13
[FISICOQUIMICA II] Aux. Rodrigo Rene Aguayo Torrez
( ) ( )
El área del plano es:
√ √
( )
Finalmente, la densidad:
d) El radio atómico
√ √
e) Factor de empaquetamiento
( )
( )
Este resultado concuerda con el de la tabla.
QMC – 1300 “A” | 14
También podría gustarte
- Indices de MillerDocumento5 páginasIndices de MillerAllen WalkerAún no hay calificaciones
- Clase 4. Índice de Miller (Hexagonal)Documento18 páginasClase 4. Índice de Miller (Hexagonal)Ruben HolmesAún no hay calificaciones
- MaterialesDocumento14 páginasMaterialesDaniel RamirezAún no hay calificaciones
- Indices de MillerDocumento30 páginasIndices de MillerAndrea PeñaAún no hay calificaciones
- Indice MillerDocumento41 páginasIndice MillerNicolle CardozoAún no hay calificaciones
- ACFrOgA8bMnLWm8gXiL5JPqOAgefFvkj I08RHFHN kGDSc344hk995SvokcQx6 5Jm kOO5l5TZL1ormdi8P3cnZ4mpBrTRTilKNr0l7fGsX1KT0XXujzZrVia4WJ6SOKqmvToV4YjO7n-plyLXDocumento3 páginasACFrOgA8bMnLWm8gXiL5JPqOAgefFvkj I08RHFHN kGDSc344hk995SvokcQx6 5Jm kOO5l5TZL1ormdi8P3cnZ4mpBrTRTilKNr0l7fGsX1KT0XXujzZrVia4WJ6SOKqmvToV4YjO7n-plyLXdavid cenAún no hay calificaciones
- Indices de Miller 2021Documento34 páginasIndices de Miller 2021Luis Alberto Laguado VillamizarAún no hay calificaciones
- Act 4Documento5 páginasAct 4Marcos Luna CervantesAún no hay calificaciones
- Puntos, Direcciones y Planos en Una Celda-C4Documento57 páginasPuntos, Direcciones y Planos en Una Celda-C4Jonathan Ramos VAún no hay calificaciones
- Examen SelectDocumento13 páginasExamen SelectJavier Segado SánchezAún no hay calificaciones
- Folleto 2.1 Teoría y Práctica Bachillerato PDFDocumento88 páginasFolleto 2.1 Teoría y Práctica Bachillerato PDFSaimon M.Aún no hay calificaciones
- Guía 1 TRASLACIÓN - Geometría 3DDocumento3 páginasGuía 1 TRASLACIÓN - Geometría 3DmarcosAún no hay calificaciones
- Trigonometría 01 Ciclo IenDocumento4 páginasTrigonometría 01 Ciclo IenBurGodAún no hay calificaciones
- GretrgDocumento13 páginasGretrgjesusgranados257Aún no hay calificaciones
- Sesion #67 - 2° - Transformaciones IsométricasDocumento2 páginasSesion #67 - 2° - Transformaciones IsométricasClaudiopatricio Radamel Morales ParedesAún no hay calificaciones
- Ejemplos de Estructuras CristalinasDocumento10 páginasEjemplos de Estructuras CristalinasMARIA CAMILA LEON DELGADOAún no hay calificaciones
- Evaluación Consolidado 2Documento2 páginasEvaluación Consolidado 2Matematica Fisica EstadisticaAún no hay calificaciones
- Crista PC 1Documento5 páginasCrista PC 1JulioAún no hay calificaciones
- Mat1mu0c6 PautaDocumento9 páginasMat1mu0c6 PautaClaudia ContrerasAún no hay calificaciones
- Portafolios #02Documento2 páginasPortafolios #02Manuel RaezAún no hay calificaciones
- Guía Cónicas Grado 10Documento12 páginasGuía Cónicas Grado 10Ángela Johana Rondón PrietoAún no hay calificaciones
- Geometria AnaliticaDocumento62 páginasGeometria AnaliticaCristhian VargasAún no hay calificaciones
- Sesion 02Documento47 páginasSesion 02Adolfo GuerreroAún no hay calificaciones
- Guía N°1 TRANSFORMACIONES ISOMÉTRICAS.Documento4 páginasGuía N°1 TRANSFORMACIONES ISOMÉTRICAS.Vicente HuenchoAún no hay calificaciones
- Videoclase Matemarica 03Documento115 páginasVideoclase Matemarica 03elizabethAún no hay calificaciones
- Organización Atómica y IonicaDocumento162 páginasOrganización Atómica y IonicavanesaangaritazapataAún no hay calificaciones
- Unidad 3 Cristalografia PDFDocumento126 páginasUnidad 3 Cristalografia PDFLuis Cortés CortesAún no hay calificaciones
- Examen GeometriaDocumento3 páginasExamen GeometriaMARIA ISABELAún no hay calificaciones
- Articles-176573 Recurso PDFDocumento12 páginasArticles-176573 Recurso PDFAdrianaCarolinaCasAún no hay calificaciones
- MC 112 - Unidad 5-2018-2.direc. PlanDocumento64 páginasMC 112 - Unidad 5-2018-2.direc. PlanDiego Mendez AyalaAún no hay calificaciones
- Analitica 2oparte CFADocumento2 páginasAnalitica 2oparte CFAsalvandoalmundo814Aún no hay calificaciones
- Actividad Sesion Presencial Upc EpeDocumento4 páginasActividad Sesion Presencial Upc EpeAndres Romero Castillejo0% (1)
- Actividad Sesion Presencial 2.2 PDFDocumento4 páginasActividad Sesion Presencial 2.2 PDFAarón M. ReyesAún no hay calificaciones
- Capitulo 1-2Documento24 páginasCapitulo 1-2Felipe CorralesAún no hay calificaciones
- t12 Tarea Circunferencia Trigonométrica IIDocumento6 páginast12 Tarea Circunferencia Trigonométrica IITatiana CervantesAún no hay calificaciones
- Planos y Direcciones PresentacionDocumento13 páginasPlanos y Direcciones PresentacionRafael MolinaAún no hay calificaciones
- Hoja 1Documento1 páginaHoja 1Daniela SalcinesAún no hay calificaciones
- PITAGORASDocumento16 páginasPITAGORASMónica Marcela Montiel GarcíaAún no hay calificaciones
- Grupo 1 Arreglos AtomicosDocumento12 páginasGrupo 1 Arreglos Atomicoskaneki kenAún no hay calificaciones
- 02 - Análisis Vectorial II - UCV 2023 IDocumento28 páginas02 - Análisis Vectorial II - UCV 2023 IMANUEL ENRIQUE GUERRA CHUMACEROAún no hay calificaciones
- Mii T3 2020Documento13 páginasMii T3 2020Luna Santiago SeguraAún no hay calificaciones
- PC2 Dinamica UPC 2022 1Documento7 páginasPC2 Dinamica UPC 2022 1Luis Fernando Contreras HilarioAún no hay calificaciones
- Formas Canónicas de Representación Por Variables de EstadoDocumento6 páginasFormas Canónicas de Representación Por Variables de Estadomiryam360Aún no hay calificaciones
- Matemáticas 3Documento55 páginasMatemáticas 3Uriel Moreno AvilaAún no hay calificaciones
- Descripción de Las Redes Bidimensionales: Tipo General.-Una Red Oblicua Tipos Espaciales. - Cuatro RedesDocumento17 páginasDescripción de Las Redes Bidimensionales: Tipo General.-Una Red Oblicua Tipos Espaciales. - Cuatro RedesDariana Llatas VargasAún no hay calificaciones
- Examenes Selectividad Resueltos MATEMARTICAS FRANCISCO FERNÁNDEZ MORALES LIBRO 1 PDFDocumento270 páginasExamenes Selectividad Resueltos MATEMARTICAS FRANCISCO FERNÁNDEZ MORALES LIBRO 1 PDFManuel Román BocanegraAún no hay calificaciones
- La ElipseDocumento4 páginasLa ElipseRodrigo YanquiAún no hay calificaciones
- Texto Transporte MineroDocumento42 páginasTexto Transporte MineroLlanos A. AlexisAún no hay calificaciones
- T. Integrador 2Documento13 páginasT. Integrador 2Pao BelesacaAún no hay calificaciones
- P2Documento1 páginaP2zpedro2323Aún no hay calificaciones
- Certamen2 FIS100 (2011)Documento10 páginasCertamen2 FIS100 (2011)Anonymous EvSLXgAún no hay calificaciones
- Exámenes Resueltos Selectividad Andalucía 2000Documento10 páginasExámenes Resueltos Selectividad Andalucía 2000Almudena PardalAún no hay calificaciones
- T S7 Circunferencia TrigonométricaDocumento9 páginasT S7 Circunferencia TrigonométricaRicardoAún no hay calificaciones
- 07 - Circunferencia Trigonométrica PDFDocumento12 páginas07 - Circunferencia Trigonométrica PDFmatinashoAún no hay calificaciones
- ReconicaDocumento7 páginasReconicaJose MiguelAún no hay calificaciones
- Guia 2 Geometria Vectorial y SolucionesDocumento7 páginasGuia 2 Geometria Vectorial y SolucionesPablo BarahonaAún no hay calificaciones
- La ecuación general de segundo grado en dos y tres variablesDe EverandLa ecuación general de segundo grado en dos y tres variablesAún no hay calificaciones
- PonderacionesDocumento2 páginasPonderacionesJose HumeresAún no hay calificaciones
- Viscosidad Parte 2Documento17 páginasViscosidad Parte 2Jose HumeresAún no hay calificaciones
- Clase 3 FenomenosDocumento9 páginasClase 3 FenomenosJose HumeresAún no hay calificaciones
- Conductividad Termal PDFDocumento33 páginasConductividad Termal PDFJose HumeresAún no hay calificaciones
- Viscosidad Parte 1Documento16 páginasViscosidad Parte 1Jose HumeresAún no hay calificaciones
- Clase 1 Fenomenos TeoriaDocumento5 páginasClase 1 Fenomenos TeoriaJose HumeresAún no hay calificaciones
- Clase 1 FenomenosDocumento3 páginasClase 1 FenomenosJose HumeresAún no hay calificaciones
- Clase 2 FenomenosDocumento5 páginasClase 2 FenomenosJose HumeresAún no hay calificaciones
- Clase 13Documento9 páginasClase 13Jose HumeresAún no hay calificaciones
- Clase 8Documento9 páginasClase 8Jose HumeresAún no hay calificaciones
- Clase 11-1Documento4 páginasClase 11-1Jose HumeresAún no hay calificaciones
- Clase 3Documento3 páginasClase 3Jose HumeresAún no hay calificaciones
- Clase 8Documento6 páginasClase 8Jose HumeresAún no hay calificaciones
- Clase 6Documento4 páginasClase 6Jose HumeresAún no hay calificaciones
- Clase 4Documento6 páginasClase 4Jose HumeresAún no hay calificaciones
- Clase 2Documento2 páginasClase 2Jose HumeresAún no hay calificaciones
- Clase 1Documento4 páginasClase 1Jose HumeresAún no hay calificaciones
- Desarrollo de La Motricidad Fina en Niños de Edad PrescolarDocumento6 páginasDesarrollo de La Motricidad Fina en Niños de Edad PrescolarNormita Consuelo Moncada Tarazona100% (1)
- TermoDocumento8 páginasTermoRodrigo AndresAún no hay calificaciones
- Resumen Ejecutivo Energias RenovablesDocumento9 páginasResumen Ejecutivo Energias RenovablesJuan Carlos CaceresAún no hay calificaciones
- Matriz de Riesgos en Una Empresa DistribuidoraDocumento40 páginasMatriz de Riesgos en Una Empresa DistribuidoraALEIDA MARIA VARGAS VEGA100% (2)
- Marco Teórico Analisis MecanicoDocumento2 páginasMarco Teórico Analisis MecanicoDaftpunk64Aún no hay calificaciones
- Símbolos Controles Eléctricos AmericanoDocumento2 páginasSímbolos Controles Eléctricos AmericanoRoni Dominguez80% (10)
- Guia #4 FactorizacionDocumento5 páginasGuia #4 FactorizacionKarito MonsalveAún no hay calificaciones
- Ensayo Proctor 2019Documento8 páginasEnsayo Proctor 2019YanethPaccoVelasquez100% (2)
- Abad - Jesus - Unidad 1. Actividad 3. Problemas Energía PotencialDocumento2 páginasAbad - Jesus - Unidad 1. Actividad 3. Problemas Energía PotencialJesus Manuel Abad MuesesAún no hay calificaciones
- Juan Miguel Hernandez leon-LA CASA DE UN SOLO MURO PDFDocumento214 páginasJuan Miguel Hernandez leon-LA CASA DE UN SOLO MURO PDFpaoAún no hay calificaciones
- Hojas de Calculo SPT SanarateDocumento5 páginasHojas de Calculo SPT Sanaratehugo100% (1)
- t1 Taller ProbabilidadDocumento6 páginast1 Taller ProbabilidadLuis LopezAún no hay calificaciones
- Estudiante: Código / Dni: Facultad: Carrera Actual: Período de Emisión: Fecha de EmisiónDocumento1 páginaEstudiante: Código / Dni: Facultad: Carrera Actual: Período de Emisión: Fecha de EmisiónHadilson gcAún no hay calificaciones
- N042 Norma Técnica de Diseño y Construccion de Acometidas Electricas en Baja TensionDocumento40 páginasN042 Norma Técnica de Diseño y Construccion de Acometidas Electricas en Baja Tensionperez.r.orlando100% (2)
- Charlie Charlie DesafíoDocumento1 páginaCharlie Charlie DesafíoEdaAún no hay calificaciones
- Informe 1 Fisica IIIDocumento25 páginasInforme 1 Fisica IIIDaniel MaguiñaAún no hay calificaciones
- Extracción Del AdnDocumento2 páginasExtracción Del AdnIrvin RubénAún no hay calificaciones
- Informe Técnico Servicios de Mantenimiento Mecánico en Aguas y RelavesDocumento37 páginasInforme Técnico Servicios de Mantenimiento Mecánico en Aguas y RelavesQUINTIN50% (2)
- Atlas PDFDocumento122 páginasAtlas PDFMorpheus AlvarezAún no hay calificaciones
- El Buen Orador y El Nerviosismo - Vallejo Castillo Luis Fernando - 697706Documento6 páginasEl Buen Orador y El Nerviosismo - Vallejo Castillo Luis Fernando - 697706Fernando VallejoAún no hay calificaciones
- Ejercicio MatematicaDocumento32 páginasEjercicio MatematicaValentina JaraAún no hay calificaciones
- Practica 3 XDXDXDXDXDXDXDXDXDXDXDDocumento15 páginasPractica 3 XDXDXDXDXDXDXDXDXDXDXDFrancis Aldair Reyes SalasAún no hay calificaciones
- Parametros de Resistencia Del SueloDocumento2 páginasParametros de Resistencia Del Suelopeter makeitAún no hay calificaciones
- Cuadros de Resistencia TermicaDocumento3 páginasCuadros de Resistencia TermicaDiego ZhItho Aburto OlaveAún no hay calificaciones
- C81 Trabajo y Energía Sólido RígidoDocumento9 páginasC81 Trabajo y Energía Sólido RígidofatamariAún no hay calificaciones
- Control de Calidad en Camaras GAmmas PlanaresDocumento52 páginasControl de Calidad en Camaras GAmmas PlanaresJotero ZavaletaAún no hay calificaciones
- Instalaciones ElectromecanicasDocumento37 páginasInstalaciones ElectromecanicasAnyela Ylla GarciaAún no hay calificaciones
- Tarea Errores AnalisisDocumento5 páginasTarea Errores AnalisisHernan RealAún no hay calificaciones
- Conceptos de Ing ElectricaDocumento2 páginasConceptos de Ing ElectricaESTEBAN CARDENAS QUISPEAún no hay calificaciones