Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Balance Molar
Cargado por
lizeth alvarez0 calificaciones0% encontró este documento útil (0 votos)
5 vistas1 páginaTítulo original
BALANCE MOLAR
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
5 vistas1 páginaBalance Molar
Cargado por
lizeth alvarezCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 1
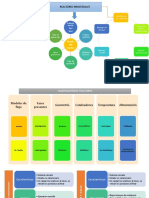
Continuo de mezcla perfecta
Opera en estado estacionario y se
asume que produce una mezcla
perfecta. No hay dependencia del
tiempo o de la posición en la
Se emplea para operaciones a pequeña Reactor Tubular
temperatura, la concentración' o
escala para probar nuevos procesos que de la velocidad de reacción Consta de un tubo cilíndrico y
aún no se han desarrollado en su totalidad, normalmente opera en estado
Ecuación general de balance molar para fabricar productos costosos y para estacionario; los reactores
procesos difíciles de convertir en tubulares se emplean con mayor
operaciones continuas frecuencia para reacciones en fase
gas los materiales que reaccionan
Reactores intermitentes (Baths) se consumen de manera continua
a medida que fluyen a lo largo del
Reactores de flujo continuo reactor
se operan en estado estacionario
Reactor Lecho Empacado
Indica con qué rapidez se consume
cierta cantidad de moles de una
especie química para formar otra
BALANCE MOLAR Intervienen reacciones
homogéneas y aquellos en los
especie químicar texto cuales se realizan reacciones
heterogéneas, fluido-
La Velocidad de Reacción (-ra) sólido, es que en el segundo caso
Reactores Industriales la reacción tiene lugar sobre la
superficie del catalizador.
Reacciones en fases liquidas
Los reactores semidiscontinuos y CSTRS se
emplean principalmente para reacciones en Reacciones en fases gaseosas
RESUMEN fase líquida. Un reactor semidiscontinuo
tiene esencialmente las mismas desventajas El reactor tubular (PFR) es relativamente fácil
que el reactor discontinuo. Sin embargo, de manejar (no tiene partes móviles) y por lo
cuenta con la ventaja de que la temperatura regular tiene la conversión más alta por
puede controlarse regulando la velocidad de volumen de reactor de todos los reactores de
alimentación y que permite minimizar flujo. La desventaja del reactor tubular es que
cualquier reacción secundaria indeseable es difícil controlar la temperatura dentro del
manteniendo una baja concentración' de uno reactor y pueden formarse puntos calientes
de los reactivos. si la reacción es exotérmica
También podría gustarte
- Modelamiento y casos especiales de la cinética química heterogéneaDe EverandModelamiento y casos especiales de la cinética química heterogéneaCalificación: 3 de 5 estrellas3/5 (1)
- Tarea 1Documento3 páginasTarea 1PATRICIA ARACELY JIMENEZ ENDARAAún no hay calificaciones
- Tipos de ReactoresDocumento2 páginasTipos de ReactoresDennis Hilario UmiyauriAún no hay calificaciones
- CUADRO COMPARATIVO - CasiDocumento3 páginasCUADRO COMPARATIVO - CasiMelany CruzAún no hay calificaciones
- Tipos de ReactoresDocumento2 páginasTipos de ReactoreslorenaAún no hay calificaciones
- U1ACTIVIDAD3Documento5 páginasU1ACTIVIDAD3yeseniaAún no hay calificaciones
- Actividad Entregable 1-Unidad 3 PDFDocumento1 páginaActividad Entregable 1-Unidad 3 PDFCRISTOFER NAPOLEON IBA�EZ FRANCOAún no hay calificaciones
- Lab 1Documento5 páginasLab 1Rodrigo AquipuchoAún no hay calificaciones
- Biorreactor PistonDocumento6 páginasBiorreactor PistonsalvadorAún no hay calificaciones
- Ingenieria de Las ReaccionesDocumento30 páginasIngenieria de Las ReaccionesAdda OropezaAún no hay calificaciones
- Pregunta 1Documento1 páginaPregunta 1DARWIN STALIN ALCACIEGA PILCOAún no hay calificaciones
- Reactores Tipos ZFX PDFDocumento1 páginaReactores Tipos ZFX PDFjhamirAún no hay calificaciones
- Reactores 4.Documento40 páginasReactores 4.Yefer Salazar ValdiviaAún no hay calificaciones
- Reactor de BATCHDocumento27 páginasReactor de BATCHlilian tatiana alvarado0% (1)
- Reactores HomogeneosDocumento20 páginasReactores Homogeneosapu19Aún no hay calificaciones
- Reactores BibliografiaDocumento27 páginasReactores Bibliografiaapu19Aún no hay calificaciones
- Tipos de Reactores Con Sus CaracteristicDocumento5 páginasTipos de Reactores Con Sus CaracteristicSoledad ColmenarezAún no hay calificaciones
- ReactoresDocumento6 páginasReactoresTakeshi Andres RoblezAún no hay calificaciones
- Equipo 5 - Práctica 6 y 7Documento13 páginasEquipo 5 - Práctica 6 y 7Mishel GarzonAún no hay calificaciones
- Modos de Operación de Los Biorreactores.Documento23 páginasModos de Operación de Los Biorreactores.ALAM DANIEL- HERNμNDEZ MALDONADOAún no hay calificaciones
- Laboratorio 1 Tipos de ReactoresDocumento3 páginasLaboratorio 1 Tipos de ReactoresLuis Fernando Colca SotoAún no hay calificaciones
- Reactores Presentaion DiseñoDocumento10 páginasReactores Presentaion DiseñoEnya Vives BntzAún no hay calificaciones
- Comparación de Tipos de ReactorDocumento3 páginasComparación de Tipos de ReactorAlonso VelazquezAún no hay calificaciones
- Fundamentos de Diseño de Reactores: Ingenieria de Reacciones Quimicas IDocumento60 páginasFundamentos de Diseño de Reactores: Ingenieria de Reacciones Quimicas IPatriciaLlacsaLázaroAún no hay calificaciones
- Tabla Comparativa de Diferentes Tipos de ReactoresDocumento3 páginasTabla Comparativa de Diferentes Tipos de ReactoresArmando CeballosAún no hay calificaciones
- Comparacion de Tipos de ReactoresDocumento2 páginasComparacion de Tipos de ReactoresJoseAún no hay calificaciones
- Resumen Reactor CSRTDocumento3 páginasResumen Reactor CSRTJuliana Suárez OlayaAún no hay calificaciones
- Fundamentos de Diseño de Reactotres (Corregido)Documento33 páginasFundamentos de Diseño de Reactotres (Corregido)Jhon Paul SanchezAún no hay calificaciones
- Ejercicio ReactoresDocumento2 páginasEjercicio ReactoresDaniel NuñoAún no hay calificaciones
- Tipos de Reactores PDFDocumento5 páginasTipos de Reactores PDFfernandoAún no hay calificaciones
- CineticaDocumento18 páginasCineticaGagomaaxAún no hay calificaciones
- Inv. CatalisisDocumento14 páginasInv. CatalisisPEDRO JOAQUIN S�NCHEZ TENORIOAún no hay calificaciones
- Mapa ConceptualDocumento2 páginasMapa ConceptualHeber Enrique Dominguez MayoAún no hay calificaciones
- Trabajo de Ejercicios Método SimpsonDocumento2 páginasTrabajo de Ejercicios Método Simpsonfreddy0% (1)
- Operaciones de ReacciónDocumento28 páginasOperaciones de ReacciónMarcioLazAún no hay calificaciones
- Proceso - ReactoresDocumento23 páginasProceso - ReactoresKevin HernandezAún no hay calificaciones
- 5.5-Y-5.14 Ejercicios Rectores QuimicosDocumento35 páginas5.5-Y-5.14 Ejercicios Rectores QuimicosPerrobigdawgAún no hay calificaciones
- Reactores HomogéneosDocumento1 páginaReactores HomogéneosharyAún no hay calificaciones
- Ingeniería Bioquímica - 202134 - 916Documento2 páginasIngeniería Bioquímica - 202134 - 916Kelly Johana Caicedo ZamoraAún no hay calificaciones
- Considerar Una Alimentación A Un Reactor en EstadoDocumento14 páginasConsiderar Una Alimentación A Un Reactor en EstadoMartin TowersAún no hay calificaciones
- REACTORES Algo MejoradoDocumento5 páginasREACTORES Algo MejoradoJean Pierre Gerónimo FloresAún no hay calificaciones
- CineticaDocumento2 páginasCineticaLuna GarcíaAún no hay calificaciones
- Analisis Reactores Homogeneos Dangela BarrosoDocumento1 páginaAnalisis Reactores Homogeneos Dangela BarrosomiguelAún no hay calificaciones
- Tema 5 (1) IRQDocumento29 páginasTema 5 (1) IRQFroilán Otero100% (1)
- Unidad 2Documento56 páginasUnidad 2Yennifer Giselle Martinez100% (1)
- Tríptico IR 2023-1Documento2 páginasTríptico IR 2023-1Ávila Marino NataliaAún no hay calificaciones
- Mapa ConceptualDocumento7 páginasMapa ConceptualJordan Lopez Fernandez100% (1)
- Reactor PFR - Exposición - BDocumento51 páginasReactor PFR - Exposición - BAlessandrx Montenegro ValenciaAún no hay calificaciones
- Expo ReactorsDocumento4 páginasExpo ReactorsAlberto Jose Zabala MalenoAún no hay calificaciones
- Tipos de BiorreactoresDocumento7 páginasTipos de BiorreactoresJOKE MARION AQUINO BRETONAún no hay calificaciones
- ANÁLISIS DE FLUJOS Y FACTORES QUE DETERMINAN LOS PERÍODOS DE RETENCIÓN - WordDocumento58 páginasANÁLISIS DE FLUJOS Y FACTORES QUE DETERMINAN LOS PERÍODOS DE RETENCIÓN - WordLucho OchoAún no hay calificaciones
- Flujo TapónDocumento3 páginasFlujo TapónKenia Carrera R.Aún no hay calificaciones
- ReactoresDocumento29 páginasReactoresvanessaAún no hay calificaciones
- Infografía. Lab. de Ing. Química I. Dahiana GamarraDocumento1 páginaInfografía. Lab. de Ing. Química I. Dahiana GamarraGalac TicosAún no hay calificaciones
- Tarea JorgeDocumento1 páginaTarea JorgeJonathan HernándezAún no hay calificaciones
- Reactor QuímicoDocumento96 páginasReactor Químicoomar0% (1)
- Reactore BatchDocumento5 páginasReactore BatchRosario UreñaAún no hay calificaciones
- Catalisis Homogenea - Catálisis Por Ácidos y Por BasesDocumento24 páginasCatalisis Homogenea - Catálisis Por Ácidos y Por Baseslizeth alvarezAún no hay calificaciones
- Catalisis Homogenea - IntroducciónDocumento22 páginasCatalisis Homogenea - Introducciónlizeth alvarezAún no hay calificaciones
- Catálisis Homogénea - Catálisis de Reacciones Elementales y No ElementalesDocumento13 páginasCatálisis Homogénea - Catálisis de Reacciones Elementales y No Elementaleslizeth alvarezAún no hay calificaciones
- Taller 02 - Valor Del Dinero en El Tiempo y Conversión de Tasas de InterésDocumento2 páginasTaller 02 - Valor Del Dinero en El Tiempo y Conversión de Tasas de Interéslizeth alvarezAún no hay calificaciones
- LaboratorioDocumento2 páginasLaboratoriolizeth alvarezAún no hay calificaciones
- Informe Quimica Inorganica V2Documento5 páginasInforme Quimica Inorganica V2lizeth alvarezAún no hay calificaciones
- Informe Quimica Inorganica V2Documento5 páginasInforme Quimica Inorganica V2lizeth alvarezAún no hay calificaciones
- Taller Aplicación Ley de GaussDocumento2 páginasTaller Aplicación Ley de Gausslizeth alvarezAún no hay calificaciones
- Informe Quimica Inorganica V1Documento5 páginasInforme Quimica Inorganica V1lizeth alvarezAún no hay calificaciones
- Informe Quimica Inorganica 2Documento7 páginasInforme Quimica Inorganica 2lizeth alvarezAún no hay calificaciones
- Cuestionario Práctica CuDocumento2 páginasCuestionario Práctica Culizeth alvarezAún no hay calificaciones
- Informe Quimica Inorganica V2Documento5 páginasInforme Quimica Inorganica V2lizeth alvarezAún no hay calificaciones
- 110 Fenantrolina PDFDocumento6 páginas110 Fenantrolina PDFProfa ClarkeAún no hay calificaciones
- 110 Fenantrolina PDFDocumento6 páginas110 Fenantrolina PDFProfa ClarkeAún no hay calificaciones
- Lab 5Documento2 páginasLab 5lizeth alvarezAún no hay calificaciones
- Manual de Usuario Registrador v3 - SISTEMA SINEDocumento31 páginasManual de Usuario Registrador v3 - SISTEMA SINEPabloAún no hay calificaciones
- Diseño Del Soporte de Una Obra SubterraneaDocumento62 páginasDiseño Del Soporte de Una Obra SubterraneaJose PepeAún no hay calificaciones
- Diseno y Construccion de Una Maquina PerforadoraDocumento167 páginasDiseno y Construccion de Una Maquina PerforadoraGabriel0% (1)
- Laboratorio 10 PDFDocumento7 páginasLaboratorio 10 PDFMario Alberto Molina PandiaAún no hay calificaciones
- Hoja de Metrados Casa Multifamiliar 1Documento14 páginasHoja de Metrados Casa Multifamiliar 1Alfredo AlfreditoAún no hay calificaciones
- Diapos Pitot Final Final 5Documento35 páginasDiapos Pitot Final Final 5MaJuTorresRimeyAún no hay calificaciones
- Capacitor MicroondasDocumento1 páginaCapacitor MicroondasBaltazar VargasAún no hay calificaciones
- Tarea Extra Clase No. 3 - Curvas de Enfriamientos.Documento12 páginasTarea Extra Clase No. 3 - Curvas de Enfriamientos.Thaily Arias MayAún no hay calificaciones
- Manual Guia VozDocumento48 páginasManual Guia VozLuis Guillermo Rodríguez A.Aún no hay calificaciones
- Teclas para Arranque PCDocumento3 páginasTeclas para Arranque PCAndres Mauricio HernandezAún no hay calificaciones
- Soldadura MejiaDocumento28 páginasSoldadura MejiaMilton AlfaroAún no hay calificaciones
- Medición de Temperatura - Trabajo PracticoDocumento11 páginasMedición de Temperatura - Trabajo PracticoPamela Rojas Díaz de VivarAún no hay calificaciones
- Tuberia Adosada A Muro PDFDocumento1 páginaTuberia Adosada A Muro PDFANGEL JAVIERAún no hay calificaciones
- Unidad 2Documento26 páginasUnidad 2Angeles GonzalezAún no hay calificaciones
- Instalacion Energetica de Una Casa de Campo - IMA301DDocumento507 páginasInstalacion Energetica de Una Casa de Campo - IMA301DCIFP Mantenimiento y Servicios a la ProducciónAún no hay calificaciones
- RD500 20201105Documento1 páginaRD500 20201105Juan Carlos Ludeña ChoqueAún no hay calificaciones
- Propuesta ExpocienciaDocumento6 páginasPropuesta Expocienciasince1365Aún no hay calificaciones
- Reporte de Manometro CaseroDocumento4 páginasReporte de Manometro CaseroULISES ANTONIO DE LA CRUZ VENEGASAún no hay calificaciones
- Matriz de EppDocumento12 páginasMatriz de EppJOSTAL GAMER PROAún no hay calificaciones
- Nicol Molecula DipolarDocumento3 páginasNicol Molecula DipolarLixmelys VillarroelAún no hay calificaciones
- El ProyectorDocumento4 páginasEl ProyectorFelix HuarachiAún no hay calificaciones
- Diagnostico y Mejoramiento de Los Servicios de Agua Potable, Saneamiento y Alcantarillado para El Municipio de Zamora, Michoacan.Documento163 páginasDiagnostico y Mejoramiento de Los Servicios de Agua Potable, Saneamiento y Alcantarillado para El Municipio de Zamora, Michoacan.juanAún no hay calificaciones
- Construcción de Cajas AcústicasDocumento7 páginasConstrucción de Cajas AcústicascamacholucAún no hay calificaciones
- Diagnostico Basico de AlineacionDocumento15 páginasDiagnostico Basico de AlineacionJONH JAIRO SIERRA GUALTEROS100% (1)
- Afilado de BurilDocumento13 páginasAfilado de Burilʙᴀʀʀɪᴏs ᴍᴀʀᴛɪ́ɴᴇᴢ ᴍɪᴄʜᴇʟAún no hay calificaciones
- Estudio TopograficoDocumento54 páginasEstudio TopograficoYesmit Tania Doroteo MoralesAún no hay calificaciones
- Proyecto de ElectricidadDocumento19 páginasProyecto de ElectricidadJulio RCAún no hay calificaciones
- Valor Posicional 05 de MayoDocumento14 páginasValor Posicional 05 de MayoElizabeth Maribel Bravo TorresAún no hay calificaciones
- Ensayo Soldadura de Gas Inerte de TungstenoDocumento3 páginasEnsayo Soldadura de Gas Inerte de TungstenoJuan Daniel Felix PalominoAún no hay calificaciones
- Presupuesto Obra Diseño POR ESPACIO APTO 915Documento2 páginasPresupuesto Obra Diseño POR ESPACIO APTO 915Paula LosadaAún no hay calificaciones