Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Actividad Enzimatica
Cargado por
Sunilda Meza Pariamancco0 calificaciones0% encontró este documento útil (0 votos)
99 vistas11 páginasCATALASA ... EN UNA PRACTICA DE LABORATORIO EN UNA HIGADO DE POLLO
Título original
ACTIVIDAD ENZIMATICA
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCATALASA ... EN UNA PRACTICA DE LABORATORIO EN UNA HIGADO DE POLLO
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
99 vistas11 páginasActividad Enzimatica
Cargado por
Sunilda Meza PariamanccoCATALASA ... EN UNA PRACTICA DE LABORATORIO EN UNA HIGADO DE POLLO
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 11
PRACTICA N°6
ACTIVIDAD ENZIMATICA DE
LA CATALASA
TOXICOLOGIA Y SEGURIDAD ALIMENTARIA
I. INTRODUCCION
En este presente informe trataremos el tema sobre la actividad de la
enzima de la catalasa, esta enzima esta presente en todos los seres
vivos; la función de la catalasa es oxidar y descomponer el peróxido
de hidrógeno que se crea dentro de las células como se da en el
proceso de metabolismo tanto catabolismo y anabolismo que resultan
ser residuos tóxicos para el organismo transformándola en sustancia
no toxica (H2O2 en H2O y O2 ). La catalasa en él ser humano se
encuentra en el hígado y peroxidasa, que se encuentra en las plantas.
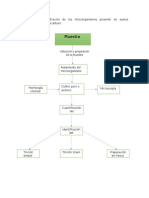
En esta práctica de laboratorio consistió en observar la presencia de
catalasa que está en el hígado de pollo y hojas de planta (muestras),
reactivos como el peróxido de hidrogeno (comúnmente llamada agua
oxigenada) y agua destilada. se llevará dos muestras a tratamiento
térmico y otras dos sin tratamiento térmico ahí veremos cómo influye
la temperatura en la acción de la enzima de la catalasa.
II. CAPACIDADES
• Demuestro la presencia de la enzima catalasa en los tejidos
animales y vegetales
• Analizo la acción enzimática de la catalasa y la formación de
producto en forma de gas O2 y líquido H2O.
• Desarrollo habilidades y destrezas en la manipulación de los
equipos y materiales.
III. FUNDAMENTO
En el organismo existe un sistema de protección antioxidante formado por
enzimas y compuestos de bajo peso molecular. Una de las enzimas que
interviene en la protección y, en consecuencia, en el mantenimiento
del balance oxidante/antioxidante es la catalasa(CAT). La catalasa es una
enzima hemo proteica, que se caracteriza por poseer una estructura
tetramérica, en la cual casa subunidad contiene un grupo Hem (Fe+3)
Esta presenta en la mayoría de las bacterias aeróbicas estrictas,
facultativas y anaeróbicas aerotolerantes. La catalasa manifiesta
actividad de peroxidasa, cataliza la oxidación de sustratos acoplada a
la reducción del peróxido de hidrogeno, para formar agua y oxigeno
molecular.
“El peróxido de hidrogeno es muy toxico para las bacterias. Generalmente
los miroorganismos que carecen de citocromos también carecen de
catalasa, así la mayoría de las bacterias anaerobias no la poseen”
(Rodríguez Cavallini, Evelyn, 2005, p 217)
Para Elmer Koneman (2008) El peróxido de hidrogeno se forma como
uno de los productos finales de oxidación del metabolismo aerobio e los
hidratos de carbono. Si se permite que se acumule, resulta letal para las
células bacterianas. La catalasa convierte el peróxido de hidrogeno en
agua y oxigeno según la siguiente reacción:
2 H2O2 2 H2O +O2
Para José M. Macarulla (1994) La catalasa a nivel celular se localiza en
las mitocondrias y peroxisomas, excepto en los eritrocitos, donde se
encuentra el citosol. Esta enzima es una metaloproteinatetramerica, cuyo
peso molecular se encuentra en el rango de 210-280 kD. Constade 4
subunidades idénticas que se mantienen unidad por interacciones no
covalentes. Cada subunidad contiene un grupo prostético de
protoporfirina IX y el contenido protohémico y el hierro representan un
1,1% y 0,09% respectivamente en el peso molecular total de la enzima
La temperatura puede tener un efecto importante sobre la actividad de las
enzimas y las velocidades de reacción. A bajas temperaturas, el aporte
de calor usualmente aumenta la velocidad de una reacción enzimática,
porque los reactivos tienes mayor energía y pueden alcanzar l nivel de la
energía de activación con mayor facilidad. Sin embargo, si la temperatura
se eleva demasiado, es posible que se desnaturalice la enzima,
provocando la desorganización de su estructura terciaria y la pérdida de
su actividad catalítica.
IV. MATERIALES, EQUIPO Y REACTIVOS
Muestra: 1 hígado de pollo, 2 hojas de planta.
Materiales y equipos: 4 tubos de ensayo, 1 gradilla, 1 pipeta de
10ml, baño maría, 1 cuchillo.
Reactivos: Agua oxigenada (H2O2), agua destilada.
V. PROCEDIMIENTO
✓ El hígado de pollo se pica en pequeños trozos a igual las hojas
de planta
✓ Colocamos cuatro tubos de ensayo del 1 al 4 sobre la gradilla
✓ Luego se introduce las muestras en los tubos de ensayo
✓ Tubo 1: hojas con 4ml de agua destilada.
✓ Tubo 2: hígado con 4ml de agua destilada.
✓ Tubo 3: hojas con 4ml de H2O2
✓ Tubo 4: hígado con 4ml de H2O2
✓ Se observa las reacciones y se registra
✓ Al tubo 1 y 2 lo llevamos a tratamiento térmico (baño maría 60°C
X 10´)
✓ Observo los cambios que ocurrió y se deja enfriar
✓ añado al tubo 1 y 2; 4ml de agua oxigenada (H2O2).
✓ Observo los cambios que se dan en los tubos y se registró
VI. CÁLCULOS Y RESULTADOS
CUADRO 1: CARACTERÍSTICA DE LA MUESTRA ANTES Y
DESPUÉS DE LA APLICACIÓN DE H2O2:
MUESTRA MUESTRA + H2O MUESTRA + H2O2
Apareció poquísimas Hubo una reacción notoria
burbujas presencia de burbujas al
máximo
Hígado de Pollo
No hubo ninguna reacción Hubo presencia de
Hoja de la Planta
pequeñas burbujas
CUADRO 2: CARACTERÍSTICA DE LA MUESTRA CON APLICACIÓN
DE CALOR Y APLICACIÓN DE H2O2:
MUESTRA + CALOR +
MUESTRA MUESTRA + CALOR
H2O2
Solo se apreció pequeñísimas Hubo reacción, pero solo en
burbujas mínima presencia de burbuja
Hígado de pollo
No hubo reacción Poca presencia de burbujas
Hoja de la Planta
VII. DISCUSION DE LOS RESULTADOS
En el hígado de pollo (sin tratamiento térmico) hubo más reacción ya
que hay mayor presencia de la enzima catalasa al estar en contacto
con el peróxido de hidrógeno ahora con el tratamiento térmico se notó
en menor reacción ya que la enzima catalasa al someterse al calor
reduce su actividad entonces la temperatura influye bastante. Estos
datos indican que la actividad de la catalasa tiende a disminuir al
aumentar la temperatura. - Cuando un tejido permanece por encima
de los 100ºC (se cuece) la catalasa se desnaturaliza y pierde su
actividad biológica; Que las bajas temperaturas no afectan a su
actividad, incluso después de congelar el órgano, la catalasa sigue
con su misma funcionalidad. (L. CANCHO; C. GARCÍA; L. MOLANO;
J. MORENO Y F. ALFONSO 2012)
En las hojas de planta no hubo reacción en ambos casos ya que están
producen o tienen en sus células como mecanismos de defente ante
ataque de patógenos en sus tejidos vegetales.
VIII. CONCLUSIONES
en esta práctica lo que se observó y se registró fue que la enzima
catalasa presentes tanto en el tejido animal y vegetal
con agua destilada no hay mucha reacción en cambio con el peróxido
de hidrogeno si la hay, pero solamente en el hígado de pollo hubo
mayor efervescencia, al someterse al calor la actividad de la catalasa
se reduce ya que se desnaturaliza porque es una enzima hemo
proteica
IX. CUESTIONARIO
1. ¿Por qué presenta un intenso burbujeo cuando el hígado entra en
contacto con el H2O2?
Si el hígado se macera, las células se rompen, con lo cual la reacción
con peróxido de hidrógeno se lleva a cabo con más rapidez y la
espuma burbujeo) que resulta se debe al desprendimiento de
oxígeno gaseoso de la mezcla de la reacción. (Brown, T, Bursten, B.
y Le May, H.2004)
2. ¿Por qué la reacción se da en una menor intensidad al entrar en
contacto el H202 con la hoja?
porque estas producen naturalmente en su composición el peróxido
de hidrogeno quiere decir que ya contienen dicha enzima
3. ¿Qué sucede cuando la muestra de hígado se somete a
calentamiento?
La enzima catalasa, al ser una proteína puede desnaturalizarse al
someterse al calor. La desnaturalización de una proteína implica la
alteración de sus estructuras secundaria, terciaria o cuaternaria,
dejando intacta la estructura primaria; el resultado de esto es que la
proteína nativa (como se encuentra en la célula) pierde su actividad
biológica.
X. REFERENCIAS
https://es.scribd.com/doc/80995770/Reaccion-de-higado-de-res-en-
presencia-de-agua-oxigenada
https://issuu.com/danielafonseca38/docs/practica_no.5_bq
http://slideplayer.es/slide/11618275/
http://cprbrozas.juntaextremadura.net/REVISTA_FINAL.pdf
https://es.scribd.com/doc/81014235/Practica-Higado
También podría gustarte
- Actividad enzimática de la catalasa y amilasaDocumento6 páginasActividad enzimática de la catalasa y amilasaSandy Ingaruca Baez0% (1)
- BIOLOGÍA GENERAL Lab. - Acidos Nucleicos UnalmDocumento8 páginasBIOLOGÍA GENERAL Lab. - Acidos Nucleicos UnalmXIWXIAún no hay calificaciones
- Guia 3. Identificación de AminoacidosDocumento7 páginasGuia 3. Identificación de AminoacidosCarolinaQuimbayaAún no hay calificaciones
- Práctica 6. Efecto de La Ósmosis en La Papa.Documento4 páginasPráctica 6. Efecto de La Ósmosis en La Papa.Antonio VázquezAún no hay calificaciones
- Reporte Practica 2 Etapa 2 Efecto de La Osmosis en La PapaDocumento7 páginasReporte Practica 2 Etapa 2 Efecto de La Osmosis en La PapaPriscillaAún no hay calificaciones
- Ensayo de La Llama InformeDocumento4 páginasEnsayo de La Llama Informealaya datAún no hay calificaciones
- Elementos BiogenesicosDocumento6 páginasElementos BiogenesicosGiulliana Rubio Reque100% (1)
- Reconocimiento de CarbohidratosDocumento6 páginasReconocimiento de CarbohidratosAngel Alcazar50% (2)
- 04 Elementos Biogenesicos y Minerales de La Materia VivaDocumento2 páginas04 Elementos Biogenesicos y Minerales de La Materia VivaJudith CcAún no hay calificaciones
- Observación microscópica de estomas en hojasDocumento12 páginasObservación microscópica de estomas en hojasNilreyam FerAún no hay calificaciones
- Reconocimiento y Diferenciación de CarbohidratosDocumento16 páginasReconocimiento y Diferenciación de CarbohidratosVictor CruzAún no hay calificaciones
- Determinación Cuantitativa de CarbohidratosDocumento2 páginasDeterminación Cuantitativa de CarbohidratosMateo GomezAún no hay calificaciones
- Acción catalizadora enzimas tejidosDocumento18 páginasAcción catalizadora enzimas tejidosLaura OteroAún no hay calificaciones
- Balance de materia laboratorio UMSADocumento9 páginasBalance de materia laboratorio UMSAPAOLA ANDREA QUENALLATA CHIPANAAún no hay calificaciones
- Informe Práctica Laboratorio 7Documento6 páginasInforme Práctica Laboratorio 7Diana Samaniego OlivaresAún no hay calificaciones
- Examen en Fresco de Microorganismos en AguasDocumento3 páginasExamen en Fresco de Microorganismos en AguasJesica NogueraAún no hay calificaciones
- PRÁCTICA #07 EnzimasDocumento7 páginasPRÁCTICA #07 EnzimasAnonymous xLsjIE53mjAún no hay calificaciones
- INFORME III - Extracción de ADN CaseroDocumento14 páginasINFORME III - Extracción de ADN CaseroJosé Valverde CarbonelAún no hay calificaciones
- ACTIVIDAD 2: Estructuras de MedicamentosDocumento3 páginasACTIVIDAD 2: Estructuras de MedicamentosMiirelle RZAún no hay calificaciones
- Biotecnologia - Laboratorio 1Documento14 páginasBiotecnologia - Laboratorio 1Sergio Andia SanchezAún no hay calificaciones
- CLASE 14 - RadioisotoposDocumento53 páginasCLASE 14 - RadioisotoposRonald Alejandro Perez Ortiz100% (2)
- Aromatic OsDocumento4 páginasAromatic OsFernando MacedaAún no hay calificaciones
- Informe de Laboratorio Celulas Procariotas y EucariotasDocumento6 páginasInforme de Laboratorio Celulas Procariotas y EucariotaswilliamAún no hay calificaciones
- BIOSEGURIDADDocumento10 páginasBIOSEGURIDADKarla VelaasteguiAún no hay calificaciones
- Guia de Practicas Química Analitica I - 2021-IDocumento45 páginasGuia de Practicas Química Analitica I - 2021-IOswaldo SanabriaAún no hay calificaciones
- El AtomoDocumento8 páginasEl AtomoCristhianAún no hay calificaciones
- Practica No 1 Algunas Propiedades Del AguaDocumento6 páginasPractica No 1 Algunas Propiedades Del AguaDiana Laura Zumaya AlavezAún no hay calificaciones
- Energias Renovables - HuarazDocumento40 páginasEnergias Renovables - Huarazdolo1234Aún no hay calificaciones
- Louis Pasteur Y El Perro RabiosoDocumento15 páginasLouis Pasteur Y El Perro RabiosoEsmeralda BlancoAún no hay calificaciones
- Informe Azúcares ReductoresDocumento5 páginasInforme Azúcares ReductoresHolman PinzónAún no hay calificaciones
- N°3 Compuestos Organicos e InorganicosDocumento9 páginasN°3 Compuestos Organicos e InorganicosKatherine TorresAún no hay calificaciones
- N 1. Amilasa Salival PDFDocumento6 páginasN 1. Amilasa Salival PDFivanAún no hay calificaciones
- Práctica N°07 - Funciones Químicas InorgánicasDocumento2 páginasPráctica N°07 - Funciones Químicas InorgánicasJosé Agreda100% (1)
- Informe 3. Indicadores de PH CaserosDocumento4 páginasInforme 3. Indicadores de PH CaserosMiguelÁngelGuerraIIIAún no hay calificaciones
- Determinación pH Sustancias DomésticasDocumento4 páginasDeterminación pH Sustancias DomésticasJosé Muñoz GarciaAún no hay calificaciones
- Transporte de membrana: difusión y osmosisDocumento15 páginasTransporte de membrana: difusión y osmosisCristian TrujilloAún no hay calificaciones
- Obtener Archivo RecursoDocumento6 páginasObtener Archivo RecursoJhon CarrionAún no hay calificaciones
- Informe Practica 4Documento12 páginasInforme Practica 4Emelyn SaldivarAún no hay calificaciones
- Práctica #5Documento22 páginasPráctica #5BAUTISTA TERRONES GILMERAún no hay calificaciones
- Accion de La Amilasa Sobre El AlmidonDocumento8 páginasAccion de La Amilasa Sobre El AlmidonLivia NinaAún no hay calificaciones
- Practica 4Documento5 páginasPractica 4Luisa OrtizAún no hay calificaciones
- Informe NDocumento7 páginasInforme NEver LuisAún no hay calificaciones
- Informe 5 Reconocimiento de Vitaminas Helber Rojas, Danny Bautista.Documento10 páginasInforme 5 Reconocimiento de Vitaminas Helber Rojas, Danny Bautista.Helber Fernando Rojas BarajasAún no hay calificaciones
- Reacción catalasa tejidos hígado manzanaDocumento2 páginasReacción catalasa tejidos hígado manzanaelenaAún no hay calificaciones
- EnzimasHígadoDocumento4 páginasEnzimasHígadojahelAún no hay calificaciones
- Exam Pract BM Farm 2020-IiDocumento1 páginaExam Pract BM Farm 2020-IiJhon Jhosmel H CcAún no hay calificaciones
- Practica Del Benceno Marco Teorico y Refe BiblioDocumento4 páginasPractica Del Benceno Marco Teorico y Refe BiblioJhomy MazaAún no hay calificaciones
- Laboratorio de Biologia HuevoDocumento15 páginasLaboratorio de Biologia HuevoNiz Cohen100% (2)
- Aislamiento e Identificación de Los MicroorganismosDocumento2 páginasAislamiento e Identificación de Los MicroorganismosRocío Gordillo SanchezAún no hay calificaciones
- GRAVIMETRIADocumento23 páginasGRAVIMETRIAPUTODIXONVOL2Aún no hay calificaciones
- CONCLUSIONES y ObserbacionesDocumento2 páginasCONCLUSIONES y ObserbacionesFernandoAún no hay calificaciones
- Marco TeóricoDocumento8 páginasMarco TeóricoDaniel Arroyo AedoAún no hay calificaciones
- Catabolismo de Aminoacidos 1Documento12 páginasCatabolismo de Aminoacidos 1Bárbara VictoriaaAún no hay calificaciones
- Semana 2 Guia de Laboratorio 2017Documento7 páginasSemana 2 Guia de Laboratorio 2017Bryan SantiagoAún no hay calificaciones
- Practica Reconocimiento de Enzimas 6Documento9 páginasPractica Reconocimiento de Enzimas 6Leonardo Francisco Sanchez GuerreroAún no hay calificaciones
- Identificación y desnaturalización de la catalasa en tejidosDocumento15 páginasIdentificación y desnaturalización de la catalasa en tejidosÁlvaro Chamorro CalixtoAún no hay calificaciones
- Practica #3Documento5 páginasPractica #3Roberto AvilaAún no hay calificaciones
- Trabajo de Bioprocesos (Autoguardado)Documento18 páginasTrabajo de Bioprocesos (Autoguardado)jheni quispe santiagoAún no hay calificaciones
- Informe Biologia Nº5Documento5 páginasInforme Biologia Nº5ROSAFLOR ALEXANDRA VIDAL PACHECOAún no hay calificaciones
- Química de macrocomponentes de alimentosDe EverandQuímica de macrocomponentes de alimentosAún no hay calificaciones
- Fluido SupercríticoDocumento4 páginasFluido SupercríticoRicardo SeminarioAún no hay calificaciones
- TP7 Valoraciones RedoxDocumento6 páginasTP7 Valoraciones RedoxJavier Angel VegaAún no hay calificaciones
- Esteroides de Importancia ClínicaDocumento4 páginasEsteroides de Importancia Clínicaanthonnydaniel3Aún no hay calificaciones
- Ua 3 Temas #5 y 6 Nomenclatura y Reacciones QuimicasDocumento38 páginasUa 3 Temas #5 y 6 Nomenclatura y Reacciones QuimicasMonografia MoreroAún no hay calificaciones
- Produccion y Comercializacion de Hierro en El Peru y El Mundo (Trabajo)Documento23 páginasProduccion y Comercializacion de Hierro en El Peru y El Mundo (Trabajo)Moises Garcia CanoAún no hay calificaciones
- AlcanosDocumento11 páginasAlcanosEmmanuel VillagomezAún no hay calificaciones
- TubocurarinaaDocumento10 páginasTubocurarinaaELIA CELESTE CONTRERAS MERCADOAún no hay calificaciones
- NormasTécnicasAguaPotableDocumento87 páginasNormasTécnicasAguaPotableDaniel Valdez Gonzalez100% (1)
- Guia AlquenosDocumento11 páginasGuia Alquenosyolima vivasAún no hay calificaciones
- MIS OJOS Niveles de Energia Modelos Atomicos Espectros Masa Atomica RelativaDocumento20 páginasMIS OJOS Niveles de Energia Modelos Atomicos Espectros Masa Atomica RelativaConde DracoAún no hay calificaciones
- Hibridacion SomaticaDocumento12 páginasHibridacion SomaticaNegroYomagaAún no hay calificaciones
- Hg02 - As - Determinación Del Umbral de Diferencia (Dulce, Ácido, Saldo)Documento2 páginasHg02 - As - Determinación Del Umbral de Diferencia (Dulce, Ácido, Saldo)Marcelitito VayitassAún no hay calificaciones
- Ariston AV61 enDocumento60 páginasAriston AV61 enΓρηγορία ΝικολέτουAún no hay calificaciones
- 3d Patologias en Puentes PDFDocumento28 páginas3d Patologias en Puentes PDFEverardo Citalán MadridAún no hay calificaciones
- POLARIMETRIADocumento20 páginasPOLARIMETRIAJhoselin Haro SebastianAún no hay calificaciones
- Fenomenos AntropometricosDocumento24 páginasFenomenos AntropometricosAlbert SerwayAún no hay calificaciones
- 1 GUIA Tejidos y TensadoDocumento13 páginas1 GUIA Tejidos y TensadoDANIEL LEONARDO ROA GARCIAAún no hay calificaciones
- Calculos FlashDocumento79 páginasCalculos FlashJair NaranjoAún no hay calificaciones
- ReinosDocumento63 páginasReinosmoisesX111Aún no hay calificaciones
- Refrigeración Agosto 2010 Secadores RefrigerativosDocumento62 páginasRefrigeración Agosto 2010 Secadores RefrigerativosÁlvaro Arango100% (2)
- Examen Vega Flores YanellaoDocumento4 páginasExamen Vega Flores YanellaoYanella Vega FloresAún no hay calificaciones
- Ejercicios de Gases IdealesDocumento20 páginasEjercicios de Gases IdealesELSA LOREN PAUCAR PEREZAún no hay calificaciones
- GUIA GRADO 4° - MateriaDocumento12 páginasGUIA GRADO 4° - MateriaFederTuiranGarciaAún no hay calificaciones
- Mejoramiento de Una Mezcla Asfáltica Con La Adición Del Residuo de Caucho Obtenido Tras Su Remoción de La Pista de Aterrizaje Del Aeropuerto Internacional Mariscal Sucre, Por Vía Seca PDFDocumento127 páginasMejoramiento de Una Mezcla Asfáltica Con La Adición Del Residuo de Caucho Obtenido Tras Su Remoción de La Pista de Aterrizaje Del Aeropuerto Internacional Mariscal Sucre, Por Vía Seca PDFFabio AmbrocioAún no hay calificaciones
- Informe de Laboratorio Nro 6 - AFODocumento9 páginasInforme de Laboratorio Nro 6 - AFODánica Nicoll Rojas MolinaAún no hay calificaciones
- Fisica de SemiconductoresDocumento116 páginasFisica de SemiconductoresJoel Rojas DuarteAún no hay calificaciones
- Aerre CatalogoDocumento78 páginasAerre CatalogojulicesarAún no hay calificaciones
- Reporte 1 Determinación Constante de EquilibrioDocumento14 páginasReporte 1 Determinación Constante de EquilibrioFranciscoRosalesRivera100% (1)
- Prueba Formativa Biología Celular y Molecular 3° MedioDocumento3 páginasPrueba Formativa Biología Celular y Molecular 3° MedioLisette MendietaAún no hay calificaciones
- Quemaduras solares y fotoprotecciónDocumento58 páginasQuemaduras solares y fotoprotecciónalejandroesco100% (2)