Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Termo Tema 5 - Clase 21
Cargado por
Carolina CastroDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Termo Tema 5 - Clase 21
Cargado por
Carolina CastroCopyright:
Formatos disponibles
Cátedra de Termodinámica General
Universidad de Carabobo
Facultad de Ingeniería
Estudios Básicos
Departamento de Física
Cátedra de Termodinámica General
Clase #21
Prof. Alberto Martínez M.
Tema #5. (continuación)
Desigualdad de Clausius: Para procesos cíclicos.
Ta
Qa Qa
Wrev Wirrev
MTrev MTirrev
Qb,rev Qb,irrev
Tb
Balance de energía: 𝐸𝑒𝑛𝑡𝑟𝑎𝑑𝑎 − 𝐸𝑠𝑎𝑙𝑖𝑑𝑎 = 0 ⇒ 𝐸𝑒𝑛𝑡𝑟𝑎𝑑𝑎 = 𝐸𝑠𝑎𝑙𝑖𝑑𝑎
𝑊𝑟𝑒𝑣 = 𝑄𝑎 − 𝑄𝑏,𝑟𝑒𝑣
𝑊𝑖𝑟𝑟𝑒𝑣 = 𝑄𝑎 − 𝑄𝑏,𝑖𝑟𝑟𝑒𝑣
𝑊𝑟𝑒𝑣 > 𝑊𝑖𝑟𝑟𝑒𝑣 ⇒ 𝑄𝑏,𝑖𝑟𝑟𝑒𝑣 > 𝑄𝑏,𝑟𝑒𝑣
𝑄𝑎 𝑇 𝑄 𝑄𝑏,𝑟𝑒𝑣 𝛿𝑄
Máq. reversible: 𝑄𝑏,𝑟𝑒𝑣
= 𝑇𝑎 ⇒ 𝑇𝑎 − 𝑇𝑏
= 0 ⇒ ∮𝑟𝑒𝑣 𝑇
=0
𝑏 𝑎
𝑄𝑎 𝑄𝑏,𝑖𝑟𝑟𝑒𝑣 𝛿𝑄
Máq. irreversible: 𝑇𝑎
− 𝑇𝑏
< 0 ⇒ ∮𝑖𝑟𝑟𝑒𝑣 𝑇
<0
La integral cíclica de Q/T siempre es menor o igual a cero. Esta desigualdad es válida
durante todos los ciclos, tanto reversibles como irreversibles.
= 0 ciclo reversible
𝛿𝑄
∮𝑇 ≤0 < 0 ciclo irreversible
> 0 ciclo imposible
Prof. Alberto Martínez M. Facultad de Ingeniería - UC Página 1
Cátedra de Termodinámica General
Ejemplo: Considere una central eléctrica de vapor que opera con un flujo másico de
1 kg/s. Verifique el cumplimiento de la segunda ley de la termodinámica.
P2 = 12,5 MPa
2 T2 = 550 °C
𝑊̇𝑡𝑢𝑟𝑏𝑖𝑛𝑎,𝑠𝑎𝑙𝑖𝑑𝑎
P3 = 10 kPa
550 °C
3 x3 = 0,88
1
P1 = P2 4
T1 = 50 °C Líq. sat.
Cumplimiento de la segunda ley de la termodinámica:
𝛿𝑄
∮ ≤0
𝑇
𝛿𝑄 𝑄𝑎 𝑄𝑏 𝑄𝑐𝑎𝑙𝑑𝑒𝑟𝑎 𝑄𝑐𝑜𝑛𝑑𝑒𝑛𝑠𝑎𝑑𝑜𝑟
∮ = − = − (𝑏𝑎𝑠𝑒 𝑑𝑒 𝑐á𝑙𝑐𝑢𝑙𝑜 = 1 𝑠)
𝑇 𝑇𝑎 𝑇𝑏 𝑇𝑎 𝑇𝑏
Edo. 1:
P1 = 12,5 MPa Líquido comprimido
T1 = 50 °C
h1 ≈ hf a 50 °C = 209,34 kJ/kg
Edo. 2:
P2 = P1 = 12,5 MPa Vapor sobrecalentado
T2 = 550 °C
h2 = 3476,5 kJ/kg
VC: Caldera
𝐸̇𝑒𝑛𝑡𝑟𝑎𝑑𝑎 = 𝐸̇𝑠𝑎𝑙𝑖𝑑𝑎
𝑄̇𝑐𝑎𝑙𝑑𝑒𝑟𝑎,𝑒𝑛𝑡𝑟𝑎𝑑𝑎 + 𝑚̇ℎ1 = 𝑚̇ℎ2 ⇒ 𝑄̇𝑐𝑎𝑙𝑑𝑒𝑟𝑎,𝑒𝑛𝑡𝑟𝑎𝑑𝑎 = 𝑚̇(ℎ2 − ℎ1 )
𝑄̇𝑐𝑎𝑙𝑑𝑒𝑟𝑎,𝑒𝑛𝑡𝑟𝑎𝑑𝑎 = 3267,16 𝑘𝐽/𝑠
Prof. Alberto Martínez M. Facultad de Ingeniería - UC Página 2
Cátedra de Termodinámica General
Edo. 3 (mezcla líquido-vapor):
P3 = 10 kPa
x3 = 0,88
ℎ3 = ℎ𝑓 + 𝑥3 ℎ𝑓𝑔 = 2296,86 𝑘𝐽/𝑘𝑔
Edo. 4 (líquido saturado):
P4 = P3 = 10 kPa
T4 = Tsat a 10 kPa = 45,81 °C
h4 = hf a 10 kPa = 191,81 kJ/kg
VC: Condensador
𝐸̇𝑒𝑛𝑡𝑟𝑎𝑑𝑎 = 𝐸̇𝑠𝑎𝑙𝑖𝑑𝑎
𝑚̇ℎ3 = 𝑄̇𝑐𝑜𝑛𝑑𝑒𝑛𝑠𝑎𝑑𝑜𝑟,𝑠𝑎𝑙𝑖𝑑𝑎 + 𝑚̇ℎ4 ⇒ 𝑄̇𝑐𝑜𝑛𝑑𝑒𝑛𝑠𝑎𝑑𝑜𝑟,𝑠𝑎𝑙𝑖𝑑𝑎 = 𝑚̇(ℎ3 − ℎ4 )
𝑄̇𝑐𝑜𝑛𝑑𝑒𝑛𝑠𝑎𝑑𝑜𝑟,𝑠𝑎𝑙𝑖𝑑𝑎 = 2105,05 𝑘𝐽/𝑠
Sustituyendo: pueden indicar otras
𝛿𝑄 3267,16 𝑘𝐽 2105,05 𝑘𝐽 temperaturas
∮ = −
𝑇 (550 + 273,15)𝐾 (45,81 + 2713,15)𝐾
𝛿𝑄 𝑘𝐽
∮ = −2,63 < 0 ⇒ 𝑠í 𝑠𝑒 𝑐𝑢𝑚𝑝𝑙𝑒
𝑇 𝐾
Definición termodinámica de entropía
En un ciclo: ∮ 𝑑𝑃 = 0 ∮ 𝑑𝑣 = 0 ∮ 𝑑𝑇 = 0
𝛿𝑄
∮( ) =0
𝑇 𝑖𝑛𝑡 𝑟𝑒𝑣
Se tiene:
𝛿𝑄
( ) = 𝑑𝑆
𝑇 𝑖𝑛𝑡 𝑟𝑒𝑣
2
𝛿𝑄
∆𝑆 = 𝑆2 − 𝑆1 = ∫ ( )
1 𝑇 𝑖𝑛𝑡 𝑟𝑒𝑣
Prof. Alberto Martínez M. Facultad de Ingeniería - UC Página 3
Cátedra de Termodinámica General
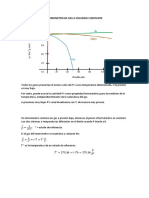
Proceso
T irreversible
2
∆𝑆 = 𝑆2 − 𝑆1 = 0,4 𝑘𝐽/𝐾
1
Proceso
reversible
0,3 0,7 S (kJ/K)
Diagrama T-s
T
T Punto crítico
P1
𝑠1 ≈ 𝑠𝑓 𝑎 𝑇1 P3 Línea de líq.
T1
𝑠3 sat.
T3
Líquido P = cte
comprimido Vapor
(1) (2) sobrecalentado
Mezcla (3)
Líquido-vapor
T2 Línea de vapor
𝑠2 = 𝑠𝑓 + 𝑥2 𝑠𝑓𝑔 saturado
x2
v = cte
s
s
Procesos reversibles Ciclo de Carnot
T qa
(1) (2)
Ta
Tb
(4) (3)
qb
s1 = s4 s2 = s3 s
Prof. Alberto Martínez M. Facultad de Ingeniería - UC Página 4
Cátedra de Termodinámica General
Proceso 1-2: Expansión isotérmica
2
𝛿𝑞 𝑞𝑎
𝑠2 − 𝑠1 = ∫ ( ) = ⇒ 𝑞𝑎 = 𝑇𝑎 (𝑠2 − 𝑠1 )
1 𝑇 𝑖𝑛𝑡 𝑟𝑒𝑣 𝑇𝑎
Proceso 2-3: Expansión adiabática
0
3
𝛿𝑞
𝑠3 − 𝑠2 = ∫ ( ) ⇒ 𝑠2 = 𝑠3
2 𝑇 𝑖𝑛𝑡 𝑟𝑒𝑣
Proceso adiabático reversible Isentrópico
Proceso 3-4: Compresión isotérmica
4
𝛿𝑞 𝑞𝑏
𝑠4 − 𝑠3 = ∫ ( ) = ⇒ 𝑞𝑏 = 𝑇𝑏 (𝑠4 − 𝑠3 )
3 𝑇 𝑖𝑛𝑡 𝑟𝑒𝑣 𝑇𝑏
Proceso 4-1: Compresión adiabática
0
1
𝛿𝑞
𝑠1 − 𝑠4 = ∫ ( ) ⇒ 𝑠1 = 𝑠4
4 𝑇 𝑖𝑛𝑡 𝑟𝑒𝑣
Demostración: Eficiencia de una máquina térmica de Carnot
𝑄𝑏 𝑞𝑏
=1− =1−
𝑄𝑎 𝑞𝑎
𝑇𝑏 (𝑠3 − 𝑠4 )
𝑟𝑒𝑣𝑒𝑟𝑠𝑖𝑏𝑙𝑒 = 1 − , 𝑠𝑖𝑒𝑛𝑑𝑜: 𝑠2 − 𝑠1 = 𝑠3 − 𝑠4
𝑇𝑎 (𝑠2 − 𝑠1 )
𝑇𝑏
𝑟𝑒𝑣𝑒𝑟𝑠𝑖𝑏𝑙𝑒 = 1 − 𝐿𝑄𝑄𝐷
𝑇𝑎
Relaciones básicas de la termodinámica
- Balance de energía:
Sistema cerrado, sin efectos de ec, ep:
𝛿𝑒𝑒𝑛𝑡𝑟𝑎𝑑𝑎 − 𝛿𝑒𝑠𝑎𝑙𝑖𝑑𝑎 = 𝛿𝑒𝑠𝑖𝑠𝑡𝑒𝑚𝑎 ⇒ 𝛿𝑞𝑖𝑛𝑡 𝑟𝑒𝑣 − 𝛿𝑤𝑖𝑛𝑡 𝑟𝑒𝑣 = 𝑑𝑢
𝛿𝑞𝑖𝑛𝑡 𝑟𝑒𝑣 − 𝑃𝑑𝑣 = 𝑑𝑢 (1)
Prof. Alberto Martínez M. Facultad de Ingeniería - UC Página 5
Cátedra de Termodinámica General
- Definición de entropía:
𝛿𝑞
( ) = 𝑑𝑠 ⇒ 𝛿𝑞𝑖𝑛𝑡 𝑟𝑒𝑣 = 𝑇𝑑𝑠 (2)
𝑇 𝑖𝑛𝑡 𝑟𝑒𝑣
Combinando las ecuaciones (1) y (2):
𝑑𝑢 = 𝑇𝑑𝑠 − 𝑃𝑑𝑣 ⇒ 𝑇𝑑𝑠 = 𝑑𝑢 + 𝑃𝑑𝑣 Primera ecuación Tds o de Gibbs
Por otro lado: ℎ = 𝑢 + 𝑃𝑣 ⇒ 𝑑ℎ = 𝑑𝑢 + 𝑑(𝑃𝑣) = 𝑑𝑢 + 𝑃𝑑𝑣 + 𝑣𝑑𝑃
𝑑𝑢 = 𝑑ℎ − 𝑃𝑑𝑣 − 𝑣𝑑𝑃
Sustituyendo:
𝑇𝑑𝑠 = 𝑑ℎ − 𝑃𝑑𝑣 − 𝑣𝑑𝑃 + 𝑃𝑑𝑣 ⇒ 𝑇𝑑𝑠 = 𝑑ℎ − 𝑣𝑑𝑃 Segunda ecuación Tds
Cambio de entropía de gases ideales
Para un gas ideal se cumple: 𝑃𝑣 = 𝑅𝑇
𝑑𝑢 = 𝑐𝑣 𝑑𝑇 𝑑ℎ = 𝑐𝑃 𝑑𝑇
- Suponiendo calores específicos constantes:
𝑑𝑢 𝑃 𝑐𝑣 𝑑𝑇 𝑅
𝑑𝑠 = + 𝑑𝑣 ⇒ 𝑑𝑠 = + 𝑑𝑣
𝑇 𝑇 𝑇 𝑣
𝑇2 𝑣2
𝑠2 − 𝑠1 = 𝑐𝑣 𝐿𝑛 ( ) + 𝑅𝐿𝑛 ( )
𝑇1 𝑣1
𝑇2 𝑣2
𝑠̅2 − 𝑠̅1 = 𝑐̅𝑣 𝐿𝑛 ( ) + 𝑅𝑢 𝐿𝑛 ( )
𝑇1 𝑣1
𝑑ℎ 𝑣 𝑐𝑃 𝑑𝑇 𝑅
𝑑𝑠 = − 𝑑𝑃 ⇒ 𝑑𝑠 = − 𝑑𝑃
𝑇 𝑇 𝑇 𝑃
𝑇2 𝑃2
𝑠2 − 𝑠1 = 𝑐𝑃 𝐿𝑛 ( ) − 𝑅𝐿𝑛 ( )
𝑇1 𝑃1
𝑇2 𝑃2
𝑠̅2 − 𝑠̅1 = 𝑐̅𝑃 𝐿𝑛 ( ) − 𝑅𝑢 𝐿𝑛 ( )
𝑇1 𝑃1
- Suponiendo calores específicos variables:
2
𝑐𝑃 𝑑𝑇 𝑅 𝑑𝑇 𝑃2
𝑑𝑠 = − 𝑑𝑃 ⇒ 𝑠2 − 𝑠1 = ∫ 𝑐𝑃 (𝑇) − 𝑅𝐿𝑛 ( )
𝑇 𝑃 1 𝑇 𝑃1
Prof. Alberto Martínez M. Facultad de Ingeniería - UC Página 6
Cátedra de Termodinámica General
𝑇 𝑑𝑇
Se definió: 𝑠 𝑜 = ∫0 𝑐𝑃 (𝑇)
𝑇
2
𝑑𝑇
𝑠2𝑜 − 𝑠1𝑜 = ∫ 𝑐𝑃 (𝑇)
1 𝑇
- Los valores de 𝑠1𝑜 y 𝑠2𝑜 solo dependen de las temperaturas T1 y T2, respectivamente.
Se encuentran disponibles en las tablas de gas ideal.
𝑃
La ecuación queda: 𝑠2 − 𝑠1 = 𝑠2𝑜 − 𝑠1𝑜 − 𝑅𝐿𝑛 (𝑃2 )
1
𝑃2
𝑠̅2 − 𝑠̅1 = 𝑠̅2𝑜 − 𝑠̅1𝑜 − 𝑅𝑢 𝐿𝑛 ( )
𝑃1
Procesos isentrópicos de gas ideal
- Suponiendo calores específicos constantes:
0
𝑇2 𝑣2
𝑠2 − 𝑠1 = 𝑐𝑣 𝐿𝑛 ( ) + 𝑅𝐿𝑛 ( )
𝑇1 𝑣1
𝑇2 𝑅 𝑣2 𝑐𝑃
𝐿𝑛 ( ) = − 𝐿𝑛 ( ) ; 𝑠𝑖𝑒𝑛𝑑𝑜: 𝑅 = 𝑐𝑃 − 𝑐𝑣 𝑘=
𝑇1 𝑐𝑣 𝑣1 𝑐𝑣
𝑅
=𝑘−1
𝑐𝑣
𝑇2 𝑣1 𝑅/𝑐𝑣 𝑇2 𝑣1 𝑘−1
𝐿𝑛 ( ) = 𝐿𝑛 ( ) ⇒ ( ) =( )
𝑇1 𝑣2 𝑇1 𝑠=𝑐𝑡𝑒 𝑣2
De manera similar:
𝑇2 𝑃2 (𝑘−1)/𝑘
( ) =( )
𝑇1 𝑠=𝑐𝑡𝑒 𝑃1
𝑃2 𝑣1 𝑘
( ) =( )
𝑃1 𝑠=𝑐𝑡𝑒 𝑣2
En forma compacta: 𝑇𝑣 𝑘−1 = 𝑐𝑡𝑒
𝑇𝑃(1−𝑘)/𝑘 = 𝑐𝑡𝑒
𝑐𝑃
𝑃𝑣 𝑘 = 𝑐𝑡𝑒, 𝑐𝑜𝑛: 𝑘 = (𝑇𝑎𝑏𝑙𝑎 𝐴 − 2)
𝑐𝑉
Válidas para: 1) Gas ideal
2) Procesos isentrópicos
3) Calores específicos constantes
Prof. Alberto Martínez M. Facultad de Ingeniería - UC Página 7
Cátedra de Termodinámica General
- Suponiendo calores específicos variables:
0
𝑃2
𝑠2 − 𝑠1 = 𝑠2𝑜 − 𝑠1𝑜 − 𝑅𝐿𝑛 ( )
𝑃1
𝑃2 𝑠2𝑜 − 𝑠1𝑜 𝑃2 𝑒𝑥𝑝(𝑠2𝑜 /𝑅)
= 𝑒𝑥𝑝 ( ) ⇒ =
𝑃1 𝑅 𝑃1 𝑒𝑥𝑝(𝑠1𝑜 /𝑅)
Se definió: 𝑃𝑟 = 𝑒𝑥𝑝(𝑠 𝑜 /𝑅) ⇒ Presión relativa
𝑃2 𝑃𝑟2
( ) =
𝑃1 𝑠=𝑐𝑡𝑒 𝑃𝑟1
Procedimiento: Proceso isentrópico
Dados: P1, T1 y P2 Determinar: T2
T Pr
. .
. .
. .
se lee 𝑃2
T2 𝑃𝑟2 = 𝑃
𝑃1 𝑟1
T1 se lee 𝑃𝑟1
En caso de trabajar con razones de volúmenes:
𝑃1 𝑣1 𝑃2 𝑣2 𝑣2 𝑇2 𝑃1 𝑇2 𝑃𝑟1
= ⇒ = =
𝑇1 𝑇2 𝑣1 𝑇1 𝑃2 𝑇1 𝑃𝑟2
𝑇
Se definió: 𝑣𝑟 = 𝑃 ⇒ Volumen específico relativo
𝑟
𝑣2 𝑣𝑟2
( ) =
𝑣1 𝑠=𝑐𝑡𝑒 𝑣𝑟1
Prof. Alberto Martínez M. Facultad de Ingeniería - UC Página 8
Cátedra de Termodinámica General
Procedimiento: Proceso isentrópico
Dados: v1, T1 y v2 Determinar: T2
T vr
. .
. .
. .
se lee 𝑣
T2 𝑣𝑟2 = 𝑣2 𝑣𝑟1
1
se lee
T1 𝑣𝑟1
Prof. Alberto Martínez M. Facultad de Ingeniería - UC Página 9
También podría gustarte
- Ingeniería química. Soluciones a los problemas del tomo IDe EverandIngeniería química. Soluciones a los problemas del tomo IAún no hay calificaciones
- Termo Tema 5 - Clase 19Documento7 páginasTermo Tema 5 - Clase 19Carolina CastroAún no hay calificaciones
- Ayudantía 10 (Con Solucionario)Documento6 páginasAyudantía 10 (Con Solucionario)Salomon SotoAún no hay calificaciones
- Propiedades de Los LiquidosDocumento2 páginasPropiedades de Los LiquidosFrancisco MendozaAún no hay calificaciones
- Primera LeyDocumento44 páginasPrimera Leyjuan retamalAún no hay calificaciones
- Termodinámica 3 PDFDocumento9 páginasTermodinámica 3 PDFMarcosToreroSoraluzAún no hay calificaciones
- Certamen 1 ResueltoDocumento3 páginasCertamen 1 ResueltoLuciaRiquelmeMartínezAún no hay calificaciones
- Guia-Extra QUIM300 202-1Documento4 páginasGuia-Extra QUIM300 202-1catalinaalejandra18Aún no hay calificaciones
- Resumen de ResultadosDocumento12 páginasResumen de ResultadosArturo Hernandez de la CruzAún no hay calificaciones
- Resolucion de Ejercicios QuimicaDocumento29 páginasResolucion de Ejercicios QuimicaYessica Yocelin Cari MoralesAún no hay calificaciones
- Formulario de Termodinámica-1-1Documento2 páginasFormulario de Termodinámica-1-1CristhianMauricioAguilarAún no hay calificaciones
- Semana1 PPT Q2Documento18 páginasSemana1 PPT Q2DEDI CHANCA BALVINAún no hay calificaciones
- Unidad 7 Teorico QuiimicaDocumento29 páginasUnidad 7 Teorico QuiimicaYessica Yocelin Cari MoralesAún no hay calificaciones
- Entalpía de VaporizaciónDocumento3 páginasEntalpía de VaporizaciónSebastian ArangoAún no hay calificaciones
- T1 Psicrometria ComplementosDocumento8 páginasT1 Psicrometria ComplementosLucasAún no hay calificaciones
- Entalpia de CombustionDocumento14 páginasEntalpia de CombustionWilliam Anderson Muñoz OcampoAún no hay calificaciones
- Problemas Segunda Ley de Termodinámica y EntropíaDocumento6 páginasProblemas Segunda Ley de Termodinámica y EntropíaMontse ZárateAún no hay calificaciones
- Termodinámica-Parte 2Documento17 páginasTermodinámica-Parte 2Denilson Chuquipoma SantosAún no hay calificaciones
- Formulario de Termodinámica-1Documento2 páginasFormulario de Termodinámica-1Osvaldo VascoAún no hay calificaciones
- Secme 16183Documento62 páginasSecme 16183Anonymous 8PpE59CICAún no hay calificaciones
- Equivalente Electrico RevisarDocumento2 páginasEquivalente Electrico RevisarGuillermo LarreaAún no hay calificaciones
- Practica 2Documento5 páginasPractica 2Mauricio SaMoAún no hay calificaciones
- Semana 09 - Termodinámica - TeoriaDocumento17 páginasSemana 09 - Termodinámica - TeoriaMafer TCAún no hay calificaciones
- Tarea 5 MTDocumento12 páginasTarea 5 MTArturo Hernandez de la CruzAún no hay calificaciones
- Examen Final Albino Ledesma MacDocumento5 páginasExamen Final Albino Ledesma MacJULIO OSCAR QUINCHO ROJASAún no hay calificaciones
- Ex010207 Feb TD SolDocumento8 páginasEx010207 Feb TD Soljeisbel perez0% (1)
- Ejercicios Individuales Jorge ArroyaveDocumento6 páginasEjercicios Individuales Jorge ArroyaveAndres ArroyaveAún no hay calificaciones
- U-3 PROBLEMAS INTERCAMBIADORES CALOR ADocumento69 páginasU-3 PROBLEMAS INTERCAMBIADORES CALOR A20690431 TANIA GUADALUPE SANCHEZ MARTINEZAún no hay calificaciones
- Termodinamica 2Documento3 páginasTermodinamica 2Cesar Garrido MedelAún no hay calificaciones
- Primera LeycDocumento47 páginasPrimera Leycjuan retamalAún no hay calificaciones
- EJERCICIOS 2do y 3er principioTERMODINAMICADocumento23 páginasEJERCICIOS 2do y 3er principioTERMODINAMICAWalter Jhimmy Flores AlcocerAún no hay calificaciones
- Resumen Científico - Semana 09-10-11Documento8 páginasResumen Científico - Semana 09-10-11Andy XiaoAún no hay calificaciones
- Gases Quim Gral UJAP 2020Documento4 páginasGases Quim Gral UJAP 2020Ivan VAún no hay calificaciones
- Practica No 4 Química Aplicada "Termodinamica"Documento12 páginasPractica No 4 Química Aplicada "Termodinamica"Juan Vargas0% (1)
- Práctica 10Documento7 páginasPráctica 10Marco Antonio RodríguezAún no hay calificaciones
- Otc No EstacionarioDocumento22 páginasOtc No EstacionarioAna Maria Estrada CorreaAún no hay calificaciones
- Termodinámica - Tipo A Examen FinalDocumento5 páginasTermodinámica - Tipo A Examen FinalRyuzaki KuroShin クロしんAún no hay calificaciones
- BE 2006 4 Calor LatenteDocumento15 páginasBE 2006 4 Calor LatenteJavier RivmatamAún no hay calificaciones
- Lab 09 - FQ IDocumento10 páginasLab 09 - FQ Ianais zambranoAún no hay calificaciones
- Aporte - IndividualDocumento5 páginasAporte - IndividualMaria Del RosarioAún no hay calificaciones
- UNAD Unidad 2Documento215 páginasUNAD Unidad 2Brayan SarmientoAún no hay calificaciones
- Oficial Informe 4 FisicoquímicaDocumento11 páginasOficial Informe 4 FisicoquímicaPaola MenendezAún no hay calificaciones
- Unad PDFDocumento215 páginasUnad PDFSamir Eduardo Martinez Sagbini100% (1)
- TermodinamicaDocumento7 páginasTermodinamicaharles mercadoAún no hay calificaciones
- Problema TermodinamicaDocumento5 páginasProblema TermodinamicaCarlos CollinsAún no hay calificaciones
- Boletín 1-Resueltos-IETC-16 - 17-V1Documento14 páginasBoletín 1-Resueltos-IETC-16 - 17-V1Yassin BehdaouiAún no hay calificaciones
- Energia y Calor PDFDocumento11 páginasEnergia y Calor PDFNick AmayaAún no hay calificaciones
- Laboratorio #6 Primera Ley de La TermodinamicaDocumento25 páginasLaboratorio #6 Primera Ley de La TermodinamicaAlejandra Guerrero100% (1)
- PistonDocumento6 páginasPistonCristian SánchezAún no hay calificaciones
- Semana 11 - Termodinamica - Transfrencia de Energía - PDFDocumento24 páginasSemana 11 - Termodinamica - Transfrencia de Energía - PDFmiloxe7428Aún no hay calificaciones
- Practica de Balance de Materia y Energia N 2Documento18 páginasPractica de Balance de Materia y Energia N 2Cami ApazaAún no hay calificaciones
- EJERCICIOSDocumento22 páginasEJERCICIOSYORDI ALDAIR LAVADO FLORESAún no hay calificaciones
- Termodinámica PDFDocumento24 páginasTermodinámica PDFMarcosToreroSoraluzAún no hay calificaciones
- Informe TermodinamicaDocumento4 páginasInforme TermodinamicaAaron AcuñaAún no hay calificaciones
- TEO-2020 - TermodinamicaDocumento14 páginasTEO-2020 - TermodinamicaJOSE LUIS QUISPE GARAYAún no hay calificaciones
- Problemas - LAB 6docxDocumento10 páginasProblemas - LAB 6docxJerry ValdezAún no hay calificaciones
- 418836517-EF-TERMODINAMICA UpnDocumento14 páginas418836517-EF-TERMODINAMICA UpnMelyna Vega100% (3)
- Quillupangui Belen NRC 1922Documento4 páginasQuillupangui Belen NRC 1922Belen QuillupanguiAún no hay calificaciones
- Poryecto ColaborativoDocumento2 páginasPoryecto ColaborativoCarolina CastroAún no hay calificaciones
- PROYECTO DE ADMINISTRACION Y GESTION PDF-convertido-convertido-comprimido-páginas-eliminadasDocumento61 páginasPROYECTO DE ADMINISTRACION Y GESTION PDF-convertido-convertido-comprimido-páginas-eliminadasCarolina CastroAún no hay calificaciones
- UNIDAD - 7 - Nomenclatura AduaneraDocumento8 páginasUNIDAD - 7 - Nomenclatura AduaneraCarolina CastroAún no hay calificaciones
- Ética y Deontología ProfesionalesDocumento2 páginasÉtica y Deontología ProfesionalesCarolina CastroAún no hay calificaciones
- La Deontologia La Etica y La MoralDocumento3 páginasLa Deontologia La Etica y La MoralCarolina CastroAún no hay calificaciones
- Análisis Del Funcionamiento Del Circuito EconómicoDocumento6 páginasAnálisis Del Funcionamiento Del Circuito EconómicoCarolina Castro100% (1)
- Tid Monografia Capitulo 1Documento10 páginasTid Monografia Capitulo 1Carolina CastroAún no hay calificaciones
- Termo Tema 5Documento7 páginasTermo Tema 5Carolina CastroAún no hay calificaciones
- Tablas 1Documento3 páginasTablas 1Carolina CastroAún no hay calificaciones
- Clase 2, Tema IDocumento6 páginasClase 2, Tema ICarolina CastroAún no hay calificaciones
- Impactos de La RsuDocumento3 páginasImpactos de La RsuCarolina CastroAún no hay calificaciones
- Practica 2 Valoracion Aduanera Corte 2Documento2 páginasPractica 2 Valoracion Aduanera Corte 2Carolina CastroAún no hay calificaciones
- Incoterms 2020Documento6 páginasIncoterms 2020Carolina CastroAún no hay calificaciones
- Caracteristicas de Los Proyectos de Intervencion SocialDocumento6 páginasCaracteristicas de Los Proyectos de Intervencion SocialCarolina Castro100% (1)
- Unidad 2Documento3 páginasUnidad 2Carolina CastroAún no hay calificaciones
- Fisica OkDocumento15 páginasFisica Okkatherine villanuevaAún no hay calificaciones
- T6 Termodinamica EjerciciosDocumento4 páginasT6 Termodinamica Ejerciciosleandro cardarelliAún no hay calificaciones
- Guia 2 Optativo LLLDocumento10 páginasGuia 2 Optativo LLLCesar MejiaAún no hay calificaciones
- CALCULOS TermoquimicaDocumento4 páginasCALCULOS TermoquimicaDenisAún no hay calificaciones
- Cataluña 1999Documento2 páginasCataluña 1999Marta CabaAún no hay calificaciones
- Comparativo de Presiones de Alto VacíoDocumento1 páginaComparativo de Presiones de Alto VacíoPablo TovarAún no hay calificaciones
- Taller 4Documento10 páginasTaller 4Giancarlo ColcaAún no hay calificaciones
- Escalas TermicasDocumento8 páginasEscalas TermicasFlorencia GarciaAún no hay calificaciones
- 10 CalorimetríaDocumento18 páginas10 CalorimetríaJorge Enrique MolloAún no hay calificaciones
- Dependencia de G Con La TemperaturaDocumento9 páginasDependencia de G Con La TemperaturaAlexandra MarleneAún no hay calificaciones
- Fisica Avanzada AlvarezDocumento138 páginasFisica Avanzada AlvarezMilton Paredes Avalos100% (1)
- Laboratorio de Física Calor Ondas: Andrea Angulo Código: 200030232 Email: Cangulo@uninorte - Edu.coDocumento14 páginasLaboratorio de Física Calor Ondas: Andrea Angulo Código: 200030232 Email: Cangulo@uninorte - Edu.cocristian seguraAún no hay calificaciones
- Problemas Resueltos de Transferencia de CalorDocumento13 páginasProblemas Resueltos de Transferencia de CalorMetzly Maldonado0% (1)
- 3º Bloque Calor y TemperaturaDocumento15 páginas3º Bloque Calor y TemperaturaAnto GiardinaAún no hay calificaciones
- Informe #2 de FisicoquimciaDocumento4 páginasInforme #2 de FisicoquimciaEvelyn TapiaAún no hay calificaciones
- Ejercicio de Procesos Termodinamicos CompressDocumento4 páginasEjercicio de Procesos Termodinamicos CompressHijo De la nocheAún no hay calificaciones
- Informe lm35Documento11 páginasInforme lm35SantiagoLozadaAún no hay calificaciones
- Termometro de Gas A Volumen ConstanteDocumento2 páginasTermometro de Gas A Volumen ConstanteDidier Ortiz InocencioAún no hay calificaciones
- Calor Especifico de Un Solido-InformeDocumento7 páginasCalor Especifico de Un Solido-Informebreiner mejiaAún no hay calificaciones
- Balance Energetico Calculos Segun ISO 13790Documento16 páginasBalance Energetico Calculos Segun ISO 13790Jose Rayan100% (1)
- Problemas Terperatura Resuelto IIDocumento12 páginasProblemas Terperatura Resuelto IIbismar100% (1)
- Ejercicios de Dilatación de Líquidos 201902Documento2 páginasEjercicios de Dilatación de Líquidos 201902Carlos Daniel Vanegas MarchenaAún no hay calificaciones
- RESUELTO Ejercicio Extra 2 TermoDocumento4 páginasRESUELTO Ejercicio Extra 2 Termoleonel lopezAún no hay calificaciones
- Aire Acondicionada ManualDocumento4 páginasAire Acondicionada ManualDave LpzAún no hay calificaciones
- MEDIDAS DE TEMPERATURA PresentacionDocumento30 páginasMEDIDAS DE TEMPERATURA PresentacionAlvaro De La Rosa TapiaAún no hay calificaciones
- Examen Final - Semana 8 - CB - SEGUNDO BLOQUE-FUNDAMENTOS DE QUIMICA - (GRUPO1)Documento6 páginasExamen Final - Semana 8 - CB - SEGUNDO BLOQUE-FUNDAMENTOS DE QUIMICA - (GRUPO1)eliana medinaAún no hay calificaciones
- Calorimetria - Transferencia de Calor - TermometriaDocumento42 páginasCalorimetria - Transferencia de Calor - TermometriaYaricsa Varas HornaAún no hay calificaciones
- Calorimetría PPTDocumento24 páginasCalorimetría PPTFreddy Vilca100% (1)
- Cuestionario Equilibrio TermicoDocumento4 páginasCuestionario Equilibrio TermicoAndrés ValenciaAún no hay calificaciones
- Actividad5 FísicaDocumento12 páginasActividad5 FísicaAlfredo CoronadoAún no hay calificaciones