Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Configuración Electrónica
Cargado por
Luz Nelly Maya Ortiz0 calificaciones0% encontró este documento útil (0 votos)
24 vistas2 páginasDerechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
24 vistas2 páginasConfiguración Electrónica
Cargado por
Luz Nelly Maya OrtizCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 2
CONFIGURACIÓN ELECTRÓNICA
La configuración electrónica de un átomo muestra cómo se distribuyen sus electrones en los
orbitales en su estado fundamental, es decir, cuando se encuentra en el nivel de energía más
bajo. Esta distribución permite explicar, por ejemplo, las propiedades de los elementos, su
ubicación en la tabla periódica, la formación de enlaces, entre otras características.
El principio de mínima energía o de Aufbau
Indica que los electrones deben ocupar los orbitales en orden
creciente de energía, ya que, el estado de mínima energía es el
más estable, y los niveles de mayor energía solo deben ser
ocupados cuando la cantidad máxima de orbitales de mayor
energía ha sido completada. Para cumplir con este principio se
debe utilizar la regla de las diagonales, las cuales indican el
orden creciente de los subniveles de energía.
¿Cómo se representa la configuración electrónica de un elemento?
Para poder realizar la configuración electrónica de un elemento, se debe tener en consideración,
lo siguiente:
En primer lugar, se debe tener en consideración la cantidad de electrones que presenta la
especie. Para ello, hay que fijarse en su número atómico (Z). Si corresponde a un catión
(átomo con carga positiva), significa que perdió electrones, si se trabaja con un anión (átomo
con carga negativa), significa que ganó electrones.
Se debe seguir la regla de las diagonales en el diagrama de Aufbau hasta completar el número
de electrones del átomo a representar
Ejemplo 1: El sodio (Na) con Z = 11
Na: 1s2 2s2 2p6 3s1
Al sumar todos los exponentes, el total será el número atómico, en este caso Z =
11.
Ejemplo 2: Utilizando el diagrama de la Figura 1: Diagrama de Aufbau, realice la distribución
electrónica del bromo con Z = 35
Br: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5
Al sumar todos los exponentes, el total será el número atómico, en este caso Z=35
Ejemplo 3: Utilizando el diagrama de la Figura 1: Diagrama de Aufbau, la distribución
electrónica del anión F-1,
El Flúor tiene número atómico Z=9, como nos dicen que es un anión F -1 significa
que el Flúor gano 1 electrón por lo tanto queda con 10 electrones, la configuración
electrónica es entonces
Para el Flúor, F: 1s2 2s2 2p5, Pero para el anión F-1 queda así: 1s2 2s2 2p6
Ejemplo 4: Utilizando el diagrama de la Figura 1: Diagrama de Aufbau, la distribución
electrónica del Catión Al+2,
El Aluminio tiene número atómico Z=13, como nos dicen que es un catión Al +2
significa que el Aluminio perdió 2 electrones por lo tanto queda con 11 electrones, la
configuración electrónica es entonces
Para el Aluminio, Al: 1s2 2s2 2p6 3s2 3p1, Pero para el catión Al+2 queda así: 1s2 2s2
2p6 3s1
ACTIVIDAD
1. Escribe la configuración electrónica de los siguientes elementos
a) Nitrógeno ( Z=7)
b) Silicio ( Z=14)
c) Cloro ( Z=17)
d) Plata ( Z=47)
2. Escribe la configuración electrónica de los siguientes iones:
a) N+2
b) Cl -3
c) Ag+1
d) Si -1
3. Dadas las siguientes configuraciones electrónicas de átomos neutros:
X: 1s2 2s2 2p6 3s2 3p6
Y: 1s2 2s2 2p6 3s2 3p6 4s1
a) ¿Cuál será la configuración electrónica del ión X+2?
b) ¿Cuál será la configuración electrónica del ión Y-2?
También podría gustarte
- Hoja de Trabajo Configuracion Electronica BorradorDocumento4 páginasHoja de Trabajo Configuracion Electronica BorradorDELMY NOEMY ROSALES FUENTESAún no hay calificaciones
- Experiencias sobre circuitos eléctricos en serie operados por corriente directaDe EverandExperiencias sobre circuitos eléctricos en serie operados por corriente directaAún no hay calificaciones
- Configuración O Distribución ElectrónicaDocumento7 páginasConfiguración O Distribución ElectrónicasantiagoariaseduardomeraAún no hay calificaciones
- Electron DiferencialDocumento11 páginasElectron DiferencialJavi Quiñonez50% (2)
- CONFIGURACIÓN ELECTRÓNICA (Separata)Documento6 páginasCONFIGURACIÓN ELECTRÓNICA (Separata)Ana Nomberto LuperdiAún no hay calificaciones
- BII-Sesión de Aprendizaje 03Documento6 páginasBII-Sesión de Aprendizaje 03Adiel Sebastian Panduro EspinozaAún no hay calificaciones
- Ej. Selectividad Resueltos T1 y T2Documento4 páginasEj. Selectividad Resueltos T1 y T2emmaperaltaAún no hay calificaciones
- Semana 3 - Configuracion ElectronicaDocumento39 páginasSemana 3 - Configuracion ElectronicaCARMEN ROSA YARLEQUE MEJIAAún no hay calificaciones
- Taller 2 MaterialesDocumento7 páginasTaller 2 MaterialesJhelena MartinezAún no hay calificaciones
- Exercicis Tema 1 (Amb Tota La Solució)Documento4 páginasExercicis Tema 1 (Amb Tota La Solució)Isla Jane Maria O HalloranAún no hay calificaciones
- 1.1 - Átomo y TPDocumento14 páginas1.1 - Átomo y TPYeferson Anchari HuancaAún no hay calificaciones
- Configuración ElectrónicaDocumento8 páginasConfiguración ElectrónicaMariana VasquezAún no hay calificaciones
- Apuntes Configuracion ElectronicaDocumento6 páginasApuntes Configuracion ElectronicaAngy NGAún no hay calificaciones
- Quimica - Guia de Ejercicios ConfiguracinDocumento6 páginasQuimica - Guia de Ejercicios ConfiguracinAngela Simpson0% (1)
- Sbmb010322-Qu-t02-Estudio Del Átomo (Átomo Actual)Documento25 páginasSbmb010322-Qu-t02-Estudio Del Átomo (Átomo Actual)Jorge GuarnízAún no hay calificaciones
- Regla de La LluviaDocumento5 páginasRegla de La Lluviapanky199650% (2)
- Valores de Los Números CuánticosDocumento8 páginasValores de Los Números CuánticosHeriberto I. FdezAún no hay calificaciones
- Configuracion Electronica 2018Documento3 páginasConfiguracion Electronica 2018Diego Ignacio Parra Zenteno100% (1)
- Ficha 1 Periferia - AtomicaDocumento5 páginasFicha 1 Periferia - Atomicalevs508Aún no hay calificaciones
- Enlace Químico-RepuestasDocumento30 páginasEnlace Químico-RepuestasCelso Aguirre Quinde100% (1)
- GUÍA °N 10 Qca7d Niveles de EnergíaDocumento5 páginasGUÍA °N 10 Qca7d Niveles de EnergíaAngie Xiomara Tejada MolanoAún no hay calificaciones
- Ejercicios de Números Cuánticos Resueltos 2023-20Documento5 páginasEjercicios de Números Cuánticos Resueltos 2023-20Mayumi FigueroaAún no hay calificaciones
- Periferia AtomicaDocumento5 páginasPeriferia Atomicalevs508Aún no hay calificaciones
- Practica 4. Numeros CuanticosDocumento10 páginasPractica 4. Numeros Cuanticosdavid cruzAún no hay calificaciones
- U0 FNSL 3 Eso 0Documento7 páginasU0 FNSL 3 Eso 0FABIAN CORREA CORREAAún no hay calificaciones
- Configuracion Electronica de Un AtomoDocumento9 páginasConfiguracion Electronica de Un AtomoNathi BonilloAún no hay calificaciones
- Configuracion ElectrónicaDocumento6 páginasConfiguracion ElectrónicaAixa BrusaAún no hay calificaciones
- QuímicaDocumento43 páginasQuímicaTorres Atencio AlonsoAún no hay calificaciones
- Configuración ElectrónicaDocumento4 páginasConfiguración Electrónicaangela moyaAún no hay calificaciones
- Configuración ElectrónicaDocumento13 páginasConfiguración ElectrónicaFelipe Alejandro JaraAún no hay calificaciones
- Configuración Electrónica-EjerciciosDocumento6 páginasConfiguración Electrónica-EjerciciosnikonovoaAún no hay calificaciones
- Tabla Periódica - Propiedades PeriódicasDocumento28 páginasTabla Periódica - Propiedades PeriódicasCRISTIAN MARTINEZ OREAún no hay calificaciones
- Guia #6 Forma de Orbitales AtómicosDocumento4 páginasGuia #6 Forma de Orbitales Atómicosjhon francoAún no hay calificaciones
- EXPERIMENTO No 9Documento8 páginasEXPERIMENTO No 9Lia ZamoraAún no hay calificaciones
- Configuracion ElectronicaDocumento14 páginasConfiguracion ElectronicaJenny Castro JaraAún no hay calificaciones
- Los Elementos Químicos y La Tabla PeriódicaDocumento12 páginasLos Elementos Químicos y La Tabla PeriódicaLaura Gemma Rodríguez PastorAún no hay calificaciones
- Configuración ElectrónicaDocumento28 páginasConfiguración ElectrónicaEliezer Xivir88% (8)
- CONFIGURACION ELECTRONICA No 3Documento4 páginasCONFIGURACION ELECTRONICA No 3ANDREA MILENA PRADA YARAAún no hay calificaciones
- Ejercicios de Configuracion Electronica 2023-20Documento4 páginasEjercicios de Configuracion Electronica 2023-20Mayumi FigueroaAún no hay calificaciones
- Ejemplos Notacion EspectralDocumento1 páginaEjemplos Notacion EspectralRomina60% (5)
- Configuracion ElectronicaDocumento9 páginasConfiguracion ElectronicaNewciberAún no hay calificaciones
- CG-Sem2-Ejercicios - Números CuánticosDocumento3 páginasCG-Sem2-Ejercicios - Números Cuánticosyordan reyna100% (1)
- 3Documento14 páginas3Ing. Dante Omar Panta CarranzaAún no hay calificaciones
- Tema 2 Capítulo 4. Ejercicios Resueltos de Numeros Cuanticos y Configuración Electrónica PDFDocumento4 páginasTema 2 Capítulo 4. Ejercicios Resueltos de Numeros Cuanticos y Configuración Electrónica PDFRuben Espasa ServersAún no hay calificaciones
- EJERCICIOS Res #CUÁNTICOSDocumento4 páginasEJERCICIOS Res #CUÁNTICOSLiliana Amp33% (3)
- Guia Configuracion Electronica Grado 904 905Documento11 páginasGuia Configuracion Electronica Grado 904 905Andrea ChavezAún no hay calificaciones
- Configuracion Electronica RVDocumento8 páginasConfiguracion Electronica RVAmauri BautistaAún no hay calificaciones
- Temas 3 y 4 Quimica IntensivaDocumento55 páginasTemas 3 y 4 Quimica IntensivaLuis ContrerasAún no hay calificaciones
- Números CuánticosDocumento1 páginaNúmeros Cuánticossilviacr054Aún no hay calificaciones
- Semana 3 - Configuracion ElectronicaDocumento39 páginasSemana 3 - Configuracion ElectronicaCYNTHIA MILAGROS BACA ALVAREZAún no hay calificaciones
- Clase 26 de NovDocumento24 páginasClase 26 de NovBradon Becerril MateoAún no hay calificaciones
- Configuracion ElectronicaDocumento28 páginasConfiguracion ElectronicaAnonymous cWKbRCtUQIAún no hay calificaciones
- 2014 Solucionario Clase 3 Teoría Atómica IIDocumento13 páginas2014 Solucionario Clase 3 Teoría Atómica IIIgnacio ZuñigaAún no hay calificaciones
- Configuración ElectrónicaDocumento8 páginasConfiguración ElectrónicaAndrés AndrésAún no hay calificaciones
- Configuración ElectrónicaDocumento7 páginasConfiguración ElectrónicaEnmanuel CruzAún no hay calificaciones
- Ficha 1. El Átomo Ejercicios ResueltosDocumento4 páginasFicha 1. El Átomo Ejercicios ResueltosLía Noya MahíaAún no hay calificaciones
- Configuraciones Electrc3b3nicas ResueltoDocumento3 páginasConfiguraciones Electrc3b3nicas ResueltoJade Banesa Velasquez BenavidezAún no hay calificaciones
- Propiedades PeriódicasDocumento2 páginasPropiedades PeriódicasLuz Nelly Maya OrtizAún no hay calificaciones
- Funciones InorgánicasDocumento3 páginasFunciones InorgánicasLuz Nelly Maya OrtizAún no hay calificaciones
- Enlace Ionico, Covalente y Metalico - ActividadesDocumento4 páginasEnlace Ionico, Covalente y Metalico - ActividadesLuz Nelly Maya OrtizAún no hay calificaciones
- Propiedades Del AtomoDocumento4 páginasPropiedades Del AtomoLuz Nelly Maya OrtizAún no hay calificaciones
- Cómo Determinar El Grupo y El Periodo de Un ElementoDocumento2 páginasCómo Determinar El Grupo y El Periodo de Un ElementoLuz Nelly Maya OrtizAún no hay calificaciones
- 1 Configuracion Electrónica y Tabla PeriodicaDocumento19 páginas1 Configuracion Electrónica y Tabla PeriodicaLuz Nelly Maya OrtizAún no hay calificaciones
- Anexo No 2 Modelos AtómicosDocumento4 páginasAnexo No 2 Modelos AtómicosLuz Nelly Maya OrtizAún no hay calificaciones
- Enlace Entre AtomosDocumento1 páginaEnlace Entre AtomosLuz Nelly Maya OrtizAún no hay calificaciones
- Guias Quimica 10Documento12 páginasGuias Quimica 10Luz Nelly Maya OrtizAún no hay calificaciones
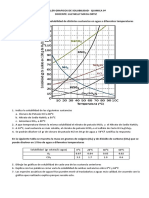
- Taller Graficos de SolubilidadDocumento1 páginaTaller Graficos de SolubilidadLuz Nelly Maya OrtizAún no hay calificaciones
- Examen U1 Sdlle 2021 83v Final BDocumento1 páginaExamen U1 Sdlle 2021 83v Final BEduardo TorresAún no hay calificaciones
- Sesion11 Corriente AlternaDocumento41 páginasSesion11 Corriente AlternaDiego MasiasAún no hay calificaciones
- Categorías OntológicasDocumento118 páginasCategorías Ontológicaswilbert_tapia_1Aún no hay calificaciones
- Lista 2 MeDocumento2 páginasLista 2 MejesusAún no hay calificaciones
- Capa Límite, Viento, AOA, Ángulo de Incidencia, PerfilDocumento99 páginasCapa Límite, Viento, AOA, Ángulo de Incidencia, PerfilJose TejedaAún no hay calificaciones
- Enfoques de La InvestigaciónDocumento36 páginasEnfoques de La InvestigaciónNardis RodriguezAún no hay calificaciones
- Blanco-Peck, Richard - Los Enfoques Metodológicos y La Administración Pública ModernaDocumento10 páginasBlanco-Peck, Richard - Los Enfoques Metodológicos y La Administración Pública ModernaL Felipe AlarcónAún no hay calificaciones
- Trabajo de InvestigacionDocumento24 páginasTrabajo de InvestigacionBrayan David Estavez IbarraAún no hay calificaciones
- Curvas y Superficies ParametricasDocumento225 páginasCurvas y Superficies ParametricasErica antonella FredericksenAún no hay calificaciones
- Análisis Del Pib de EE - UU A Través Del Modelo KeynesianoDocumento39 páginasAnálisis Del Pib de EE - UU A Través Del Modelo Keynesianosofia avendañoAún no hay calificaciones
- GPM y HHVDocumento5 páginasGPM y HHVLuis SegarraAún no hay calificaciones
- Introducción A La Agrimensura Tarea 7Documento5 páginasIntroducción A La Agrimensura Tarea 7Ramón Leandro Ozoria De la CruzAún no hay calificaciones
- Clases de Palabras PDFDocumento14 páginasClases de Palabras PDFN D YAún no hay calificaciones
- Estudistica Financiera Ejercicio 17, 19, 21, 25, 29Documento3 páginasEstudistica Financiera Ejercicio 17, 19, 21, 25, 29Ariel AmadorAún no hay calificaciones
- Cajas de Cambios 1Documento5 páginasCajas de Cambios 1Leidy Stefany100% (1)
- (Informe) Metamorfismo Hidrotermal - KilopascalesDocumento14 páginas(Informe) Metamorfismo Hidrotermal - KilopascalesJAMBER SCOTT LUQUE RIVERAAún no hay calificaciones
- Actividad 6 - Protocolo RIPv2Documento1 páginaActividad 6 - Protocolo RIPv2wilAún no hay calificaciones
- Guia Fisica II 265137 Downloable 2325798Documento54 páginasGuia Fisica II 265137 Downloable 2325798angelosolorzano3927Aún no hay calificaciones
- Potenciación de Números Naturales para Quinto de PrimariaDocumento3 páginasPotenciación de Números Naturales para Quinto de PrimariaROJAS CASTILLO AIDE CLARAAún no hay calificaciones
- Analisis RCM Planta Oleofinas - FMEA PDFDocumento1 páginaAnalisis RCM Planta Oleofinas - FMEA PDFjose angel PinzonAún no hay calificaciones
- Bitacora AutocadDocumento4 páginasBitacora AutocadOscar Cervera TimanáAún no hay calificaciones
- Generaciones de Las ComputadorasDocumento6 páginasGeneraciones de Las ComputadorasRicardo LlanoAún no hay calificaciones
- Complicaciones BacterianasDocumento4 páginasComplicaciones BacterianasAlejandro RipepiAún no hay calificaciones
- 1 Logica ProposicionalDocumento13 páginas1 Logica ProposicionalRodrigo David Ulo CondoriAún no hay calificaciones
- Manual de Matlab Metodos NumericosDocumento119 páginasManual de Matlab Metodos NumericosJuan Carlos S Q100% (1)
- Teorema de Pitagoras y Euclides - Paulo Mu Oz LozanoDocumento9 páginasTeorema de Pitagoras y Euclides - Paulo Mu Oz LozanoPaulo Muñoz LozanoAún no hay calificaciones
- Elasticidad INFORMEDocumento10 páginasElasticidad INFORMEjpintor-1Aún no hay calificaciones
- 9 Causas de Porque Se Congela Un Aire AcondicionadoDocumento3 páginas9 Causas de Porque Se Congela Un Aire AcondicionadorafaelAún no hay calificaciones
- Cuestionario de La UnidadDocumento4 páginasCuestionario de La UnidadJaqueline MorenoAún no hay calificaciones
- Sensor Virtual Fundamentos PDFDocumento7 páginasSensor Virtual Fundamentos PDFSebas de la TorreAún no hay calificaciones
- Anatomía & 100 estiramientos Esenciales (Color): Técnicas, beneficios, precauciones, consejos, tablas de series, dolenciasDe EverandAnatomía & 100 estiramientos Esenciales (Color): Técnicas, beneficios, precauciones, consejos, tablas de series, dolenciasCalificación: 4.5 de 5 estrellas4.5/5 (21)
- Trucos para Leer la Mente de los Demás: Cómo Adivinar el Pensamiento de los Demás con Poco Esfuerzo. 2 Libros en 1 - Secretos de la Psicología Oscura, Cómo ser un Detector de MentirasDe EverandTrucos para Leer la Mente de los Demás: Cómo Adivinar el Pensamiento de los Demás con Poco Esfuerzo. 2 Libros en 1 - Secretos de la Psicología Oscura, Cómo ser un Detector de MentirasCalificación: 4.5 de 5 estrellas4.5/5 (3)
- La metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceDe EverandLa metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceCalificación: 5 de 5 estrellas5/5 (8)
- Reconstrucción de dientes endodonciados: Pautas de actuación clínicaDe EverandReconstrucción de dientes endodonciados: Pautas de actuación clínicaCalificación: 5 de 5 estrellas5/5 (4)
- Disciplina Mental: Técnicas infalibles para lograr todo lo que te propones y eliminar la pereza y la procrastinación de tu vida para siempreDe EverandDisciplina Mental: Técnicas infalibles para lograr todo lo que te propones y eliminar la pereza y la procrastinación de tu vida para siempreCalificación: 5 de 5 estrellas5/5 (3)
- Zensorialmente : Dejá que tu cuerpo sea tu cerebroDe EverandZensorialmente : Dejá que tu cuerpo sea tu cerebroAún no hay calificaciones
- La revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaDe EverandLa revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaCalificación: 5 de 5 estrellas5/5 (201)
- Batidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoDe EverandBatidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoCalificación: 5 de 5 estrellas5/5 (2)
- La vibración de las ondas cerebrales: Recuperar el ritmo de una vida saludable y felizDe EverandLa vibración de las ondas cerebrales: Recuperar el ritmo de una vida saludable y felizCalificación: 5 de 5 estrellas5/5 (7)
- Interpretación del ECG: Una Guía Práctica e Intuitiva para Aprender a Leer el ECG y Diagnosticar y Tratar ArritmiasDe EverandInterpretación del ECG: Una Guía Práctica e Intuitiva para Aprender a Leer el ECG y Diagnosticar y Tratar ArritmiasAún no hay calificaciones
- El concepto Mulligan de terapia manual (Color)De EverandEl concepto Mulligan de terapia manual (Color)Calificación: 5 de 5 estrellas5/5 (3)
- Neurocuántica: La nueva frontera de la neurocienciaDe EverandNeurocuántica: La nueva frontera de la neurocienciaCalificación: 5 de 5 estrellas5/5 (1)
- Proyectos Arduino con Tinkercad: Diseño y programación de proyectos electrónicos basados en Arduino con TinkercadDe EverandProyectos Arduino con Tinkercad: Diseño y programación de proyectos electrónicos basados en Arduino con TinkercadCalificación: 5 de 5 estrellas5/5 (1)
- Neurociencia para vencer la depresión: La esprial ascendenteDe EverandNeurociencia para vencer la depresión: La esprial ascendenteCalificación: 4.5 de 5 estrellas4.5/5 (10)
- Alimentación antiinflamatoria: Primeros pasos para poner en práctica una alimentación saludableDe EverandAlimentación antiinflamatoria: Primeros pasos para poner en práctica una alimentación saludableCalificación: 4.5 de 5 estrellas4.5/5 (119)
- Cardiología y enfermedades cardiovascularesDe EverandCardiología y enfermedades cardiovascularesCalificación: 5 de 5 estrellas5/5 (1)
- El péndulo de sanación: Péndulo hebreo. Investigación y sistematización de la técnicaDe EverandEl péndulo de sanación: Péndulo hebreo. Investigación y sistematización de la técnicaCalificación: 4.5 de 5 estrellas4.5/5 (27)
- Guía de cálculo y diseño de conductos para ventilación y climatizaciónDe EverandGuía de cálculo y diseño de conductos para ventilación y climatizaciónCalificación: 5 de 5 estrellas5/5 (1)
- Neuroanatomía: Fundamentos de neuroanatomía estructural, funcional y clínicaDe EverandNeuroanatomía: Fundamentos de neuroanatomía estructural, funcional y clínicaCalificación: 4 de 5 estrellas4/5 (16)