Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Ruiz Bravo LeyesPonderales
Cargado por
Fatima Paola Ruiz BravoTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Ruiz Bravo LeyesPonderales
Cargado por
Fatima Paola Ruiz BravoCopyright:
Formatos disponibles
Ruiz Bravo Fátima Paola.
Grupo:1253
LEYES PONDERALES
Son leyes que estudian las reacciones químicas en función de las cantidades de materia de
los diferentes elementos que intervienen.
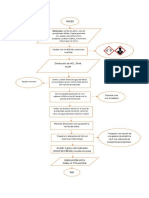
- Ley de Conservación de la Masa (Lavoisier 1789):
Esta ley afirma que en una reacción química la masa permanece constante. Esto
implica que la masa que se consume de los reactivos es la misma que se obtiene de
los productos de la reacción.
“En una reacción química, la materia no se crea ni se destruye, sino que se
transforma permaneciendo constante.”
Ejemplo: cuando un hielo se derrite se convierte en agua con la misma cantidad de
masa que el hielo.
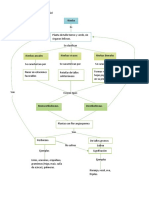
- Ley de Proporciones Constantes o Proporciones definidas (Proust):
Afirma que cuando dos o más elementos se unen para formar un compuesto
determinado, lo hacen siempre en una relación de masa constante, es decir en una
proporción fija o definida.
Ejemplo: el agua siempre se formara debido a dos átomos de hidrógeno y un átomo
de oxígeno. Esa proporción siempre se mantiene.
- Ley de Proporciones Múltiples (Dalton):
Cuando dos o más elementos pueden formar más de un compuesto, las cantidades
de uno de ellos que se combinan con una cantidad fija del otro, guardan entre sí
relación de números enteros sencillos.
Ejemplo: El agua tiene la formula química de H₂O, los índices de cada elemento
siempre serán enteros y sencillos.
- Ley de Proporciones Equivalentes (Richter):
Indica que si dos elementos diferentes, cada uno con un cierto peso, son capaces de
combinarse con un peso dado de un tercer elemento común a ambos, los pesos de
aquellos elementos son capaces de combinarse entre sí, o bien múltiplos o
submúltiplos de dichos pesos.
Ejemplo: si combino azufre con una cantidad de oxígeno y luego hierro con la
misma cantidad de oxígeno, estas masas son proporcionales entre sí.
VIDEO: Uvigo. Leyes ponderales. Estequiometría https://www.youtube.com/watch?
v=or9gijhz-2A
Ruiz Bravo Fátima Paola. Grupo:1253
Referencias:
- Maya GM. Leyes ponderales. Estado de México: UAEMEX Facultad de Química;
2015 [Internet]. [Consultado 23 Feb 2021]. Disponible en:
http://ri.uaemex.mx/handle/20.500.11799/34726
- López NM. Curso de Química General 1. México: UNAM Facultad de Química;
2019 [Internet]. [Consultado 23 Feb 2021]. Disponible en:
http://depa.fquim.unam.mx/amyd/archivero/Unidad5_20191.pdf
- QUIMICAS. Las Leyes Ponderales. Quimicas.net; 2015 [Internet]. [Consultado 23
Feb 2021]. Disponible en: https://www.quimicas.net/2015/09/las-leyes-
ponderales.html
- Químico L. T. P. Ley de las Proporciones Múltiples (Ley de Dalton). TP -
Laboratorio Químico. 2017 [Internet]. [Consultado 23 Feb 2021]. Disponible en:
https://www.tplaboratorioquimico.com/quimica-general/las-propiedades-de-la-
materia/ley-de-dalton-o-ley-de-las-proporciones-multiples.html
También podría gustarte
- PDF Trabajo de Campo 4 Curso Quimica Inorganica CompressDocumento4 páginasPDF Trabajo de Campo 4 Curso Quimica Inorganica CompressAlex AlcantaraAún no hay calificaciones
- Term Odin A MicaDocumento2 páginasTerm Odin A MicaFatima Paola Ruiz BravoAún no hay calificaciones
- Calibración Del CalorímetroDocumento3 páginasCalibración Del CalorímetroFatima Paola Ruiz BravoAún no hay calificaciones
- Anteproyecto TITULACIÓNDocumento21 páginasAnteproyecto TITULACIÓNFatima Paola Ruiz BravoAún no hay calificaciones
- CalorDeDescomposicionde PeroxidoDocumento3 páginasCalorDeDescomposicionde PeroxidoFatima Paola Ruiz BravoAún no hay calificaciones
- DERIVADADocumento2 páginasDERIVADAFatima Paola Ruiz BravoAún no hay calificaciones
- Mapa Conceptual FISICADocumento1 páginaMapa Conceptual FISICAFatima Paola Ruiz BravoAún no hay calificaciones
- HexagramaDocumento1 páginaHexagramaFatima Paola Ruiz BravoAún no hay calificaciones
- Energia, Calor, Temperatura y TrabajoDocumento3 páginasEnergia, Calor, Temperatura y TrabajoFatima Paola Ruiz BravoAún no hay calificaciones
- Mapa Conceptual HierbasDocumento2 páginasMapa Conceptual HierbasFatima Paola Ruiz BravoAún no hay calificaciones
- LeyCero y Primera Ley de La TermidinamicaDocumento2 páginasLeyCero y Primera Ley de La TermidinamicaFatima Paola Ruiz BravoAún no hay calificaciones
- Sistema, Alrededores, Proceso y Funcion de EstadoDocumento7 páginasSistema, Alrededores, Proceso y Funcion de EstadoFatima Paola Ruiz BravoAún no hay calificaciones
- Procesos Cognitivos y AprendizajeDocumento2 páginasProcesos Cognitivos y AprendizajeFatima Paola Ruiz BravoAún no hay calificaciones
- Mapa Cognitivode AlgoritmoDocumento1 páginaMapa Cognitivode AlgoritmoFatima Paola Ruiz BravoAún no hay calificaciones
- Ruiz Bravo Fátima Paola - Atencion-ConcentracionDocumento2 páginasRuiz Bravo Fátima Paola - Atencion-ConcentracionFatima Paola Ruiz BravoAún no hay calificaciones
- Investigación - Ruiz Bravo Fatima PaolaDocumento3 páginasInvestigación - Ruiz Bravo Fatima PaolaFatima Paola Ruiz BravoAún no hay calificaciones
- Generacion Sin Hijos - ENSAYODocumento11 páginasGeneracion Sin Hijos - ENSAYOFatima Paola Ruiz BravoAún no hay calificaciones
- Generacion Sin Hijos - ENSAYODocumento11 páginasGeneracion Sin Hijos - ENSAYOFatima Paola Ruiz BravoAún no hay calificaciones
- CuadroSinopticoBioquimica - Ruiz Bravo Fátima PaolaDocumento1 páginaCuadroSinopticoBioquimica - Ruiz Bravo Fátima PaolaFatima Paola Ruiz BravoAún no hay calificaciones
- LaPobreza ENSAYODocumento13 páginasLaPobreza ENSAYOFatima Paola Ruiz BravoAún no hay calificaciones
- InformeBPL RuizBravoFátimaPaolaDocumento11 páginasInformeBPL RuizBravoFátimaPaolaFatima Paola Ruiz BravoAún no hay calificaciones
- ENSAYO RuizBravoFatimaPaolaDocumento3 páginasENSAYO RuizBravoFatimaPaolaFatima Paola Ruiz BravoAún no hay calificaciones
- Nomenclatura de Alcanos y Halogenuros de AlquiloDocumento7 páginasNomenclatura de Alcanos y Halogenuros de AlquiloChristian Paul Fausto RuizAún no hay calificaciones
- Esquemas de OrganelosDocumento6 páginasEsquemas de OrganelosJaime Velazquez Esquivel100% (1)
- Practica 1Documento7 páginasPractica 1Huaylla LourAún no hay calificaciones
- Preguntas de Biologia Imagenes CitologiaDocumento7 páginasPreguntas de Biologia Imagenes CitologiaMaría Hidalgo PlataAún no hay calificaciones
- Tabla PeriodicaDocumento14 páginasTabla Periodicagoth_sycoticAún no hay calificaciones
- Esponja de HierroDocumento25 páginasEsponja de HierroBorisvc8100% (1)
- 2-Distribudir Vial PRDocumento74 páginas2-Distribudir Vial PRErick vidal hernandezAún no hay calificaciones
- U5 - Cálculos EstequiométricosDocumento16 páginasU5 - Cálculos EstequiométricosRenzoMurilloAún no hay calificaciones
- Ficha 1000Documento4 páginasFicha 1000DISTRIBUIDORA DIBROCA C.AAún no hay calificaciones
- NatrosoldoctradDocumento32 páginasNatrosoldoctradKenneth SaganAún no hay calificaciones
- Capitulo 4.enlace Químico 2022-IDocumento10 páginasCapitulo 4.enlace Químico 2022-IJesus Miguel Anaya DoriaAún no hay calificaciones
- Informe Escrito Aplicar La Importancia de Los Cambios Por Alteración en Los Productos Cárnicos PDFDocumento3 páginasInforme Escrito Aplicar La Importancia de Los Cambios Por Alteración en Los Productos Cárnicos PDFGeraldine Palomares GuevaraAún no hay calificaciones
- Rocas IgneasDocumento8 páginasRocas IgneasYocastaHerbasTejerinaAún no hay calificaciones
- Produción de Agua Potable y Tratamiento de Aguas ResidualesDocumento11 páginasProdución de Agua Potable y Tratamiento de Aguas ResidualesElton George Tala FelixAún no hay calificaciones
- Hidrocarburos - AvanceDocumento27 páginasHidrocarburos - AvanceDiego MendozaAún no hay calificaciones
- Práctica 2Documento12 páginasPráctica 2Juan del CarmenAún no hay calificaciones
- Realiza Los Análisis Físicos, Químicos Y Microbiológicos de Los Productos de Cereales U Oleaginosas Y Productos DerivadosDocumento151 páginasRealiza Los Análisis Físicos, Químicos Y Microbiológicos de Los Productos de Cereales U Oleaginosas Y Productos DerivadosJOSE PORTILLOAún no hay calificaciones
- Hibridación de OrbitalesDocumento5 páginasHibridación de OrbitalesYANELY GIZEH REYES HERN�NDEZAún no hay calificaciones
- Medicamentos Laxantes y AntidiarreicosDocumento5 páginasMedicamentos Laxantes y AntidiarreicosMaria fernanda Tibaduiza gallegoAún no hay calificaciones
- Pc2-Repaso Ma 465 2020-02Documento6 páginasPc2-Repaso Ma 465 2020-02Yedsem Nuñez RufinoAún no hay calificaciones
- Sintesis de HidatoinasDocumento5 páginasSintesis de HidatoinasRafael González100% (1)
- Aniones y Cationes Mas Usuales 2Documento3 páginasAniones y Cationes Mas Usuales 2Gaby Cortés 7u7Aún no hay calificaciones
- Abstraccion de Conceptos - Modulo IIDocumento38 páginasAbstraccion de Conceptos - Modulo IIFlorencia TerragniAún no hay calificaciones
- CPK TotalDocumento4 páginasCPK TotalMichel Erick Yauri DuranAún no hay calificaciones
- Mapa Conceptual de Las BiomoleculasDocumento1 páginaMapa Conceptual de Las Biomoleculasgregorio flores aquinoAún no hay calificaciones
- Recuperación FinalDocumento3 páginasRecuperación Finalviviana bohorquezAún no hay calificaciones
- Cuestionario 5 Lab QMC-100Documento4 páginasCuestionario 5 Lab QMC-100Richard SangalliAún no hay calificaciones
- Plantilla de Etiqueta Q.86.04Documento4 páginasPlantilla de Etiqueta Q.86.04Ronald Pacheco ChoezAún no hay calificaciones
- Informe de La Unidad1 de Refinacion de Gas. 8vo Semestre.Documento16 páginasInforme de La Unidad1 de Refinacion de Gas. 8vo Semestre.Denny Fuentes0% (1)