Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Pregunta 7
Cargado por
Sara Campos Chavez0 calificaciones0% encontró este documento útil (0 votos)
64 vistas3 páginasTítulo original
PREGUNTA 7
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
64 vistas3 páginasPregunta 7
Cargado por
Sara Campos ChavezCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 3
Ejemplo 6.8.
- A una columna de absorción entran 40 m3/h de una mezcla
gaseosa de composición 35% en volumen de amoniaco y 65% en volumen de
aire. La absorción se verifica en contracorriente con agua que contiene el 2%
en peso de amoniaco, a 20°C y 1 atm y se ha de recuperar el 90 % del
amoniaco contenido en la mezcla gaseosa. Calculese la cantidad minima
necesaria de agua
Solucion: Calculamos las concentraciones en fracciones molares y relaciones
molares correspondientes a las condiciones de equilibrio a partir de los datos
kilogramos de amoniaco/100 Kg de agua frente a la presión parcial del
amoniaco en la fase gaseosa, a 20°C. para el primer punto dad en la tabla
siguiente, los cálculos serán:
MW N=14
MW H=1.01*3
MW NH3 = 17.03
2% en peso = 2/17
H2O = 16+2(1.01) = 18
Valores de fracción molar del amoniaco en fase liquida:
2/17
x= =0.207 37
2/17+100/18
Solubilidad vs presión parcial:
con la tabla 6-1:
12.0
y= =0.0157
760
La composición del gas de entrada será:
Del 35%
Yent=0.35
0.35
Yent= =0.5385
1−0.35
Composicion de liquido de entrada:
2/17
x= =0.02115
2/17+98 /18
0.02115
X= =0.0216
1−0.02115
Sobre el diagrama X-Y el punto correspondiente a la cúspide de la columna
tendrá coordenadas:
A(0.0216;0.05385)
La máxima concentración de liquido a la salida de la columna, que corresponde
al empleo de la minima cantidad de agua, será la de equilibrio con el gas de
entrada, que leída sobre el diagrama resulta:
Xsal = Xn = 0.2960
Por consiguiente, el punto corresponde a la base de la columna, tiene
coordenadas:
B(0.2960;0.5385)
El coeficiente angular de la recta AB da el valor de (L´/G´)min:
0.5385−0.05385
( L ´ /G¨ )min = =1.766
0.296−0.0216
El numero de moles de gas que entra al sistema por hora es:
pV 40 Kmol
G= = =1.665
RT 0.082∗293 h
aire
G ¨ =G ( 1− y )=1.665 ( 1−0.35 ) =1.082 Kmol de
h
L ¨ min =1.766∗1.082=1.911 Kmol de agua=34.39 Kg de agua
La cantidad total de liquido que entra al sistema es:
L¨ 1.911 Kmol
L= = =1.952
1− X 1−0.02114 h
La cantidad de amoniaco que entra en la corriente liquida es:
Kmol
L−L ´ =1.952−1.911=0.041
h
También podría gustarte
- Ejemplo 6 86 96 10Documento7 páginasEjemplo 6 86 96 10aldo subiranaAún no hay calificaciones
- Aplicación de Las Derivadas Parciales en La QuímicaDocumento4 páginasAplicación de Las Derivadas Parciales en La QuímicaBoris Milton Mamani Ichuta80% (5)
- Recalentamiento y SubenfriamientoDocumento1 páginaRecalentamiento y SubenfriamientoRubén Bastida Pascual100% (3)
- Problema Motor StirlingDocumento8 páginasProblema Motor StirlingEdu Márquez Jaramillo67% (3)
- Iii Sol Flores Mondragón Iqa Operaciones Ii 2020 IDocumento8 páginasIii Sol Flores Mondragón Iqa Operaciones Ii 2020 IJazmin Flores MondragónAún no hay calificaciones
- Determinación de la AEPT, número de etapas teóricas y número de unidades de transferencia en una columna de destilación con rellenoDocumento13 páginasDeterminación de la AEPT, número de etapas teóricas y número de unidades de transferencia en una columna de destilación con rellenoJavier JulianAún no hay calificaciones
- Asignación AbsorciónDocumento6 páginasAsignación AbsorciónWendy RiveraAún no hay calificaciones
- Reacciones químicasDocumento4 páginasReacciones químicasDaniel LautaroAún no hay calificaciones
- Ejer Cicio 1Documento2 páginasEjer Cicio 1Sara Campos ChavezAún no hay calificaciones
- 1 NDCJDDocumento2 páginas1 NDCJDSara Campos ChavezAún no hay calificaciones
- Experimento N°8: Relación Entre El Volumen y La Presión Aplicada A Una Muestra Gaseosa: Ley de Boyle.Documento7 páginasExperimento N°8: Relación Entre El Volumen y La Presión Aplicada A Una Muestra Gaseosa: Ley de Boyle.Henry MolinaAún no hay calificaciones
- Problemas de Tranferencia de Masa 1 Absorcion de GasesDocumento32 páginasProblemas de Tranferencia de Masa 1 Absorcion de GasesXioMarilloAún no hay calificaciones
- Laboratorio # 6 Determinación de La Velocidad de Reacción Química Por El Método de Las Velocidades InicialesDocumento9 páginasLaboratorio # 6 Determinación de La Velocidad de Reacción Química Por El Método de Las Velocidades InicialesJǝnnifǝr GonzalǝZzAún no hay calificaciones
- Problemas Resueltos de MetalurgiaDocumento5 páginasProblemas Resueltos de MetalurgiaJoseAún no hay calificaciones
- Produccion Del Metanol Con Reformado AutotermicoDocumento3 páginasProduccion Del Metanol Con Reformado AutotermicoKarina Giselle Castellon Fernandez LA MonitaAún no hay calificaciones
- GUIA DE ACTIVIDAD DE APRENDIZAJE PARA CLASE PRÁCTICA DE TRANSFERENCIA DE MASADocumento6 páginasGUIA DE ACTIVIDAD DE APRENDIZAJE PARA CLASE PRÁCTICA DE TRANSFERENCIA DE MASAjavier gagoAún no hay calificaciones
- Bloques FormaldehidoDocumento4 páginasBloques FormaldehidoAnonymous OsyZ4eLAún no hay calificaciones
- Cilindro CriogénicoDocumento7 páginasCilindro CriogénicoPaula Andrea Rodelo ZuñigaAún no hay calificaciones
- Ejemplo 16. de FoustDocumento3 páginasEjemplo 16. de FoustGustavo MayenAún no hay calificaciones
- Clase de Repaso para El Primer Parcial Clase 6Documento5 páginasClase de Repaso para El Primer Parcial Clase 6lolaAún no hay calificaciones
- SERIE N8 Evaporacion 2020Documento32 páginasSERIE N8 Evaporacion 2020Andrés GidekelAún no hay calificaciones
- Ejercicios de Secado 2018 - IIDocumento7 páginasEjercicios de Secado 2018 - IIINGRID ROSSANA SÁNCHEZ CALDERÓNAún no hay calificaciones
- Tecnicas GeneralescentrifugaciónDocumento17 páginasTecnicas GeneralescentrifugaciónJer RodriguezAún no hay calificaciones
- Problemas Filtración-Mecánica de PartículasDocumento12 páginasProblemas Filtración-Mecánica de PartículasTakeshi Tanohuye TanohuyeAún no hay calificaciones
- Wankat 4D33Documento15 páginasWankat 4D33MaruriAún no hay calificaciones
- Laboratorio #6 AnaliticaDocumento14 páginasLaboratorio #6 AnaliticaSamir VelezAún no hay calificaciones
- 2oParTaller PDFDocumento1 página2oParTaller PDFJuan Pablo Cabra GonzalezAún no hay calificaciones
- Modelamiento de Un Reactor Batch en MatlabDocumento10 páginasModelamiento de Un Reactor Batch en MatlabDerly Tatiana Mendez HernandezAún no hay calificaciones
- PROCESOS DE SEPARACIÒN Destilacion PDFDocumento80 páginasPROCESOS DE SEPARACIÒN Destilacion PDFFELIPE DURANAún no hay calificaciones
- Propiedades físicas de materiales de laboratorioDocumento18 páginasPropiedades físicas de materiales de laboratorioDaniela VelascoAún no hay calificaciones
- Practicos Ind 176Documento14 páginasPracticos Ind 176Maria Inés MorenoAún no hay calificaciones
- Ejercicios de Torres Agotamiento y EnriqueciminetoDocumento1 páginaEjercicios de Torres Agotamiento y EnriqueciminetoCristhian CarrizalesAún no hay calificaciones
- Ejercicio de Destilación Hexano C6 - Benceno Con Ecuación de AntoineDocumento5 páginasEjercicio de Destilación Hexano C6 - Benceno Con Ecuación de AntoineCluisantony Jayco DizeAún no hay calificaciones
- Piezoelectric Polymer Composites for Energy HarvestingDocumento2 páginasPiezoelectric Polymer Composites for Energy HarvestingDavid RamirezAún no hay calificaciones
- Diseño - Sulca Jota Jose LuisDocumento49 páginasDiseño - Sulca Jota Jose LuisJose Luis Sulca JotaAún no hay calificaciones
- Problema de Aplicación - Sistema de Bombeo PDFDocumento14 páginasProblema de Aplicación - Sistema de Bombeo PDFJoseph bryan Gamarra floresAún no hay calificaciones
- Solucion XDpor FinDocumento6 páginasSolucion XDpor Finflorencio ramos montanoAún no hay calificaciones
- Ejemplo 27.2 WordDocumento5 páginasEjemplo 27.2 Wordeduardo salvadorAún no hay calificaciones
- Destilación del sistema benceno-toluenoDocumento11 páginasDestilación del sistema benceno-toluenoSalvador SantosAún no hay calificaciones
- Informe Rio AtoyacDocumento34 páginasInforme Rio AtoyacLa Zarzuela SantiagoAún no hay calificaciones
- InformacionDocumento2 páginasInformacionJayson Andy0% (1)
- Segundo Examen de Calor ChalotexDocumento9 páginasSegundo Examen de Calor ChalotexGonzalo Arom Caceres MachacaAún no hay calificaciones
- A4-Brayan AguilarDocumento15 páginasA4-Brayan AguilarBrayan AguilarAún no hay calificaciones
- Análisis del acetato de nopiloDocumento9 páginasAnálisis del acetato de nopiloVictor BarbosaAún no hay calificaciones
- Karina Chambergo Roman (Solucionario Del Primer Parcial)Documento5 páginasKarina Chambergo Roman (Solucionario Del Primer Parcial)Ces CrAún no hay calificaciones
- Seader Henley Roper 2011Documento10 páginasSeader Henley Roper 2011Piermarco ContrerasAún no hay calificaciones
- FENÓMENOS DE TRANSPORTE Y EVAPORACIÓNDocumento4 páginasFENÓMENOS DE TRANSPORTE Y EVAPORACIÓNLuisa Fernanda Gil HenaoAún no hay calificaciones
- Dennis Banda Ou3Documento15 páginasDennis Banda Ou3Abel HbAún no hay calificaciones
- Problema 1. Teorema Pi de BuckinghamDocumento6 páginasProblema 1. Teorema Pi de BuckinghamAna Sordo CastilloAún no hay calificaciones
- Practica No 1 Propiedades Molares ParcialesDocumento11 páginasPractica No 1 Propiedades Molares ParcialesArturo Dominguez AdriaoAún no hay calificaciones
- Capitulo 3Documento23 páginasCapitulo 3William BernalAún no hay calificaciones
- Tarea 03Documento2 páginasTarea 03Roger Rojas PadillaAún no hay calificaciones
- Sem4 Jazmin JimenezDocumento38 páginasSem4 Jazmin JimenezJAZMIN VALESKA JOHANNA JIMENEZ FABIANAún no hay calificaciones
- Transferencia de Masa ProfesorDocumento5 páginasTransferencia de Masa ProfesorL Roberto Bonilla EspinozaAún no hay calificaciones
- Propiedades Molares ParcialesDocumento18 páginasPropiedades Molares ParcialesFrancisco LaraAún no hay calificaciones
- Problemas Adicionales Hinostroza Meza Ayda Irene IqDocumento8 páginasProblemas Adicionales Hinostroza Meza Ayda Irene IqIrene HinostrozaAún no hay calificaciones
- Evaluación del almidón de maíz como coagulante naturalDocumento145 páginasEvaluación del almidón de maíz como coagulante naturalChanez BacilioAún no hay calificaciones
- Problemas de Termo1Documento3 páginasProblemas de Termo1LOPEZ GARCÍA VANIA ABIGAILAún no hay calificaciones
- Practica 13 UnitariasDocumento8 páginasPractica 13 UnitariasJose MiguelAún no hay calificaciones
- Ejercicios ResueltosDocumento12 páginasEjercicios ResueltoserikaAún no hay calificaciones
- 6 Balance de MasaDocumento12 páginas6 Balance de MasaBastian Andaur0% (1)
- Ejercicios ImparesDocumento8 páginasEjercicios ImparesbyronAún no hay calificaciones
- Directorio de Escuelas TecamacDocumento45 páginasDirectorio de Escuelas TecamacRUBENAún no hay calificaciones
- Bajar AlimentosDocumento5 páginasBajar AlimentosCidoAún no hay calificaciones
- Ejer D Trans D Masa II Con Graficos ADocumento20 páginasEjer D Trans D Masa II Con Graficos AJulian SoloAún no hay calificaciones
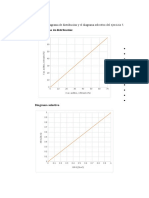
- Representa El Diagrama de Distribución y El Diagrama Selectivo Del Ejercicio 5. Diagrama de DistribuciónDocumento1 páginaRepresenta El Diagrama de Distribución y El Diagrama Selectivo Del Ejercicio 5. Diagrama de DistribuciónSara Campos ChavezAún no hay calificaciones
- FCCDocumento1 páginaFCCSara Campos ChavezAún no hay calificaciones
- Huecos Tetraédricos en La Estructura HCDocumento2 páginasHuecos Tetraédricos en La Estructura HCSara Campos ChavezAún no hay calificaciones
- DownloadDocumento12 páginasDownloadSara Campos ChavezAún no hay calificaciones
- Aguade Mar Agua Demar Agua DemarDocumento2 páginasAguade Mar Agua Demar Agua DemarSara Campos ChavezAún no hay calificaciones
- Anexo11 Aplicacion Mecanismo OxiDocumento5 páginasAnexo11 Aplicacion Mecanismo OxiGreisy EsquivelAún no hay calificaciones
- Ejercicio 2Documento2 páginasEjercicio 2Sara Campos ChavezAún no hay calificaciones
- Ejercicio 4Documento1 páginaEjercicio 4Sara Campos ChavezAún no hay calificaciones
- Representa El Diagrama de Distribución y El Diagrama Selectivo Del Ejercicio 5. Diagrama de DistribuciónDocumento1 páginaRepresenta El Diagrama de Distribución y El Diagrama Selectivo Del Ejercicio 5. Diagrama de DistribuciónSara Campos ChavezAún no hay calificaciones
- Representa El Diagrama de Distribución y El Diagrama Selectivo Del Ejercicio 5. Diagrama de DistribuciónDocumento1 páginaRepresenta El Diagrama de Distribución y El Diagrama Selectivo Del Ejercicio 5. Diagrama de DistribuciónSara Campos ChavezAún no hay calificaciones
- FCCDocumento1 páginaFCCSara Campos ChavezAún no hay calificaciones
- Equilibrio de FasesDocumento10 páginasEquilibrio de FasesElizabeth MirandaAún no hay calificaciones
- 2 Soluciones Ideales Ley RaoultDocumento22 páginas2 Soluciones Ideales Ley RaoultAntonia Castillo CuevaAún no hay calificaciones
- Cárdenas-Jorgge - Mata. Informe - 4Documento14 páginasCárdenas-Jorgge - Mata. Informe - 4Antonella Cristhel Moya MoreiraAún no hay calificaciones
- Serie N°4 Absorción de GasesDocumento3 páginasSerie N°4 Absorción de GasesS. P.Aún no hay calificaciones
- 5 Componentes Sistemas de ControlDocumento17 páginas5 Componentes Sistemas de ControlJuan Valencia RuizAún no hay calificaciones
- Presión AbsolutaDocumento2 páginasPresión AbsolutaMaglis YdrogoAún no hay calificaciones
- Capítulo 5 Propiedades y Teoria de Los GasesaDocumento34 páginasCapítulo 5 Propiedades y Teoria de Los GasesacesarumsaAún no hay calificaciones
- Lic Fisica 20-02-15 Adscripción MaterialExperimentalDeLosLaboratoriosDeFisicaBasicaI II IIIDelEquipamientoAdquiridoEn2013Documento338 páginasLic Fisica 20-02-15 Adscripción MaterialExperimentalDeLosLaboratoriosDeFisicaBasicaI II IIIDelEquipamientoAdquiridoEn2013davidAún no hay calificaciones
- Proyecto Final Campo Dorado SurDocumento31 páginasProyecto Final Campo Dorado SurTamara Uriona CuellarAún no hay calificaciones
- UDV (Finalizado)Documento4 páginasUDV (Finalizado)Diño CamonesAún no hay calificaciones
- Lechos PorososDocumento15 páginasLechos PorososShirley Vargas RamosAún no hay calificaciones
- Ecuaciones de EstadoDocumento26 páginasEcuaciones de EstadoCristian ZuñigaAún no hay calificaciones
- Informe de Compresibilidad y ElasticidadDocumento5 páginasInforme de Compresibilidad y ElasticidadKevinSigueñasFernandez100% (1)
- Gases y sus propiedades físicasDocumento110 páginasGases y sus propiedades físicasBravo Montoya Adrian DavidAún no hay calificaciones
- 2.1 Generalidades Del Estado Gaseoso y Leyes de Los GasesDocumento3 páginas2.1 Generalidades Del Estado Gaseoso y Leyes de Los GasesMEJIA EUTIMIO GABRIELA100% (1)
- Guia1eraparte1erc2020 PDFDocumento21 páginasGuia1eraparte1erc2020 PDFLuciano HuenuvilAún no hay calificaciones
- Deber 1Documento8 páginasDeber 1Lilibeth CastroAún no hay calificaciones
- Tema 8 - Hidrostática e Hedrodinámica - Mañana B OrdinarioDocumento27 páginasTema 8 - Hidrostática e Hedrodinámica - Mañana B Ordinariojulio cajigasAún no hay calificaciones
- Hidraulica 1: Ejercicios Propuestos Cap. 2 Estática de FluidosDocumento4 páginasHidraulica 1: Ejercicios Propuestos Cap. 2 Estática de FluidosRamirez Chinche Jose LuisAún no hay calificaciones
- Punto Triple SO2Documento3 páginasPunto Triple SO2Jess TellezAún no hay calificaciones
- FDocumento12 páginasFRCTR XD0% (1)
- Destilación 07.07.21Documento42 páginasDestilación 07.07.21María José GarzónAún no hay calificaciones
- Porque El Oxigeno Es Gas y El Agua Es Un VaporDocumento22 páginasPorque El Oxigeno Es Gas y El Agua Es Un VaporJuan Esteban BurbanoAún no hay calificaciones
- Estado Líquido-InvestigacionDocumento3 páginasEstado Líquido-InvestigacionJesus GonzalezAún no hay calificaciones
- Reporte de Practica 3 Ley de CharlesDocumento16 páginasReporte de Practica 3 Ley de CharleslizAún no hay calificaciones
- UC Semestre 1-2018. Flujo compresible isoentropicoDocumento24 páginasUC Semestre 1-2018. Flujo compresible isoentropicoJose RojasAún no hay calificaciones