Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Equilibrio Entre Fases Construcción Del Diagrama de Fases Del Ciclohexano
Cargado por
Aster PoreyTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Equilibrio Entre Fases Construcción Del Diagrama de Fases Del Ciclohexano
Cargado por
Aster PoreyCopyright:
Formatos disponibles
EQUILIBRIO ENTRE FASES CONSTRUCCIÓN DEL DIAGRAMA DE FASES DEL
CICLOHEXANO
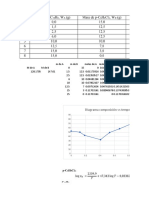
a) Se calcularon los datos de T2 para el equilibrio líquido-vapor y se realizó la gráfica
correspondiente utilizando la ecuación de Clausius-Clapeyron.
Presión vs Temperatura (L-V) T2 (K) P (atm)
1.4
553,4
9 40,2
1.2 359,6
1 7 1,18421053
353,7
Presión (atm)
0.8
3 1
0.6 350,9
0.4 1 0,92105263
344,9
0.2
7 0,77105263
0 339,8
270.00 280.00 290.00 300.00 310.00 320.00 330.00 340.00 350.00 360.00 370.00
3 0,65789474
Temperatura (K)
332,8
6 0,52631579
324,2
8 0,39473684
b) Para este equilibrio sólido-vapor se utilizó la misma ecuación de 312,9
Clausius-Clapeyron para calcular la P2 en cada punto de la curva. 1 0,26315789
Luego se realizó la gráfica correspondiente. 295,2
3 0,13157895
279,9
Presión vs Temperatura (S-V) 0 0,05394737
0.06
T (K) P2 (atm)
0.05 279,9 0,0539
0.04
278 0,0490
Presión (atm)
277 0,0465
0.03 276 0,0442
0.02 275 0,0419
274 0,0398
0.01 273 0,0378
0 268 0,0288
250 255 260 265 270 275 280 285
263 0,0218
Temperatura (atm) 253 0,0121
Daniela Baldome – Emiliano Pérez
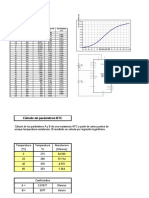
c) Para este caso, debido a que es un equilibrio sólido-líquido, se utilizó la siguiente fórmula
para calcular los valores de temperatura de la curva. Para calcular la variación de volumen,
se utilizó los valores de densidad del ciclohexano para cada estado y su peso molecular.
Presión vs Temperatura (S-L)
1.4000 T (K) P (atm)
279,73 1,1842
1.2000
279,72 1,0000
1.0000
279,71 0,9211
Presión (atm)
0.8000 279,7 0,7711
0.6000 279,69 0,6579
279,68 0,5263
0.4000
279,6792 0,3947
0.2000
279,6704 0,2632
0.0000 279,65 0,1316
279.6 279.65 279.7 279.75 279.8 279.85 279.9 279.95
279,9 0,0539
Temperatura (K)
Daniela Baldome – Emiliano Pérez
d) Luego de realizadas las gráficas se procedió a graficar el diagrama de fases para el
ciclohexano a partir de los datos obtenidos en los equilibrios anteriores. La gráfica que se
obtuvo fue la siguiente:
Diagrama de fases ciclohexano
Datos:
1.2
1
1= punto de ebullición normal
0.8 2= punto de fusión normal
Presión (atm)
0.6 3= punto triple
0.4
0.2
0
225 275 325 375
Temperatura (K)
2 1
Sól Líq
Gas
Daniela Baldome – Emiliano Pérez
Conclusión: A partir de los cálculos realizados y uniendo las gráficas de las tres fases
Líquido-vapor, Sólido-vapor y Sólido-líquido, se puede observar que el punto triple
coincide y es a una P=0.0539 atm y T=279.9K.
Debido a que punto crítico se encuentra a una temperatura de 553 K, y una presión de
40,2 atm no lo incluimos en la gráfica.
Daniela Baldome – Emiliano Pérez
También podría gustarte
- Reactores Datos P3, P4 y P5Documento6 páginasReactores Datos P3, P4 y P5Saul GonzalezAún no hay calificaciones
- Doc1PRESION DE VAPORDocumento2 páginasDoc1PRESION DE VAPOR36 Alan Deymar Corazón SuxoAún no hay calificaciones
- Deber 1 TermoDocumento4 páginasDeber 1 TermoRuben GualotuñaAún no hay calificaciones
- Cálculo de TransformadoresDocumento3 páginasCálculo de Transformadoresdepartamento mantenimientoAún no hay calificaciones
- Examen EyCDocumento4 páginasExamen EyCJonathan VargasAún no hay calificaciones
- 1.-Discretizacion y Numeracion de Nodos y Elementos TriangularesDocumento28 páginas1.-Discretizacion y Numeracion de Nodos y Elementos TriangularesSonia holaAún no hay calificaciones
- Taller Examen 3 Ecuación de EstadoDocumento6 páginasTaller Examen 3 Ecuación de Estadogustavo alzate patiñoAún no hay calificaciones
- PDF AnovaDocumento2 páginasPDF AnovaLia PukerainbowsAún no hay calificaciones
- Practica 2 TEQFDocumento1 páginaPractica 2 TEQFEduardo Fernando Ayala MontañoAún no hay calificaciones
- Informee 4 FQDocumento5 páginasInformee 4 FQSAYRA SCHMITT SÁNCHEZ PEÑAAún no hay calificaciones
- Práctica 5. Propiedades ColigativasDocumento10 páginasPráctica 5. Propiedades ColigativasDavid Emmanuel Pérez Cruz100% (1)
- Como Hallar El Calibre Del Alambre Del Devanado PrimarioDocumento1 páginaComo Hallar El Calibre Del Alambre Del Devanado PrimarioEdward CastleAún no hay calificaciones
- Avaluo de Cargas y Analisis Sismico Proyecto FinalDocumento8 páginasAvaluo de Cargas y Analisis Sismico Proyecto FinalOSCAR RIVEROAún no hay calificaciones
- Calculo de TrafosDocumento2 páginasCalculo de Trafoshernancau0% (1)
- Chart TitleDocumento9 páginasChart TitleAyyoub badine louraneAún no hay calificaciones
- Excel Práctica 3 CyRHDocumento3 páginasExcel Práctica 3 CyRHAlfredo EscamillaAún no hay calificaciones
- Examen Final de Presas ResueltoDocumento8 páginasExamen Final de Presas ResueltoMarielaAún no hay calificaciones
- Practica 6 Propiedades ColigativasDocumento12 páginasPractica 6 Propiedades ColigativasSergio Martinez RamirezAún no hay calificaciones
- Caida LibreDocumento18 páginasCaida LibreGuido Angel Frias CorderoAún no hay calificaciones
- Calculos de FisicoquimicaDocumento5 páginasCalculos de FisicoquimicaPIERO MATIAS HERRERA SUAREZAún no hay calificaciones
- Cuestionario Dinamica PT2Documento2 páginasCuestionario Dinamica PT2Roberto SuárezAún no hay calificaciones
- Calculo Sismo Resistente EtabsDocumento9 páginasCalculo Sismo Resistente EtabsRaul Arroyo PalaciosAún no hay calificaciones
- Análisis Comparativo de Cálculo de Diámetros y Presiones en Un Modelo Hidráulico de Red de DistribuciónDocumento20 páginasAnálisis Comparativo de Cálculo de Diámetros y Presiones en Un Modelo Hidráulico de Red de Distribucióncristhian jesus gaspar crispinAún no hay calificaciones
- Parte de ExperimentoDocumento4 páginasParte de ExperimentoDANA SHARIK ROMERO BUSTAMANTEAún no hay calificaciones
- EntalpíaDocumento8 páginasEntalpíaJuan GómezAún no hay calificaciones
- Como Calcular Un TransformadorDocumento3 páginasComo Calcular Un TransformadorYamandu CortesAún no hay calificaciones
- Libro1 UltimoDocumento8 páginasLibro1 UltimoDavid Alejandro Serrano RodríguezAún no hay calificaciones
- Reporte 3 Equilibrio QuimicoDocumento7 páginasReporte 3 Equilibrio QuimicoArmando Chávez RojasAún no hay calificaciones
- Catalogo Tuberia Novariego Agricola 2013Documento3 páginasCatalogo Tuberia Novariego Agricola 2013Joshy Huanca JuarezAún no hay calificaciones
- Dependencia Del Valor de PotencialDocumento3 páginasDependencia Del Valor de PotencialRoco neluAún no hay calificaciones
- Cálculo de Termistores NTCDocumento2 páginasCálculo de Termistores NTCcarlosAún no hay calificaciones
- MQ 3Documento5 páginasMQ 3Alex SotoAún no hay calificaciones
- Taller Minimos CuadradosDocumento1 páginaTaller Minimos Cuadradosalex fajardoAún no hay calificaciones
- Resultados de Análisis de Deformación y Vibración en Un Perfil NACA 2415Documento13 páginasResultados de Análisis de Deformación y Vibración en Un Perfil NACA 2415LuisRodriguezAún no hay calificaciones
- LAB. Hidraulica Curva EspecificaDocumento8 páginasLAB. Hidraulica Curva EspecificaAngie GutierrezAún no hay calificaciones
- Profundidad EfectivaDocumento1 páginaProfundidad EfectivaJose ZamoraAún no hay calificaciones
- Determinación de Cafeína Por Espectrofotometría UV-VisibleDocumento7 páginasDeterminación de Cafeína Por Espectrofotometría UV-VisibleAlfonso Martínez BravoAún no hay calificaciones
- LosCheems P9G4Documento14 páginasLosCheems P9G4Luis EmilioAún no hay calificaciones
- Taller 3 - Simulacion Con Datos Empiricos 1Documento173 páginasTaller 3 - Simulacion Con Datos Empiricos 1quistis10Aún no hay calificaciones
- TemperaturaDocumento2 páginasTemperaturaLauraRosasAún no hay calificaciones
- AvancefluidizacionDocumento6 páginasAvancefluidizacionJuanAún no hay calificaciones
- Tablas Viscosidades - GeankoplisDocumento11 páginasTablas Viscosidades - GeankoplisEstefanny TorresAún no hay calificaciones
- C22Documento9 páginasC22Daniel DíazAún no hay calificaciones
- Examen 2Documento12 páginasExamen 2perezaide487Aún no hay calificaciones
- Practica 9, Suelos 2Documento5 páginasPractica 9, Suelos 2kampAún no hay calificaciones
- Espectro de AceleracionesDocumento6 páginasEspectro de Aceleracionesjulio oliveraAún no hay calificaciones
- Trabajo de ExcelDocumento27 páginasTrabajo de ExcelleohammerAún no hay calificaciones
- Practica 3Documento7 páginasPractica 3Pepe Arturo GonzalezAún no hay calificaciones
- LABN°2-QMC-1206 B Univ. Juaniquina Pacheco IsraelDocumento6 páginasLABN°2-QMC-1206 B Univ. Juaniquina Pacheco IsraelStefy Nina RuedaAún no hay calificaciones
- Asignacion 4 2Documento6 páginasAsignacion 4 2Luider RodriguezAún no hay calificaciones
- Nerys Salazar Asignacion 4Documento6 páginasNerys Salazar Asignacion 4Luider RodriguezAún no hay calificaciones
- Guia Problema ELV Calculo de CoeficientesDocumento23 páginasGuia Problema ELV Calculo de CoeficientesAntoniaAún no hay calificaciones
- Metodo SimultaneidadDocumento1 páginaMetodo Simultaneidadanon_901274768Aún no hay calificaciones
- COMPUTOS METRICOS BAñO ZONA 9Documento7 páginasCOMPUTOS METRICOS BAñO ZONA 9Omar CruzAún no hay calificaciones
- TallerDocumento3 páginasTallerStiven VictorAún no hay calificaciones
- Informe Final 3.1Documento3 páginasInforme Final 3.1Jossue OlivaresAún no hay calificaciones
- Solucion de Las 4 Preguntas Moina Montalvan Percy AlvaroDocumento38 páginasSolucion de Las 4 Preguntas Moina Montalvan Percy AlvaroPercy Moina MontalvanAún no hay calificaciones
- Reporte. Distribución de Tiempos de ResidenciaDocumento7 páginasReporte. Distribución de Tiempos de ResidenciaOscar GarziaAún no hay calificaciones
- Exp Queda LivreDocumento1 páginaExp Queda LivrefelipeAún no hay calificaciones
- Estudio de Cargas TermicasDocumento11 páginasEstudio de Cargas TermicasLuis RevillaAún no hay calificaciones
- Flujo Fabno y RDocumento12 páginasFlujo Fabno y RRonald ARAún no hay calificaciones
- 3 Compresores de TornilloDocumento37 páginas3 Compresores de TornilloDeyner Ayala RamosAún no hay calificaciones
- GUIA 5 Problemas 10 y 19Documento3 páginasGUIA 5 Problemas 10 y 19cruzsilvaAún no hay calificaciones
- Equipo 3 - Fluidos Sometidos A PresionDocumento19 páginasEquipo 3 - Fluidos Sometidos A PresionIan CarreñoAún no hay calificaciones
- Lubricacion Aplicada KDocumento28 páginasLubricacion Aplicada KSaul Mena VargasAún no hay calificaciones
- Práctica Tubo de Venturi y Placa de OrificioDocumento6 páginasPráctica Tubo de Venturi y Placa de OrificioHector Pedraza RomeroAún no hay calificaciones
- Diagrama 1. DPDocumento4 páginasDiagrama 1. DPvanesaAún no hay calificaciones
- Cap II-Din de Fluidos 2019Documento19 páginasCap II-Din de Fluidos 2019Scarleth AguileraAún no hay calificaciones
- Flete TerrestreDocumento5 páginasFlete TerrestreedsonAún no hay calificaciones
- Actividad Virtual N°3 - TERMODINAMICADocumento4 páginasActividad Virtual N°3 - TERMODINAMICAGustavo ElTravieso0% (1)
- Informe Pérdida de Calor FinalDocumento41 páginasInforme Pérdida de Calor FinalCriz Espinoza ChavezAún no hay calificaciones
- 351 Evaluacion Jumbo Atlas s1d Dpj-43 AndaychaguaDocumento7 páginas351 Evaluacion Jumbo Atlas s1d Dpj-43 AndaychaguaAlexis Vega Reyes100% (1)
- Sesion 01 Ecuación General de Las Turbo MaquinasDocumento2 páginasSesion 01 Ecuación General de Las Turbo MaquinasHelder TejadaAún no hay calificaciones
- Jitorres - Ejercicios Propuestos Conservacion de La Masa y BernoulliDocumento2 páginasJitorres - Ejercicios Propuestos Conservacion de La Masa y BernoulliJonathan BlancoAún no hay calificaciones
- Fisicoquimica Informe de La Practica 2Documento6 páginasFisicoquimica Informe de La Practica 2Daniela HuérfanoAún no hay calificaciones
- Brochure Tomo I - Dehidro V 1.5 - 2023Documento11 páginasBrochure Tomo I - Dehidro V 1.5 - 2023Anthony CanalesAún no hay calificaciones
- Grupos de WSP de MetalurgiaDocumento6 páginasGrupos de WSP de MetalurgiaEdward LujanAún no hay calificaciones
- Diseno Hidraulico Del SifonDocumento9 páginasDiseno Hidraulico Del SifonyeniferAún no hay calificaciones
- Manual de BombasDocumento69 páginasManual de BombasNivardo Rodriguez CruzAún no hay calificaciones
- Diagnóstico Del Mercado Laboral Del Ingeniero Químico en El Salvador PDFDocumento263 páginasDiagnóstico Del Mercado Laboral Del Ingeniero Químico en El Salvador PDFClasical RVVAún no hay calificaciones
- Taller ResueltoDocumento6 páginasTaller ResueltoNicolás Tovar38% (8)
- 8287222Documento5 páginas8287222MarcosAún no hay calificaciones
- (Document Title) : Pedro Jose Sirias Castillo (COMPANY NAME) (Company Address)Documento11 páginas(Document Title) : Pedro Jose Sirias Castillo (COMPANY NAME) (Company Address)Pedro SiriasAún no hay calificaciones
- Luis Santi Practica 6 Tubos Concentricos 7-Junio-2017 PDFDocumento7 páginasLuis Santi Practica 6 Tubos Concentricos 7-Junio-2017 PDFLuis SantiAún no hay calificaciones
- OPU 08-Transferencia de CalorDocumento15 páginasOPU 08-Transferencia de CalorDiego RiveraAún no hay calificaciones
- PERMEABILIDAD DE SUELOS GRANULARES HaroldDocumento7 páginasPERMEABILIDAD DE SUELOS GRANULARES Haroldjavier soto hernandezAún no hay calificaciones
- En Iso 6946 Aenor 5a099ed01723dd3f8cfeb2aaDocumento3 páginasEn Iso 6946 Aenor 5a099ed01723dd3f8cfeb2aaWilliam Berrospi GarciaAún no hay calificaciones
- Limitaciones y Uso Correcto de La Ecuación de HazenDocumento11 páginasLimitaciones y Uso Correcto de La Ecuación de Hazendiana luzAún no hay calificaciones
- Problema Resuelto Ciclo de OTTO PDFDocumento9 páginasProblema Resuelto Ciclo de OTTO PDFraul cabanillasAún no hay calificaciones