0% encontró este documento útil (0 votos)
408 vistas4 páginasModelo Atomico de Dalton
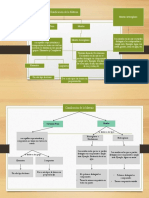
El documento describe el modelo atómico del químico inglés John Dalton. Dalton propuso que toda la materia está compuesta de átomos indivisibles e idénticos dentro de cada elemento. Formuló seis postulados sobre la estructura atómica, incluyendo que los átomos se combinan en proporciones fijas para formar compuestos y que las reacciones químicas implican el reordenamiento de átomos. Aunque revolucionario para su época, el modelo de Dalton tenía limitaciones como no considerar la existencia de partículas sub
Cargado por
maria figueroaDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como DOCX, PDF, TXT o lee en línea desde Scribd
0% encontró este documento útil (0 votos)
408 vistas4 páginasModelo Atomico de Dalton
El documento describe el modelo atómico del químico inglés John Dalton. Dalton propuso que toda la materia está compuesta de átomos indivisibles e idénticos dentro de cada elemento. Formuló seis postulados sobre la estructura atómica, incluyendo que los átomos se combinan en proporciones fijas para formar compuestos y que las reacciones químicas implican el reordenamiento de átomos. Aunque revolucionario para su época, el modelo de Dalton tenía limitaciones como no considerar la existencia de partículas sub
Cargado por
maria figueroaDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como DOCX, PDF, TXT o lee en línea desde Scribd