Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Moles
Cargado por
JesikaLopezTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Moles
Cargado por
JesikaLopezCopyright:
Formatos disponibles
Qu es el mol?
Un mol es un nmero de Avogadro de partculas. Es decir 6,023 x 10 23 partculas elementales ya sean tomos,
molculas, iones, protones, electrones o neutrones.
1 mol = 6,023 x 1023 partculas
Es tremendamente grande. Para que os hagis una idea, si pudiramos contar partculas de 10 en 10 cada
segundo, tardaramos en llegar a ese nmero la friolera de 2 x 10 16 aos (la edad del universo se estima en
1.4 x 1010 aos)
Un nmero de partculas tan grande debe de ser suficiente como para que si colocamos un mol de cualquier
sustancia en una balanza podamos medir su masa.
As un mol de cualquier sustancia pesa lo mismo que su masa atmica o molecular pero
expresndola en g
1
1
1
1
1
1
tomo
tomo
tomo
tomo
tomo
tomo
de
de
de
de
de
de
H tiene una masa de 1 u
He tiene una masa de 4 u
Li tiene una masa de 7 u
As tiene una masa de 75 u
B tiene una masa de 10 u
N tiene una masa de 14 u
1
1
1
1
1
1
mol
mol
mol
mol
mol
mol
de
de
de
de
de
de
H tiene una masa de 1 g
He tiene una masa de 4 g
Li tiene una masa de 7 g
As tiene una masa de 75 g
B tiene una masa de 10 g
Ni tiene una masa de 14 g
A partir de la tabla que est en la ltima pgina podemos saber tambin la masa molecular de compuestos
como:
H2O
H2SO4
CaCO3
Al2(SO4)3
1 molcula de H 2O pesa 18 u
1 molcula de H 2SO 4 pesa 98 u
1 molcula de CaCO 3 pesa 100 u
1 mol de molculas H 2O pesan 18 g
1 mol de molculas H 2SO 4 pesan 98 g
1 mol de molculas CaCO 3 pesan 100 g
1 molcula de Al 2(SO 4) 3 pesa 342 u
1 mol de molculas Al 2(SO 4) 3 pesan 342 g
Por lo tanto, parece que hay una relacin entre moles, masa y nmero de partculas. Vemoslo con
estos ejemplos:
En 1 mol de H2O hay 6,023 x 1023 molculas de H2O y pesan 18 g
En 1 mol de H2SO4 hay 6,023 x 1023 molculas de H2SO4 y pesan 98 g
En 1 mol de CaCO3 hay 6,023 x 1023 molculas de CaCO3 y pesan 100 g
En 1 mol de Al2(SO4)3 hay 6,023 x 1023 molculas de Al2(SO4)3 y pesan 342 g
Podemos contar el nmero de molculas que hay en 80 g de H 2O? Lo podemos hacer
con una regla de 3 que tanto os gusta
6,023 x 1023 molculas de H2O
X
X = 2.67 x 1024 molculas de H2O
18 g
80 g
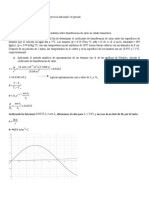
Quiz, este esquema os pueda ser de utilidad:
Para pasar de masa a moles dividimos por el peso molecular del compuesto
Para pasar de moles a masa multiplicamos por el peso molecular del compuesto
Para pasar de moles a partculas multiplicamos por el nmero de Avogadro
Para pasar de partculas a moles dividimos por el nmero de Avogadro
EJERCICIOS:
1
Cuntas molculas de metano hay en 6 moles del mismo?. metano = CH 4
Cuntos moles son 100 g de cloruro de bario?. Cloruro de bario = BaCl 2
Cuntos moles de tomos de aluminio hay en 135 g de dicho metal?.
Cuntas molculas de propano hay en 0,88 g del mismo? Propano = C 3H8
Cuntas molculas hay en 2 cm3 de agua?. La densidad del agua es 1 g/cm3. Agua = H2O
Cuntos cm3 de etanol deben medirse en una probeta, para tener 0,5 moles de etanol?. La
densidad del etanol es 0,789 g/cm3. Etanol C2OH6
Disponemos de 100 gramos de Fe2(SO4)3. Cuntas molculas contienen?. Cuntos tomos de
hierro?. Cuntos tomos de oxgeno?. Cuntos tomos de azufre?.
Tabla de masas atmicas
También podría gustarte
- Mol - Concepto y EjerciciosDocumento7 páginasMol - Concepto y EjerciciosMiguel Angel Olivares100% (1)
- Cálculos químicos: conversiones entre moles, moléculas y átomosDocumento2 páginasCálculos químicos: conversiones entre moles, moléculas y átomosAlejandra MoraAún no hay calificaciones
- Taller de Mol y Relaciones de Masa 2.2 Quimica UnoDocumento4 páginasTaller de Mol y Relaciones de Masa 2.2 Quimica Unoharry j o ruiz0% (1)
- Qué Es Un Mol BRAYANDocumento10 páginasQué Es Un Mol BRAYANBrayan RamirezAún no hay calificaciones
- 4 ESO. Fundamentos de química: masa atómica, masa molecularDocumento8 páginas4 ESO. Fundamentos de química: masa atómica, masa molecularSonia MorenoAún no hay calificaciones
- Concepto de Mol y Numero de AvogadroDocumento3 páginasConcepto de Mol y Numero de AvogadrojhonjisAún no hay calificaciones
- Mol ActividadesDocumento6 páginasMol Actividadesluciano1987Aún no hay calificaciones
- Magnitudes Atómico Moleculares ESTDocumento19 páginasMagnitudes Atómico Moleculares ESTPablo CancliniAún no hay calificaciones
- Guia Quimica NM2 - Guia Reforzamiento N°1Documento7 páginasGuia Quimica NM2 - Guia Reforzamiento N°1Damy Clavijo SepulvedaAún no hay calificaciones
- Definición de MolDocumento10 páginasDefinición de Molrodrigo Aragón100% (1)
- Cálculos estequiométricos y su importancia en procesos químicosDocumento37 páginasCálculos estequiométricos y su importancia en procesos químicosPau AdornoAún no hay calificaciones
- Fórmulas químicas, masa molar, moles y composición porcentualDocumento4 páginasFórmulas químicas, masa molar, moles y composición porcentualCarolina AguileraAún no hay calificaciones
- Qué Es Un MolDocumento6 páginasQué Es Un MolLINDA LILIETH TAPIAS ZAMBRANOAún no hay calificaciones
- LEYES-PONDERALES-ESTEQUIOMETRIA MOL AlimentosDocumento26 páginasLEYES-PONDERALES-ESTEQUIOMETRIA MOL Alimentostatiana Huillca QuispeAún no hay calificaciones
- Los globos de helio pesanDocumento9 páginasLos globos de helio pesanemerson alejandro basto alvaradoAún no hay calificaciones
- PreparacionDocumento4 páginasPreparacionDrakøAún no hay calificaciones
- Leyes Ponderales EstequiometriaDocumento26 páginasLeyes Ponderales EstequiometriaVittaAún no hay calificaciones
- Leyes Ponderales EstequiometriaDocumento23 páginasLeyes Ponderales EstequiometriajuanAún no hay calificaciones
- F2 MolDocumento4 páginasF2 MoluliAún no hay calificaciones
- Mol masa relativaDocumento11 páginasMol masa relativaJuanC27Aún no hay calificaciones
- Las Cantidades en La Química-El MolDocumento7 páginasLas Cantidades en La Química-El MolLeandro Lisowiec SonclaireAún no hay calificaciones
- Masa atómica y molecularDocumento10 páginasMasa atómica y molecularJorge Ramon100% (1)
- MOLDocumento27 páginasMOLAlejandro MartinezAún no hay calificaciones
- ÁTOMO, MATERIA Y CONVERSIONESDocumento5 páginasÁTOMO, MATERIA Y CONVERSIONESRobinson jhovanny gutierrez velasquesAún no hay calificaciones
- Quimica Del Carbono - Unidad 3 (Guia Especial Estequiometria)Documento9 páginasQuimica Del Carbono - Unidad 3 (Guia Especial Estequiometria)Martin CrispinoAún no hay calificaciones
- T5 F4 Mol 1SOLDocumento4 páginasT5 F4 Mol 1SOLLaura FernándezAún no hay calificaciones
- INVESTIGACIÓNDocumento8 páginasINVESTIGACIÓNNaoki ParkAún no hay calificaciones
- A) B) El Número de Moléculas. C) Los Moles de CarbonoDocumento5 páginasA) B) El Número de Moléculas. C) Los Moles de CarbonoWILSON STEVEN BEDOYA DIAZAún no hay calificaciones
- Ejercicios de Estequiometria I MedioDocumento10 páginasEjercicios de Estequiometria I MedioGuillermo Paniagua Valdebenito100% (1)
- Cantidades y Reacciones Químicas Tema 4Documento31 páginasCantidades y Reacciones Químicas Tema 4Josue alonsoAún no hay calificaciones
- 04 SOLUCIONES Ejercicios Cantidad de SustanciaDocumento4 páginas04 SOLUCIONES Ejercicios Cantidad de SustancialexabethAún no hay calificaciones
- Clase 2. INQ-111Documento14 páginasClase 2. INQ-111Alejandro LorenzoAún no hay calificaciones
- Leyes Ponderales EstequiometriaDocumento30 páginasLeyes Ponderales EstequiometriaAlejandra ParraAún no hay calificaciones
- Magnitudes Atómico Moleculares ESTDocumento17 páginasMagnitudes Atómico Moleculares ESTNoelia BaezAún no hay calificaciones
- FQ3 Jes ReaccionesDocumento11 páginasFQ3 Jes Reaccionesisabel montillaAún no hay calificaciones
- Taller 10° Masa Molecular ListoDocumento5 páginasTaller 10° Masa Molecular ListoANDREA TORRESAún no hay calificaciones
- 4° Medio Plan Comun Quimica EjerciciosI EstequimetriaDocumento10 páginas4° Medio Plan Comun Quimica EjerciciosI EstequimetriaDaniel Alejandro Rodríguez PérezAún no hay calificaciones
- Estequiometria y Formula Empirica y MolecularDocumento54 páginasEstequiometria y Formula Empirica y Molecularjuansari2019Aún no hay calificaciones
- Mol, Masa Molar, No Avogadro TeamsDocumento26 páginasMol, Masa Molar, No Avogadro TeamsJoanna RodriguezAún no hay calificaciones
- EstequiometríaDocumento46 páginasEstequiometríadanaAún no hay calificaciones
- Informe 2 CompletoDocumento9 páginasInforme 2 CompletoAlex GuillenAún no hay calificaciones
- Masa atómica, molecular y el concepto de mol en químicaDocumento7 páginasMasa atómica, molecular y el concepto de mol en químicamariaAún no hay calificaciones
- La Mol D LuchisDocumento2 páginasLa Mol D LuchisLuis Carlos MosqueraAún no hay calificaciones
- Leyes Ponderales EstequiometriaDocumento31 páginasLeyes Ponderales EstequiometriaDiego Soto RoaAún no hay calificaciones
- El NÚMERO DE AVOGADRO PDFDocumento4 páginasEl NÚMERO DE AVOGADRO PDFalex huamanAún no hay calificaciones
- Texto4°Final (2020) PDFDocumento142 páginasTexto4°Final (2020) PDFOscar Zegarra0% (1)
- ESTEQUIOMETRIADocumento21 páginasESTEQUIOMETRIAABOGADO & INGENIEROAún no hay calificaciones
- DEFINICIÓN DEL MOL Y SUS APLICACIONESDocumento29 páginasDEFINICIÓN DEL MOL Y SUS APLICACIONESRoberto Santiago0% (1)
- Peso MolecularDocumento16 páginasPeso MolecularDocente Juanpablino 31Aún no hay calificaciones
- 349 BFoZ360YJB 2020-09-13 67Documento13 páginas349 BFoZ360YJB 2020-09-13 67Cristian SolisAún no hay calificaciones
- Número de Avogadro Ejercicios - Docx BASICODocumento8 páginasNúmero de Avogadro Ejercicios - Docx BASICOAndrea CatutoAún no hay calificaciones
- EsteqDocumento12 páginasEsteqOrlando RGAún no hay calificaciones
- EstequiometriaDocumento12 páginasEstequiometriaMariajoAún no hay calificaciones
- Mol. Masa Atómica y Masa Molecular.Documento4 páginasMol. Masa Atómica y Masa Molecular.pinedarodrigueseAún no hay calificaciones
- Estequiometría Unidades Químicas de MasaDocumento4 páginasEstequiometría Unidades Químicas de MasaRoland M Reyes100% (1)
- Ejercicios de Estequ 540038 Downloadable 4285068Documento11 páginasEjercicios de Estequ 540038 Downloadable 4285068averosdavid7Aún no hay calificaciones
- Repartido Cantidad QuimicaDocumento3 páginasRepartido Cantidad QuimicaNacholin 360Aún no hay calificaciones
- La masa de un molDocumento43 páginasLa masa de un molDavidAún no hay calificaciones
- Problemas de Entretenimiento e Ingenio MatemáticoDe EverandProblemas de Entretenimiento e Ingenio MatemáticoAún no hay calificaciones
- Transferencia 36 EjerciciosDocumento40 páginasTransferencia 36 EjerciciosjohanaAún no hay calificaciones
- Practica #12 Gelatinizacion de Almidon en Harinas InstantaneasDocumento15 páginasPractica #12 Gelatinizacion de Almidon en Harinas InstantaneasMarisabel Sarmiento MillioAún no hay calificaciones
- Apuntes de Cromatografia 02 15 20111Documento130 páginasApuntes de Cromatografia 02 15 20111adnil1402100% (1)
- Revisar Entrega de Examen: Semana 8: Sumativa 5 - ControlDocumento2 páginasRevisar Entrega de Examen: Semana 8: Sumativa 5 - ControlnelsonAún no hay calificaciones
- Laboratorio Semana 9 Uso y Cuidados Del PotenciometroDocumento4 páginasLaboratorio Semana 9 Uso y Cuidados Del Potenciometroroyser avellaneda alarconAún no hay calificaciones
- Informe Tema 1Documento14 páginasInforme Tema 1Daniel Vargas TrujilloAún no hay calificaciones
- Metodos ASTM Analisis para DieselDocumento3 páginasMetodos ASTM Analisis para Dieselcayofurio2Aún no hay calificaciones
- Adsorcion CuizanoVargas NormaDocumento181 páginasAdsorcion CuizanoVargas NormaDavid OsorioAún no hay calificaciones
- Medición de presión con manómetrosDocumento19 páginasMedición de presión con manómetrosDalmiro LopezAún no hay calificaciones
- Cuestionario de 100 PreguntasDocumento10 páginasCuestionario de 100 PreguntasUlises OlveraAún no hay calificaciones
- Asignación 5Documento4 páginasAsignación 5Grecia Cajigas VelásquezAún no hay calificaciones
- Preparación de Disoluciones y Determinación Del PHDocumento6 páginasPreparación de Disoluciones y Determinación Del PHStephani R. GiraldoAún no hay calificaciones
- Descomposicion de Los EcosistemaDocumento3 páginasDescomposicion de Los EcosistemaIrene Harris100% (1)
- Grupos Iv A y Vi ADocumento6 páginasGrupos Iv A y Vi AMarvin Veizaga ClarosAún no hay calificaciones
- Evaluación TEORIA CINETICA IIIPDocumento2 páginasEvaluación TEORIA CINETICA IIIPJuan BermúdezAún no hay calificaciones
- Marco Teorico y ObjetivosDocumento3 páginasMarco Teorico y ObjetivosDarla Monserar Santin VidalAún no hay calificaciones
- Formulacion Inorganica Iupac 2005Documento8 páginasFormulacion Inorganica Iupac 2005Deisy HernandezAún no hay calificaciones
- 02 Bioenergetica y TermodinámicaDocumento48 páginas02 Bioenergetica y TermodinámicaJhordy Mamani100% (1)
- FISICADocumento8 páginasFISICAMiguel Ángel Cardenas AbrilAún no hay calificaciones
- Electroquímica Tema1 2023Documento15 páginasElectroquímica Tema1 2023Maria Celina MoyanoAún no hay calificaciones
- Proceso Obtención GasolinaDocumento45 páginasProceso Obtención GasolinaErick CabezasAún no hay calificaciones
- Balance de Reacciones RedoxDocumento5 páginasBalance de Reacciones RedoxARMY CARATAún no hay calificaciones
- Jhoan Grullon - 1097919 PRACTICA #7Documento5 páginasJhoan Grullon - 1097919 PRACTICA #7CapeexAún no hay calificaciones
- Quiz - Primer Corte - 2017 - 1Documento2 páginasQuiz - Primer Corte - 2017 - 1maicolahumedom84Aún no hay calificaciones
- Isocorica LAB 7Documento18 páginasIsocorica LAB 7Enrique Neyra FloresAún no hay calificaciones
- Items Fisica YesidDocumento6 páginasItems Fisica YesidyesidgomezcmgacAún no hay calificaciones
- Produccion de Acido NitricoDocumento28 páginasProduccion de Acido NitricoluzbendezuAún no hay calificaciones
- TEMA 3 CALOR Y TRABAJO MECANICO V2 Santa CruzDocumento70 páginasTEMA 3 CALOR Y TRABAJO MECANICO V2 Santa CruzFabiana CuellarAún no hay calificaciones
- Intercambiadores de calor: tipos y clasificaciónDocumento35 páginasIntercambiadores de calor: tipos y clasificaciónJ Val Palomino ChaucaAún no hay calificaciones
- Aldehidos y Cetonas Laboratorio FundamentosDocumento5 páginasAldehidos y Cetonas Laboratorio Fundamentosmaga_azulAún no hay calificaciones