Documentos de Académico
Documentos de Profesional
Documentos de Cultura
2do Trabajo de Hidro... Electrolisis Del Alumino
Cargado por
ronxx0 calificaciones0% encontró este documento útil (0 votos)
44 vistas33 páginasEl documento describe el proceso de electrólisis del aluminio. Explica que la electrólisis es un proceso para separar un compuesto en sus elementos usando electricidad. Luego detalla que la producción de aluminio involucra la extracción de bauxita, producción de alúmina y electrólisis del aluminio, donde la alúmina es reducida a aluminio líquido a altas temperaturas en celdas electrolíticas. Finalmente, resume las aplicaciones extensas del aluminio en la industria y vida cotidiana.
Descripción original:
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoEl documento describe el proceso de electrólisis del aluminio. Explica que la electrólisis es un proceso para separar un compuesto en sus elementos usando electricidad. Luego detalla que la producción de aluminio involucra la extracción de bauxita, producción de alúmina y electrólisis del aluminio, donde la alúmina es reducida a aluminio líquido a altas temperaturas en celdas electrolíticas. Finalmente, resume las aplicaciones extensas del aluminio en la industria y vida cotidiana.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
44 vistas33 páginas2do Trabajo de Hidro... Electrolisis Del Alumino
Cargado por
ronxxEl documento describe el proceso de electrólisis del aluminio. Explica que la electrólisis es un proceso para separar un compuesto en sus elementos usando electricidad. Luego detalla que la producción de aluminio involucra la extracción de bauxita, producción de alúmina y electrólisis del aluminio, donde la alúmina es reducida a aluminio líquido a altas temperaturas en celdas electrolíticas. Finalmente, resume las aplicaciones extensas del aluminio en la industria y vida cotidiana.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 33
REPBLICA BOLIVARIANA DE VENEZUELA
UNIVERSIDAD CENTRAL DE VENEZUELA
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE LOS MATERIALES
DEPARTAMENTO DE METALURGIA QUMICA
HIDRO Y ELECTROMETALURGIA
PROF. J. RUS
CARACAS, 11/12/2012
ELECTRLISIS DEL ALUMINIO. EQUIPO Y PROCESOS.
INTEGRANTES:
WANNY DIAZ C.I 20.330.595
LUIS VICENTE RIVERO C.I 19.276.988
INTRODUCCION
La mayor parte de los metales industriales se conocen desde muchas
dcadas atrs, sin embargo la historia del aluminio apenas se remonta ms all
del ltimo siglo. El carcter tardo del descubrimiento de este metal obedece a
diversas razones. Si bien es el ms extendido por la naturaleza despus del silicio,
no se encuentra jams en estado nativo. Por otra parte las rocas o tierras en las
cuales se presenta no ofrecen las caractersticas que llamaban la atencin de los
antiguos buscadores de minerales. Una vez descubierto el ALUMINIO es
importante resaltar que es uno de los elementos ms abundantes de la corteza
terrestre, sus excelentes propiedades de conduccin de calor y electricidad, hacen
de este elemento uno de los ms usados en la vida cotidiana, debido a que su
ventaja ms interesante es su ligereza ya que pesa tres veces menos que el
acero.
Uno de los mtodos de obtencin del aluminio es la electrolisis de dicho
mineral, que se define como el proceso para separar un compuesto en los
elementos que los conforman, usando para ella la electricidad, el mismo se lleva a
cabo por medio de un proceso llamado Hall- Herault.La electrlisis industrial tiene
lugar en cubas electroqumicas que actan a la vez como hornos de fusin y
electrolizadores. La parte catdica (negativa) est formada por una cuba abierta,
rectangular, de chapa de acero, con revestimiento de aislante trmico, refractario
y el fondo de carbono con rales de acero incrustados para la conduccin de la
corriente catdica. La parte andica (positiva) es un electrodo de carbono que
permite diferenciar el tipo de celda empleada. En la actualidad se utilizan dos
variantes principales, las que tienen nodos mltiples precocidos y las de nodo
autococido o nodo Soderberg.
En el trabajo a continuacin se explicara detalladamente los procesos
pertinentes para obtener el ALUMINIO, as tambin las reacciones involucradas,
equipos y principales funcionamiento; tomando en cuenta la evolucin industrial de
las cubas electrolticas.
ELECTROLISIS DEL ALUMINIO
Electrlisis:
Concepto
La Electrlisis es un proceso para separar un compuesto en los elementos
que lo conforman, usando para ello la electricidad. La palabra Electrlisis viene de
las races electro, electricidad y lisis, separacin.
Tambin es parte de la qumica que trata de la relacin entre las corrientes
elctricas y las reacciones qumicas, y de la conversin de la energa qumica en
elctrica y viceversa. En un sentido mas amplio, la electrolisis es el estudio de las
reacciones qumicas que producen efectos elctricos y de los fenmenos qumicos
causados por la accin de las corrientes o voltajes.
Aplicaciones de la Electrlisis
Produccin de Aluminio, Litio, Sodio, Potasio y Magnesio
Produccin de Hidrgeno con mltiples usos en la industria: como
combustible, en soldaduras, etc.
Produccin de Cloro, Hidrxido de Sodio, Clorato de Sodio y Clorato de
Potasio.
La Electrometalurgia es un proceso para separar el metal puro de
compuestos usando la electrlisis. Por ejemplo, el Hidrxido de sodio es
separado en Sodio puro, Oxgeno Puro y agua.
La Anodizacin es usada para proteger los metales de la corrosin,
La Galvanoplastia, tambin usada para evitar la corrosin de metales, crea
una pelcula delgada de un metal menos corrosivo sobre otro metal.
Aluminio;
Es uno de los elementos ms abundantes de la corteza terrestre de la cual
forma ms del 7%, sin embargo fue descubierto a principios del siglo XIX.
El Aluminio (Al) es un excelente conductor de calor y de electricidad. Su
mayor ventaja es su ligereza, pues pesa casi tres veces menos que el acero
ordinario.
La Bauxita, la cual se presenta generalmente en forma de mezcla de
Gibsita Al(OH)
3
y Caolinita Al
2
Si
2
O
5
(OH)
4
, y que se conoce tambin como
boehmita, es la materia prima de la cual se obtiene la almina, del procesamiento
de esta se obtiene el Aluminio. Este procesamiento exige un alto consumo de
energa elctrica, debido a esto se dice que la energa elctrica es materia prima
esencial en la obtencin del Aluminio.
Este metal posee una combinacin de propiedades que lo hacen muy til
en ingeniera de materiales, tales como su baja densidad (2.700 kg/m
3
) y su alta
resistencia a la corrosin. Mediante aleaciones adecuadas se puede aumentar
sensiblemente su resistencia mecnica (hasta los 690 MPa). Es buen conductor
de la electricidad y del calor, se mecaniza con facilidad y es relativamente barato.
Por todo ello es desde mediados del siglo XX
el metal que ms se utiliza despus
del acero.
Aplicaciones:
El Aluminio es empleado para construir utensilios de uso domstico, y en
aleacin con el hierro y otros metales, se utiliza en la construccin de vehculos,
tales como aviones, trenes, automviles, etc., y tambin para la edificacin de
puentes y edificios de muchas plantas, sus aplicaciones son cada da ms
numerosas. Por otro lado, la Bauxita aparte de servir como materia prima para la
obtencin del Aluminio, tiene otros importantes usos industriales, como en la
fabricacin de material refractario, abrasivos, qumicos, cementos y procesos de
refinacin de hidrocarburos.
La utilizacin industrial del aluminio ha hecho de este metal uno de los ms
importantes, tanto en cantidad como en variedad de usos, siendo hoy un material
polivalente que se aplica en mbitos econmicos muy diversos y que resulta
estratgico en situaciones de conflicto. Hoy en da, tan slo superado por el
hierro/acero. El aluminio se usa en forma pura, aleado con otros metales o en
compuestos no metlicos. En estado puro se aprovechan sus propiedades pticas
para fabricar espejos domsticos e industriales, como pueden ser los de
los telescopios reflectores. Su uso ms popular, sin embargo, es como papel
aluminio, que consiste en lminas de material con un espesor tan pequeo que
resulta fcilmente maleable y apto por tanto para embalaje alimentario. Tambin
se usa en la fabricacin de latas.
Dado que, a igual longitud y masa, el conductor de aluminio tiene ms
conductividad, resulta un componente til para utilidades donde el exceso de peso
es importante. Es el caso de la aeronutica y de los tendidos elctricos donde el
menor peso implica en un caso menos gasto de combustible y mayor autonoma, y
en el otro la posibilidad de separar las torres de alta tensin.
Adems de eso, aleado con otros metales, se utiliza para la creacin de
estructuras portantes en la arquitectura y para fabricar piezas industriales de todo
tipo de vehculos y calderera. Tambin est presente en enseres domsticos tales
como utensilios de cocina y herramientas. Se utiliza as mismo en la soldadura
aluminotermia y como combustible qumico y explosivo por su alta reactividad.
Como presenta un buen comportamiento a bajas temperaturas, se utiliza para
fabricar contenedores criognicos.
Proceso:
La produccin de aluminio consiste de 3 pasos: Extraccin de bauxita,
produccin de almina y Electrolisis del aluminio.
Con un porcentaje de 8%, el aluminio es el tercer metal ms abundante en
la superficie de la tierra. La materia prima para la produccin de aluminio, bauxita,
esta compuesta principalmente por uno o ms componentes de hidrxido de
aluminio y oxido de titanio como las principales impurezas.
Extraccin de bauxita:
La bauxita es extrada principalmente por mtodos de mina abierta. Los cuales
tienen un bajo impacto en el ambiente. Los principales aspectos ecolgicos a
considera estn relacionados con la limpieza del suelo, impacto en la flora y fauna
local y la erosin del suelo. Cuatro toneladas de bauxita son requeridas para
producir dos toneladas de almina, las cuales producirn una tonelada de aluminio
en una reductora.
Produccin de almina:
La bauxita tiene que ser convertida en oxido de aluminio puro (almina) antes de
que pueda ser transformada en aluminio por medio de la electrolisis. Esto es
realizado a travs del uso del proceso qumico Bayer en las refineras de almina.
El oxido de aluminio es separado de las otras sustancias de la bauxita mediante
una solucin de soda caustica; la mezcla obtenida es filtrada para remover todas
las partculas insolubles. Despus de esto, el hidrxido de aluminio es precipitado
de la solucin de soda, lavado y secado, mientras que la solucin de soda es
reciclada.
Electrolisis de aluminio:
El aluminio primario es producido en plantas de reduccin, donde el aluminio puro
es extrado de la almina por medio del proceso Hall-Hrault. El proceso de
reduccin de almina en aluminio liquido es realizado a una temperatura promedio
de 950 grados Celsius en un ao fluorinado y bajo una alta intensidad de corriente.
Este proceso es realizado en celdas electrolticas, donde los ctodos de carbn
forman el fondo de la celda y actan como electrodo negativo.
Proceso Hall-Hrault y Proceso Bayer
El proceso Hall-Hrault:
Es el principal proceso de obtencin de aluminio.
En este proceso la almina (Al
2
O
3
) es disuelta dentro de una cuba
electroltica revestida interiormente de carbn en un bao electroltico
con criolita (Na
3
AlF
6
) fundida. La cuba acta como ctodo, mientras que como
nodos se suelen utilizar unos electrodos de carbn de Soldberg. La reaccin
qumica total es la siguiente (no esta del todo bien):
Al
2
O
3
+ 3 C 2 Al + 3 CO
La almina se descompone en aluminio y oxgeno molecular. Como el aluminio
lquido es ms denso que la criolita se deposita en el fondo de la cuba, de forma
que queda protegido de la oxidacin a altas temperaturas. El oxgeno se deposita
sobre los electrodos de carbn, quemndose y produciendo el CO
2
.
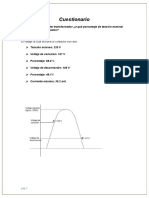
Los parmetros del proceso son los siguientes:
Tensin: 5-6 V.
Densidad de corriente: 1,5-3 A/cm
2
, lo que supone una corriente de 150 000
amperios.
Los electrodos han de estar siempre a la misma altura, por lo que hay que
regularlos ya que se van descomponiendo durante la reaccin.
Hay que controlar que la proporcin de almina sea constante durante el
proceso, por lo que habr que ir vertiendo ms segn avance el proceso.
Este proceso fue descubierto independientemente en 1886 por el
estadounidense Charles Martin Hall y el francs Paul Hrault. Resulta curioso que
ambos cientficos naciesen y muriesen en las mismas fechas y que patentaran su
descubrimiento con tan poca diferencia sin conocerse.
Este proceso se usa en todo el mundo y es el nico utilizado actualmente por la
industria para producir aluminio.
Recuerden que un compuesto inico en estado slido no conduce la
corriente elctrica. Los iones no pueden moverse libremente transportando carga
elctrica cuando estn formando parte de la red cristalina. En cambio, s pueden
hacerlo en estado fundido (vean las actividades Iones I y II).
La temperatura de fusin de la almina (Al
2
O
3
) es superior a los 1500 C. El
costo en energa y construccin de un reactor que opere a tan alta temperatura es
muy elevado. Sin embargo, una mezcla de almina y criolita (Na
3
AlF
6
) funde a
1000 C, aproximadamente. La criolita entonces acta como fundente.
En la celda electroltica tiene lugar la siguiente reaccin:
El carbono es el material que constituye el nodo (electrodo positivo de la
celda), y dado que se forma CO
2
(g), ste se va consumiendo, es decir, que las
barras de carbono son un insumo en la produccin del aluminio.
El aluminio no puede ser producido por la electrlisis de una sal de aluminio
disuelto en el agua debido a la alta reactividad del aluminio con los protones del
agua y la subsiguiente formacin de hidrgeno. Como, en una solucin acuosa,
los protones (H
+)
son preferentemente reducido a hidrgeno atmico antes de
iones Al
3 +,
la reduccin de Al
3 +
se realiza por electrlisis de una sal de aluminio
fundido. Este es un medio libre de agua y, por tanto, la reduccin de H
+
es
evitada.
En el proceso Hall-Hrault almina , Al
2
O
3,
se disuelve en un industrial de
carbono forrado tanque de fundido de criolita , Na
3
AlF
6
( Hexafluoroaluminato de
sodio ), llamada "celda". xido de aluminio tiene un punto de fusin de ms
de 2.000 C (3630 F), mientras que criolita puro tiene un punto de fusin
de 1.012 C (1.854 F). Con un pequeo porcentaje de almina disuelta en ella,
criolita tiene un punto de fusin de aproximadamente 1.000 C (1.830
F)Algunos fluoruro de aluminio , AlF
3
tambin se aade en el proceso para reducir
el punto de fusin de la mezcla de criolita-almina.
La mezcla fundida de criolita, fluoruro de almina, el aluminio es
entonces electrolizada pasando un directo de corriente elctrica a travs de
l. La reaccin electroqumica hace que el metal de aluminio lquido que se
deposita en el ctodo como un precipitado, mientras que el oxgeno de la almina
se combina con el carbono del nodo para producir dixido , CO
2.
Un potencial
elctrico de tres a cinco voltios es necesario para conducir la reaccin, y la tasa de
produccin es proporcional a la corriente elctrica .Una fundicin a escala
industrial consume tpicamente cientos de miles de amperios para cada celda.
La oxidacin del nodo de carbono reduce el voltaje requerido a travs de
cada clula, aumentando la eficiencia elctrica, a un costo de reemplazar
continuamente los electrodos de carbono con otras nuevas, y tambin el coste de
liberar dixido de carbono a la atmsfera . Cientos de Hall-Hrault clulas
normalmente estn conectados elctricamente enserie , y se les
suministra corriente directa (DC) a partir de un nico conjunto
de rectificadores que convierten la corriente alterna (AC) suministrada a
la fbrica en corriente directa. La corriente elctrica muy alta es suministrado a las
clulas a travs de pesados, de baja resistencia elctrica de metal barras de
aluminio puro o cobre . Las clulas son calentados elctricamente para alcanzar
la temperatura de funcionamiento con esta corriente, y el sistema regulador de
nodo vara la corriente que pasa a travs de la clula elevando o bajando los
nodos y el cambio de la resistencia de la clula. Si necesita cualquier clula
puede ser anulada por derivacin barras.
El aluminio lquido es extrado con la ayuda de un sifn de funcionamiento
con un vaco, con el fin de evitar tener que utilizar vlvulas de temperatura
extremadamente alta y bombas. El aluminio lquido puede entonces ser transferida
en lotes o por medio de una lnea de flujo continuo en caliente a una ubicacin en
la que se echa en aluminio lingotes .El aluminio puede ser echado en la forma de
finales de aluminio fundido de los productos, o de los lingotes se pueden enviar en
otros lugares tales como un tren de laminacin a prensar en forma de lminas, o
un molino de trefilado producir alambres de aluminio y cables.
Mientras criolita slido es ms denso que el aluminio slido a temperatura
ambiente, el producto de aluminio lquido es ms denso que la criolita fundida a
temperaturas alrededor de 1.000 C (1.830 F), y los sumideros de aluminio a la
parte inferior de la celda electroltica, donde es peridicamente recogi. La parte
superior y los lados de las clulas estn cubiertas con capas de criolita slida que
actan tambin como aislamiento trmico. La resistencia elctrica inevitable dentro
de cada clula produce suficiente calor para mantener la mezcla de criolita-
almina fundida.
Con el porcentaje de aluminio disuelto en cada clula que se agote por la
electrlisis en la criolita fundida, almina adicional se dej caer continuamente en
las clulas para mantener el nivel requerido de almina. Cada vez que se forma
una costra slida a travs de la superficie del fundido de criolita-almina, esta
costra se rompe de vez en cuando para permitir que la almina aadido a caer en
la criolita fundida y se disuelve all.
El proceso de electrlisis produce gases de escape que se escapa en la
campana de humos y se evacua. El escape est principalmente CO
2
producido a
partir del consumo del nodo y fluoruro de hidrgeno (HF) de la criolita y flujo.
Las partculas tambin se capturan y se reutiliza con electrostticos o filtros de
bolsa. El CO restante
2
generalmente se ventila a la atmsfera.
La gran corriente elctrica que pasa a travs de las celdas electrolticas
genera un campo magntico potente, y esto puede agitar el aluminio fundido
con hidrodinmica fuerzas en clulas correctamente diseadas. La agitacin del
aluminio fundido en cada celda tpicamente aumenta su rendimiento, pero la
pureza del aluminio se reduce, ya que se mezcla con pequeas cantidades de
criolita y fluoruro de aluminio. Si las clulas estn diseadas para no agitar, se
pueden hacer funcionar con grupos estticos de aluminio fundido de modo que las
impurezas ya sea la altura de la parte superior del aluminio metlico, o bien se
hunden hasta el fondo, dejando aluminio de gran pureza en el medio.
Una fuente alternativa de energa, usada por Islandia fundiciones, es la
electricidad geotrmica , que Islandia tiene en abundancia debido a su ubicacin
en la Cordillera del Atlntico Medio , pero no se puede utilizar en el pas debido a
su escasa poblacin. Islandia manera que las importaciones de mineral de
aluminio en bruto y utiliza el proceso Hall-Hroult como un medio de exportar la
electricidad y por lo tanto explotar de manera eficiente es la abundancia de
energa geotrmica.
Muchas dcadas atrs, antes de la existencia de la Autoridad del Valle de
Tennessee , las compaas de aluminio como Alcoa incluso construyeron sus
propias represas hidroelctricas y centrales elctricas en las montaas
Apalaches de Carolina del Norte y Tennessee .
Proceso Bayer:
El proceso Bayer se basa en la variacin de solubilidad en soda castica,
que experimenta el xido de aluminio hidratado con la variacin de temperatura y
concentracin de castica, esto como consecuencia de las propiedades del
hidrxido de aluminio.
En el proceso se plantean bsicamente dos estados de equilibrio:
Primer equilibrio:
Se favorece a alta temperatura y alta concentracin de NaOH. Se produce
la disolucin de los hidratos de almina de la bauxita, mientras que la mayora de
las impurezas no lo hacen.
De manera que se forma una suspensin conteniendo una solucin de aluminato
de sodio y un residuo insoluble "lodos rojos". Reaccin general:
Al2O3 . nH2O + 2NaOH 2NaAlO2 + (n + 1) H2O
Donde n= N de molculas de agua (1 3)
Segundo equilibrio:
Se favorece a baja concentracin de NaOH y baja temperatura. Una vez
que los residuos insolubles han sido separados de la solucin de aluminato, sta
es sembrada con una carga seminal de almina trihidratada, favorecindose
entonces la velocidad de la reaccin anterior en el sentido inverso precipitndose
un xido de aluminio trihidratado.
Purificacin de bauxita, obtencin de almina.
El mineral bauxita se muele y se trata con cal (CaO) en caliente. Por
precipitacin, se separa el material ms grueso (arena). Se enfra la mezcla y
precipita un slido. Este se lava con agua. Luego se calcina (tratamiento a alta
temperatura) y se obtiene finalmente la almina (Al
2
O
3
).
Diagrama de flujo del proceso Bayer.
Los distintos subprocesos del proceso Bayer son:
La digestin de la bauxita molida en una solucin de sosa concentrada, en
la que se produce la reaccin siguiente:
Al2O3 n H2O(s) + 2NaOH(ac) --------- 2NaAlO2(ac) + (n+1) H2O
Mediante el cual se pasa a solucin el aluminio, dejando como residuo
slido inatacado la mayora de las impurezas que le acompaan en la bauxita,
principalmente xidos de hierro y titanio.
El subproceso siguiente es la precipitacin del aluminio de la solucin rica,
lo que se consigue por enfriamiento de aqulla y dilucin, favorecindose la
precipitacin del hidrxido mediante la siembra. La reaccin es la siguiente:
2NaAlO2 (ac) + 4H2O-------- Al2 O3 . 3H2O(s) + 2NaOH(ac)
El hidrato que se precipita es siempre el trihidrato, independientemente de
que, en la bauxita, el aluminio se encuentre como monohidrato (boehmita y
disporo) o trihidrato (gibsita). El producto precipitado se denomina hidrargirita,
bayerita o gibbsita.
Una vez separado el trihidrato, se seca y calcina segn la reaccin:
Al2O3 . 3H2O -------- Al2O3 + 3 H2O
Obtenindose el producto que alimentar las cubas de electrlisis.
El proceso requiere un tancaje importante, pues se procesan muchos miles
de metros cbicos de pulpas y soluciones. Las instalaciones de molienda y
digestin, los reactores, la central de vapor, los equipos de espesado y decantado,
filtrado, lavado y calcinado, hacen que una instalacin actual.
La ubicacin de una planta de almina es un asunto que se estudia hoy
cuidadosamente. La tendencia actual es la construccin de plantas cada vez ms
cerca de los yacimientos de bauxitas. Si no se es pas productor, hay que hacer un
contrato de suministro de bauxita adecuado, y disponer de unas buenas
instalaciones portuarias para dar entrada a grandes buques graneleros.
La slice soluble es fundamentalmente aquella que se introduce con la bauxita en
forma de caolinita. Este mineral arcilloso es atacado con facilidad a las
temperaturas de digestin del proceso Bayer de baja temperatura. Cuando, por
imperativo del tipo de hidrato o hidratos presentes en la bauxita (boehmita o
disporo), se utilizan temperaturas en el entorno de los 240C, tambin es atacada
la slice del cuarzo. Las reacciones, que se producen, son las siguientes:
Al2O32SiO2 . 2H2O(s) + 6NaAl(OH) (ac) -------- 2NaAl(OH) 4(ac) + 2Na2SiO3(ac)
+ H2O
SiO 2(s) + 2Na(OH) (ac) ------------- Na2SiO3(ac) + H2O
La slice disuelta se precipita nuevamente sobre la pulpa en forma de un
producto insoluble, denominado sodalita Bayer, segn la reaccin:
6NaAl(OH) 4(ac) + 6Na2SiO3(ac) + 2NaX(ac) ----------3(Na2O. Al2O3 . 2SiO2
.2H2O). Na2X2(s) + 12Na(OH)(ac)
Donde X puede ser: CO32-, 2AlO2-, 2OH-, SO2-4, etc.
Esta precipitacin sobre los lodos rojos supone una clara prdida de
castico y de almina y, si precipita en el circulo de conduccin de licores ricos, se
produce un encostramiento que llega a recubrir los conductos, inutilizndolos. Por
esta razn, sobre todo, en las plantas modernas que utilizan alta temperatura para
digestin de bauxitas con monohidrato, el problema puede ser tan grave que un
proceso Bayer no puede normalmente tratar menas con ms del 4-5% de slice
soluble incluso aunque se tenga previsto una desilificacin del licor.
Para eliminar la slice del licor se puede adicionar cal en la propia molienda, con lo
que se consigue al menos liberar el reactivo que se quedara atrapado en la
sodalita:
3Ca(OH)2(ac) + Na2SiO3(ac) + 2NaAl(OH)4(ac) --------3(CaO). Al2O3. SiO2(s) +
4Na(OH)(ac) + 5H2O
La slice precipita en forma de silicio-aluminato-triclcico, regenerndose el
reactivo. La almina ligada a este compuesto se pierde en los lodos rojos.
Descripcin del Proceso Bayer
Aunque las condiciones del proceso son influenciadas por el tipo de bauxita
usada, hay 5 etapas principales en todas las plantas. Ellas son:
I. Preparacin de la bauxita.
II. Digestin.
III. Dilucin y separacin de residuos.
IV. Precipitacin.
V. Calcinacin.
Composicin
La presente invencin se refiere a la composicin de un electrolito para la
obtencin de aluminio. El electrolito contiene como fuente de fluoruro de potasio
(KF) una mezcla de KAlF
4
y K
3
AlF
6
(K
1-3
AlF
4-6
- criolita de potasio). La mezcla de
KAlF
4
y K
3
AlF
6
presenta propiedades ventajosas debido a que posee propiedades
higroscpicas bajas, al contrario que el fluoruro potsico y no tiene efecto daino y
agresivo como el KF*HF. La adicin directa de fluoruro potsico en el electrolito
puede ser daina ya que al ser un compuesto muy higroscpico, podra ser la
fuente de agua en el electrolito, algo que se evita utilizando la referida mezcla de
KAlF
4
y K
3
AlF
6
.
La composicin del electrolito de la presente invencin para la obtencin de
aluminio mediante un proceso electroltico comprende los siguientes compuestos:
- Criolita de sodio (Na
3
AlF
6
).
- Almina (Al
2
O
3
).
- Fluoruro de aluminio (AlF
3
).
- Criolita de potasio. La criolita de potasio, utilizada como fuente de KF, se refiere
a una mezcla de KAlF
4
y K
3
AlF
6
, donde el porcentaje en peso vara entre 50-100%
para KAlF
4
y entre 0-50% para K
3
AlF
6
. A partir de ahora nos referiremos a la
mezcla de KAlF
4
y K
3
AlF
6
como criolita de potasio.
Opcionalmente, la composicin de electrolito puede incluir otros
compuestos como el fluoruro de calcio (CaF
2
), fluoruro de magnesio (MgF
2
),
fluoruro de litio (LiF) y fluoruro de sodio (NaF).
Las proporciones en peso de estos componentes puede variar dentro de los
rangos que de indican a continuacin:
a) El porcentaje en peso en la composicin de electrolito de criolita de sodio
(Na
3
AlF
6
) puede ser de 20-80% en peso, el de almina puede variar entre el
2%-5%, el de fluoruro de aluminio puede variar entre el 0% y el 15%.
b) El porcentaje en peso en la composicin de electrolito de criolita de potasio
es de 0,01-80% en peso.
En el caso de que la composicin incluya los componentes opcionales
indicados anteriormente, su composicin en peso se indica a continuacin:
Fluoruro de Calcio 2-5% en peso.
Fluoruro de Magnesio 0-2% en peso.
Fluoruro de Litio 0-3% en peso.
Fluoruro de Sodio 0-5% en peso.
Variables Operativas
Las operaciones que habitualmente se realizan sobre la cuba de electrlisis.
Se describen brevemente a continuacin:
Picada en frio: aportar almina al bao de la cuba para que contine la
electrlisis.
Colada: Obtener el aluminio que se produce. Contribuye a mantener el nivel
de metal y por lo tanto, el equilibrio trmico.
Cambio de agujas: asegurar que la corriente llega desde el crucero hasta el
nodo siguiendo el ciclo del consumo del nodo. Las agujas mantienen el
nodo sujeto al crucero.
Carga de pasta: reponer el consumo del nodo y mantener el nivel de pasta
necesario para garantizar una buena coccin del nodo.
Subida de crucero: para compensar la prdida de carrera de husillo como
consecuencia del consumo de nodo.
Embalajes: es un fenmeno que se produce cuando el bao se empobrece
en almina y se manifiesta con un aumento "repentino" en la tensin.
El embalaje nos asegura que la cantidad de almina introducida en las
picadas en fro ha sido consumida y limpia la superficie inferior del nodo.
Las desventajas que tiene es que hay prdida de productos fluorados, sube
la tensin con prdida energtica y perturba el rgimen de marcha.
Para apagar el embalaje se pica y se introducen los palos de madera para
eliminar la polarizacin del nodo.
Aditivos: para reponer la composicin y nivel de bao: AlF3, costras,
carbonato de litio. Medidas: para tomar decisiones sobre el control y
equilibrio de la cuba.
Regulacin: tanto de intensidad como de tensin para control del equilibrio
de la cuba.
Leyes de Faraday:
Entre 1800-1830 Michael Faraday fsico y qumico ingles, realiz estudios
cuantitativos referente a la relacin entre la cantidad de electricidad que pasa por
una solucin y resultado de sus investigaciones las enuncio entre los aos 1833-
1834 en las leyes que tienen su nombre.
La primera ley de Faraday seala que la masa de una sustancia
involucrada en la reaccin de cualquier electrodo es directamente
proporcional a la cantidad de electricidad que pasa por una solucin.
Muchos metales como el sodio, el magnesio o el aluminio se producen
industrialmente por electrlisis de alguna de sus sales fundidas. En el
proceso se consumen grandes cantidades de electricidad, que pueden
relacionarse matemticamente con la cantidad de producto formado sobre
los electrodos de la celda electroltica. Por ejemplo, durante las electrlisis
del cloruro de sodio, el ion sodio se reduce segn la reaccin:
La carga elctrica transportada por un mol (6,02 1023) electrones equivale
a un Faraday (F), que a su vez es igual a 96500 culombios y se conoce
tambin la constante de Faraday.
La relacin entre la cantidad de cargas invertidas en la produccin de una
determinada masa de producto se resume en el postulado de la primera ley
de Faraday que establece que la masa de producto obtenido o de reactivo
consumido en un electrodo durante la electrlisis, es directamente
proporcional a la cantidad de electricidad en culombios, que pasa a travs
del electrlito.
En trminos matemticos esto es: m = E Q, donde, m es la masa (g)
depositada o liberada, E es el equivalente electroqumico, que relaciona la
masa (g) de un compuesto, capaz de generar o de consumir un mol de
electrones (equivalente qumico), con la caga de estos, es decir, un Farady
(96500 C)
Por ltimo, Q representa la carga invertida, y su valor se obtiene al
multiplicar la intensidad de la corriente por el tiempo transcurrido. La
intensidad de la corriente, I, se expresa en amperios (A) y es la carga que
atraviesa una seccin determinada de un conductor, relacionada con el
tiempo, t. por ejemplo, si una batera suministra una intensidad de 1
amperio durante un tiempo, t, la carga elctrica, Q, que atraviesa la celda
ser: Q = I t.
La segunda Ley, Establece que si varias soluciones electrolticas son
atravesadas por la misma cantidad de electricidad, las masas, m, de las
sustancias depositadas o liberadas en los electrodos son proporcionales a
sus masas equivalentes. O Las masas de diferentes sustancias producidas
por el paso de la misma cantidad de electricidad, son directamente
proporcionales a sus equivalentes gramos.
Esta ley permite calcular la masa de diferentes sustancias depositadas por
la misma cantidad de electricidad.La cantidad de elemento depositado por
un Faraday (96.500 c) se conoce como equivalente electroqumico.
Las dos leyes de Faraday se cumplen para los electrolitos tanto fundidos como en
solucin. Su validez no se altera por variaciones de temperatura, presin, naturaleza
del solvente y del voltaje aplicado.
Entre los muchos factores que influyen en el rendimiento Faraday, que
depende de la marcha de las cubas, podemos destacar cinco:
1. La distancia interpolar, esto es, la distancia que hay entre la superficie
del nodo o plano andico y la parte superior del metal lquido, o lo que es lo
mismo, la altura del bao debajo del nodo. Se ha observado que el
rendimiento Faraday no aumenta cuando la distancia interpolar supera los 50
mm. y por el contrario disminuye notablemente, cuando se reduce por debajo
de los 30 mm.
2. La densidad de corriente, es decir, la intensidad que atraviesa la cuba
dividida por la superficie del nodo. Se sabe que por encima de un valor
determinado ( o,6Ncm2) su influenciables muy dbil. Por debajo de esa cifra
su influencia es notable.
3. Composicin del bao, que debe favorecer la disolucin de la almina.
4. Diseo de la cuba, en sus aspectos de equilibrio trmico y
electromagntico.
5. La temperatura del bao electroltico, que hace que la eficiencia suba
un 3% por cada 10 e que baje la temperatura.
Eficiencia energtica
En nuestro negocio de aluminio que la intencin de hacer ms eficiente la
produccin y asegurar el acceso necesario al poder de almina y elctricos. Los
esfuerzos de mejora giran en torno a la tecnologa de la electrlisis y la capacidad
de un nuevo posicionamiento en lugares donde hay un exceso de poder. La
produccin de aluminio consume mucha energa. Por lo tanto, conceden gran
importancia a soluciones de eficiencia energtica en nuestras plantas. Estamos
desarrollando la tecnologa de clulas mientras que al mismo tiempo que aumenta
el amperaje. De esta manera se pueden producir ms de aluminio, mientras que al
mismo tiempo aumenta la productividad.
Adems, estamos usando menos energa elctrica por tonelada de aluminio
producido. Propietaria proceso electroltico de Hydro se encuentra entre las ms
eficientes del mundo. Se utiliza en las plantas en Sunndal y en Qatar. Innovacin
en las plantas existentes gira principalmente en torno a las continuas mejoras en
la tecnologa y nuestra metodologa de trabajo.
Equipos
La cuba
El anlisis del aluminio puede hacerse hoy en da a partir de cubas de
electrlisis. La corriente elctrica conducida a la cuba por un juego de barras
conductoras se convierte en el sistema andico, atraviesa el bao de criolita en
fusin que contiene la almina, donde la electrlisis se efecta, se rene en el
sistema catdico en forma de crisol que contiene el bao y abandona la cuba por
otras barras conductoras que la llevan a la cuba siguiente. La cuba est
constituida por cuatro partes:
Los conductores. Se trata de una serie de barras conductoras de aluminio
que transporta la corriente de una cuba a la otra, en condiciones
econmicas, creando perturbaciones magnticas tan dbiles como sea
posible. Los colectores catdicos recogen la corriente a lo largo del ctodo
de una cuba; las subidas positivas suben hasta el nivel del nodo siguiente.
En l la densidad de la corriente va de 20 a 50 A/cm
2
.
Sistema andico. La densidad de corriente se reduce a un valor que
convenga para la electrlisis: menos de 1 A/cm
2
. La corriente de las subidas
positivas alimenta un conductor de aluminio horizontal, el cuadro pasa por
un gran nmero de barras verticales de aluminio soldadas o atornilladas
ellas mismas a patas (cubas de nodos precalentados) o a esprragos
(cubas de nodos Sderberg) de hierro que aseguran la unin de barras
con el nodo de carbono bien por medio de anclaje de fundicin, en los
casos de nodos de cubas precalentados, o buen por medio de un anclaje
directo por el carbono, en el caso de las cubas Sderberg. El nodo est
constituido por carbono casi puro.
El consumo de energa en el sistema andico, debe ser mnima tanto en el
carbono como el la cadena de conductores y en los contactos.
El bao: El bao en fusin es la parte activa de la cuba. Es una mezcla
cuaternaria que contiene sobre todo criolita (del 75 al 90%) y de la almina
(1 al 8%), del fluoruro de aluminio (hasta el 10%) y del fluoruro de calcio
(usualmente el 5%). Sobre los bordes del crisol de carbono, as como en su
superficie libre, el bao se solidifica y constituye respectivamente los
taludes y la corteza coronada de almina que se introduce de cuando en
cuando en el bao lquido.
El espesor de la capa de bao entre nodo y ctodo debe ser
suficientemente grande para asegurar un buen rendimiento de corriente y lo
bastante dbil para que el rendimiento de energa se mantenga
conveniente.
El sistema catdico. En ste la densidad de corriente se lleva de nuevo a un
valor conveniente al transporte. Comprende un cajn de palastro, rgido,
rectangular, asentado sobre hormign, que contiene un crisol de bloques
antracitososprecalentados, unidos por una pasta apisonada, el refractario.
El enladrillado representa un papel importante, ya que su constitucin
determina el equilibrio trmico de la cuba. Finalmente las barras catdicas
de acero, barras solera o lingotes, atraviesan el cajn y conectan las barras
conductoras a las cuales estn unidas por flexibles de aluminio. La cantidad
de aluminio producido, que separa el bao del crisol, constituye el ctodo
propiamente dicho.
Avances de las cubas electrolticas al pasar los aos
Cubas Froges 1888. El horno cuadrado: esta cuba sirve para fabricar las
aleaciones Cu-Al. El nodo es nico, largo, mantenido y alimentado por una pinza
de bronce del tipo utilizado en electrotermia. La caja cuadrada de 1x1 m es la
chapa, el ctodo cubierto de revestimiento refractario con barras negativas
ahogadas. La intensidad deba aproximarse a 1000 1500 A, la densidad de
corriente a 3 4 A/cm
2
y el consumo de energa de 90000 kWh/t.
Cubas Froges 1889. La marmita giratoria. Es la primera fbrica de aluminio puro.
El nico nodo es cuadrado, de 25 cm de lado, siempre del tipo empleado en
electrotermia. Tiene el cajn cilndrico en chapa de 62 cm de dimetro, el ctodo
est lleno de revestimiento refractario con negativo de cobre humedecido en
mercurio. El ctodo es giratorio, adaptacin de Hroult para la patente de
fabricacin Kiliani, para producir el cese del efecto andico. Esta rotacin, intil y
costosa puesto que impone el contacto lquido; se suprimi en 1890. La intensidad
alcanza 4000 A, el voltaje 10 V, la densidad de corriente 6,4 A/cm
2
. El consumo de
energa deba ser del orden de 40000 a 50000 kWh/t.
Cubas Froges 1892. Cuba en taza. Es la primera cuba poliandicaprecocida, en
la que el sistema andico no est muy lejos del sistema actual. Cuatro nodos
cuadrados, de 25x25 cm, reciben corriente de un travesao cuadrado. Aparecen
dos gatos de rosca con manubrio. El cajn es de fundicin en forma de taza, con
armazn para hacer que se adhiera el revestimiento refractario. El cajn forma
polo negativo. Marca un progreso considerable sobre las primeras cubas. El
dimetro mide casi 1m. La densidad de corriente es de 1,6 A/cm
2
, lo que
representa tambin un gran progreso. La intensidad alcanza 4000 A. el voltaje de
8 a 10 V, el rendimiento de la corriente 75 % y el consumo de energa de 35 a
40000 kWh/t.
Cuba La Praz 1893. Esta cuba es, en principio, idntica a las precocidas actuales
en cuanto se refiere al sistema andico. Ideas de los perfeccionamientos de la
cuba en forma de taza se percibe: los nodos con barra y pata, blocaje por cua y
no ms los nodos largos de electrotermia; el travesao alargado; y la baja
densidad de corriente de 1,33 A. La cuba contiene seis nodos de 25x25 cm;
funciona a 5000 A, bajo 6 7 V. Segn ensayos contradictorios en presencia de
Kiliani y Hroult esta cuba tiene un rendimiento de corriente del 77 % y consume
26000 kWh/t, cantidad extraordinaria para la poca.
Cuba La Praz 1894
Cuba Calypso 1891
Cuba Calypso 1895. Se utiliza el procedimiento Hall en principio, ya que la
realizacin difiere ya mucho de la patente Hall caracterizado, por un bao cido
muy cargado de fluoruro de calcio. Los nodos son pequeos y numerosos. El
ms interesante se compone de cuarenta y cuatro nodos en cuatro lneas. Los
nodos cilndricos son de 10 cm de dimetro aproximadamente. La densidad de
corriente es de 2,3 A/cm
2
, la intensidad de 8000 A bajo 7,5 V; el consumo de
energa de 30000kWh/t. Estas son las cubas ms potentes de la poca que
poseen una caracterstica nueva: la lmpara que seala los efectos andicos,
stos se paran por atizamiento bajo el nodo, casi como hoy. El cajn sirve como
negativo y est unido a los conductores de corriente por orejas. El ctodo est
lleno de refractario, cocido en un horno especial antes del arranque.
Cuba la Praz 1898
Cubas Saint-Jean 1907 Calypso 1910.Estas son cubas de 10000 A bajo 7 V
aproximadamente con diez nodos 28x28 cm, despus cubas de 12000 A de doce
nodos 28x28 cm, funcionando ambas con una densidad de corriente de 1,4
A/cm
2
aproximadamente, que equipan la nueva fbrica Saint-Jean. Su consumo
de energa es del orden de 25000 kWh/t. Otras cubas muy similares, si no es por
el nmero de nodos, se instalan en Calypso en 1910. Comprenden lingote
acanalado y el cajn ovalado.
Cubas Chedde y Auzat.
La explotacin Industrial 1914-1939 en la compaa Pechiney
Cubas Saint-Jean 1914.Una serie de cuarenta cubas 20000 A con doce nodos
43x43 cm, de densidad de corriente 1,2 A/cm
2
se construye con losas en los
lados, ctodo lleno de refractario, lingote de fundicin acanalado. Su rendimiento
alcanza casi al de las cubas de 12000.
Cubas La Praz 1918.
Ctodos 1924-1927. Ensayos decisivos sobre los ctodos se emprendieron
primeramente, en Saint-Jean sobre cubas de 20000 A llamadas americanas, que
comprenden un lingote liso con bloques anclados en el refractario sobre este
lingote. Calypso y La Saussaz hacen los primeros ensayos de anclaje a la
fundicin; IArgentire reanuda estos ensayos y en lugar de anclar directamente
lingote y bloque, ancla la fundicin sobre el lingote con ayuda de una cabeza de
perno que sobre pasa el lingote y sobre el bloque por una ranura de 2 cm de
altura. En 1927, Chedde sustituye el lingote liso por una serie de barras de acero
ancladas en la fundicin con una ranura de cada bloque. La masa de fundicin de
anclaje continua siendo muy importante ya que se envuelven todas las barras en
la misma masa, pero la cada catdica pasa a ser de unos 0,2 V. Fue unos aos
mas tarde cuando nuestros ctodos actuales aparecen: anclaje a la fundicin de
las barras en las ranuras de los bloques, siendo cada barra independiente a las
dems. La cada catdica sube un poco (0,3 V) pero la duracin de vida pasa de 2
a 4 5 aos, la construccin es mucho menos costosa y sobre todo el
calorifugado del ctodo aumenta.
Cubas 50000 A 1937. Las primeras cubas de este tipo se construyen en
lrgentire en 1937. Llevan veinte nodos 35x65 cm, con una densidad de
corriente de 1,1 A/cm
2
bajo una tensin aproximada de 5,6 V. El rendimiento de
Faraday alcanza el 80 % aproximadamente y el consumo de energa 21000 kWh/t.
Cubas con nodo Sderberg
A los largo de este perodo, las cubas con nodo Srderberg han hecho su
aparicin. La primera era una cuba de 8000 A instalada en Vigeland en Noruega,
con un nodo nico y chimenea axial (1924).
Cubas 1925, 9000 A.
Cubas 1927, 11000 ARiouproux. Una primera mejora decisiva se lleva a cabo
por la sustitucin de nervios de la placa. La camisa lleva dos serie de nervios:
unos internos, que aseguran un buen contacto camisa-pasta, y los otros externos,
sobre los cuales estn enroscadas las conducciones de corriente. A cada andica
pasa de 0,5 a 0,8 V.
Cubas 1930, 11000 A Riouproux.
Cubas 1930, 22000 A Riouproux.Se busca aumentar inmediatamente la
potencia (22000 A) obtenida por dos nodos rectangulares. Pero al comprobar la
imposibilidad de poner en funcionamiento dos electrodos en paralelo en el mismo
crisol, se vuelve a los nodos nicos.
Cubas 1935, 33000 A Riouproux.
Poco despus de 1930, los baos bsicos hasta entonces se volvieron
progresivamente cidos. Correlativamente, las temperaturas de funcionamiento
descendieron hacia los 960C. Los baos bsicos no daban ms que mediocres
rendimientos de corriente prximos al 75%; ya en 1939, una acidificacin ligera
haba permitido obtener mas del 80%.
Perodo contemporneo 1939-1962 (Pechiney)
Cubas Sderberg con cuas verticales La Praz
Cubas Precocidas Saint-Jean 1951. Estas son cubas de 100000 A, provistas de
veintisis nodos de 40x83 cm, que funcionan a 5,1V y consumen en esta poca
unos 18000kWh/t.
Cubas Sderberg Saint-Jean 1952con cuas verticales. Alcanzo rpidamente
excelentes resultados: 16000kWh/t para un rendimiento de Faraday del 90% y una
tensin de 4,8 V permitan, desde el origen, reducir la mano de obra alrededor de
7h/t de aluminio.
Cubas Auzat 1956 con cuas verticales. Cubas de ensayo de 150000 A, las ms
potentes del mundo, se pusieron en marcha. Se tropez en seguida con una
dificultad, ya encontradas en las precocidas 100000 A y las Sderberg 100000 A:
la existencia de efectos magnticos muy marcados que, sobre las cubas de alta
intensidad, perjudican al rendimiento Faraday.
Naturalmente las mejores cubas en explotacin industrial de cada categora
obtienen mejores resultados de aproximadamente 13000 y 14000 kWh/t para las
precocidas y de Sderberg respectivamente.
Cuba v350
El aluminio es producido en celdas electrolticas, donde las materias primas
son bsicamente almina, electricidad y carbn. La produccin de las celdas es
proporcional a la corriente de operacin de las mismas.
La celda V-350, desarrollada por el grupo de Investigacin y Desarrollo de
CVG-Venalum, es una celda de reduccin electroltica de alto amperaje, diseada
para operar en un rango de amperaje entre 300 y 350 kA.
Diseo de la celda
El diseo de los sistemas que integran la celda: superestructura, casco-
revestimiento y barras conductoras se realiz utilizando modelos matemticos, de
esta manera se minimiz el nmero de prototipos y ensayos experimentales
requeridos para obtener el diseo ptimo final.
El diseo de la celda incluye mejoras en la alimentacin puntual de la
almina, compensacin magntica, revestimiento de carburo de silicio y control
automtico.
El tiempo de vida de la celda V-350 excede los 2000 das de operacin.
Hasta ahora la celda ha sido operada hasta un amperaje mximo de 325 kA.
Algunos de los elementos tales como, alimentadores puntuales de almina,
superestructura, casco, paredes laterales, y sistemas de elevacin han sido
mejorados despus de evaluar su desempeo durante el perodo de optimizacin.
Se estudiaron resultados tpicos de la modelacin termo-elctrica del
revestimiento, de la modelacin mecnico-estructural del casco y de la
superestructura, entre otros.
El sistema de control V-350 tiene una arquitectura totalmente distribuida (un
controlador por celda), lo cual permite un control automtico de los principales
parmetros del proceso, tales como voltaje, alimentacin de almina y
alimentacin de fluoruro de aluminio.
Este sistema de control fue desarrollado completamente en el Centro de
Investigacin y Desarrollo de CVG Venalum. El sistema de control usa tecnologa
de ltima generacin, microprocesadores y dispositivos de E/S, que permiten
ampliaciones de capacidad y/o reemplazo sin mayores efectos sobre el software.
El diseo del sistema se basa en el uso de dispositivos de estndar
industrial que hacen mnimo el costo de inversin con un mejor desempeo de la
celda de reduccin. Adicionalmente a los algoritmos de control de celdas, se ha
incorporado un nuevo control de temperatura de celda basado en lgica difusa, as
como tambin se ha incluido un programa de deteccin de inestabilidades.
Cabe destacar la facilidad de cambios y/o incorporacin de nuevos
algoritmos de control sin la necesidad de interrumpir la ejecucin del control de
celdas. La red de supervisin ha sido implementada como una red Industrial
Ethernet.
Rendimiento de la celda
CONCLUSIONES
El aluminio es uno de los metales ms abundante de la corteza terrestre,
con propiedades peculiares de gran utilidad.
El procedimiento ideado por Hroult y hall en 1886 es aun el nico proceso
a nivel industrial, debido a que se han realizados otros pero ninguno supera
la escala semi-industrial.
A pesar q se han realizado pruebas de ensayo y error para mejorar el
diseo de celdas electrolticas, aun no se ha asegurado un mtodo correcto
para fabricar celdas ni el rendimiento electroltico.
Se desconoce an el por qu de las fallas tempranas en las cubas.
En la actualidad se siguen estudiando el mejoramiento de las celdas y las
cubas, para as garantizar incremento en el rendimiento del proceso
utilizado para la obtencin del ALUMINIO.
BIBLIOGRAFIA
Enciclopedia del Aluminio. Vol 1.Produccin del Aluminio. Ediciones URMO
http://www.ikkaro.com/node/406
http://www.buenastareas.com/materias/electrolisis-del-cobre/80
http://www.pdv.com/lexico/museo/minerales/aluminio.htm
http://www.monografias.com/trabajos89/la-electroquimica/la-
electroquimica.shtml
http://es.scribd.com/doc/84878486/Trabajo-Tecnologia-Del-Aluminio
http://es.wikipedia.org/wiki/Aluminio
http://es.answers.yahoo.com/question/index?qid=20090122114601AAFjPcC
http://www.cintal.com.ve/aluminio/proceso/index.php
http://www.hydro.com/es/Hydro-en-Argentina/Aluminio/Innovacion/
Tecnologa de la Reduccin del Aluminio. ALCASA. Hugo Castillo. 1982
http://misdescargas.educ.ar/ver/15048/Obtenci%C3%B3n_del_aluminio/
http://descargas-api.educ.ar/dinamico/UnidadHtml__get__2b088488-c851-
11e0-823e-e7f760fda940/anexo.htm
http://www.aprendizaje.com.mx/Curso/Proceso1/Temario1_IVAlu.html
http://www.monografias.com/trabajos14/proceso-bayer/proceso-bayer.shtml
http://translate.google.co.ve/translate?hl=es&langpair=en%7Ces&u=http://e
n.wikipedia.org/wiki/Hall%25E2%2580%2593H%25C3%25A9roult_process
&ei=tYsdUdywFpPW8gS6kIH4DQ
También podría gustarte
- Oficios Artísticos. Forja: Las técnicas de la forja explicadas paso a pasoDe EverandOficios Artísticos. Forja: Las técnicas de la forja explicadas paso a pasoCalificación: 5 de 5 estrellas5/5 (1)
- Manual MP CDocumento30 páginasManual MP Ceduar fernandoAún no hay calificaciones
- Sistema de Encendido ConvencionalDocumento49 páginasSistema de Encendido ConvencionalKEVINAún no hay calificaciones
- Bladesmithing: Secretos del tratamiento térmico de la forja de cuchillosDe EverandBladesmithing: Secretos del tratamiento térmico de la forja de cuchillosAún no hay calificaciones
- ALUMINIODocumento11 páginasALUMINIOJosue Benavides MosqueraAún no hay calificaciones
- FDGFDocumento19 páginasFDGFRicardo Eliseo TlvAún no hay calificaciones
- El Aluminio Presentacion TareaDocumento21 páginasEl Aluminio Presentacion TareaBrandon Josué Marroquín AmayaAún no hay calificaciones
- AluminioDocumento10 páginasAluminioTc IngenieriaAún no hay calificaciones
- WEG w11 Motor 50042645 Catalogo EspanolDocumento16 páginasWEG w11 Motor 50042645 Catalogo EspanolDaniel PaganoAún no hay calificaciones
- Sistemas Trifasicos Desequilibrados G4Documento18 páginasSistemas Trifasicos Desequilibrados G4Josué David Sarabia100% (1)
- Primera Prueba FS-415Documento3 páginasPrimera Prueba FS-415David Jafet Mendoza Castillo100% (1)
- Boletas VTRDocumento2 páginasBoletas VTRlowpalmeraAún no hay calificaciones
- Aluminio 1Documento22 páginasAluminio 1Stephanny VLAún no hay calificaciones
- Electroquimica 3Documento14 páginasElectroquimica 3Eduardo Martínez0% (1)
- Alumino y MagnesioDocumento20 páginasAlumino y Magnesiomandrake1233Aún no hay calificaciones
- AluminioDocumento7 páginasAluminioGrover Quiquisani100% (1)
- ALUMINIO, Ciencias de Los Materiales.Documento4 páginasALUMINIO, Ciencias de Los Materiales.Santiago AgudeloAún no hay calificaciones
- Investigación Del AluminioDocumento9 páginasInvestigación Del AluminioAlejandra YarceAún no hay calificaciones
- AluminioDocumento11 páginasAluminioWilder WilderbrAún no hay calificaciones
- Alianza Metalurgica WordDocumento44 páginasAlianza Metalurgica WordCarlos Huertas0% (1)
- Word Reciclaje de Aluminio 1Documento13 páginasWord Reciclaje de Aluminio 1Maricarmen BenaventeAún no hay calificaciones
- ALUMINIODocumento24 páginasALUMINIOGabiis Rdz MAún no hay calificaciones
- Obtencion de AluminaDocumento22 páginasObtencion de AluminaJUAN EDUARD SANTOS CAMPOSAún no hay calificaciones
- AluminioDocumento13 páginasAluminioTornero Alonso Juan CruzAún no hay calificaciones
- Aluminio y Sus AplicacionesDocumento11 páginasAluminio y Sus AplicacionesDánica JuárezAún no hay calificaciones
- Aleaciones Del Aluminio MonografiaDocumento29 páginasAleaciones Del Aluminio MonografiakevinestAún no hay calificaciones
- Elaluminio y Su Desarrolloactual1 PDFDocumento75 páginasElaluminio y Su Desarrolloactual1 PDFCarlos Alberto Lozano EscobedoAún no hay calificaciones
- Elementos Quimicos DayaDocumento17 páginasElementos Quimicos DayaJaider Rovira MartinezAún no hay calificaciones
- Tercer Parcial Acero 4140Documento32 páginasTercer Parcial Acero 4140Miguel Angel López NavarreteAún no hay calificaciones
- Aluminio y Sus PropiedadesDocumento21 páginasAluminio y Sus PropiedadesSilver RayónAún no hay calificaciones
- El AluminioDocumento5 páginasEl AluminioDavid ArangoAún no hay calificaciones
- AluminioDocumento16 páginasAluminiocristiancruz1303Aún no hay calificaciones
- Introducción Al AluminioDocumento49 páginasIntroducción Al AluminioJuan Carlos Torres100% (1)
- Al. Ni. MNDocumento20 páginasAl. Ni. MNkenjiemiAún no hay calificaciones
- Aluminio TrabajoDocumento6 páginasAluminio Trabajoronilso ibarraAún no hay calificaciones
- Introduccion Al AluminioDocumento48 páginasIntroduccion Al AluminioAlexandra ArroyoAún no hay calificaciones
- Guia Argentina de AluminioDocumento82 páginasGuia Argentina de AluminioSebastián VillagránAún no hay calificaciones
- Aplicaciones Del AluminioDocumento10 páginasAplicaciones Del AluminioAngel RicardezAún no hay calificaciones
- El Aluminio Presentacion 1.1Documento21 páginasEl Aluminio Presentacion 1.1Brandon Josué Marroquín AmayaAún no hay calificaciones
- Origen Y Composicion Del AluminioDocumento4 páginasOrigen Y Composicion Del AluminioRuben VargasAún no hay calificaciones
- Química Proyecto Aluminio (PF)Documento8 páginasQuímica Proyecto Aluminio (PF)RicardoAún no hay calificaciones
- Usos y Aopkicaciones de Los MetalesDocumento22 páginasUsos y Aopkicaciones de Los MetalesKevin Chilo PumaAún no hay calificaciones
- Aplicaciones en La Industria y La Tecnologia de AluminioDocumento2 páginasAplicaciones en La Industria y La Tecnologia de Aluminioanaid14gAún no hay calificaciones
- Descripcion AluminioDocumento29 páginasDescripcion AluminioMonikiya Zuluaga PelaezAún no hay calificaciones
- INFORME TECNICO #3 - Tecnologia Industrial IDocumento5 páginasINFORME TECNICO #3 - Tecnologia Industrial IAmy CastilloAún no hay calificaciones
- Aluminio - Materiales y Materia PrimaDocumento4 páginasAluminio - Materiales y Materia PrimaCesar CortesAún no hay calificaciones
- Consulta AluminioDocumento6 páginasConsulta AluminioElito ZagalAún no hay calificaciones
- AluminioDocumento5 páginasAluminioAlan Islas100% (1)
- DocumentoDocumento3 páginasDocumentoenoc uliszerAún no hay calificaciones
- Metales Más ComunesDocumento10 páginasMetales Más ComunesRicky AlejandroAún no hay calificaciones
- Usos Del Aluminio en La ActualidadDocumento26 páginasUsos Del Aluminio en La ActualidadmiguelAún no hay calificaciones
- Aluminio 20 - 21Documento25 páginasAluminio 20 - 21Jim AcuñaAún no hay calificaciones
- BBBBBBBBBBBBBBBBBBBBBBDocumento21 páginasBBBBBBBBBBBBBBBBBBBBBBMicaela BustosAún no hay calificaciones
- AluminioDocumento29 páginasAluminioFederico MendozaAún no hay calificaciones
- El Aluminio IntroduccionDocumento3 páginasEl Aluminio IntroduccionLuisa Luna IsazaAún no hay calificaciones
- 6 Metales y Aleaciones No FerrosasDocumento22 páginas6 Metales y Aleaciones No FerrosasCesar Fernando Sanchez GuerreroAún no hay calificaciones
- Forma de La DiapositivaDocumento5 páginasForma de La DiapositivaTHAYLOR DAVITHSON MEZA BORJAAún no hay calificaciones
- AluminioDocumento55 páginasAluminioEstebanAún no hay calificaciones
- AluminioDocumento1 páginaAluminiocataAún no hay calificaciones
- Metalurgia Descriptiva Del AluminioDocumento5 páginasMetalurgia Descriptiva Del AluminioGuillermo SosaAún no hay calificaciones
- El Libro Del Aluminio 5 - Capítulo 10 - El AluminioDocumento12 páginasEl Libro Del Aluminio 5 - Capítulo 10 - El AluminioAluStock100% (1)
- Quim Act1Documento7 páginasQuim Act1CandeAún no hay calificaciones
- Aluminio InfoDocumento13 páginasAluminio InfoViky RasgadoAún no hay calificaciones
- Diagrama de Fases de Las Aleaciones Del AluminioDocumento17 páginasDiagrama de Fases de Las Aleaciones Del AluminioByron Castro78% (9)
- AluminioDocumento90 páginasAluminioFacundo BenitezAún no hay calificaciones
- Ingeniería de procesos siderúrgicos: La experiencia de AHMSADe EverandIngeniería de procesos siderúrgicos: La experiencia de AHMSAAún no hay calificaciones
- CPT Cirprotec PSC4 12 - 5 230 TT 77738400Documento7 páginasCPT Cirprotec PSC4 12 - 5 230 TT 77738400Jose GuillermoAún no hay calificaciones
- Sílabo 5431C17438-273346Documento15 páginasSílabo 5431C17438-273346Sasha UllonAún no hay calificaciones
- Problemario SgeDocumento13 páginasProblemario SgeRogelio EspinozaAún no hay calificaciones
- Capacitancia en Líneas de TransmisiónDocumento13 páginasCapacitancia en Líneas de TransmisiónCristhian Barrera0% (2)
- Merlin Gerin Multi9 CEr PDFDocumento2 páginasMerlin Gerin Multi9 CEr PDFlord byronAún no hay calificaciones
- Organizador VisualDocumento1 páginaOrganizador VisualOriana Alejandra Huanca HuisaAún no hay calificaciones
- Central Hidroeléctrica de Machu PicchuDocumento5 páginasCentral Hidroeléctrica de Machu PicchuFrancisco Guerrero Zurita100% (1)
- Informe de Pulsador de ParoDocumento5 páginasInforme de Pulsador de ParoJackson Javier MendezAún no hay calificaciones
- Admitancia de Circuitos RLC en ParaleloDocumento3 páginasAdmitancia de Circuitos RLC en ParaleloRoger RangelAún no hay calificaciones
- Cómo Funcionan Las Fuentes de Alimentación Conmutadas IDocumento6 páginasCómo Funcionan Las Fuentes de Alimentación Conmutadas IAngel VelasquezAún no hay calificaciones
- Taller Sistemas de TransmisiónDocumento3 páginasTaller Sistemas de TransmisiónMelizza DiazAún no hay calificaciones
- FREETOX N2XSOH C 0 6 1 KV PDFDocumento3 páginasFREETOX N2XSOH C 0 6 1 KV PDFRaul Coila QuispeAún no hay calificaciones
- ExperimentosDocumento2 páginasExperimentosrosana_20100Aún no hay calificaciones
- Inf1 Labo Circ1Documento8 páginasInf1 Labo Circ1MIGUEL ALFREDO PRADO SAN MARTINAún no hay calificaciones
- 01 Diagnosis Gestion Del Motor EsDocumento62 páginas01 Diagnosis Gestion Del Motor EsCastillo Badillo IvanAún no hay calificaciones
- Códigos de Protecciones de Media y Baja Tensión para Planos EléctricosDocumento4 páginasCódigos de Protecciones de Media y Baja Tensión para Planos EléctricosjosepablohgAún no hay calificaciones
- Monografia Realimentacion NegativaDocumento37 páginasMonografia Realimentacion NegativaRaúl Dylan CapchaAún no hay calificaciones
- Medicionesdevoltajecorrienteyresistenciacon1 150627202555 Lva1 App6892Documento18 páginasMedicionesdevoltajecorrienteyresistenciacon1 150627202555 Lva1 App6892Raul muñozAún no hay calificaciones
- Contactor CuestionarioDocumento7 páginasContactor CuestionarioJAIRO MANUEL ZUMARAN CACERESAún no hay calificaciones
- Continuity 1k 120V MAN en-UPS 1000Documento45 páginasContinuity 1k 120V MAN en-UPS 1000Ricardo RicceAún no hay calificaciones
- 100000I34N AnálisisdeCircuitosenCorrienteAlterna Guía N°3 - Rev0001Documento14 páginas100000I34N AnálisisdeCircuitosenCorrienteAlterna Guía N°3 - Rev0001Jossé 544Aún no hay calificaciones
- Practica No.1 (Aplicación de Ley de Ohm y Ley de Watt)Documento6 páginasPractica No.1 (Aplicación de Ley de Ohm y Ley de Watt)Angel FraveAún no hay calificaciones
- 01 Proyeccion de La Canalización de Los Circuitos de Alumbrado y TomacorrienteDocumento6 páginas01 Proyeccion de La Canalización de Los Circuitos de Alumbrado y TomacorrienteIpa HubberAún no hay calificaciones
- Proyecto Integrador ExperimentoDocumento18 páginasProyecto Integrador ExperimentoJUAN CARLOS DIAS CAISAAún no hay calificaciones