Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Carga Nuclear Efectiva
Carga Nuclear Efectiva
Cargado por
AlejandraSánchez0 calificaciones0% encontró este documento útil (0 votos)
6 vistas8 páginasQuimica Inorganica
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PPTX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoQuimica Inorganica
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPTX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
6 vistas8 páginasCarga Nuclear Efectiva
Carga Nuclear Efectiva
Cargado por
AlejandraSánchezQuimica Inorganica
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPTX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 8
CARGA NUCLEAR
EFECTIVA.
En los tomos polielectrnicos, los protones que
se encuentran en el ncleo no ejercen la misma
fuerza de atraccin sobre todos los electrones
por igual. Esto se debe a los efectos pantalla que
causan los electrones ms cercanos al ncleo
sobre los que se encuentran ms alejados. Se le
llama carga nuclear efectiva a la diferencia entre
la carga nuclear neta (que depende del nmero
atmico del elemento) y la constante del efecto
pantallas,es la fuerza real que ejerce el ncleo
sobre un electrn en particular.
Zes el nmero de protones y electrones
del tomo, dado por su nmero atmico,
ysel valor de la constante de
apantallamiento, que depende del
nmero de electrones que separan al
ncleo del electrn en cuestin, y
tambin depende de los orbitales
atmicos en que se hallen los electrones
que causan el efecto pantalla.
Tambin infl uyen en este efecto los
electrones que se encuentran en el mismo
nivel de energa que el electrn considerado.
No tienen infl uencia en esta constante los
electrones que se hallan en niveles de
energa.
La carga nuclear efectiva puede calcularse
segn las reglas de Slater, quien las formul
en 1930:
Los electrones ubicados en un orbital de
mayor nivel contribuyen en 0 (para la
sumatoria que da como resultado la
constante de apantallamientos)
Cada electrn en el mismo nivel contribuye
en 0,35.(excepto si el nivel es 1s, que resta
0,30).
Electrones en el nivel inmediato inferior, si
estn en orbitalessopcontribuyen en 0,85,
Entonces, para calcular la carga nuclear
efectiva, primero, situamos los
electrones del tomo en sus orbitales
atmicos:
1s, 2s,2p, 3s,3p,3d,4s,4p, 4d, 4f,
etc.
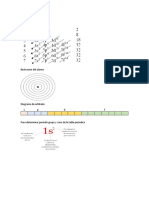
Luego, para el clculo de la carga nuclear efectiva sobre un
electrn determinado, debemos calcularsy para
ellotomamos en consideracin los electrones que se
encuentran en niveles de energa inferiores o iguales, que
son los que causan apantallamiento del mismo, como indica
la tabla de arriba, segn las reglas de Slater.
Entonces, por ejemplo para calcular la carga nuclear efectiva
sobre un electrn 4s del tomo de Zinc (nmero atmico 30),
Luego calcular el valor que cada electrn del mismo nivel y de
niveles inferiores va a restar a la carga nuclear total, esto es,
segn la tabla de arriba:
1 electrn en el nivel 4 s....resta 0,35
8 electrones en el nivel 3 sy 3p..restan 0,85 cada uno
10 electrones en el nivel 3 d....restan 1,0 cada uno
8 electrones en el nivel 2 sy 2p.restan 1,0 cada uno.
2 electrones en el nivel 1 s.. restan 1,0 cada uno.
Entoncescalculamos s :
s=(1 . 0,35) + (20 . 1) + (8 . 0,85)=27,15
La carga nuclear efectiva para un electrn del orbital 4s de
Zinc sera
Z ef= 30 27,15= 2,85
Este clculo se sencillo, aunque no es exacto, dado que Slater
consider los electrones de orbitales sypcon el mismo valor,
lo que no es exactamente as.
También podría gustarte
- Encuadre Temas Selectos de Fisica IDocumento4 páginasEncuadre Temas Selectos de Fisica IYoSoyAngel100% (2)
- Actividad 1 - Matriz Historia ToxicologiaDocumento22 páginasActividad 1 - Matriz Historia ToxicologiaJhon E Álvarez71% (14)
- Quiz de QuimicaDocumento3 páginasQuiz de QuimicaAndres TapiaAún no hay calificaciones
- L - GRADO UNDÉCIMO (11°) - Guía 5 QUÍMICADocumento7 páginasL - GRADO UNDÉCIMO (11°) - Guía 5 QUÍMICAKiara Hernández CruzAún no hay calificaciones
- Taller de Recuperacion de Genetica Humana y MolecularDocumento2 páginasTaller de Recuperacion de Genetica Humana y MolecularShasipla Rodriguez100% (3)
- Examen Tipo Icfes de Quimica Grado 8Documento3 páginasExamen Tipo Icfes de Quimica Grado 8harry salas hurtadoAún no hay calificaciones
- Taller 1 Grado Octavo FísicaDocumento5 páginasTaller 1 Grado Octavo FísicaCarlos Caceres100% (1)
- CrucigramaDocumento4 páginasCrucigramaLuis Miguel VakAún no hay calificaciones
- Guia Autoaprendizaje Estudiante 9no Grado Ingles s1Documento9 páginasGuia Autoaprendizaje Estudiante 9no Grado Ingles s1kathy ReyesAún no hay calificaciones
- Respuestas Taller Parcial Atomo 7 y 10Documento2 páginasRespuestas Taller Parcial Atomo 7 y 10victor hugo ocampo57% (7)
- Examen de Recuperacion Formula EmpiricaDocumento2 páginasExamen de Recuperacion Formula EmpiricaAna BorjaAún no hay calificaciones
- PLANIFICACIONCiencias Naturales 10 Mo - 6 Semana 6 Actividad Proyecto 5 - ArchivoDocumento3 páginasPLANIFICACIONCiencias Naturales 10 Mo - 6 Semana 6 Actividad Proyecto 5 - Archivowalter aguirreAún no hay calificaciones
- TallerDocumento2 páginasTallerOdair Prada0% (1)
- Guía Temodinámica III Medio Química. LabDocumento6 páginasGuía Temodinámica III Medio Química. Labcarloscontrerasgalleguillos100% (3)
- Crucigrama de La Tabla Periodica UrgenteDocumento7 páginasCrucigrama de La Tabla Periodica UrgenteElvi MurilloAún no hay calificaciones
- Taller de Recuperación 10° Ciencias Naturales-QuimicaDocumento7 páginasTaller de Recuperación 10° Ciencias Naturales-Quimicawilson dAún no hay calificaciones
- Taller Recuper Quimica 8Documento4 páginasTaller Recuper Quimica 8gotisamiAún no hay calificaciones
- Actividades Principios Pascal y Arquímedes PDFDocumento1 páginaActividades Principios Pascal y Arquímedes PDFjuliofelice0% (2)
- Configuracion ElectronicaDocumento7 páginasConfiguracion ElectronicaJuan Carlos Arias VegaAún no hay calificaciones
- Prueba Química NuclearDocumento5 páginasPrueba Química NuclearMiguel Polanco100% (1)
- Guia QuimicaDocumento20 páginasGuia Quimicali_t23Aún no hay calificaciones
- Taller Campo ElecDocumento4 páginasTaller Campo ElecJose Manuel Molina CuariteAún no hay calificaciones
- Taller Del Atomo GRADOS OCTAVOSDocumento2 páginasTaller Del Atomo GRADOS OCTAVOSsedelsa80% (5)
- Taller 1Documento5 páginasTaller 1cam0% (1)
- Fotosintesis Taller Con GraficosDocumento3 páginasFotosintesis Taller Con GraficosChimbo BlancaAún no hay calificaciones
- Taller de Química Cuarto Periodo Grado Noveno ITEIPADocumento3 páginasTaller de Química Cuarto Periodo Grado Noveno ITEIPADuqueiro Cordon RinconAún no hay calificaciones
- Guias Quimica Grado Séptimo Tercer PeriodoDocumento15 páginasGuias Quimica Grado Séptimo Tercer PeriodoLIDIBETH MARTINEZ GARCIAAún no hay calificaciones
- Evaluacion Atomo 1Documento5 páginasEvaluacion Atomo 1imatesmariaAún no hay calificaciones
- Prueba Enlaces QuimicosDocumento2 páginasPrueba Enlaces QuimicosDanniel AlexisAún no hay calificaciones
- Actividad - Niveles de Organización de La Materia VivaDocumento2 páginasActividad - Niveles de Organización de La Materia VivaBranco Costa Ortega100% (1)
- Taller Quimica PolimerosDocumento7 páginasTaller Quimica PolimerosJuancho Juarez0% (1)
- Taller de 10 CARGAS E ISOTOPOSDocumento4 páginasTaller de 10 CARGAS E ISOTOPOSMARIA ALEJANDRA MARINO RODRIGUEZAún no hay calificaciones
- MIni Test Chem 3Documento1 páginaMIni Test Chem 3Héctor DomínguezAún no hay calificaciones
- Examen Mensual de Quimica 5toDocumento2 páginasExamen Mensual de Quimica 5toJavier Rojas FranciaAún no hay calificaciones
- Examen Quimica y Fisica Grado 8 1 2022Documento4 páginasExamen Quimica y Fisica Grado 8 1 2022LiyiPaterninaAún no hay calificaciones
- Repaso Mol, Numero Avogadro y Formulas QuimicasDocumento6 páginasRepaso Mol, Numero Avogadro y Formulas QuimicasJairo Alexis QuinteroAún no hay calificaciones
- Ejercicio Numeros Cuanticos PDFDocumento2 páginasEjercicio Numeros Cuanticos PDFMariza Martina Camones MaguiñaAún no hay calificaciones
- Evaluacion de Quimica Grado OctavoDocumento2 páginasEvaluacion de Quimica Grado OctavoManuel CuentasAún no hay calificaciones
- Plan Virtual de PrevenciónDocumento112 páginasPlan Virtual de PrevenciónjaimehernanpabloAún no hay calificaciones
- Ficha de Estudio 1 Cqu 210 Particulas SubatómicasDocumento2 páginasFicha de Estudio 1 Cqu 210 Particulas SubatómicasadrianitayanyAún no hay calificaciones
- Física OctavoDocumento4 páginasFísica OctavoGabriel González SantibañezAún no hay calificaciones
- Examen Semestral QuimicaDocumento6 páginasExamen Semestral QuimicaIzamary Lizarraga DuarteAún no hay calificaciones
- Pruebas y Ejercicios UdlaDocumento14 páginasPruebas y Ejercicios UdlaCarlos Revelo NavarreteAún no hay calificaciones
- @ 2da Prueba Sumativa Fisica Quimica 2 BguDocumento2 páginas@ 2da Prueba Sumativa Fisica Quimica 2 BgusancuniAún no hay calificaciones
- Taller de Fisicoquimica Sobre La Energia Grado 7 Segundo PeriodoDocumento26 páginasTaller de Fisicoquimica Sobre La Energia Grado 7 Segundo PeriodoHarry Salas HurtadoAún no hay calificaciones
- Taller 21 Tabla de FrecuenciasDocumento1 páginaTaller 21 Tabla de FrecuenciasLETS COLOMBIAAún no hay calificaciones
- Prueba Unidad N°1 Diferenciado Química 2023 RedoxDocumento5 páginasPrueba Unidad N°1 Diferenciado Química 2023 RedoxLeslie ParraAún no hay calificaciones
- Taller Atomos, Moléculas y Iones PDFDocumento6 páginasTaller Atomos, Moléculas y Iones PDFDeco526Aún no hay calificaciones
- Grado 7 Movimiento Rectilineo Taller 3Documento3 páginasGrado 7 Movimiento Rectilineo Taller 3Alejandra Ocampo RinconAún no hay calificaciones
- Guia Psu Numeros CuanticosDocumento6 páginasGuia Psu Numeros CuanticosJozi Ñiquen BejaranoAún no hay calificaciones
- Taller de Nivelacion Notacion CientificaDocumento2 páginasTaller de Nivelacion Notacion Cientificaleonardo martinezAún no hay calificaciones
- Plan de Mejoramiento - Química 11Documento1 páginaPlan de Mejoramiento - Química 11Pedro Luis Gonzalez100% (1)
- Evaluacion de QuimicaDocumento4 páginasEvaluacion de Quimicamprm2579Aún no hay calificaciones
- 2do ParcialDocumento3 páginas2do Parcialganicus2014Aún no hay calificaciones
- Examen de Fisica ElectricidadDocumento2 páginasExamen de Fisica Electricidadomar delgadoAún no hay calificaciones
- Carga Nuclear EfectivaDocumento2 páginasCarga Nuclear EfectivaDiana Laura Torres HernándezAún no hay calificaciones
- Carga Nuclear EfectivaDocumento3 páginasCarga Nuclear EfectivaCRISTINA PATRICIA PINEDA BELMONTESAún no hay calificaciones
- Tarea Quimica... DefinicionesDocumento2 páginasTarea Quimica... DefinicionesCecilia Denisse LeviatanAún no hay calificaciones
- Carga Nuclear EfectivaDocumento8 páginasCarga Nuclear EfectivaRoberto Del AngelAún no hay calificaciones
- Carga Nuclear EfectivaDocumento4 páginasCarga Nuclear EfectivaBryan J. Ignacio VicenteAún no hay calificaciones
- Carga Nuclear EfectivaDocumento10 páginasCarga Nuclear EfectivaTony TotorresAún no hay calificaciones
- Succinato DH 1432Documento7 páginasSuccinato DH 1432AlejandraSánchezAún no hay calificaciones
- Práctica-9 Colorantes AzoicosDocumento4 páginasPráctica-9 Colorantes AzoicosAlejandraSánchezAún no hay calificaciones
- Mecanismos de Transporte de Membrana CelularDocumento15 páginasMecanismos de Transporte de Membrana CelularAlejandraSánchezAún no hay calificaciones
- Tarea MicologiaDocumento7 páginasTarea MicologiaAlejandraSánchezAún no hay calificaciones
- Toxicidad Del FenolDocumento8 páginasToxicidad Del FenolAlejandraSánchezAún no hay calificaciones
- Granos PracticaDocumento12 páginasGranos PracticaAlejandraSánchezAún no hay calificaciones
- Cuestionario Levaduras BiologiaDocumento3 páginasCuestionario Levaduras BiologiaAlejandraSánchezAún no hay calificaciones
- CONICET Digital Nro. ADocumento217 páginasCONICET Digital Nro. AnataliaAún no hay calificaciones
- Banco Icfes Enlaces QuimicosDocumento6 páginasBanco Icfes Enlaces Quimicoshermann peñaloza sernaAún no hay calificaciones
- Quimica Organica - A - 7 - 3Documento14 páginasQuimica Organica - A - 7 - 3Ariana Rodriguez MunisacaAún no hay calificaciones
- Endedurecedor Epoxi TeknoDocumento6 páginasEndedurecedor Epoxi TeknoLiliana TrigosoAún no hay calificaciones
- Semana 3-2-Tratamiento TérmicoDocumento10 páginasSemana 3-2-Tratamiento TérmicoCARLOS oAún no hay calificaciones
- Tema 02 - PLanteo de Ecuaciones IIDocumento4 páginasTema 02 - PLanteo de Ecuaciones IIHugo Lopez PajueloAún no hay calificaciones
- Brugmansia Candida - NORA.. (VER)Documento11 páginasBrugmansia Candida - NORA.. (VER)Edith Mosquera PalacioAún no hay calificaciones
- Capitulo 3 ACIDocumento21 páginasCapitulo 3 ACIShirleyFernándezAún no hay calificaciones
- Pozo PercoladorDocumento26 páginasPozo PercoladorEnrique Rojas PerezAún no hay calificaciones
- Archivo 2 - Grupo 3 PointDocumento11 páginasArchivo 2 - Grupo 3 PointMelba NoboaAún no hay calificaciones
- Informe 1Documento5 páginasInforme 1Johana MejillonesAún no hay calificaciones
- Herramientas y Equipo para BobinarDocumento8 páginasHerramientas y Equipo para BobinarBryan RamirezAún no hay calificaciones
- Proyecto Corregido 1Documento14 páginasProyecto Corregido 1travesuras de anitaAún no hay calificaciones
- ARMAS Dino - La Curva de La Felicidad (Monologo)Documento21 páginasARMAS Dino - La Curva de La Felicidad (Monologo)Kike Castañeda CuatindioyAún no hay calificaciones
- Ficha 1 Historia de La BQCADocumento6 páginasFicha 1 Historia de La BQCAAlejo VázquezAún no hay calificaciones
- PlaguicidasDocumento6 páginasPlaguicidasDon FructuosoAún no hay calificaciones
- Triptico Elaboracion de QuesoDocumento2 páginasTriptico Elaboracion de QuesoElizabeth Del Aguila Olano83% (6)
- Evaluación de La Transferencia de Oxígeno en Un BiorreactorDocumento9 páginasEvaluación de La Transferencia de Oxígeno en Un BiorreactorYordan HernandezAún no hay calificaciones
- Taller GravimetriaDocumento1 páginaTaller GravimetriaJohana Sierra BernalAún no hay calificaciones
- HidrurosDocumento30 páginasHidrurosYesenia LagosAún no hay calificaciones
- Trabajo Sobre Las DrogasDocumento29 páginasTrabajo Sobre Las DrogasAlbania Díaz SanchezAún no hay calificaciones
- PRÁCTICA No.2 Absorcion de Farmacos y PHDocumento3 páginasPRÁCTICA No.2 Absorcion de Farmacos y PHOMAR VALENCIA100% (1)
- Cerro Matoso ContextoDocumento18 páginasCerro Matoso ContextoDamian RestrepoAún no hay calificaciones
- NB 1225001 Cap 09 Req de Resist y FuncionamDocumento13 páginasNB 1225001 Cap 09 Req de Resist y FuncionamAnahir Vallejos100% (1)
- 201 Estudio Analítico Des Sulfaminas PDFDocumento344 páginas201 Estudio Analítico Des Sulfaminas PDFNatalia MurilloAún no hay calificaciones
- Acidos y Bases (1) 16032021Documento54 páginasAcidos y Bases (1) 16032021SHARON OSSA CABALLEROAún no hay calificaciones
- 2 06-01-2022 Protocolo, CementaciónDocumento20 páginas2 06-01-2022 Protocolo, CementaciónKelly EscalanteAún no hay calificaciones
- Guia07 (2020)Documento1 páginaGuia07 (2020)Rulos QueteimportaAún no hay calificaciones
- Procesamiento de Los Residuos PesadosDocumento22 páginasProcesamiento de Los Residuos PesadosKerly EspinozaAún no hay calificaciones