Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Ejercicios Resueltos
Ejercicios Resueltos
Cargado por
Karen Paola Castaño PerezTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Ejercicios Resueltos
Ejercicios Resueltos
Cargado por
Karen Paola Castaño PerezCopyright:
Formatos disponibles
Tecnologa Farmacutica II.
Ejercicios
Tcnicas de solubilizacin
1.1
He y cols. (Int. J. Pharmaceutics 246 (2003), 25) estudiaron la solubilidad del fluasteron utilizando
HPCD, cosolventes y mezcla de cosolventes y CD. En la tabla siguiente se recogen la concentracin
total del frmaco (mM) en funcin de la concentracin de HPCD (g/100 ml). Identificar el tipo de
complejo formado y estimar la constante de formacin del complejo sabiendo que la relacin frmaco
: HPCD es 1 : 1. (peso molecular de la HPCD: 1191 g/mol).
fluasteron
mM
HPCD
g/100 ml
0,0
1,25
2,5
5,0
7,5
10,0
15,0
20,0
1.2
0,000155
0,23
0,49
0,96
1,49
1,96
2,93
4,04
La tabla siguiente muestra los datos de un estudio de un complejo ciclodextrina frmaco (todos los
datos en mg/ml). El peso molecular de la ciclodextrina es 1.190,0 y el del frmaco 375,0. Resolver:
a) Analizar los datos y estimar la constante de equilibrio del complejo suponiendo una relacin
frmaco:ciclodextrina 1:1.
b) Calcular la concentracin libre de frmaco de una disolucin que contiene 5,0 mg/ml de
frmaco y 200,0 mg/ml de ciclodextrina.
Conc. total de CD
Conc. total de frmaco
1.3
0,0
0,375
50,0
100,0
150,0
200,0
3,00
5,63
8,25
10,9
Para estimar las constantes de equilibrio del complejo de un frmaco de carcter cido (pKa = 6,5) con
una ciclodextrina se obtuvieron los diagramas de solubilidad de fase a tres pH diferentes (5,0, 6,5 y
7,5). La tabla siguiente muestra la s concentraciones totales de frmaco (mM) en funcin de la
concentracin total de ciclodextrina (LT , mM). Resolver:
a) Estimar la solubilidad intrnseca de frmaco y las constantes de equilibrio de los complejos
formados con el frmaco no ionizado y con el frmaco ionizado.
b) Explicar las diferencias entre las ordenadas en el origen y entre las pendientes de los
diagramas de fase de solubilidad obtenidos para los tres pH.
mllabres@ull.es
Tecnologa Farmacutica II. Ejercicios
c) Explicar los resultados esperados si la constante de formacin de equilibrio del complejo
ciclodextrina frmaco ionizado fuera igual a cero.
pH
LT
5,0
6,5
7,5
25,0
0,138
0,244
1,209
50,0
0,265
0,446
2,093
100,0
0,518
0,851
3,859
200,0
1,025
1,661
7,392
Sistemas dispersos
2.1
Kwok y Neumann (Colloids Surf. A: Physicochem. Eng. Aspects 161 (2000) 31) recopilaron los datos
siguientes relativos al ngulo de contacto sobre poli(propeno-N-metil maleimida).
()
disolvente
diyodometano
30,71
glicerol
60,25
agua
69,81
Verificar la consistencia de los datos con la ecuacin de Young. (tomar los datos necesarios del tema
Tensin Superficial y Tensioactivos):
2.2
Representar el reograma esperado para el agua a 20 C sabiendo que su viscosidad es igual a 1 cp para
velocidades de cizalla comprendidas entre 0 y 100 s-1 (una velocidad de cizalla de 100 s-1 es
ligeramente superior a la experimentada por el agua cuando se vierte desde una botella).
2.3
Haciendo uso del modelo de Harschel Bulkely, demostrar que la viscosidad de un fluido
pseudoplstico disminuye con la velocidad de cizalla, mientras que la de un fluido dilatante aumenta.
2.4
La tabla siguiente muestra los resultados de un estudio reolgico de un gel natural de aloe recin
extrado. Identificar el tipo de fluido, caracterizarlo mediante un modelo adecuado y calcular las
viscosidades aparente y dinmica para una velocidad de cizalla igual a 1 s-1 .
velocidad cizalla (1/s)
2
tensin de cizalla (dinas/cm )
0,13
0,66
1,06
1,32
10,4
26,7
32,7
35,5
mllabres@ull.es
Tecnologa Farmacutica II. Ejercicios
2.5
La siguiente tabla muestra los valores de la tensin de cizalla (Pa) en funcin de la velocidad de cizalla
(s-1) de una dispersin de un polmero biodegradable (cido poli (dl lctico gliclico), peso
molecular 48.000) al 30% en Cl2CH2. Los datos han sido obtenidos en un viscosmetro de cono y
placa a 25 C (A. Santovea, 2001). Estudiar las propiedades de flujo de la dispersin.
1/s
Pa
9,058
29,38
49,91
60,34
81,16
114,2
124,7
147,2
157,8
179,1
189,7
199,3
1,241
3,715
6,237
7,48
9,983
13,68
14,95
17,46
18,71
21,22
22,45
23,66
Mecnica de fluidos
3.1
Calcular la potencia de la bomba necesaria para elevar una disolucin (densidad = 1,20 kg/m3) hasta
la entrada de un atomizador situada a 3 m de altura respecto del tanque donde se encuentra la
disolucin. El caudal necesario es de 30,0 l/min y la presin manomtrica a la entrada de 3,0 105 Pa.
La tubera es de 2 de dimetro (seccin 0,21646 dm2), las prdidas por friccin 30,0 J/kg y el
rendimiento de la bomba 65%.
mllabres@ull.es
Tecnologa Farmacutica II. Ejercicios
Psicrometra
4.1
Calcular el calor especfico, la temperatura hmeda y el punto de roco de un aire cuya temperatura es
22 C y su humedad relativa 60% (a) utilizando los datos de la tabla de presin de vapor del agua y (b)
utilizando el diagrama psicromtrico.
4.2
Una estufa de desecacin toma el aire del ambiente que se encuentra a 20 C y humedad relativa del
70%. El aire se calienta hasta 80 C antes de entrar en el secadero; a la salida la temperatura del aire es
45C y la temperatura del termmetro hmedo 32,5 C. Calcular el calor necesario durante la
calefaccin del aire y la cantidad de agua extrada. Expresar los resultados por kg de aire seco que
entre en la estufa.
Secado de slidos
5.1
Durante la etapa de velocidad de secado constante se observa que el aire a entra en la estufa a 80 C
con una humedad relativa del 2% y sale a 34 C y humedad relativa del 76%. La presin de vapor de
agua a 80 C es igual a 355,1 mmHg y a 34 C igual a 37,7 mmHg. Calcular la velocidad de secado del
slido sabiendo que la superficie expuesta es de 0,8 m2 , el peso seco del slido 2,5 kg y el caudal de
aire a la entrada, expresado en aire seco, 1.000 l/min.
Liofilizacin
6.1
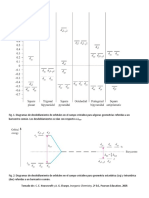
El esquema siguiente muestra de forma esquemtica la transmisin del calor por conduccin en la
liofilizacin. La base del vial de vidrio que contiene la disolucin descansa sobre una bandeja que se
encuentra a -10 C, y la temperatura en la cara superficial de la disolucin del vial se encuentra a 15
C, de forma que la base del vial y la disolucin congelada puede interpretarse como una pared
compuesta. Calcular el flujo de calor debido a la conduccin del calor desde la base del vial a la
superficie de la disolucin congelada.
Datos: conductividad calorfica del vidrio: 1,2 J/s m2 K; espesor de la base del vial: 2 mm;
conductividad calorfica de la disolucin congelada: 0,8 J/s m2 K; espesor de la disolucin congelada:
1 cm.
disolucin
congelada
base del vial
bandeja
(20 C)
mllabres@ull.es
Tecnologa Farmacutica II. Ejercicios
Mezclado de slidos pulverulentos
7.1
Unas cpsulas duras contienes 50 microesferas de cesin inmediata y 200 microesferas de cesin
sostenida. Resolver:
a) Calcular el valor medio y la desviacin tpica del contenido de microesferas de cesin
inmediata de la mezcla perfecta y de la mezcla segregada cuando se toman muestras de 250
partculas.
b) Verificar si es posible aproximar la distribucin del contenido de microesferas de cesin
inmediata utilizando la distribucin normal y en su caso calcular el intervalo de confianza
del contenido medio, [ - 1,96 , + 1,96 ].
7.2
Se desean elaborar unas cpsulas que contienen 1,0 mg de principio activo y 49,0 mg de excipiente
(peso total del contenido 50 mg), ambos de igual densidad (1,4 g/cm3) y tamao de partcula
(dvn = 30 m). El criterio de homogeneidad de contenido utilizado es del 10%. Verificar si la mezcla
ideal satisface el criterio de homogeneidad de contenido.
7.3
Se desea validar una operacin de mezclado de una mezcla de principio activo y excipiente con
caracterstica granulomtrica similares (dv,n = 50,0 m y = 1,3 g/cm3 ) destinada a la elaboracin de
comprimidos de 75 mg de peso y 1,0 mg de contenido de principio activo; el criterio de uniformidad
de contenido es 10%. Los resultados del anlisis de 10 muestras de 75,0 mg de peso extradas de
distintos puntos del mezclador fueron las siguientes (mg de principio activo/75 mg de muestra).
0,875
0,961
1,00
1,05
0,952
1,02
0,930
0,979
0,979
1,06
a) Verificar si es factible el proceso de mezclado y en su caso si los resultados experimentales
obtenidos validan el proceso de mezclado.
b) Calcular el ndice de mezclado M3 (ndice de Kramers). Qu valor debera tomar este
ndice para que el grado de mezcla satisfaga el criterio de homogeneidad de contenido?
Esterilizacin
8.1
Durante la validacin del ciclo de esterilizacin mediante vapor hmedo a 121 C de un frmaco
rellativamente termolbil en disolucin dosificado en ampollas de 10 ml se desea ajustar el valor
F0 = 15 min. Los valores de tiempo temperatura durante un ciclo de prueba se muestran en la tabla
siguiente. Verificar si se satisface el criterio para validar el ciclo de esterilizacin; en caso contrario
ajustar el tiempo total de esterilizacin. Las condiciones de referencia son TR = 121 C, z = 10 C,
t = 15 min.
mllabres@ull.es
Tecnologa Farmacutica II. Ejercicios
t (min)
T ( C)
t (min)
T ( C)
18,0
15,0
119,4
2,0
62,2
17,5
120,2
4,0
87,4
20,0
120,6
6,0
101,8
22,5
120,9
8,0
110,0
25,0
121,0
10,0
114,7
27,5
121,1
12,5
117,9
30,0
121,0
mllabres@ull.es
Tecnologa Farmacutica II. Ejercicios
SOLUCIONES DE LOS EJERCICIOS SELECIONADOS
Ejercicio 1.1
Para interpretar los datos de acuerdo con el diagrama de fases de solubilidad utilizaremos las
concentraciones expresadas en mmol/l:
-->// datos del problema
-->pmCD = 1191.0; ...
// peso molecular HPbCD, g/mol
-->CDconc = [0.0, 1.25, 2.5, 5.0, 7.5, ...
-->10.0, 15.0, 20.0]; ...
// conc. HPbCD, g/100 ml
-->FluMol = [1.55e-4, 0.23, 0.49, 0.96, ...
-->1.49, 1.96, 2.93, 4.04]; ...
// conc fluasteron, mM
--> // clculo tabla concentraciones mM
-->CdMol = 1.0e4*CDconc/(pmCD); ...
-->[CdMol ; FluMol]'
ans =
0.
10.495382
20.990764
41.981528
62.972292
83.963056
125.94458
167.92611
// conc. HPbCD mM
// tabla concentraciones mM
0.000155
0.23
0.49
0.96
1.49
1.96
2.93
4.04
-->// representacin grfica de los datos transformados
-->plot2d(CdMol , FluMol, style = -5, rect = [0, 0, 200, 5])
-->b = regress(CdMol, FluMol)
b =
// estimacin parmetros regresin lineal
- 0.0225519
0.0238794
-->ypred = b(1) + b(2)*CdMol; ...
-->plot2d(CdMol, ypred)
Comentarios:
Los valores experimentales (ver grfico) se encuentran alineados, tal como es de esperar en
la formacin de un complejo AL.
La ordenada en el origen es negativa debido al error de estimacin, lo que nos obliga a
tomar como S0 el valor obtenido experimentalmente para la concentracin de HPCD cero
para calcular la constante de formacin del complejo.
-->S0 = FluMol(1); ...
-->K = b(2)/(S0 * (1 - b(2)))
K =
// conc. fluast. para [HPbCD] = 0
// cte. formacin complejo 1/mM
157.82982
mllabres@ull.es
Tecnologa Farmacutica II. Ejercicios
0
0
20
40
60
80
100
120
140
160
180
200
Ejercicio 1.3
La representar para cada pH las solubilidades totales en funcin de la concentracin total de CD se
observa que a medida que aumenta el pH crecen la ordenada en el origen y la pendiente, por lo que
partimos de la hiptesis de que k1 > 0 y k2 > 0 (ver figura).
-->St = [0.138, 0.244, 1.209;
-->
0.256, 0.446, 2.093;
-->
0.518, 0.851, 3.859;
-->
1.025, 1.661, 7.329];
-->Lt = [25, 50, 100, 200];
-->plot2d(Lt, St, style = [-1, -2, -3, -4], rect = [0, 0, 250, 8])
-->plot2d(Lt, St, style = [1,1,1,1], rect = [0, 0, 250, 8])
mllabres@ull.es
Tecnologa Farmacutica II. Ejercicios
0
0
50
100
150
200
Estimacin de las ordenadas en el origen y pendientes para cada serie de datos
-->pH = [5.0; 6.5; 7.5]; ...
-->pka = 6.0;
-->for i=1:3,
-->
bz = regress(Lt, St(:,i));
-->
b0(i) = bz(1);
-->
b1(i) = bz(2);
-->
clear('bz');
-->end
-->[b0, b1]
ans =
0.0070870
0.0413043
0.3452609
0.0050897
0.0080981
0.0349572
Estimacin de la solubilidad intrnseca
-->z1 = 1 + 10.^(pH - pka);
-->s0 = (z1' * b0)/(z1' * z1);
-->s0
s0 =
0.0105682
Ver el grfico siguiente.
-->spred = s0 * [0; z1];
-->plot2d(z1, b0, style = -3, rect = [0, 0, 40, 0.5])
-->plot2d([0; z1], spred, rect = [0, 0, 40, 0.5])
mllabres@ull.es
250
Tecnologa Farmacutica II. Ejercicios
10
0.50
0.45
0.40
0.35
0.30
0.25
0.20
0.15
0.10
0.05
0.00
0
10
15
20
25
30
35
Clculo de kap a partir de la solubilidad intrnseca y de las pendientes estimadas
-->// resumen
-->[b0, b1, kap]
ans =
0.0070870
0.0050897
0.0413043
0.0080981
0.3452609
0.0349572
0.4840707
0.7725221
3.427579
Estimacin de k1 y k2
-->z2 = 10.^(pH-pka); ...
-->[z2, kap]
ans =
0.1
0.4840707
3.1622777
0.7725221
31.622777
3.427579
-->K = regress(z2, kap);
-->K
K =
0.4759758
0.0933421
Ver el grfico siguiente.
-->Khat = K(1) + K(2)*z2;
-->plot2d(z2, kap, style = -2, rect = [0, 0, 40, 4])
-->plot2d(z2, Khat, style = 1, rect = [0, 0, 40, 4])
mllabres@ull.es
40
Tecnologa Farmacutica II. Ejercicios
11
4.0
3.5
3.0
2.5
2.0
1.5
1.0
0.5
0.0
0
10
15
20
25
30
35
40
-->// resumen
-->[z2, kap, Khat]
ans =
0.1
3.1622777
31.622777
0.4840707
0.7725221
3.427579
0.4853100
0.7711494
3.4277123
Ejercicio 2.1
De acuerdo con la ecuacin de Young, los valores SV (mJ/m2 ) calculados para cada disolvente son:
-->ac = [30.71, 60.25, 69.81]; ... // ngulos de contacto,
-->acr = (%pi / 180) * ac; ... // ngulos de contacto, rad
-->gsv = (1/4) * glv .* (1 + cos(acr)) .^2; ... // ec. de Young
-->[glv; ac; gsv]'
ans =
44.4
64.
72.9
30.71
60.25
69.81
38.391781
35.818621
32.97607
Las diferencias entre los valores de SV calculados indican claramente que la ec. de Young Berthelot
no es adecuada para interpretar los datos del problema.
De acuerdo con la ecuacin de Young van Oss, el componente Lisfhitz van der Waals de SV para
el poli(propeno-N-metil meleimida puede calcularse a partir del ngulo de contacto con el
LW
diyodometano ( SL
= 50,8 mJ/m2 ; +LV = LV = 0):
LW
SV
= LW
LV
(1 + cos ()) 2
4
mllabres@ull.es
Tecnologa Farmacutica II. Ejercicios
12
LW
Por lo tanto SV
= 38,4 mJ/m2 .
Ejercicio 2.4
Ver en la figura siguiente los datos experimentales representados en escala lineal y logartmica; se
concluye que se trata de un fluido pseudoplstico y que es de aplicacin la funcin potencial (n < 1).
Las estimadas de la ordenada en el origen y de la pendiente de los logartmos de los datos son:
-->b
b =
1.50132
0.53895
Y los parmetros de la funcin potencial:
-->[a, n]
ans =
31.7193
0.53895
Por lo tanto, la tensin de cizalla viene dada por la funcin:
= 31,72 & 0.539
40
10
35
30
25
20
10
15
10
0
0.0
0.5
1.0
1.5
10 -1
10
mllabres@ull.es
10
10
Tecnologa Farmacutica II. Ejercicios
13
Ejercicio 7.1
Datos del problema y clculo de p, q:
-->n1 = 50; n2 = 200; n = n1 + n2; ...
-->p = n1/n; q = 1 - p; [p, q]
ans =
0.2
0.8
Clculo de (mu) y R (sr):
-->mu = n*p; sr = sqrt(n*p*q); [mu, sr]
ans =
50.
6.3245553
El nmero de partculas en la muestra (250) es superior al criterio para el uso de la distribucin
normal:
-->9/(p*q)
ans =
56.25
Intervalo de confianza 95%:
-->[mu - 1.96*sr , mu + 1.96*sr]
ans =
37.603872
62.396128
Ver en la parte izquierda de figura siguiente el histograma de la distribucin generada a partir de 1.000
nmero aleatorios con distribucin binomial con parmetros n = 250 y p = 0,2. En la parte derecha se
muestra el histograma normalizado junto con la funcin de densidad normal de media 50,0 y
desviacin tpica 6,324. El cuadro siguiente muestra el cdigo Scilab para generar las figuras.
X = grand(1000, 1, 'bin', n, p);
c = 20:80;
subplot(1,2,1)
histplot(c, X, normalization = %f)
z = 30:70;
f = 1/(sr*sqrt(2*%pi)) * exp(-((z - mu).^2)/(2*sr^2));
subplot(1,2,2)
histplot(c, X)
plot2d(z, f)
Cdigo Scilab para generar las figuras del ejercicio 7.1
mllabres@ull.es
Tecnologa Farmacutica II. Ejercicios
14
70
0.07
60
0.06
50
0.05
40
0.04
30
0.03
20
0.02
10
0.01
0
20
0.00
30
40
50
60
70
80
20
30
40
50
60
70
80
Ejercicio 7.3
Ver en el cuadro siguiente los clculos necesarios para la resolucin del problema. Obsrvese que los
clculos se han realizado sobre la base del peso de comprimido y del contenido en principio activo.
El nmero de partculas en la muestra, p y q calculados son:
-->[n, p, q]
ans =
881473.
0.0133333
0.9866667
La desviacin tpica de la mezcla perfecta (R) y la mxima desviacin tpica aceptable (A ) son:
-->format('e', 10)
-->[sr, sa]
ans =
9.162D-03
1.667D-02
R < A ; por lo tanto la capacidad potencial del mezclado es aceptable. La desviacin tpica de los
datos muestrales es:
-->s
s =
5.575D-02
s > A , por lo que el proceso de mezclado no puede darse por validado.
Los valores del ndice de mezclado M3 de Kramers son prcticamente coincidentes para la mezcla
aceptable y para el grado de mezcla obtenido, y prcticamente iguales al valor mximo:
mllabres@ull.es
Tecnologa Farmacutica II. Ejercicios
15
-->[M3, M3a]
ans =
0.9999591
0.9999974
Ejercicio 8.1
La resolucin del problema requiere calcular el valor de F0 a partir de los datos de la tabla integrando
numricamente aplicando la regla trapezoidal:
t i +1
f dt = 0,5 (f
+ f i+1 ) (t i +1 t i )
ti
Para la resolucin del problema hemos de construir una tabla con los valores de la funcin
f i = 10 (Ti TR ) / z
e integrarla numricamente (ver cuadro). El resultado es el siguiente:
-->[t; T; f; [0, F]]'
ans =
0.
2.
4.
6.
8.
10.
12.5
15.
17.5
20.
22.5
25.
27.5
30.
18.
62.2
87.4
101.8
110.
114.7
117.9
119.4
120.2
120.6
120.9
121.
121.1
121.
5.012D-11
0.0000013
0.0004365
0.0120226
0.0794328
0.2344229
0.4897788
0.6918310
0.8317638
0.9120108
0.9772372
1.
1.023293
1.
0.
0.0000013
0.0004392
0.0128983
0.1043538
0.4182095
1.3234616
2.8004738
4.7049673
6.8846855
9.2462456
11.717792
14.246908
16.776025
t = [0:2:10, 12.5:2.5:30];
T = [18.0, 62.2, 87.4, 101.8, 110.0, 114.7, ...
117.9, 119.4, 120.2, 120.6, 120.9, 121.0, 121.1, 121.0];
Tr = 121; z = 10;
f = 10.^((T - Tr)/z);
F = cumsum(0.5*(f(2:$)+f(1:$-1)).*(t(2:$)-t(1:$-1)));
[t; T; f; [0, F]]'
Cdigo Scilab para la resolucin del ejercicio 8.1
Observaciones
Las figuras siguientes muestran la evolucin en funcin del tiempo de la temperatura (izquierda) y del
valor de F0 (derecha). Solamente cuando la temperatura est prxima a la temperatura de referencia el
aumento de F0 es igual al tiempo que transcurre; durante los primeros 10, en los que se ha alcanzado
mllabres@ull.es
Tecnologa Farmacutica II. Ejercicios
16
114 C, fi < 1 y el valor de F0 alcanzado es despreciable (0,41 min); sin embargo, durante este periodo
la temperatura es suficientemente alta como para que se degrade el frmaco.
20
120
18
16
100
14
80
12
10
60
8
40
6
4
20
2
0
0
0
10
15
20
25
30
35
mllabres@ull.es
10
15
20
25
30
35
También podría gustarte
- PEC2 Química Analítica Instrumental 2021 2022Documento3 páginasPEC2 Química Analítica Instrumental 2021 2022Alicia SánchezAún no hay calificaciones
- Práctica 1. %humedad en Bicarbonato de SodioDocumento1 páginaPráctica 1. %humedad en Bicarbonato de SodioCarolina LópezAún no hay calificaciones
- Cuestionario Volumenes Molares ParcialesDocumento1 páginaCuestionario Volumenes Molares ParcialesMartín PaucarAún no hay calificaciones
- Lab Oratorio 8Documento18 páginasLab Oratorio 8erickasegoviacaceresAún no hay calificaciones
- 1 Contenido de Materia Orgánica en El Árido FinoDocumento5 páginas1 Contenido de Materia Orgánica en El Árido FinoIsabella Bermudez pelaezAún no hay calificaciones
- Toxicologia Destruccion de Materia OrganicaDocumento8 páginasToxicologia Destruccion de Materia OrganicamiltonAún no hay calificaciones
- Analisis Dolomita FinalDocumento7 páginasAnalisis Dolomita FinalJavier Mauricio Posada CabreraAún no hay calificaciones
- Determinacion de Plomo en ConcentradoDocumento3 páginasDeterminacion de Plomo en ConcentradoMarycarmen Paez AdvinculaAún no hay calificaciones
- 5DeterminaciondePCB DigesaDocumento37 páginas5DeterminaciondePCB DigesaYuri OmonteAún no hay calificaciones
- AQI Julio 2020 NúñeDocumento2 páginasAQI Julio 2020 NúñeDomingo José Hernández MolinaAún no hay calificaciones
- Une 83952 Durabilidad Hormigon - H2o PHDocumento6 páginasUne 83952 Durabilidad Hormigon - H2o PHwalking deadAún no hay calificaciones
- FENÓMENOS CRÍTICOS ccr7Documento13 páginasFENÓMENOS CRÍTICOS ccr7Anonymous wH8gUfAFnAún no hay calificaciones
- Juan David Torres-Informe 04. Grupo 04. Equipo 02Documento9 páginasJuan David Torres-Informe 04. Grupo 04. Equipo 02NIKOLAS ZUÑIGA CARDONAAún no hay calificaciones
- INF 8. Síntesis de PinacolDocumento4 páginasINF 8. Síntesis de PinacolStln Alexis100% (2)
- Tema 4.-Estados de Agregacion de La Materia. Parte I. GasesDocumento73 páginasTema 4.-Estados de Agregacion de La Materia. Parte I. GasesDiana Diez PrietoAún no hay calificaciones
- Tetrayoduro de Estano Lucia BolanosDocumento3 páginasTetrayoduro de Estano Lucia BolanosLucía BolañosAún no hay calificaciones
- Absorb An CIADocumento22 páginasAbsorb An CIANayeli Romero VirruetaAún no hay calificaciones
- Granulometria LaserDocumento20 páginasGranulometria LaserMiguel Angel Garcia100% (1)
- Análisis de Humedad Y Cenizas en AlimentosDocumento2 páginasAnálisis de Humedad Y Cenizas en AlimentosElvinDaniloPincayCataguaAún no hay calificaciones
- Determinacion de CA en Una Calisa (Dirigido A Bacteriologia)Documento7 páginasDeterminacion de CA en Una Calisa (Dirigido A Bacteriologia)Kevin MuñozAún no hay calificaciones
- Quimica Comun - Guia P 35 - Soluciones Quimicas N2Documento11 páginasQuimica Comun - Guia P 35 - Soluciones Quimicas N2Beatriz Ovalle FernandezAún no hay calificaciones
- ResitividadDocumento8 páginasResitividadBrayan ArancibiaAún no hay calificaciones
- Manual Laboratorio Análisis Químico I Interciclo 2021 ModificadoDocumento67 páginasManual Laboratorio Análisis Químico I Interciclo 2021 ModificadoAndrea LemusAún no hay calificaciones
- Espectrometria de MasasDocumento57 páginasEspectrometria de Masaslg_abantoAún no hay calificaciones
- Clase 3. DZP Pac' F (PH) para Cu (II)Documento14 páginasClase 3. DZP Pac' F (PH) para Cu (II)Ramses DRHOAún no hay calificaciones
- Bibliografia Espectrometria de MasasDocumento1 páginaBibliografia Espectrometria de MasasEduardo Chalbaud MogollonAún no hay calificaciones
- Practica YesosDocumento8 páginasPractica YesosUziel ArroyoAún no hay calificaciones
- Efecto Tunel IeeeDocumento3 páginasEfecto Tunel IeeeClub D. PichotaAún no hay calificaciones
- QU434 Q2 FisicoQuímica II FDocumento5 páginasQU434 Q2 FisicoQuímica II FAngel DavidAún no hay calificaciones
- Simetrìa y Grupo PuntualDocumento10 páginasSimetrìa y Grupo PuntualLaurita Arroyave MurilloAún no hay calificaciones
- LabFIQUI-I-"PRESIÓN DE VAPOR DE LÍQUIDOS PUROS"ADocumento10 páginasLabFIQUI-I-"PRESIÓN DE VAPOR DE LÍQUIDOS PUROS"Acefiqt100% (1)
- CP 573 FTHCCDocumento431 páginasCP 573 FTHCCjfrcaroAún no hay calificaciones
- Cromatografía de Gases - Reporte 1Documento7 páginasCromatografía de Gases - Reporte 1AldoTorreAún no hay calificaciones
- Informe 2 - SolubilidadDocumento9 páginasInforme 2 - SolubilidadNatalia RodriguezAún no hay calificaciones
- Trabajo de Quimica Inorganica Ejercicios de La Semana 1 y 2Documento15 páginasTrabajo de Quimica Inorganica Ejercicios de La Semana 1 y 2Hilmer Mamani CordovaAún no hay calificaciones
- 1.2 El Método 3060 Es Un Procedimiento de Digestión Alcalina para Extraer Cromo HexavalenteDocumento15 páginas1.2 El Método 3060 Es Un Procedimiento de Digestión Alcalina para Extraer Cromo HexavalenteandreAún no hay calificaciones
- Los Compuestos Del CarbonoDocumento12 páginasLos Compuestos Del CarbonoYolanda Ruiz AyoraAún no hay calificaciones
- Clase 1. Cinetica QuímicaDocumento48 páginasClase 1. Cinetica Químicajerc1324Aún no hay calificaciones
- Informe Espectrofotometria InfrarrojoDocumento7 páginasInforme Espectrofotometria InfrarrojoJorgePedrozoCalderonAún no hay calificaciones
- 18 ElectronesDocumento9 páginas18 ElectronesRicardo Alcántara ReyesAún no hay calificaciones
- Dureza Del AguaDocumento3 páginasDureza Del AguaMaria Jose NavarroAún no hay calificaciones
- Espectroscopia InfrarrojoDocumento40 páginasEspectroscopia InfrarrojoEmanuel OsorioAún no hay calificaciones
- Sintesisorganicafundamentos 30322 PDFDocumento321 páginasSintesisorganicafundamentos 30322 PDFJacqui SegundoAún no hay calificaciones
- Qca Bioinorganica 2014Documento25 páginasQca Bioinorganica 2014Juan José100% (1)
- 3 - Carbonato de Sodio - PurezaDocumento2 páginas3 - Carbonato de Sodio - PurezaEl PeñaAún no hay calificaciones
- Introduccion Experimental Al Sistema PeriodicoDocumento14 páginasIntroduccion Experimental Al Sistema PeriodicoJose AlarconAún no hay calificaciones
- Tipos de Isotermas de Adsorción Langmuir y FreundlichDocumento4 páginasTipos de Isotermas de Adsorción Langmuir y FreundlichDavid ballena guerreroAún no hay calificaciones
- Pre-Reporte 3 ViscosimetríaDocumento11 páginasPre-Reporte 3 ViscosimetríaEmily GonzalezAún no hay calificaciones
- Desdoblamiento de Orbitales Campo CristalinoDocumento1 páginaDesdoblamiento de Orbitales Campo CristalinoNicolás GrinbergAún no hay calificaciones
- Tabla Potencial Estandar ReduccionDocumento13 páginasTabla Potencial Estandar ReduccionnataliasusanarojasbazaesAún no hay calificaciones
- Perdidas Por Friccion en El Equipo DidacticoDocumento17 páginasPerdidas Por Friccion en El Equipo DidacticoOsborn ArtolaAún no hay calificaciones
- Reporte Practica 3Documento14 páginasReporte Practica 3Alejandro SánchezAún no hay calificaciones
- Laboratorio 2 ReaccionesDocumento21 páginasLaboratorio 2 ReaccionesJessica Cristina Navarro RaveloAún no hay calificaciones
- Método QuelatométricoDocumento3 páginasMétodo QuelatométricoSharon Yanireth Castro PaganAún no hay calificaciones
- Informe Organica II Sintesis de CiclohexenoDocumento14 páginasInforme Organica II Sintesis de CiclohexenoOlivia López CarrielAún no hay calificaciones
- Determinación de La Tensión Superficial de Mezclas Binarias y TernariasDocumento4 páginasDeterminación de La Tensión Superficial de Mezclas Binarias y TernariaslosvaljtAún no hay calificaciones
- Guia de Operaciones-1Documento41 páginasGuia de Operaciones-1Lieska LopezAún no hay calificaciones
- Procedimiento 2 y 3 InformeDocumento3 páginasProcedimiento 2 y 3 Informejuan david hernandez lopez100% (1)
- Propiedades ColigativasDocumento13 páginasPropiedades Coligativasbrendads89100% (6)
- Articulo AcetilcolinaDocumento6 páginasArticulo AcetilcolinaYoanAún no hay calificaciones