Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Soluciones Ejercicios
Cargado por
Luis VacaDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Soluciones Ejercicios
Cargado por
Luis VacaCopyright:
Formatos disponibles
SOLUCIONES Y PROPIEDADES COLIGATIVAS
LUIS VACA S AYUDANTE
SOLUCIONES
1. Calcule el porcentaje en masa y fraccin molar del Na2SO4 en una disolucin que contiene 11.7 g de
Na2SO4 en 443 g de agua. Si el volumen de la solucin es 500 ml determine su molaridad.
2. El agua de mar contiene 0.0079 g de Sr
2+
por kilogramo de agua. Calcule la concentracin de Sr
2+
medida en
ppm y la molalidad de la solucin.
3. La densidad de una disolucin que contiene 5.0 g de tolueno (C7H8) y 225 g de benceno es de 0.876 g/mL,
calcule la molaridad de la disolucin.
4. La densidad de una disolucin acuosa de metanol (CH3OH) 2.45M es 0.976 g/mL. Cul es la molalidad de la
disolucin? La masa molar del metanol es 34.04 g.
5. Una disolucin blanqueadora comercial contiene 3.62% en masa de NaOCl en agua. Calcule (a) molalidad y
(b) la fraccin molar de NaOCl en la disolucin.
6. El cido sulfrico concentrado que se utiliza en el Laboratorio es H2SO4 a 98% en masa. La densidad de esta
solucin es de 1.83 g/mL. Calcule la molalidad y molaridad de la solucin cida.
7. El cido ntrico acuoso comercial tiene una densidad de 1.42 g/mL y es 16 M. Calcule el porcentaje en masa
de HNO3 en la disolucin.
8. La densidad del acetonitrilo (CH3CN) es de 0.786 g/mL, y la densidad del metanol (CH3OH) es de 0.791
g/mL. Se prepara una disolucin disolviendo 15.0 mL de CH3OH en 90.0 mL de CH3CN. (a) Calcule la
fraccin molar de metanol en la disolucin. (b) Calcule la molalidad de la disolucin. (c) Suponiendo que los
volmenes son aditivos, calcule la molaridad de CH3OH en la disolucin.
9. El propilenglicol, C3H6(OH)2, suele utilizarse en disoluciones anticongelantes para automviles. Si una
disolucin acuosa tiene una fraccin molar X = 0.100, calcule (a) el porcentaje en masa de propilenglicol; (b)
la molalidad del propilenglicol en la disolucin.
10. Determine la normalidad de una solucin de H3PO4 que tiene un volumen de 850 ml y en que estn
presentes 20 g de dicho acido.
11. Calcular el nmero de equivalentes de una solucin de 400 ml de hidrxido de calcio 12 N.
12. Determine la cantidad de gramos que se disuelven en una solucin de cido clorhdrico 0,1 N que se
prepara con 40 ml de agua y 50 ml de cido.
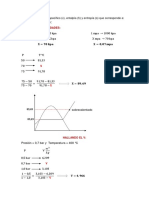
13. Calcule la concentracin de CO2 en una bebida gaseosa que se embotella bajo una presin parcial de CO2
de 4 atm sobre el lquido a 25 C. La constante de Henry para el CO2 en agua es de 3,1 * 10
-2
mol/L atm.
14. La constante de la ley de Henry para el helio gaseoso en agua a 30C es de 3.7 10
-4
M/atm; la de N2 a 30C
es de 6.0x10-4 M/atm. Si cada uno de estos gases est presente a una presin de 1.5 atm, calcule la
solubilidad de cada gas
15. La solubilidad del nitrgeno gaseoso en agua a 25C y 1 atm es de 6,8x10-4 mol/L Cul es la concentracin
(en molaridad) del nitrgeno disuelto en agua bajo condiciones atmosfricas? La presin parcial del
nitrgeno en la atmosfera es de 0.78 atm. Por qu tuvo lugar la disminucin en la solubilidad del
nitrgeno?
16. Los peces necesitan al menos 4 ppm de O2 disuelto para sobrevivir. (a) Exprese esa concentracin en
mol/L. (b) Qu presin parcial sobre el agua se requiere para tener esa concentracin a 10C? (La
constante de la ley de Henry para el O2 a esta temperatura es de 1.71x 10-3 mol/L-atm.)
17. (a) Se genera una muestra de hidrgeno gaseoso en un recipiente cerrado haciendo reaccionar 2.050 g de
zinc metlico con 15.0 mL de cido sulfrico 1.00 M. Escriba la ecuacin balanceada para la reaccin y
calcule el nmero de moles de hidrgeno que se forman, suponiendo que la reaccin es total. (b) El
volumen sobre la disolucin es de 122 mL. Calcule la presin parcial del hidrgeno gaseoso en este
volumen a 25C, suponiendo que el gas no se disuelve en la disolucin. (c) La constante de la ley de Henry
para hidrgeno en agua a 25C es de 7.8 x10
-4
mol/L-atm. Estime el nmero de moles de hidrgeno gaseoso
que permanecen disueltos en la disolucin. Qu fraccin de las molculas de gas del sistema se disuelve
en la disolucin? Fue razonable suponer, en la parte (b), que el hidrgeno no se disuelve en la disolucin?
SOLUCIONES Y PROPIEDADES COLIGATIVAS
LUIS VACA S AYUDANTE
FORMULAS DE SOLUCIONES: TIPOS Y CONCENTRACION:
SOLUCIONES: Poseen 2 partes: El soluto (sustancia que se
disuelve) y el solvente (medio disolvente). Podemos expresarlas
en trminos de masa de soluto por 100 gramos de agua. Ejm: A
20C 20 gramos de NaCl se disuelven en 100 g de agua. Existen
otras formas de calcular las concentraciones y se detallan a
continuacin:
UNIDADES DE CONCENTRACION
UNIDAD DE
CONCENTRACION
NUMERADOR DENOMINADOR EXPRESION MATEMATICA UNIDADES
TANTO POR
CIENTO EN MASA
(%)
Masa de un
componente
(sto. svte.)
Masa total de
todos los
componentes
100 % x
masa
masa
svte sto
sto
sto
Valor
matemtico
menor a 1
PARTES POR
MILLON
(ppm)
Masa de un
componente
(sto. svte.)
Masa total de
todos los
componentes
svte
sto
masa
masa
ppm
Kg
mg.
Masa de un
componente
(sto. svte.)
Volumen de la
solucin
stve Volumen
masa
ppm
sto
.
.
L
mg
FRACCION MOLAR
(X)
Moles de un
componente
(sto. svte.)
Moles totales de
todos los
componentes
svte sto
sto
sto
n
n
X
) ( svte sto
svte
svte
n
n
X
Valor
matemtico
menor a 1
+ = 1
MOLARIDAD
(M)
Moles de soluto Volumen de
solucin
.
.
sol
sto
V
n
M
L
Mol
MOLALIDAD
(m)
Moles de soluto Kilogramo de
solvente
svte
sto
Kg
n
m
.
Kg
Mol
NORMALIDAD
(N)
Equivalente-
gramo de soluto
Litro de solucin
sol
sto
V
g Eq
N
) (
L
g Eq
=
Valencia= # de H en cidos, # de OH en bases y Producto de cargas en Sales
UNIDADES DE DILUCION (CUANDO SE PREPARAN MEZCLAS MUY SEMEJANTES A UNA INICIAL)
11 = 22
CONCENTRACION DE UN GAS (LEY DE HENRY)
Cg = kPg
Dnde: Cg es la solubilidad del gas en la solucin (Molaridad), Pg es la presin parcial del gas en
la solucin, k es la constante de la ley de Henry (diferente para cada par soluto-solvente)
SOLUCIONES Y PROPIEDADES COLIGATIVAS
LUIS VACA S AYUDANTE
FORMULAS DE PROPIEDADES COLIGATIVAS
Las propiedades coligativas son aquellas propiedades de las soluciones que no dependen del tamao y de la
forma que tiene el soluto y afectan las caractersticas fsicas del solvente, esto se aplica cuando no son
electrlitos (no conducen electricidad).
Disminucin de la Presin de Vapor o Ley de Raoult
A A A
P X P
PA es la presin de vapor de la solucin; XA es la fraccin molar del solvente; PA es la presin de vapor del
solvente puro. Para medir la variacin de presin tenemos: =
; Dnde: Pa es la temperatura de
fusin de la solucin y Pa es la temperatura de fusin del solvente puro.
Elevacin del Punto de Ebullicin
m k T
b b
Tb es el cambio en la temperatura de ebullicin; Kb es la constante molal de elevacin del punto de ebullicin
m es la molalidad. Para medir el punto de ebullicin de la solucin tenemos: = ; Dnde: Tb es la
temperatura de ebullicin de la solucin y Tb es la temperatura de ebullicin del solvente puro.
Disminucin del Punto de Congelacin
m k T
f f
Tf es el cambio de la temperatura de congelacin, kf es la constante molal de la disminucin del punto de
congelacin, m es la molalidad. Para medir el punto de ebullicin de la solucin tenemos: = ;
Dnde: Tf es la temperatura de fusin de la solucin y Tf es la temperatura de fusin del solvente puro.
Presin osmtica
=
es la presin osmtica de la solucin, M es la Molaridad de la solucin, R es la constante de gases ideales, T es
la temperatura en K
SOLUCIONES Y PROPIEDADES COLIGATIVAS
LUIS VACA S AYUDANTE
DISMINUCION DE LA PRESION DE VAPOR (LEY DE RAOULT)
1. La glicerina C3H8O3 es un no electrolito no voltil con una densidad de 1.26 g / mL a 25C. Calcule la
presin de vapor a 25C de una disolucin que se prepar agregando 50.0 mL de glicerina a 500.0 mL
de agua. La presin de vapor del agua pura a 25C es de 23.8 torr. Datos: C=12 g/mol; H= 1 g/mol; O=
16 g/mol.
2. Calcule, en primer lugar, la presin de vapor de una disolucin preparada al disolver 218 g de glucosa
(masa molar = 180.2 g/mol) en 460 mL de agua a 30 C. Luego determine la disminucin en la presin de
vapor a esa temperatura luego de la intervencin de la glucosa sobre el agua. DATOS: La presin de
vapor del agua pura a 30 C= 31.82 mmHg. Densidad de la disolucin= 1.00 g/mL. Masa molar glucosa=
180.2 g/mol.
3. Una solucin contiene 8,3 g de una sustancia no electrolito y no voltil, disuelta en un mol de
cloroformo (CHCl3), esta solucin tiene una presin de vapor de 510,79 mmHg. La presin de Vapor del
cloroformo puro a esta temperatura es 525,79 mmHg. En base a esta informacin determine: A. La
fraccin molar de soluto. B. B. La masa molar de soluto.
DESCENSO DEL PUNTO DE FUSION, AUMENTO DEL PUNTO DE EBULLICION
4. Calcular el punto de congelacin de una solucin de 100g de anticongelante etilenglicol (C2H6O2), en
900 g de agua (Kc = 1,86 C/molal)
5. El etilenglicol, CH2 (OH) CH2 (OH), es un anticongelante comnmente utilizado en automviles. Se sabe
mantener esta sustancia en el radiador del automvil durante poca tropicales. Con la ayuda de los
datos, proceda a calcular el punto de congelacin de una disolucin que contiene 651 g de etilenglicol
en 2505 g de agua. Datos: Solvente Agua Kf=1.86 C/m; Kb=0.52 C/m
6. Una disolucin de 0.85 g de un compuesto orgnico en 100 g de benceno tiene un punto de congelacin
de 5.16C. Determine la molalidad de la disolucin y la masa molar del soluto. Datos: Masa molecular
(Benceno)= 78.1121 g/mol
7. El alcanfor (C10H16O) funde a 179,8C y tiene una constante de abatimiento del punto de congelacin
excepcionalmente grande, Kf = 40C/m. Si 0,186 g de una sustancia orgnica desconocida (soluto) se
disuelve en 22,01 g de alcanfor lquido, se observa que el punto de congelacin de la mezcla es de
176,7C. Calcule la masa molar del soluto. Datos: C=12g; H=1g; O=16g.
8. Una muestra de 7.85 g de un compuesto con la formula emprica C5H4 se disuelve en 301 g de
benceno. El punto de congelacin de la disolucin es 1.5C por debajo del punto de congelacin del
benceno puro. A) Calcular la masa molar del compuesto referido. B) Determinar la formula molecular
del compuesto referido. Datos: Kf= 5.12 C/m, F emprica=64 g/mol
PRESION OSMOTICA
9. Calcule la presin osmtica de una disolucin que se forma disolviendo 50.0 mg de aspirina (C9H8O4) en
0.250 L de agua a 25C.
10. El hexabarbital, empleado en medicina como sedante y anestsico intravenoso, se compone de 61.00%
de C, 6.83% de H, 11.86% de N y 20.32% de O en masa. Una muestra de 2.505 mg en 10.00 mL de
disolucin tiene una presin osmtica de 19.7 torr a 25C. Determine la frmula molecular del
hexabarbital.
11. Se prepara una muestra de 50,00 mL de una disolucin acuosa que contiene 1,08 g de seroalbmina
humana, una protena del plasma sanguneo. La disolucin tiene una presin osmtica de 5,85 mmHg a
298 K. En la tabla proceda a calcular el peso molecular (p.m.) de la albmina. Datos: R = (0,081 L x atm /
mol x K); 1 atm = 760 torr.
12. Una muestra de 2,05 g de plstico poliestireno se disolvi en suficiente tolueno para formar 100 mL de
disolucin. La presin osmtica de esta disolucin fue de 1,21 kPa a 25C. Calcule la masa molar del
poliestireno. Datos: R = (0,081 L-atm / mol-K); 1 atm = 760 torr = 101,325 kPa.
También podría gustarte
- Examenes Quimica BasicaDocumento266 páginasExamenes Quimica BasicaPao Colls100% (15)
- Parciales AnaliticaDocumento12 páginasParciales AnaliticaMario Fernando Hurtado AnguloAún no hay calificaciones
- Experimentos de Quimica DivertidosDocumento160 páginasExperimentos de Quimica DivertidosRonny Mendez100% (17)
- 8.química 2º RedoxDocumento7 páginas8.química 2º RedoxKatherine TorresAún no hay calificaciones
- Etapa 4 - Cuestionario Fundamentos de Balance de EnergíaDocumento7 páginasEtapa 4 - Cuestionario Fundamentos de Balance de EnergíaTicsAún no hay calificaciones
- Hoja 45 Equilibrio Químico IónicoDocumento4 páginasHoja 45 Equilibrio Químico IónicoCiro Rodriguez RuizAún no hay calificaciones
- Quimica ADocumento22 páginasQuimica AyulliarperezAún no hay calificaciones
- Enlace y Geometria MolecularDocumento1 páginaEnlace y Geometria MolecularLuis VacaAún no hay calificaciones
- Equilibrio QuimicoDocumento7 páginasEquilibrio QuimicoÁlvaro VelaAún no hay calificaciones
- Ejercicios Estequiometria 1-83Documento4 páginasEjercicios Estequiometria 1-83MariaAún no hay calificaciones
- Acidobase ProblemasDocumento7 páginasAcidobase ProblemasRobert OcrospomaAún no hay calificaciones
- Tarea 8Documento6 páginasTarea 8Pedro Lermanda Luza100% (1)
- Primera Evaluacion 2013 II TDocumento4 páginasPrimera Evaluacion 2013 II TLuis VacaAún no hay calificaciones
- Actividad - Integradora - 2 Mod 12 GabrileaDocumento4 páginasActividad - Integradora - 2 Mod 12 Gabrileamariel hernandezAún no hay calificaciones
- Peso Equival SolucDocumento2 páginasPeso Equival SolucEsteban TerrazasAún no hay calificaciones
- Pruebas Referente A Medias de Dos Muestras (Muestras Pequeñas)Documento3 páginasPruebas Referente A Medias de Dos Muestras (Muestras Pequeñas)CarlosAún no hay calificaciones
- Soluciones EjerciciosDocumento9 páginasSoluciones EjerciciosEber ColqueAún no hay calificaciones
- Diseño de Experimentos Tarea #9Documento17 páginasDiseño de Experimentos Tarea #9alan alvaradoAún no hay calificaciones
- Taller 3. GravimetríaDocumento1 páginaTaller 3. GravimetríaPaula VelandiaAún no hay calificaciones
- 2 Bach Qui Problemas Sin 0607Documento103 páginas2 Bach Qui Problemas Sin 0607Antonio José Vasco MerinoAún no hay calificaciones
- DisolucionesDocumento2 páginasDisolucionesMark Wiggins50% (2)
- Segundo Examen Departamental BME - 2013-2014Documento7 páginasSegundo Examen Departamental BME - 2013-2014JMGHAún no hay calificaciones
- Ejercicios de ConcentracionDocumento6 páginasEjercicios de ConcentracionmaxforrAún no hay calificaciones
- 7 Ciaduj 0 PXJQ 4 WGC 8 Huhwyaiu 2 R 3 Im 3 DDocumento3 páginas7 Ciaduj 0 PXJQ 4 WGC 8 Huhwyaiu 2 R 3 Im 3 DLeidy LujanoAún no hay calificaciones
- Ejercicios Propiedades ColigativasDocumento4 páginasEjercicios Propiedades ColigativasJhonatan Dávila100% (1)
- Problemario SinRespuestaDocumento6 páginasProblemario SinRespuestaJorge FrancoAún no hay calificaciones
- Práctica 1 de Laboratorio VirtualDocumento21 páginasPráctica 1 de Laboratorio VirtualYonathan CórdovaAún no hay calificaciones
- Fundamentos de QuimicaDocumento3 páginasFundamentos de QuimicaSergio PerezAún no hay calificaciones
- Formula Mínima y Fórmula Molecular 2Documento2 páginasFormula Mínima y Fórmula Molecular 2Roberto SantiagoAún no hay calificaciones
- Tarea 11 - Cálculo PHDocumento2 páginasTarea 11 - Cálculo PHCuau SuarezAún no hay calificaciones
- Serie Energia Libre de GibbsDocumento3 páginasSerie Energia Libre de Gibbsanon_586714185Aún no hay calificaciones
- 1º Bto. Test QuímicaDocumento37 páginas1º Bto. Test QuímicaSILVIA0% (1)
- TALLER DISOLUCIONES EN QUIMICA Fase 3Documento8 páginasTALLER DISOLUCIONES EN QUIMICA Fase 3Carlos Uriel Cortes CamposAún no hay calificaciones
- 10solubilidad, Precipitacionyredox 26331Documento5 páginas10solubilidad, Precipitacionyredox 26331Efrain GuerreroAún no hay calificaciones
- ProblemasDocumento2 páginasProblemasoswaldo950% (2)
- mol, 18.074 CM /mol, 58.673 CM /molDocumento2 páginasmol, 18.074 CM /mol, 58.673 CM /molLuisMirkoAún no hay calificaciones
- Bloques Completos Al AzarDocumento9 páginasBloques Completos Al AzarJaime Lopez100% (1)
- Taller 10 PH Acidos Poliproticos-2Documento2 páginasTaller 10 PH Acidos Poliproticos-2Andzhiita SaampeerAún no hay calificaciones
- UNIDAD 3 Disoluciones Ejercicios PropuestosDocumento4 páginasUNIDAD 3 Disoluciones Ejercicios PropuestosDlcm Born To WinAún no hay calificaciones
- Cálculos Químicos ResueltosDocumento11 páginasCálculos Químicos ResueltosCheh CHAún no hay calificaciones
- Repartido Acido BaseDocumento1 páginaRepartido Acido BasealiciamarielaAún no hay calificaciones
- Ejercicios ING 530025-1 PDFDocumento12 páginasEjercicios ING 530025-1 PDFCarolinaAún no hay calificaciones
- Guía de 1º - RecuperaciónDocumento9 páginasGuía de 1º - RecuperaciónJesús Marcos Segura MartínAún no hay calificaciones
- Taller Capitulo 3 PDFDocumento3 páginasTaller Capitulo 3 PDFJuan SebastianAún no hay calificaciones
- Seminario 5 Halogenuros de AlquiloDocumento4 páginasSeminario 5 Halogenuros de AlquiloRaúl Nicolás Caicedo VidalAún no hay calificaciones
- Método de OndaDocumento9 páginasMétodo de OndaAna VelázquezAún no hay calificaciones
- Tabla de Entalpía Chang 11 EdicionDocumento5 páginasTabla de Entalpía Chang 11 EdicionjesusAún no hay calificaciones
- Guia Ejercicos Tampones Con ResolucionDocumento7 páginasGuia Ejercicos Tampones Con ResolucionMauricioReyesAún no hay calificaciones
- Química General Guía de Ejercicios Nº2 - SolucionesDocumento6 páginasQuímica General Guía de Ejercicios Nº2 - SolucionesReyna Maria SagastumeAún no hay calificaciones
- Calor Molar de Una Reacción QuímicaDocumento6 páginasCalor Molar de Una Reacción QuímicaSebastian PertuzAún no hay calificaciones
- TAREA 1 FISICOQUIMICA - Grupo N°3Documento14 páginasTAREA 1 FISICOQUIMICA - Grupo N°3Anthony TanakaAún no hay calificaciones
- Capitulo 1 (Introduccion)Documento5 páginasCapitulo 1 (Introduccion)Rodolfo Jose Mendoza TorrealbaAún no hay calificaciones
- Tema II Química 1Documento11 páginasTema II Química 1CCAún no hay calificaciones
- Docsity Ejercicios de PH Poh Constante de Disociacion Acida Ka y Basica KBDocumento10 páginasDocsity Ejercicios de PH Poh Constante de Disociacion Acida Ka y Basica KBJimy ValentínAún no hay calificaciones
- Syllabus Química Básica IDocumento5 páginasSyllabus Química Básica IVoice Of Heart100% (1)
- Taller #1 DisoluconesDocumento1 páginaTaller #1 Disoluconesmonica ayalaAún no hay calificaciones
- Propiedades ColigativasDocumento17 páginasPropiedades ColigativasKaren Lizzeth Ortega ZamarripaAún no hay calificaciones
- Guia 04 Estequiometria QUI080Documento13 páginasGuia 04 Estequiometria QUI080Alan John Andrades100% (2)
- Problemas de Quimica I - 8 JulioDocumento5 páginasProblemas de Quimica I - 8 JulioAndre BarrantesAún no hay calificaciones
- Equilibrio Ionico Cap ViiDocumento43 páginasEquilibrio Ionico Cap ViiPedro Leon CamposAún no hay calificaciones
- Resolucion Practica ExamenDocumento9 páginasResolucion Practica ExamenJohann StzAún no hay calificaciones
- Tarea (9) GrupoDocumento8 páginasTarea (9) GrupoKevin AndresAún no hay calificaciones
- DisolucionesDocumento7 páginasDisolucionesbarlosAún no hay calificaciones
- Soluciones 1-2013 1TDocumento2 páginasSoluciones 1-2013 1TLuis VacaAún no hay calificaciones
- CT - QUI 1 Propie ColigaDocumento9 páginasCT - QUI 1 Propie ColigaPaul LemaAún no hay calificaciones
- ColigativasDocumento33 páginasColigativasDiego ArriagadaAún no hay calificaciones
- Problemas de DisolucionesDocumento6 páginasProblemas de Disolucionesmg88mgAún no hay calificaciones
- Lab 1 Variacion Densidad de Líquidos Con La TemperaturaDocumento1 páginaLab 1 Variacion Densidad de Líquidos Con La TemperaturaLuis VacaAún no hay calificaciones
- Guia FisicoquímicaDocumento36 páginasGuia FisicoquímicaLuis VacaAún no hay calificaciones
- Ejercicios Termodinamica PDFDocumento21 páginasEjercicios Termodinamica PDFIsrael Santiago Pancca M0% (1)
- Produccion Catalitica de OxigenoDocumento3 páginasProduccion Catalitica de OxigenoLuis Vaca0% (1)
- Solidos EjerciciosDocumento1 páginaSolidos EjerciciosLuis VacaAún no hay calificaciones
- Practicas Laboratorio Fisicoquimica PDFDocumento77 páginasPracticas Laboratorio Fisicoquimica PDFGogoAún no hay calificaciones
- II. Sistemas DispersosDocumento35 páginasII. Sistemas DispersosAlexander PortilloAún no hay calificaciones
- Conceptos Teoricos Marcha AnaliticaDocumento59 páginasConceptos Teoricos Marcha AnaliticaLuis VacaAún no hay calificaciones
- Ejercicios Familias Del Nitrogeno y CarbonoDocumento9 páginasEjercicios Familias Del Nitrogeno y CarbonoLuis VacaAún no hay calificaciones
- Termoquimica 2014Documento5 páginasTermoquimica 2014Luis Vaca50% (2)
- Quimica Nuclear 2014Documento4 páginasQuimica Nuclear 2014Luis VacaAún no hay calificaciones
- Manual FisicoquimicaDocumento89 páginasManual Fisicoquimicammartinezr26095836Aún no hay calificaciones
- ESTEQUIOMETRIADocumento1 páginaESTEQUIOMETRIALuis Vaca0% (1)
- Acidos y Bases EjerciciosDocumento1 páginaAcidos y Bases EjerciciosLuis Vaca100% (1)
- CINETICA QUIMICA EjerciciosDocumento4 páginasCINETICA QUIMICA EjerciciosLuis VacaAún no hay calificaciones
- Liquidos EjerciciosDocumento3 páginasLiquidos EjerciciosLuis Vaca0% (4)
- Calorimetria 2014Documento2 páginasCalorimetria 2014Luis Vaca50% (2)
- Metalurgia 2014Documento4 páginasMetalurgia 2014Luis VacaAún no hay calificaciones
- Quimica Del Agua 2014Documento3 páginasQuimica Del Agua 2014Luis Vaca100% (1)
- Electroquimica 2014Documento4 páginasElectroquimica 2014Luis VacaAún no hay calificaciones
- Formulario Primer ParcialDocumento1 páginaFormulario Primer ParcialLuis VacaAún no hay calificaciones
- Formulario Primer ParcialDocumento1 páginaFormulario Primer ParcialLuis VacaAún no hay calificaciones
- Ejercicios 1 P Quimica 1Documento3 páginasEjercicios 1 P Quimica 1Luis VacaAún no hay calificaciones
- Segunda Evaluacion QG1 IT 2013Documento5 páginasSegunda Evaluacion QG1 IT 2013Luis Vaca0% (1)
- Ejercicios MejoramientoDocumento4 páginasEjercicios MejoramientoLuis Vaca100% (1)
- Evaluacion de Lab QG1 IT 2013Documento3 páginasEvaluacion de Lab QG1 IT 2013Luis VacaAún no hay calificaciones
- 1Documento14 páginas1chaito0% (1)
- FUERZAS HIDROSTATICAS - pdf1Documento13 páginasFUERZAS HIDROSTATICAS - pdf1Diego Hanck MartínezAún no hay calificaciones
- Construccion de Sistema de Circuito de Alarma Con ReleDocumento16 páginasConstruccion de Sistema de Circuito de Alarma Con ReleJonathan CrisAún no hay calificaciones
- Aplicaciones Basicas de Los Circuitos RLCDocumento49 páginasAplicaciones Basicas de Los Circuitos RLCNiko RamosAún no hay calificaciones
- Gases IdealesDocumento9 páginasGases IdealesEdgar Cano FrancoAún no hay calificaciones
- Atoche Roxy - Ochoa Quispe - Jacobo Dominguez - Zavaleta Ruth - Selección de BombaaaDocumento39 páginasAtoche Roxy - Ochoa Quispe - Jacobo Dominguez - Zavaleta Ruth - Selección de BombaaaPEREDA ZELADA DANIEL ARTUROAún no hay calificaciones
- Todas Las Clases PDFDocumento275 páginasTodas Las Clases PDFroymar peraltAún no hay calificaciones
- PRÁCTICA 4 Campo Eléctrico y Superficies Equipotenciales - ReporteDocumento7 páginasPRÁCTICA 4 Campo Eléctrico y Superficies Equipotenciales - ReporteFernanda DelgadoAún no hay calificaciones
- Guía de Problemas Sobre Hidrodinámica.Documento5 páginasGuía de Problemas Sobre Hidrodinámica.Amaya AlejandroAún no hay calificaciones
- Mantenimiento de La Parte de Alta TensiónDocumento28 páginasMantenimiento de La Parte de Alta TensiónFredy RoaAún no hay calificaciones
- Curso de Mantenimiento de Equipo MedicoDocumento136 páginasCurso de Mantenimiento de Equipo MedicoCarmeloAún no hay calificaciones
- Antena YugiDocumento13 páginasAntena YugiNeo RodriguezAún no hay calificaciones
- Capitulo 1 Introducción ElectricidadDocumento49 páginasCapitulo 1 Introducción ElectricidadPedro De Leon GuerraAún no hay calificaciones
- Ejercicios de Biomasa y GeotermiaDocumento3 páginasEjercicios de Biomasa y GeotermiaAimarAB SkilletAún no hay calificaciones
- Problemario Circuitos ElectricosDocumento19 páginasProblemario Circuitos ElectricosLester OrtízAún no hay calificaciones
- Trabajo Final Grupo 4 Ingenieria Mecanica ElectricaDocumento33 páginasTrabajo Final Grupo 4 Ingenieria Mecanica ElectricaJose Valdez RuizAún no hay calificaciones
- Taller de Ley de Ohm y WattDocumento5 páginasTaller de Ley de Ohm y Wattአንድሪያ ሌኒስAún no hay calificaciones
- Trabajo Realizado Por Un ResorteDocumento4 páginasTrabajo Realizado Por Un ResorteKugo BteAún no hay calificaciones
- Libro Unidad Ii - Muñoz Caja Kenye NiloDocumento13 páginasLibro Unidad Ii - Muñoz Caja Kenye NiloKENYE NILO MUÑOZ CAJAAún no hay calificaciones
- SESIÓN 9 - MF1 - Descripciones Lagrangiana y EulerianaDocumento15 páginasSESIÓN 9 - MF1 - Descripciones Lagrangiana y EulerianaAmalex AbdiAún no hay calificaciones
- Dinamo MetroDocumento5 páginasDinamo MetroDeibyM8Aún no hay calificaciones
- Centros Carga QodDocumento4 páginasCentros Carga QodLuis Miguel Vázquez PérezAún no hay calificaciones
- Circuito Tanque PaperDocumento3 páginasCircuito Tanque PaperCajamarca Alex0% (1)
- Rotacion Alrededor de Un Eje FijoDocumento27 páginasRotacion Alrededor de Un Eje FijoRaúl ChávezAún no hay calificaciones
- Avance Laboratorio 4 TransferenciaDocumento19 páginasAvance Laboratorio 4 TransferenciaFranco MendozaAún no hay calificaciones
- Antología U-4 HumidificaciónDocumento15 páginasAntología U-4 Humidificaciónmariela martinez gonzalezAún no hay calificaciones