Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Exergía
Cargado por
Lucia Galvan0 calificaciones0% encontró este documento útil (0 votos)
6 vistas15 páginasTítulo original
Exergía.pptx
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PPTX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPTX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
6 vistas15 páginasExergía
Cargado por
Lucia GalvanCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPTX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 15
Exergía
Nicolas Hurtado Ceballos
Luis Fernando Jalal Contreras
Santiago Morales Beltrán
¿Que es la exergía?
• La exergía es un parámetro que mide la calidad de la energía. Este
parámetro puede emplearse para analizar la eficiencia energética de los
procesos industriales. Con un análisis de energía pueden compararse
diferentes alternativas para comprobar cuál tiene el mayor rendimiento
energético.
Utilidad
• Una de las grandes utilidades que nos
brinda el análisis exegético es poder
evaluar la capacidad de producir trabajo
que se pierde en cada proceso dentro de
una planta de fuerza o cualquier otro
proceso y con esta visión definir en que
partes es más conveniente actuar de una
manera priorizada para ir corrigiendo los
incrementos de irreversibilidades que se
presentan durante la operación de la
planta.
Estado muerto
• La exergía se consume por completo cuando
la presión y la temperatura se igualan a la del
entorno. Una vez que se iguala la temperatura
del sistema con la del ambiente (alcanzándose
el equilibrio térmico) y se iguala su presión
con la exterior (llegándose al equilibrio
mecánico), ya no se puede extraer energía
adicional. Se dice que en ese caso el sistema
ha alcanzado el “estado muerto”.
Exergía y Energía
• Los diferentes tipos de energía presentan también diferentes calidades,
entendiendo por calidad la cantidad de trabajo útil que se puede obtener.
Estas diferencias radican en la posibilidad de producir trabajo o de
transformar un tipo de energía en otro.
• Vemos, por tanto, que la calidad de las formas desordenadas de energía
depende de la entropía, del tipo de energía y de las funciones
termodinámicas del sistema y del ambiente; las formas ordenadas, por el
contrario, no dependen de la entropía, tienen una calidad máxima e
invariable y son totalmente convertibles en otras formas de energía.
Energía Ordenada
• La energía ordenada (o de alta calidad) puede presentarse de las formas
siguientes:
• Energía potencial, tal como la almacenada en un campo gravitatorio,
eléctrico o magnético, o en la deformación de un muelle perfectamente
elástico, etc.
• Energía cinética no aleatoria, como la almacenada en un volante en
rotación, o en un chorro no turbulento de un fluido ideal.
Energía desordenada
• Pertenece a esta clase la energía interna, tanto de naturaleza física como química,
asociada con movimientos aleatorios de átomos o moléculas.
• Peculiaridades de los procesos que pretenden obtener la conversión más eficaz
de energía desordenada en energía ordenada:
• − Los procesos han de ser reversibles.
• − Hay que aplicar el Segundo Principio en el análisis.
• − El proceso origina, en general, cambios entrópicos en los sistemas que
intervienen.
Exergía asociada con la energía cinética y
potencial
• La energía cinética y potencial son
formas de energía mecánicas que
pueden convertirse en trabajo. Estos
tipos de energía pueden usarse para
calcular la exergía en ciertos procesos,
porque están completamente disponibles
para realizar trabajo, sin embargo la
energía interna y entalpia no están
completamente disponibles para realizar
trabajo.
Tipos de Exergía
• Si excluimos los efectos nucleares,
magnéticos y eléctricos, la exergía, B, de
una sustancia se puede dividir en cuatro
componentes: exergía cinética B k, exergía
potencial Bp, exergía física Bf y exergía
química B0.
• La exergía cinética es iguala la energía
cinética cuando la velocidad tiene como
nivel de referencia la superficie de la Tierra.
Lo mismo ocurre con la exergía potencial
• La exergía física es el trabajo que se puede obtener sometiendo a la sustancia
a procesos físicos reversibles desde la temperatura y presión iniciales, hasta el
estado determinado por la presión y la temperatura del entorno.
• La exergía química es el trabajo que se puede obtener de una sustancia que
se encuentra a la presión y temperatura del entorno, si alcanza un estado de
equilibrio termodinámico mediante reacciones químicas.
• En ocasiones, a la suma de la exergía física y química se le denomina exergía
térmica, Bt.
Irreversibilidades
• La causa de la destrucción de exergía son
las irreversibilidades de los sistemas, de
esta forma la exergía destruida cuantifica
en unidades de energía las
irreversibilidades presentadas en los
procesos.
• Un proceso se dice que es reversible si es posible que regresando cada
paso del mismo se reestablezcan exactamente a su estado inicial
respectivo el sistema y el medio circundante.
• Un proceso irreversible es cuando no hay forma de regresarlo, esto es,
que no hay medios por los cuales el sistema y sus alrededores pueden ser
exactamente restaurados a sus respectivos estados iníciales.
• Un sistema que ha pasado por un proceso irreversible no necesariamente
es excluido para ser restaurado a su estado inicial, sin embargo, aunque el
sistema fuera restaurado a su estado inicial, no será posible regresar el
entorno al estado en el que estaba inicialmente.
• Hay varios efectos en los que su presencia durante un proceso le causa
irreversibilidades, entre estos se incluyen los siguientes, aunque no son
limitativos:
• La transferencia de calor a través de una diferencia de temperatura finita
• La expansión de un gas o un líquido a una presión menor como la
mostrada
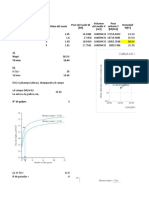
Ejemplo
También podría gustarte
- MF0624_1 - Técnicas básicas de electricidad de vehículosDe EverandMF0624_1 - Técnicas básicas de electricidad de vehículosCalificación: 5 de 5 estrellas5/5 (2)
- 1 - Introduccion A La Electricidad PDFDocumento27 páginas1 - Introduccion A La Electricidad PDFNuma Marcial GaiborAún no hay calificaciones
- UF0565 - Eficiencia energética en las instalaciones de calefacción y ACS en los edificiosDe EverandUF0565 - Eficiencia energética en las instalaciones de calefacción y ACS en los edificiosAún no hay calificaciones
- Diseño de Losas MacizasDocumento30 páginasDiseño de Losas MacizasCarlos Andres Villarroel GuerreroAún no hay calificaciones
- Caracterización de TuberíasDocumento63 páginasCaracterización de TuberíasJaime AlfonsoAún no hay calificaciones
- Trabajo MaximoDocumento13 páginasTrabajo MaximoJavier Johnson Lesciur100% (1)
- Eficiencia energética en las instalaciones de calefacción y acs en los edificios. ENAC0108De EverandEficiencia energética en las instalaciones de calefacción y acs en los edificios. ENAC0108Aún no hay calificaciones
- Manual Tubo CobreDocumento35 páginasManual Tubo CobreMlg José100% (1)
- Presentación TermoquímicaDocumento31 páginasPresentación TermoquímicaAna BussoAún no hay calificaciones
- Disponibilidad de La Energía y ExergíaDocumento20 páginasDisponibilidad de La Energía y Exergíaanon_922136214100% (3)
- Balance de Materia, Energía y ExergíaDocumento31 páginasBalance de Materia, Energía y ExergíaYosimar NC67% (3)
- Balance de Materia Energia y Exergia PDFDocumento31 páginasBalance de Materia Energia y Exergia PDFCarlos Uriel Martinez TinocoAún no hay calificaciones
- Exer GiaDocumento17 páginasExer GiaAaron EscobarAún no hay calificaciones
- EXERGÍADocumento8 páginasEXERGÍAAngie Jolley VélizAún no hay calificaciones
- PRACTICA No 5 Termodinámica FescDocumento3 páginasPRACTICA No 5 Termodinámica FescAdrian GarciaAún no hay calificaciones
- Eter2 U1 A3 JaqmDocumento4 páginasEter2 U1 A3 JaqmJavier Quintero Monsivais100% (1)
- Termodinámica Resumen Cap 8Documento3 páginasTermodinámica Resumen Cap 8Milton OrtegaAún no hay calificaciones
- DISPONIBILIDADDocumento13 páginasDISPONIBILIDADAnonymous Rf0neepQtAún no hay calificaciones
- Cap.2 Primera LeyDocumento20 páginasCap.2 Primera LeyMichael AguilarAún no hay calificaciones
- Balance de Energã - A 09 AgostoDocumento19 páginasBalance de Energã - A 09 AgostoMariana TreviñoAún no hay calificaciones
- Eter2 U1 A3 RiigDocumento5 páginasEter2 U1 A3 RiigRicardo Ibarra50% (2)
- Balance de Energía en Ingeniería QuímicaDocumento22 páginasBalance de Energía en Ingeniería QuímicaDaniel EsparzaAún no hay calificaciones
- ExergíaDocumento42 páginasExergíaSimón ZamoraAún no hay calificaciones
- Present FQ Primera Ley IIDocumento34 páginasPresent FQ Primera Ley IILuz Mery MotaAún no hay calificaciones
- Apuntes Unidad 3. Termoquímica. 1 EvDocumento8 páginasApuntes Unidad 3. Termoquímica. 1 EvLicenciado PugbertoAún no hay calificaciones
- Exergia e IrreversibilidadDocumento9 páginasExergia e IrreversibilidadEdag GadeAún no hay calificaciones
- 1° Semana - Balance de Materia y Cantidad de MovimientoDocumento24 páginas1° Semana - Balance de Materia y Cantidad de Movimientorichard suri conzaAún no hay calificaciones
- TD-Cap-4 - (4.1-4.2) Enunciados de La Segunda LeyDocumento39 páginasTD-Cap-4 - (4.1-4.2) Enunciados de La Segunda Leycras97Aún no hay calificaciones
- 2da Ley de TermodinamcaDocumento6 páginas2da Ley de Termodinamcajulian sustersickAún no hay calificaciones
- Expo de Procesos UnitariosDocumento16 páginasExpo de Procesos UnitariosJahayra BurgosAún no hay calificaciones
- Procesos Reversibles e IrreversiblesDocumento10 páginasProcesos Reversibles e IrreversiblesSony KenpachiAún no hay calificaciones
- Ova 06 - Balance de EnergíaDocumento46 páginasOva 06 - Balance de EnergíaJavier A. MontoyaAún no hay calificaciones
- Procesos Reversibles e IrreversiblesDocumento12 páginasProcesos Reversibles e IrreversiblesDianne Duarte100% (1)
- Clase 4. Semana 02, Ximena Guardia, 25.08.23Documento29 páginasClase 4. Semana 02, Ximena Guardia, 25.08.23AlternoAún no hay calificaciones
- Formas de EnergíaDocumento60 páginasFormas de EnergíaCristofer SalazarAún no hay calificaciones
- ExergíaDocumento36 páginasExergíabrandon hernandezAún no hay calificaciones
- Energia Interna - TermodinamicaDocumento13 páginasEnergia Interna - TermodinamicaReyAún no hay calificaciones
- Conceptos Generales de Termodinamica PDFDocumento19 páginasConceptos Generales de Termodinamica PDFIvan BMAún no hay calificaciones
- Balance de Materia SEMANA 9Documento46 páginasBalance de Materia SEMANA 9Adrián Lume HuayllaniAún no hay calificaciones
- Cambio de Exergía de Un SistemaDocumento17 páginasCambio de Exergía de Un SistemaOscar OsorioAún no hay calificaciones
- TERMOQUIMICA PresentacionDocumento76 páginasTERMOQUIMICA Presentaciondavid morocho100% (1)
- Balance de Materia y Energía en Planta de Potabilización de Agua IDocumento13 páginasBalance de Materia y Energía en Planta de Potabilización de Agua ICyntHya LissEtAún no hay calificaciones
- Grupo 3 Trabajo Máximo, Trabajo Reversible e IrreversibilidadDocumento11 páginasGrupo 3 Trabajo Máximo, Trabajo Reversible e Irreversibilidadjavier amaya100% (1)
- Laboratorio de Balance - Balance de Energia 1Documento14 páginasLaboratorio de Balance - Balance de Energia 1geraldineAún no hay calificaciones
- TERMODINAMICADocumento58 páginasTERMODINAMICAWences RqtAún no hay calificaciones
- Nota Técnica 2Documento16 páginasNota Técnica 2dortz55Aún no hay calificaciones
- Presentation 2 Course 1 1 743082Documento27 páginasPresentation 2 Course 1 1 743082Agustín SuárezAún no hay calificaciones
- UNIDAD 6 (Autoguardado)Documento56 páginasUNIDAD 6 (Autoguardado)Paulina LoeAún no hay calificaciones
- 2016.06.20.balance de Energia EXAMEN LUNESDocumento60 páginas2016.06.20.balance de Energia EXAMEN LUNESnormaAún no hay calificaciones
- EnergíaDocumento25 páginasEnergíaorton26Aún no hay calificaciones
- EXERGIA InformeDocumento27 páginasEXERGIA InformeAlexandra Jeniffer Ruiz CarranzaAún no hay calificaciones
- Unidad 3Documento30 páginasUnidad 3tenhuayaca60% (5)
- Balance de Energía InformeDocumento6 páginasBalance de Energía InformeOlguer Díaz ValenciaAún no hay calificaciones
- Tema 5 TermoDocumento29 páginasTema 5 TermoSandy KikeyAún no hay calificaciones
- Transferencia de Energía Por Calor, Trabajo y MasaDocumento52 páginasTransferencia de Energía Por Calor, Trabajo y Masacardu1100% (3)
- Procesos Reversibles e IrreversiblesDocumento64 páginasProcesos Reversibles e IrreversiblesOmar AlonsoAún no hay calificaciones
- Term Odin A MicaDocumento18 páginasTerm Odin A MicaPIERO JAVIER CASTILLA SEDANOAún no hay calificaciones
- Procesos de Bombeo y Compresion de HidrocarburosDocumento7 páginasProcesos de Bombeo y Compresion de HidrocarburosGonzalo TellesAún no hay calificaciones
- 2.5 TermodinamicaDocumento45 páginas2.5 TermodinamicaIvan PriegoAún no hay calificaciones
- Presentación Termodinámica ClaseDocumento34 páginasPresentación Termodinámica ClaseLuis GuevaraAún no hay calificaciones
- ExergiaDocumento3 páginasExergiaFRANCISCO EMMANUEL GODINEZ MARTINEZAún no hay calificaciones
- La Termodinamica 1 Sesion 7 y 8Documento88 páginasLa Termodinamica 1 Sesion 7 y 8gustavo_castro_17Aún no hay calificaciones
- Investigacion Tema 5 TermodinamocaDocumento4 páginasInvestigacion Tema 5 TermodinamocaTamar evansAún no hay calificaciones
- ICV312 - Clase 14 PDFDocumento38 páginasICV312 - Clase 14 PDFValentina LüengoAún no hay calificaciones
- Tarea 3 - 2022Documento9 páginasTarea 3 - 2022Lucia GalvanAún no hay calificaciones
- Capitulo 2 InviasDocumento212 páginasCapitulo 2 InviasLucia GalvanAún no hay calificaciones
- Ejercicio Taller 3Documento8 páginasEjercicio Taller 3Lucia GalvanAún no hay calificaciones
- Taller 2, Pto 2Documento3 páginasTaller 2, Pto 2Lucia GalvanAún no hay calificaciones
- Tarea 3 - 2022Documento6 páginasTarea 3 - 2022Lucia GalvanAún no hay calificaciones
- Ejercicio Proctor 1Documento3 páginasEjercicio Proctor 1Lucia GalvanAún no hay calificaciones
- SIMULcionDocumento3 páginasSIMULcionLucia GalvanAún no hay calificaciones
- Problema 2Documento5 páginasProblema 2Lucia GalvanAún no hay calificaciones
- Mini Proyecto ConstrucciónDocumento1 páginaMini Proyecto ConstrucciónLucia GalvanAún no hay calificaciones
- Tarea 3 - 2022 SuelosDocumento3 páginasTarea 3 - 2022 SuelosLucia GalvanAún no hay calificaciones
- Taller 3 Granulares y AsfaltosDocumento2 páginasTaller 3 Granulares y AsfaltosLucia GalvanAún no hay calificaciones
- MARSHALLDocumento35 páginasMARSHALLLucia GalvanAún no hay calificaciones
- Docsity Actividad de Relaciones de FaseDocumento6 páginasDocsity Actividad de Relaciones de FaseLucia GalvanAún no hay calificaciones
- Cuenta de Cobro Marzo 2022Documento2 páginasCuenta de Cobro Marzo 2022Lucia GalvanAún no hay calificaciones
- Marshall 2 PDFDocumento1 páginaMarshall 2 PDFLucia GalvanAún no hay calificaciones
- Excel SuelosDocumento4 páginasExcel SuelosLucia GalvanAún no hay calificaciones
- ELECTROTECNIA2020Documento18 páginasELECTROTECNIA2020Lucia GalvanAún no hay calificaciones
- MARSHALLDocumento35 páginasMARSHALLLucia GalvanAún no hay calificaciones
- ExergíaDocumento15 páginasExergíaLucia GalvanAún no hay calificaciones
- ELECTROTECNIA2020Documento18 páginasELECTROTECNIA2020Lucia GalvanAún no hay calificaciones
- Marshall 2 PDFDocumento1 páginaMarshall 2 PDFLucia GalvanAún no hay calificaciones
- CAP 41-Asientos ElastoméricosDocumento4 páginasCAP 41-Asientos ElastoméricossafnatpaneajAún no hay calificaciones
- Construcciones RESUMEN Y PREGUNTAS DE EXAMENDocumento41 páginasConstrucciones RESUMEN Y PREGUNTAS DE EXAMENMartinez AldanaAún no hay calificaciones
- TableroDocumento4 páginasTableroestefany blancoAún no hay calificaciones
- Columnas: Caso 2 (Sesión 7.1)Documento17 páginasColumnas: Caso 2 (Sesión 7.1)Kassandra Llontop NeciosupAún no hay calificaciones
- Transformación de Materiales - Lección Unidad 2Documento4 páginasTransformación de Materiales - Lección Unidad 2Kenneth MosqueraAún no hay calificaciones
- Reporte de Excavaciones PilotesDocumento9 páginasReporte de Excavaciones PilotesAgustin CahuanaAún no hay calificaciones
- Daniel Movilla Vega 02Documento275 páginasDaniel Movilla Vega 02BraianAún no hay calificaciones
- Deformacion de Los MaterialesaaDocumento11 páginasDeformacion de Los Materialesaa969609993Aún no hay calificaciones
- MIP Construcción Brochure v5.0Documento33 páginasMIP Construcción Brochure v5.0AlivaremarkAún no hay calificaciones
- FÍSICA Semana14Documento46 páginasFÍSICA Semana14carlos rubio garciaAún no hay calificaciones
- Hormigon 1 Cap2Documento37 páginasHormigon 1 Cap2Patricio Isaac Lopez CarrascoAún no hay calificaciones
- C.U. 04 - Instalaciones Electricas y MecanicasDocumento81 páginasC.U. 04 - Instalaciones Electricas y MecanicasYerson AraujoAún no hay calificaciones
- Clases y Tipos de TuberíasDocumento7 páginasClases y Tipos de TuberíasAlexander PeresAún no hay calificaciones
- NBR NM 36 - 1995 - Concreto Fresco - Separacao de Agregados Grandes Por Peneiramento PDFDocumento7 páginasNBR NM 36 - 1995 - Concreto Fresco - Separacao de Agregados Grandes Por Peneiramento PDFVitorMenezesAún no hay calificaciones
- Diseño de PuentesDocumento120 páginasDiseño de PuentesAngel CMAún no hay calificaciones
- Recuperacion Recristalizacion y Crecimiento de Grano UNSDocumento44 páginasRecuperacion Recristalizacion y Crecimiento de Grano UNSMarcos Oliverth Zúñiga ZapataAún no hay calificaciones
- Diagrama de FasesDocumento67 páginasDiagrama de FasessandyozAún no hay calificaciones
- ALUMINADocumento4 páginasALUMINAKsr VicsAún no hay calificaciones
- Elementos de Cimentación - Manual Del UsuarioDocumento22 páginasElementos de Cimentación - Manual Del UsuarioEdgar AlcantaraAún no hay calificaciones
- Construyendo Con SuperboardDocumento89 páginasConstruyendo Con SuperboardMiguel MamaniAún no hay calificaciones
- Practica - Calor - Específico - de - Un - Metal (A)Documento5 páginasPractica - Calor - Específico - de - Un - Metal (A)Gineth Carolina Torres MorenoAún no hay calificaciones
- Informe 1. La Ley de MeyerDocumento15 páginasInforme 1. La Ley de MeyerJSET_JOKERAún no hay calificaciones
- Fichas Tecnicas Pletinas Cobre 2.0Documento1 páginaFichas Tecnicas Pletinas Cobre 2.0JUAN DAVID MARTÍNEZ GALINDOAún no hay calificaciones
- FundicionesDocumento25 páginasFundicionescarlosiqm100% (1)
- Tablero de Demostracion Ma 2067Documento15 páginasTablero de Demostracion Ma 2067Sergio CoronadoAún no hay calificaciones
- 18.2-Mantenimiento Periodico de CarreterasDocumento29 páginas18.2-Mantenimiento Periodico de CarreterasF J Garcia Carhuas100% (1)