Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Teorico Oxidos
Cargado por
gimenaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Teorico Oxidos
Cargado por
gimenaCopyright:
Formatos disponibles
FORMACION DE COMPUESTOS: OXIDOS BASICOS Y ACIDOS
Leer detenidamente las siguientes explicaciones:
Reacciones químicas
En general, las reacciones químicas se manifiestan con desprendimiento de calor, de luz o de algún
gas. Esto sucede, por ejemplo, cuando encendemos carbón para cocinar un asado, cuando la masa
leva en el horno, o bien cuando un motor funciona (combustión). También puede ocurrir un cambio
de color o aparecer un precipitado. Sin embargo, en algunos casos, los cambios no resultan tan
evidentes. Por ejemplo, ¿Se darían cuenta a simple vista de que una planta realiza la fotosíntesis o
de que la saliva degrada alimentos en la boca?
Una transformación o reacción química se produce cuando una o varias sustancias, llamadas
reactivos, se transforman, en determinadas condiciones, en nuevas sustancias, llamadas productos
de reacción.
Una reacción química se representa
mediante
una ecuación química:
A+B→C+D
Analicemos ahora la imagen:
A la reacción que allí se ve podríamos
leerla de la
siguiente forma: El reactivo A se
combina con el
reactivo B para dar un producto C y
otro
producto D.
Por ejemplo: El hierro (reactivo) se
combina con
el oxígeno (reactivo) para dar óxido de hierro
(producto, en este ejemplo hay un solo
producto):
2 Fe + O2 → 2 FeO
En el ejemplo anterior, vemos que tenemos reactivos: Hierro (Fe) y Oxígeno (O2) y que se forma un
producto que es el óxido de hierro (FeO) se ha dado una reacción química, que hemos representado
mediante una ecuación química. El 2 que se agrega delante del Fe y del FeO, se llama “coeficiente”
se agregan para “balancear” la ecuación y que de esta manera se cumpla la “Ley de conservación
de masa”, ya que la cantidad de átomos antes y después de la reacción debe ser la misma; los
átomos no se crean ni se destruyen, sino que modifican su distribución.
Compuestos químicos inorgánicos
Los compuestos químicos inorgánicos están formados a partir de metales y no metales. El más
abundante y conocido es el agua: H2O. Otros compuestos son: La sal de mesa, llamada cloruro de
sodio (NaCl), dióxido de carbono (CO2). Además de estos, existen muchísimos más compuestos
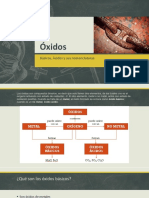
químicos, que podemos clasificar a partir del siguiente cuadro:
Prof. Isaia Vanesa QUIMICA-6º A
COMPUESTO QUÍMICOS: ÓXIDOS
Como decíamos anteriormente, los ÓXIDOS son compuestos formados por OXÍGENO y otro
elemento químico. Si este elemento es un NO METAL resulta ser un óxido ácido y si es un metal
constituye un óxido básico.
Para formar un óxido o
cualquier sustancia del
cuadro
que se mostró
anteriormente,
es necesario que los
elementos
que reaccionan, se
enlacen, es
decir se combinan y
crean
nuevas uniones, formando así
nuevos compuestos. Estos
enlaces ocurren gracias a que
los elementos toman, ceden y/o
comparten sus electrones. A la
cantidad de electrones que se ponen en juego para crear enlaces se la denomina “estado de
oxidación” (o también conocido como valencia). Deberán aprender a encontrar el estado de
oxidación de un elemento en la tabla periódica, y tené en cuenta que hay elementos que tienen
más de un estado de oxidación:
REPASEMOS COMO SE FORMA UN ÓXIDO:
Por ejemplo: SODIO + OXÍGENO --> ÓXIDO DE SODIO
Busquemos en la tabla periódica la valencia del sodio y del oxígeno:
VALENCIA SODIO (Na): 1
VALENCIA OXÍGENO (O): 2
Prof. Isaia Vanesa QUIMICA-6º A
Ahora hagámos la reacción química utilizando los símbolos de los elementos y sus valencias:
Na + O2 --> Na2O
Ahora debemos observar y respondernos: ¿Se cumple la ley de conservación de masa? Si no se
cumple, debemos BALANCEAR (O EQUILIBRAR) esta reacción química. Analicemos entonces la
cantidad de átomos que hay en reactivos y productos:
Podemos ver que la cantidad de átomos de sodio no es la misma en reactivos y productos, lo
mismo para el oxígeno. Por lo tanto, así como está esa reacción no cumple con la ley de
conservación de masa. DEBEMOS BALANCEAR…
REACTIVOS PRODUCTOS
1 átomo de sodio 2 átomos de sodio
2 átomos de oxígeno 1 átomo de oxígeno
PERO… ¿QUÉ ES
BALANCEAR?
BALANCEAR es agregar los
COEFICIENTES necesarios para que
tengamos la misma cantidad de átomos
del lado de reactivos y
productos.
¿QUÉ COEFICIENTES AGREGARÍAS PARA
“BALANCEAR” LA
REACCIÓN ANTERIOR?
Na + O2 --> Na2O
Debemos arrancar por el oxígeno, tenemos 2 átomos en reactivos, pero 1 sólo en productos.
TENEMOS QUE TENER 2 EN LOS PRODUCTOS. Por lo tanto, debemos agregar un 2 como coeficiente
Prof. Isaia Vanesa QUIMICA-6º A
en el producto:
Na + O2 → 2 Na2O
Ahora tengo 2 átomos de oxígeno en los reactivos y 2 en los productos. ¿Y el sodio? ¿Está
balanceado? Al agregar el 2 en el producto, pasamos a tener 4 átomos de sodio (se multiplica 2 x 2)
en los productos y sólo 1 en reactivos. DEBO TENER 4 ÁTOMOS DE SODIO EN REACTIVOS, por lo
tanto agregamos un coeficiente “4”:
4 Na + O2 → 2 Na2O
¡AHORA SÍ! Formamos nuestro óxido y balanceamos la reacción.
Otro ejemplo: Formación del óxido de magnesio:
Nomenclaturas de óxidos
Los óxidos podemos nombrarlos utilizando diferentes nomenclaturas, las cuales son: Nomenclatura
tradicional, nomenclatura de stock y nomenclatura por atomicidad. Para hacer cada nomenclatura
debemos tener MUY presente la valencia del metal o del no metal utilizado para formar el óxido:
# Si el óxido se formó con un metal o no metal que posee una sola valencia:
- Nomenclatura tradicional: óxido de (nombre del metal o no metal).
- Nomenclatura por atomicidad: Se deben utilizar los prefijos mono, di, tri, tetra, etc de acuerdo a
la cantidad de oxígenos que tenga, seguidos del prefijo griego para indicar cantidad de átomos del
metal/no metal.
- Nomenclatura stock: óxido de (nombre del metal/no metal) acompañado entre paréntesis la
valencia del metal/no metal.
Por ejemplo, nombremos el óxido de sodio que formamos anteriormente: Na2O Nomenclatura
tradicional: Óxido de sodio (Porque el sodio tiene una sola valencia) Nomenclatura por
atomicidad: Monóxido de disodio (Mono porque hay un átomo de oxígeno y di porque hay dos
átomos de sodio)
Nomenclatura de stock: Óxido de sodio (I) (El “I” es el número uno en números romanos, que
indica la valencia del sodio)
Prof. Isaia Vanesa QUIMICA-6º A
# Si el óxido se formó con un metal o un no metal que posee dos valencias - Nomenclatura
tradicional: óxido (nombre del metal/no metal). Agregamos terminación “oso” cuando el
elemento usa su menor valencia y terminación “ico” cuando usa la mayor. Por ejemplo: El hierro
tiene valencia 2 y 3. Entonces si usa la menor (II) para formar el óxido, será óxido ferroso y si usa
la mayor óxido férrico.
- Nomenclatura por atomicidad: prefijo (mono, di, tri, tetra) para el óxido y el correspondiente
metal/no metal.
- Nomenclatura stock: se escribe óxido de (nombre del metal/ no metal) acompañado entre
paréntesis la valencia del metal o del no metal, en números romanos.
# Si el óxido se formó con un no metal que posee tres valencias:
Su nomenclatura por atomicidad y de stock se forman como se explicó anteriormente. Pero la
nomenclatura tradicional cambia: Se pone hipo... oso cuando se usa la menor valencia, terminación
oso cuando se usa la valencia intermedia e ico cuando se usa la mayor valencia. Por ejemplo: Óxido
hiposulfuroso (cuando el azufre usa valencia II), Óxido sulfuroso (cuando usa valencia IV) y óxido
sulfúrico (cuando usa valencia VI).
# Si el óxido se formó con un no metal que posee cuatro valencias:
Su nomenclatura por atomicidad y de stock se forma como se explicó anteriormente. Pero la
nomenclatura tradicional cambia: Se pone hipo … oso cuando se usa la menor valencia, oso a la
siguiente, ico a la siguiente y per … ico a más grande. Por ejemplo, para el cloro que posee 4
valencias (1,3, 5 y 7)
Si usa valencia 1: Óxido hipocloroso
Si usa valencia 3: Óxido cloroso
Si usa valencia 5: Óxido clórico
Si usa valencia 7: Óxido perclórico
Prof. Isaia Vanesa QUIMICA-6º A
También podría gustarte
- Funciones Químicas InorgánicasDocumento30 páginasFunciones Químicas Inorgánicasvictor llorenteAún no hay calificaciones
- Tercera - Guia Quimica Nomenclatura - ÓxidosDocumento11 páginasTercera - Guia Quimica Nomenclatura - Óxidoscesar leonardo pulido chocontaAún no hay calificaciones
- Unidad 3 Guia Teorica PracticaDocumento12 páginasUnidad 3 Guia Teorica PracticaVanesa QuinterosAún no hay calificaciones
- Unidad 1 Teorico y Ejercitacion Prof Gabriela Alvarez 3 AnoDocumento13 páginasUnidad 1 Teorico y Ejercitacion Prof Gabriela Alvarez 3 AnoIsaac amadorAún no hay calificaciones
- Anexo 12 - Da 9 - 10moDocumento3 páginasAnexo 12 - Da 9 - 10moiviAún no hay calificaciones
- Trabajo de JavierDocumento9 páginasTrabajo de Javierclamemprendedor2023Aún no hay calificaciones
- Oxidos e HidrurosDocumento10 páginasOxidos e HidrurosLucia SaavedraAún no hay calificaciones
- Unidad #6Documento19 páginasUnidad #6Sergio GarcíaAún no hay calificaciones
- Formación de Óxidos, Bases y ÁcidosDocumento12 páginasFormación de Óxidos, Bases y Ácidossocorro leonAún no hay calificaciones
- FICHA 2. Reacciones QuímicasDocumento16 páginasFICHA 2. Reacciones QuímicasJo BuAún no hay calificaciones
- Semana 1. Nomenclatura de La Química InorgánicaDocumento32 páginasSemana 1. Nomenclatura de La Química Inorgánicavillajimenezrobertocarlos2000Aún no hay calificaciones
- Nomenclatura de Oxidos - ActividadesDocumento9 páginasNomenclatura de Oxidos - Actividadesmarisol_deafAún no hay calificaciones
- Funciones QuímicasDocumento13 páginasFunciones QuímicasJuliana QuispeAún no hay calificaciones
- 09 Nomenclatura InorgánicaDocumento21 páginas09 Nomenclatura InorgánicaAracelly rojasAún no hay calificaciones
- Óxidos ÁcidosDocumento5 páginasÓxidos ÁcidosGabriel lugoAún no hay calificaciones
- NomenclaturaDocumento17 páginasNomenclaturaDaniel TorrealbaAún no hay calificaciones
- Unidad 2 - Funciones Químicas y EcuacionesDocumento12 páginasUnidad 2 - Funciones Químicas y EcuacionesFranco MangarellaAún no hay calificaciones
- Semana 1. NOMENCLATURA DE LA QUÍMICA INORGÁNICADocumento24 páginasSemana 1. NOMENCLATURA DE LA QUÍMICA INORGÁNICAxdemorfeoxAún no hay calificaciones
- Material-Oxoácidos e HidróxidosDocumento4 páginasMaterial-Oxoácidos e HidróxidosPachi CarrieriAún no hay calificaciones
- ACTIVIDAD DEQUIMICA 4to N1Documento15 páginasACTIVIDAD DEQUIMICA 4to N1Rosana Maria Salazar LarezAún no hay calificaciones
- Guia 10 4p Decimo 2021Documento7 páginasGuia 10 4p Decimo 2021Jhan CastellanosAún no hay calificaciones
- Módulo Completo 5°nat 2021Documento53 páginasMódulo Completo 5°nat 2021Candela MasareAún no hay calificaciones
- NomenclaturaDocumento29 páginasNomenclaturaAdrián ZMAún no hay calificaciones
- Nomenclatura InorgánicaDocumento35 páginasNomenclatura InorgánicaRodrigo Vidal100% (1)
- Guía de QUÌMICADocumento19 páginasGuía de QUÌMICAmanuel balabuAún no hay calificaciones
- Números de OxidaciónDocumento4 páginasNúmeros de OxidaciónKevin Leonardo Espinosa CuestasAún no hay calificaciones
- Formación de ÓxidosDocumento7 páginasFormación de ÓxidosBrendaAún no hay calificaciones
- Oxidos e HidroxidosDocumento4 páginasOxidos e HidroxidosLuis RamirezAún no hay calificaciones
- Guía Quimica Inorganica-Instituto PDFDocumento10 páginasGuía Quimica Inorganica-Instituto PDFCheminar ValitaAún no hay calificaciones
- Plantilla Protocolo Colaborativo 2Documento22 páginasPlantilla Protocolo Colaborativo 2Janebis RodeloAún no hay calificaciones
- Tema #2 - Formulación y NomenclaturaDocumento6 páginasTema #2 - Formulación y NomenclaturaGervasio José MatteodaAún no hay calificaciones
- Nomenclatura de ÓxidosDocumento71 páginasNomenclatura de ÓxidosNicol ArteagaAún no hay calificaciones
- GUIA Nomenclatura AcuiculturaDocumento7 páginasGUIA Nomenclatura AcuiculturaEstebin PaterninaAún no hay calificaciones
- Valencia, EDO y Generalidades de Nomenclatura InorgánicaDocumento10 páginasValencia, EDO y Generalidades de Nomenclatura InorgánicaGxxkies. aepAún no hay calificaciones
- Balanceo de Ecuaciones QuimicasDocumento12 páginasBalanceo de Ecuaciones QuimicasKevin AjilaAún no hay calificaciones
- Nomenclatura de Los Compuestos QuimicosDocumento22 páginasNomenclatura de Los Compuestos QuimicosMiguel MartinezAún no hay calificaciones
- ÓxidosDocumento13 páginasÓxidosRICARDO PEREZ HERNANDEZAún no hay calificaciones
- CompuestosDocumento19 páginasCompuestosmarisolAún no hay calificaciones
- Tema NomenclaturaDocumento31 páginasTema Nomenclaturaluchofernanflou90Aún no hay calificaciones
- Informe Nº5 (Ensayos de Oxidacion y Reduccion) 2019Documento6 páginasInforme Nº5 (Ensayos de Oxidacion y Reduccion) 2019Franco Paniagua NicolasAún no hay calificaciones
- Tarea de Funciones Quimicas IorganicasDocumento6 páginasTarea de Funciones Quimicas IorganicasNico TafurAún no hay calificaciones
- 1-09 - 1 Reacc - QcasDocumento17 páginas1-09 - 1 Reacc - Qcasmiruiz12113281Aún no hay calificaciones
- Guia de QuimicaDocumento5 páginasGuia de QuimicaGareenAún no hay calificaciones
- IntroducciónDocumento69 páginasIntroducciónJhoel Sebastian Torres GaonaAún no hay calificaciones
- Los Compuestos InorgánicosDocumento10 páginasLos Compuestos InorgánicosGustavo CastilloAún no hay calificaciones
- Ayuda Uce 3Documento50 páginasAyuda Uce 3Michael BedonAún no hay calificaciones
- Nomenclatura InorgÁnica IntroducciÓn La Química Tiene SuDocumento7 páginasNomenclatura InorgÁnica IntroducciÓn La Química Tiene Surgrtumaco100% (2)
- Quimica InorganicaDocumento15 páginasQuimica InorganicaNadim Salomon100% (1)
- Definición DeoxisalesDocumento35 páginasDefinición DeoxisalesDaisy VergaraAún no hay calificaciones
- Las Reacciones QuímicasDocumento5 páginasLas Reacciones QuímicasAprendex BadajozAún no hay calificaciones
- Apunte Quimica - Curso Nivelación 2024-1Documento77 páginasApunte Quimica - Curso Nivelación 2024-1Luz GallardoAún no hay calificaciones
- El Lenguaje de La QuímicaDocumento112 páginasEl Lenguaje de La QuímicaDiana RojasAún no hay calificaciones
- Separata Pre 2Documento21 páginasSeparata Pre 2Juan MiguelAún no hay calificaciones
- Compuestos QuimicosDocumento11 páginasCompuestos QuimicosCarlos Alberto Lozano EscobedoAún no hay calificaciones
- Nomenclatura de Compuestos QuímicosDocumento21 páginasNomenclatura de Compuestos QuímicosamadagrsAún no hay calificaciones
- Unidad #2 (Primera Parte - Compuestos Binarios)Documento16 páginasUnidad #2 (Primera Parte - Compuestos Binarios)Anto RodriguezAún no hay calificaciones
- Cuadernillo de QuimicaDocumento43 páginasCuadernillo de QuimicaSary RojasAún no hay calificaciones
- Guia Nomenclatura NovenoDocumento9 páginasGuia Nomenclatura NovenoJaime Hernan Cortes RestrepoAún no hay calificaciones
- Cuales Son Las Funciones Quimicas Inorganicas Que Grupo Las IdentificaDocumento2 páginasCuales Son Las Funciones Quimicas Inorganicas Que Grupo Las IdentificaArmando Jose Gutierrez OlivaresAún no hay calificaciones
- Proyecto QUEREMOS SABER DE CS NS - ICSL 3 AñoDocumento5 páginasProyecto QUEREMOS SABER DE CS NS - ICSL 3 AñogimenaAún no hay calificaciones
- Evaluación de Estados de La MateriaDocumento4 páginasEvaluación de Estados de La MateriagimenaAún no hay calificaciones
- Educación AmbientalDocumento14 páginasEducación AmbientalgimenaAún no hay calificaciones
- Trabajo Practico M.8Documento3 páginasTrabajo Practico M.8gimenaAún no hay calificaciones
- Secuencia Didáctica MezclasDocumento16 páginasSecuencia Didáctica MezclasgimenaAún no hay calificaciones
- Jornada Interdisciplinaria de Integración de SaberesDocumento4 páginasJornada Interdisciplinaria de Integración de SaberesgimenaAún no hay calificaciones
- Actividad 4Documento4 páginasActividad 4gimenaAún no hay calificaciones
- Jiis Clase 1Documento1 páginaJiis Clase 1gimenaAún no hay calificaciones
- Clase N°2Documento4 páginasClase N°2gimenaAún no hay calificaciones
- Clase de NUCLEODocumento4 páginasClase de NUCLEOgimenaAún no hay calificaciones
- Evaluacion de Estados de La MateriaDocumento4 páginasEvaluacion de Estados de La MateriagimenaAún no hay calificaciones
- Clase N°1Documento2 páginasClase N°1gimenaAún no hay calificaciones
- Qué Es La QuímicaDocumento1 páginaQué Es La QuímicagimenaAún no hay calificaciones
- ProA Sede TancachaDocumento5 páginasProA Sede TancachagimenaAún no hay calificaciones
- De Qué Está Compuesta La MateriaDocumento3 páginasDe Qué Está Compuesta La MateriagimenaAún no hay calificaciones
- La Solubilidad Es La Capacidad Que Tiene Una Sustancia para Integrarse o Disolverse Con Otra Formando Un Conjunto HomogéneoDocumento2 páginasLa Solubilidad Es La Capacidad Que Tiene Una Sustancia para Integrarse o Disolverse Con Otra Formando Un Conjunto HomogéneogimenaAún no hay calificaciones
- La Solubilidad Es La Capacidad Que Tiene Una Sustancia para Integrarse o Disolverse Con Otra Formando Un Conjunto HomogéneoDocumento2 páginasLa Solubilidad Es La Capacidad Que Tiene Una Sustancia para Integrarse o Disolverse Con Otra Formando Un Conjunto HomogéneogimenaAún no hay calificaciones
- Planif o Grilla 2019 BiologiaDocumento1 páginaPlanif o Grilla 2019 BiologiagimenaAún no hay calificaciones
- Biologia 1ro PlanificacionDocumento6 páginasBiologia 1ro PlanificaciongimenaAún no hay calificaciones
- Proyecto Jabones ArtesanalesDocumento8 páginasProyecto Jabones Artesanalesgimena83% (6)
- Proyecto Jabones ArtesanalesDocumento8 páginasProyecto Jabones Artesanalesgimena83% (6)
- Nuevo Guia Hidrocarburos Aromaticos LiaDocumento8 páginasNuevo Guia Hidrocarburos Aromaticos LiaDaniiela TrujilloAún no hay calificaciones
- Cuestionario Macromoléculas OrgánicasDocumento4 páginasCuestionario Macromoléculas OrgánicasJulio Damián GarcíaAún no hay calificaciones
- Compuestos TernariosDocumento36 páginasCompuestos TernariosFrankAlbaAún no hay calificaciones
- Gta - Noveno - Setiembre - NocturnoDocumento11 páginasGta - Noveno - Setiembre - NocturnoYeudy Salas Hernández100% (1)
- PracticaDocumento4 páginasPracticaCardenas Perez Leonardo MarcosAún no hay calificaciones
- Técnicas de Laboratorio - Diferencia Entre Compuestos Organicos e InorganicosDocumento4 páginasTécnicas de Laboratorio - Diferencia Entre Compuestos Organicos e InorganicosJared AcostaAún no hay calificaciones
- Cuadro Comparativo Química Hazzel Angulo 5to BDocumento3 páginasCuadro Comparativo Química Hazzel Angulo 5to BVikxolAún no hay calificaciones
- Cuestionario Nivel Químico de OrganizaciónDocumento6 páginasCuestionario Nivel Químico de OrganizaciónEduardo AlvaradoAún no hay calificaciones
- Simbolos y Nombres de IonesDocumento1 páginaSimbolos y Nombres de IonesMaría José Villavicencio QuinterosAún no hay calificaciones
- Estere 1Documento51 páginasEstere 1api-3709811Aún no hay calificaciones
- Aminoacidos BioDocumento4 páginasAminoacidos BioZamora Ortiz Marco PoloAún no hay calificaciones
- Examen Parcial Inorganica 2 CorteDocumento6 páginasExamen Parcial Inorganica 2 CorteSANTIAGO RODRIGUEZ VELOZAAún no hay calificaciones
- Química OrgánicaDocumento10 páginasQuímica Orgánicatjw8f46vlhfduh10lsoAún no hay calificaciones
- Valoraciones Acido BaseDocumento11 páginasValoraciones Acido BaseS Andrea Bravo MirandaAún no hay calificaciones
- Guia N.5 Quimica OnceDocumento3 páginasGuia N.5 Quimica OncecarlosAún no hay calificaciones
- Reporte de AzocompuestosDocumento5 páginasReporte de AzocompuestosKev HatarAún no hay calificaciones
- Informe de Volatilizacion de AlcoholesDocumento11 páginasInforme de Volatilizacion de AlcoholesYens Angel LR Layme Reymundo100% (1)
- Vazquez Maldonado Brandon Act2Documento4 páginasVazquez Maldonado Brandon Act2Brandon MaldonadoAún no hay calificaciones
- Taller 6 EquilibrioDocumento3 páginasTaller 6 Equilibrioliz100% (1)
- Quimica Los OxidosDocumento3 páginasQuimica Los OxidosBANI ZAún no hay calificaciones
- TP Nº3 Biomoleculas 1Documento12 páginasTP Nº3 Biomoleculas 1Yamila MardonesAún no hay calificaciones
- Lab 6 Oxidacion de Alcoholes Enero 2017Documento5 páginasLab 6 Oxidacion de Alcoholes Enero 2017victor javier moran guinAún no hay calificaciones
- 5sqi3 3TDocumento30 páginas5sqi3 3Trosa luz0% (1)
- Taller de Quimica III Trimestre Grupo ?Documento10 páginasTaller de Quimica III Trimestre Grupo ?guadalupe guadalupeAún no hay calificaciones
- 1718 QOFarm AV Tema 7 CuestDocumento4 páginas1718 QOFarm AV Tema 7 CuestNatxo OlalAún no hay calificaciones
- Ejercicios Moles, Moleculas y AtomosDocumento2 páginasEjercicios Moles, Moleculas y AtomosalbaAún no hay calificaciones
- Act Integ 1 Mod15Documento9 páginasAct Integ 1 Mod15Jessy RomeroAún no hay calificaciones
- Informe de Laboratorio #4Documento9 páginasInforme de Laboratorio #4valeriaAún no hay calificaciones
- Los Hidrocarburos Ciclicos y Aromaticos para Quinto de SecundariaDocumento7 páginasLos Hidrocarburos Ciclicos y Aromaticos para Quinto de SecundariaCecilia Chumbiauca LozaAún no hay calificaciones
- Alquinos CiclicosDocumento14 páginasAlquinos Ciclicosmariangel durantAún no hay calificaciones