Documentos de Académico
Documentos de Profesional
Documentos de Cultura
4
Cargado por
perladz120 calificaciones0% encontró este documento útil (0 votos)
5 vistas6 páginasTítulo original
Doc4
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
5 vistas6 páginas4
Cargado por
perladz12Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 6
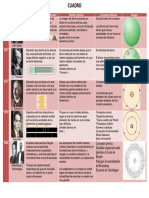
Modelo de Thomson.
Modelo de Schrödinger
Este modelo se le conoce Este es el modelo aceptado en la
como el modelo del budín de actualidad.
pasas.
Schrödinger, establece que los
Thomson establece que los electrones no tienen una órbita definida;
átomos poseen cargas; existe sino que estos se encuentran en
una masa grande positiva constante movimiento alrededor de su
núcleo formando una
con una carga definida en
En 1808, John Dalton forma de nube, y en ella Modelo de Rutherford. nube de electrones.
propuso el primer modelo existen cargas depositas
En este modelo viene del Si bien Schrödinger explica que los
atómico que fue aceptado.
negativas (las pasas). experimentación; en donde electrones no tienen una órbita definida,
El usó sus experimentos
Rutherford encuentra que si
científicos para probar la
existencia de los átomos. existe un conglomerado de cuentan con una probabilidad de
Dalton creía que los átomos cargas positivas en el centro, posición; esto quiere decir que existen
de un elemento eran rodeado de cargas lugares más
exactamente iguales en
tamaño y peso. En su negativas que giraran a su probables para encontrar el electrón, de
modelo atómico, Dalton alrededor de forma definida. esta forma se definen los diferentes
sugirió que los átomos eran tipos de orbitales.
Bohr, tomó como punto de
similares a bolas
partida el modelo de
Rutherford para explicar la
interacción de los orbitales y
El modelo del átomo cúbico1 fue de los electrones desde el punto
los primeros modelos atómicos en el de vista energético, sin
que los electrones del átomo embargo sólo explica al
estaban situados en los ocho hidrogeno.
vértices de un cubo. Esta teoría se
desarrolló en 1902 por Gilbert N.
Lewis, que la publicó en 1916 en el
artículo
John Dalton (1766-
1844) propuso que los El modelo atómico de
átomos eran los Rutherford es teoría sobre
bloques de la estructura interna del
construcción básicos átomo propuesto por el
de la materia y los químico y físico británico-
representaba como
neozelandés Ernest
esferas sólidas.
Rutherford en 1911
1750-1850 1900-1910 1910
En 1904, Thomson Según él,
el átomo era una esfera de
masa positiva uniforme, en la
que se encontraban insertas
las cargas negativas, lo que
explicaba la neutralidad
eléctrica de la materia. Este
modelo fue conocido con
budín de pasas.
Esta teoría fue enunciada por
Gilbert Newton Lewis en el año
1916. En ella se demostró que
los iónes de los elementos
periódicos tienen tendencia a
completar sus últimos niveles
de energía con la cantidad de 8
electrones.
1910-1930
En 1913 Bohr propuso su El modelo atómico de
modelo cuantizado del átomo Schrödinger se desarrolló en
para explicar cómo los 1926. Se trata del modelo
electrones pueden tener mecánico cuántico del átomo
que partía de la ecuación de
órbitas estables alrededor del
Schrödiger. Con esta ecuación se
núcleo. Bohr se dio cuenta de
podía conocer la probabilidad de
que para construir un modelo encontrar un electrón en un
atómico satisfactorio tenía que determinado punto de un
incluir de alguna manera el átomo.
cuanto de energía de Planck-
Einstein.
Joseph John Thomson/Lugar Ernest
John Dalton/Lugar de de nacimiento Rutherford/Lugar de
nacimiento
Cheetham Hill, Mánchester, nacimiento
Eaglesfield, Reino Unido Reino Unido Brightwater, Nueva
Zelanda
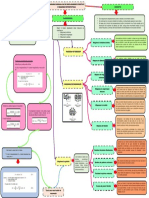
Surgimiento de los modelos atómicos
Niels Bohr/Lugar de Erwin Schrödinger/Lugar de
nacimiento Lewis. Gilbert Newton Lewis nacimiento
(Massachusetts, 23 de octubre
Copenhague, Dinamarca Erdberg, Viena, Austria
de 1875 - Berkeley, 23 de marzo
de 1946) fue un fisicoquímico
estadounidense, famoso por su
trabajo sobre la denominada
"Estructura de Lewis" o
"diagramas de punto".
Nacimiento: 23 de octubre de
1875; Massachu...
Educado en: Universidad de
Harvard
También podría gustarte
- Linea de Tiempo-Yurisell Nieto-LicFísica-QuímicaGeneralADocumento2 páginasLinea de Tiempo-Yurisell Nieto-LicFísica-QuímicaGeneralAYurisell NietoAún no hay calificaciones
- Modelos Del AtomoDocumento2 páginasModelos Del Atomocamiv14ygAún no hay calificaciones
- La Teoría Atómica Unidad 2Documento3 páginasLa Teoría Atómica Unidad 2Luis Manuel Garcia de la CruzAún no hay calificaciones
- Guia QuimicaDocumento26 páginasGuia QuimicaANA KAREN HERNANDEZ BERUMENAún no hay calificaciones
- Química 2 Guia 1Documento16 páginasQuímica 2 Guia 1Alexander GustavoAún no hay calificaciones
- Hernández Cruz Frida Pamela - Modelos Átomicos - 551Documento3 páginasHernández Cruz Frida Pamela - Modelos Átomicos - 551ho liAún no hay calificaciones
- Modelos Atomicos TripticoDocumento2 páginasModelos Atomicos TripticoRichard Qvispe CAún no hay calificaciones
- Actividad de Aprendizaje Biii Modelo Atomico-1Documento3 páginasActividad de Aprendizaje Biii Modelo Atomico-1Angie OchoaAún no hay calificaciones
- Modelo Atomico de Jhon DaltonDocumento3 páginasModelo Atomico de Jhon DaltonAdhesiveSki8518 ChikitoAún no hay calificaciones
- Modelo de Esfera SolidaDocumento4 páginasModelo de Esfera Solidaamezcuasantiago2006Aún no hay calificaciones
- Teoria Atomica de DaltonDocumento2 páginasTeoria Atomica de DaltonAndres SilvaAún no hay calificaciones
- Linea Del Tiempo PDFDocumento1 páginaLinea Del Tiempo PDFFranklin Enmanuel Cordero BobadillaAún no hay calificaciones
- Qui MicaDocumento235 páginasQui MicaJupiter GonzalezAún no hay calificaciones
- Mapa Conceptual de Los Modelos Atomicos 5Documento1 páginaMapa Conceptual de Los Modelos Atomicos 5Soledad MateoAún no hay calificaciones
- Linea de Tiempo Aportaciones en El Modelo AtomicoDocumento5 páginasLinea de Tiempo Aportaciones en El Modelo AtomicoJuan PabloAún no hay calificaciones
- Ciencias 3Documento4 páginasCiencias 3Sebastian Cuello OlivaresAún no hay calificaciones
- ModelosDocumento3 páginasModelosricky hernandezAún no hay calificaciones
- Folleto Tríptico Productos Ecológicos Ilustrado VerdeDocumento2 páginasFolleto Tríptico Productos Ecológicos Ilustrado VerdeAna Sofia MadridAún no hay calificaciones
- Línea de Tiempo: Modelos AtómicosDocumento1 páginaLínea de Tiempo: Modelos AtómicosMisael Ruiz Gutiérrez100% (2)
- Cuadro Comparativo - Modelos AtomicosDocumento3 páginasCuadro Comparativo - Modelos AtomicosEuan Sánchez Gabriel EduardoAún no hay calificaciones
- Alcances y Limitaciones de Los Modelos AtomicosDocumento4 páginasAlcances y Limitaciones de Los Modelos Atomicosmariafernanda herreramartinezAún no hay calificaciones
- Infografia Informativa Bellas Artes Cuadros Simple Llamativa AzulDocumento2 páginasInfografia Informativa Bellas Artes Cuadros Simple Llamativa Azulwtgw4nw66gAún no hay calificaciones
- AtomosDocumento5 páginasAtomosRay LeonAún no hay calificaciones
- Tarea Evidencias de Estructura AtómicaDocumento5 páginasTarea Evidencias de Estructura Atómicaalanntorres09ctrlAún no hay calificaciones
- Research Methods Lesson by SlidesgoDocumento3 páginasResearch Methods Lesson by SlidesgoLuis Eduardo Sanchez PerezAún no hay calificaciones
- Linea Del Tiempo VBVADocumento1 páginaLinea Del Tiempo VBVAVanee VillanuevaAún no hay calificaciones
- El Átomo A Través Del TiempoDocumento8 páginasEl Átomo A Través Del Tiempoorlando pachecoAún no hay calificaciones
- Guia QuímicaDocumento20 páginasGuia Químicaswtdny89bhAún no hay calificaciones
- Atomo Sda51Documento1 páginaAtomo Sda51Guerrero CristhianAún no hay calificaciones
- Clase ESTRUCTURA DE LA MATERIA Y SUS PROPIEDADESDocumento24 páginasClase ESTRUCTURA DE LA MATERIA Y SUS PROPIEDADESBerny DiazAún no hay calificaciones
- Infografía Cronológica Línea de Tiempo Scrapbook Doodle MarrónDocumento1 páginaInfografía Cronológica Línea de Tiempo Scrapbook Doodle MarrónangierubyminchanocasAún no hay calificaciones
- Modelos Atomicos 2Documento3 páginasModelos Atomicos 2Jhoe Henrriquez0% (1)
- 3ºA Carazas Linea de Tiempo AtomoDocumento26 páginas3ºA Carazas Linea de Tiempo AtomoAmparo Rodriguez0% (1)
- TAHUANTINSUYODocumento3 páginasTAHUANTINSUYOAdhesiveSki8518 ChikitoAún no hay calificaciones
- Teorias Atomicas en Orden Cronologico PDFDocumento1 páginaTeorias Atomicas en Orden Cronologico PDFManuel José Rodríguez MillánAún no hay calificaciones
- El Modelo Atómico de Dalton1 Surgido en El Contexto de La QuímicaDocumento6 páginasEl Modelo Atómico de Dalton1 Surgido en El Contexto de La QuímicaMariaElizabeth14Aún no hay calificaciones
- Cuadro Comparativo de Los Modelos AtómicosDocumento6 páginasCuadro Comparativo de Los Modelos AtómicosJesús Alexander MejíazAún no hay calificaciones
- Repaso Modelos AtómicosDocumento4 páginasRepaso Modelos AtómicosNatalia Arias Figueroa100% (1)
- Exposicion Los Modelos AtomicosDocumento9 páginasExposicion Los Modelos Atomicoslarasaranatalia51Aún no hay calificaciones
- Resumen Modelos AtómicosDocumento6 páginasResumen Modelos Atómicosyour.worst.nightmare79417873Aún no hay calificaciones
- Cuadro Comparativo de Los Modelos AtomicosDocumento1 páginaCuadro Comparativo de Los Modelos Atomicoslautarobre10Aún no hay calificaciones
- MÓDULO 2 - Fundamentos de QuímicaDocumento52 páginasMÓDULO 2 - Fundamentos de Químicajose.torres1Aún no hay calificaciones
- Modelo Atómico de DaltonDocumento3 páginasModelo Atómico de Daltonpokemon gonAún no hay calificaciones
- Presentación1 Linea de TiempoDocumento1 páginaPresentación1 Linea de Tiempoluis zavala (luisito)Aún no hay calificaciones
- Eiao La Materia y Sus TransformacionesDocumento5 páginasEiao La Materia y Sus TransformacionesElizabeth VerneAún no hay calificaciones
- Linea de Tiempo Modelos Atomicos QuimicaDocumento2 páginasLinea de Tiempo Modelos Atomicos QuimicaLeidy Yohana Bayona Florez86% (7)
- El Átomo - Su Historia y EstructuraDocumento8 páginasEl Átomo - Su Historia y EstructuraEmilio RaschiaAún no hay calificaciones
- Modelos AtomicosDocumento1 páginaModelos AtomicosSantiago LedesmaAún no hay calificaciones
- NIVELACIÓN FORMATIVA 2 - 2do. CURSODocumento4 páginasNIVELACIÓN FORMATIVA 2 - 2do. CURSOVanessa CBAún no hay calificaciones
- Modelos Atomicos TripticoDocumento2 páginasModelos Atomicos TripticoBruno Luis Medina Olea50% (8)
- Teoría AtómicaDocumento6 páginasTeoría AtómicaAngello MolinaAún no hay calificaciones
- Modelos AtomicosDocumento28 páginasModelos AtomicosGuillermo PintoAún no hay calificaciones
- Linea de Tiempo Teoria AtomistaDocumento4 páginasLinea de Tiempo Teoria AtomistaEsperanza López MosquedaAún no hay calificaciones
- Linea de TiempoDocumento6 páginasLinea de TiempoYamilet ReyesAún no hay calificaciones
- Presentación de María Paula La Bella PDFDocumento6 páginasPresentación de María Paula La Bella PDFAnthony WilmerAún no hay calificaciones
- Bohr SommerfeldDocumento10 páginasBohr SommerfeldXimena OrtegaAún no hay calificaciones
- Infografia CytDocumento1 páginaInfografia Cytteresa cinchayAún no hay calificaciones
- V ARIOSDocumento2 páginasV ARIOSPaty LuxAún no hay calificaciones
- 006 Sondeo Electrico de Terrenos PDFDocumento20 páginas006 Sondeo Electrico de Terrenos PDFSebastian Eduardo Ordoñez VegaAún no hay calificaciones
- Distribución F, Alfa 0.01Documento3 páginasDistribución F, Alfa 0.01Cristian Contreras0% (1)
- Cuestionario 1. Ciencia de Materiales PDFDocumento2 páginasCuestionario 1. Ciencia de Materiales PDFSebastian Llanos Contreras Sercus100% (1)
- Taller Química Organica N. 1 Alcanos 11 CDocumento3 páginasTaller Química Organica N. 1 Alcanos 11 CSbsagamer09Aún no hay calificaciones
- Sesion 14 - M - P4Documento6 páginasSesion 14 - M - P4Sharol Estefani QUISPE DE LA CRUZAún no hay calificaciones
- Descarboxilacion Oxidativa Del PiruvatoDocumento8 páginasDescarboxilacion Oxidativa Del PiruvatoSofia Micaela Franco ZevallosAún no hay calificaciones
- Deber 2 de Matemáticas Fracciones ParcialesDocumento8 páginasDeber 2 de Matemáticas Fracciones ParcialesJeffersonPalaciosAún no hay calificaciones
- Tarea 3Documento11 páginasTarea 3Sebastián PillajoAún no hay calificaciones
- Leyes de La VentilacionDocumento51 páginasLeyes de La VentilacionBruno Estela ObregonAún no hay calificaciones
- La SacarosaDocumento6 páginasLa SacarosaEver Eliú Ruíz ArchilaAún no hay calificaciones
- EZ-SCREEN LP Cortinas de Seguridad de BaDocumento105 páginasEZ-SCREEN LP Cortinas de Seguridad de BaManufactura SmartAún no hay calificaciones
- Controlador Bombeo InvtDocumento61 páginasControlador Bombeo InvtCARLOS ALBERTO UCEDA BALLENAAún no hay calificaciones
- Maquinas Hidraulicas RotoestaticasDocumento1 páginaMaquinas Hidraulicas RotoestaticasCarlos PerezAún no hay calificaciones
- Bitacora AutocadDocumento4 páginasBitacora AutocadOscar Cervera TimanáAún no hay calificaciones
- Estado Del ArteDocumento3 páginasEstado Del ArteMAURICIO VELASCO LOPEZAún no hay calificaciones
- Serie y ParaleloDocumento7 páginasSerie y ParalelolucasAún no hay calificaciones
- Fuera de Este MundoDocumento21 páginasFuera de Este Mundoconstanza aguirre100% (2)
- Diseño de Experimentos y CorrelaciónDocumento323 páginasDiseño de Experimentos y CorrelaciónVictor HugoAún no hay calificaciones
- Fica RocasDocumento10 páginasFica RocassofiabAún no hay calificaciones
- Areas y Volumenes en La Geologia PetroleraDocumento16 páginasAreas y Volumenes en La Geologia PetroleradairimarAún no hay calificaciones
- Sesión Resolvemos Problemas de La Propiedad DistributivaDocumento4 páginasSesión Resolvemos Problemas de La Propiedad DistributivaJohanaAún no hay calificaciones
- PRACTICA 8 REMASTERIZADA - WordDocumento13 páginasPRACTICA 8 REMASTERIZADA - WordRony CalderonAún no hay calificaciones
- Pca de Física 2do Bgu ADocumento15 páginasPca de Física 2do Bgu AInfornata Sueds Amd TurionAún no hay calificaciones
- Croquet A de Pescado Grupo 1 TerminadoDocumento19 páginasCroquet A de Pescado Grupo 1 Terminadomiyagui ñaccha castañedaAún no hay calificaciones
- FOTOMETRODocumento2 páginasFOTOMETROMelina MoncayoAún no hay calificaciones
- Actividad de Puntos Evaluables - Escenario 6 - Primer Bloque-Ciencias Basicas - Virtual - Cálculo 2 - (GrupoDocumento7 páginasActividad de Puntos Evaluables - Escenario 6 - Primer Bloque-Ciencias Basicas - Virtual - Cálculo 2 - (GrupoYHEISONAún no hay calificaciones
- Teorema de Pitagoras y Euclides - Paulo Mu Oz LozanoDocumento9 páginasTeorema de Pitagoras y Euclides - Paulo Mu Oz LozanoPaulo Muñoz LozanoAún no hay calificaciones
- S - Matematica - II 11 1Documento13 páginasS - Matematica - II 11 1Tristan ParkerAún no hay calificaciones
- Biofisica Carga ElectricaDocumento9 páginasBiofisica Carga ElectricaSharonmcAún no hay calificaciones
- Condiciones de Operacion de Equipo de BombeoDocumento8 páginasCondiciones de Operacion de Equipo de BombeoVictor Hugo Gomez Hernandez0% (1)