Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Difusion Cienciademat
Cargado por
Covers JLTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Difusion Cienciademat
Cargado por
Covers JLCopyright:
Formatos disponibles
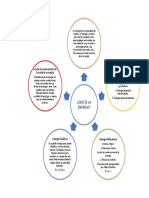
En sólidos a temperaturas suficientemente elevadas,
sus átomos se mueven y la estructura puede cambiar.
La dirección de los cambios (transformaciones) queda
La ecuación de Arrhenius es una
dada por consideraciones de equilibrio. Por ejemplo,
expresión matemática que se utiliza para
los tratamientos térmicos de los aceros realizados para
comprobar la dependencia de la
mejorar ciertas propiedades, tiene por propósito
constante de velocidad (o cinética) de una
modificar la estructura del material y, de esta manera,
reacción química con respecto a la
las propiedades de este último, lo cual obviamente
temperatura a la que se lleva a cabo esa
requiere que los átomos se desplacen desde sus
reacción.
posiciones iniciales. A esta movilidad atómica se le
denomina difusión
Ecuación de Arrhenius
Difusión atómica
Energía de activación
Difusión
Difusión intersticial.
Difusión por
La energía de activación suele utilizarse
vacantes
para denominar la energía mínima
necesaria para que se produzca una
reacción química dada. Para que ocurra una
reacción entre dos moléculas, estas deben
colisionar en la orientación correcta y
poseer una cantidad de energía mínima. A
La difusión intersticial de los átomos medida que las moléculas se aproximan, sus
en las redes cristalinas tiene lugar nubes de electrones se repelen. Para
cuando éstos se trasladan de un superar esto se requiere energía (energía
de activación), que proviene de la energía
intersticio a otro contiguo sin
térmica del sistema, es decir la suma de la
desplazar permanentemente a energía traslacional, vibracional, y
ninguno de los átomos de la matriz rotacional de cada molécula. Si la energía es
de la red cristalina. suficiente, se vence la repulsión y las
moléculas se aproximan lo suficiente para
Para que el mecanismo intersticial que se produzca una reordenación de sus
sea efectivo, el tamaño de los átomos Los átomos pueden moverse en las redes enlaces
que se difunden debe ser cristalinas desde una posición a otra si hay
relativamente pequeño comparado suficiente energía de activación proporcionada
con los de la red. por la vibración térmica de los átomos, y si hay
vacancias u otros defectos cristalinos en la
estructura para que ellos los ocupen. Las
vacancias en metales y aleaciones son defectos
en equilibrio, y como se dice más arriba,
siempre existe una cierta cantidad, lo que
facilita la difusión sustitucional de los átomos.
Bibiano Medina Juan Luis 3MV6
También podría gustarte
- Cuadro SinopticoDocumento1 páginaCuadro Sinopticowilbert100% (1)
- Triptico de Termodinamica TerminadoDocumento2 páginasTriptico de Termodinamica TerminadoSuk LeeJong83% (6)
- Cuadro Comparativo de Los Tipos de EnergiaDocumento1 páginaCuadro Comparativo de Los Tipos de EnergiaArtt Gomez33% (3)
- Movimiento de Los Átomos en Los MaterialesDocumento12 páginasMovimiento de Los Átomos en Los MaterialesLeonel UrbinaAún no hay calificaciones
- Copia de MAPA CONCEPTUAL DE LA EVOLUCIÓN DE LA ESTRUCTURA ATÓMICA DEL ÁTOMODocumento1 páginaCopia de MAPA CONCEPTUAL DE LA EVOLUCIÓN DE LA ESTRUCTURA ATÓMICA DEL ÁTOMOfavioleta96Aún no hay calificaciones
- 1.1.5 Fenómenos de DifusiónDocumento62 páginas1.1.5 Fenómenos de DifusiónGustavo BecerrilAún no hay calificaciones
- Definiciones Fundamentales de FísicaDocumento5 páginasDefiniciones Fundamentales de FísicaKarla RubíAún no hay calificaciones
- Fuerzas Diversas. P8Documento2 páginasFuerzas Diversas. P8Harold DanielAún no hay calificaciones
- Conceptos Basicos de Formas de EnergiaDocumento5 páginasConceptos Basicos de Formas de EnergiaEdson Euresti JuárezAún no hay calificaciones
- Modelo Atomico QuimicaDocumento1 páginaModelo Atomico QuimicaaleAún no hay calificaciones
- Tema V Difusión de SólidosDocumento52 páginasTema V Difusión de SólidosGisel Viviana Molina MoreAún no hay calificaciones
- Esquema de EnlaceDocumento8 páginasEsquema de EnlaceDanielAún no hay calificaciones
- Fisica EnergiaDocumento13 páginasFisica EnergiaErnesto ZeladaAún no hay calificaciones
- La Electricidad y El MagnetismoDocumento9 páginasLa Electricidad y El MagnetismoEsmeralda SotoAún no hay calificaciones
- Taller de Fisica Mecanica.Documento6 páginasTaller de Fisica Mecanica.AngelinAún no hay calificaciones
- Infrarrojo 2Documento11 páginasInfrarrojo 2Maii MolinaAún no hay calificaciones
- FISICA LaialDocumento7 páginasFISICA LaialCarmen Yraida Martinez BastardoAún no hay calificaciones
- Mapa Conceptual - PrincipiosDocumento1 páginaMapa Conceptual - Principiosgenesis mendoza100% (1)
- Energia Transferencia de Energia y AnaliDocumento62 páginasEnergia Transferencia de Energia y AnaliMatías Ignacio Suarez RudolphAún no hay calificaciones
- La EnergíaDocumento2 páginasLa EnergíaganimedesAún no hay calificaciones
- Jalgongo - Difusion Atomica 2018Documento40 páginasJalgongo - Difusion Atomica 2018jose daniel sarmiento blancoAún no hay calificaciones
- Mapa ConceptualDocumento6 páginasMapa ConceptualPedro Magaña MayAún no hay calificaciones
- Tarea 1 Estructura MolecularDocumento5 páginasTarea 1 Estructura Moleculardolly marinAún no hay calificaciones
- Actividad de Aprendizaje 32 TerminadaDocumento4 páginasActividad de Aprendizaje 32 Terminadadanii miusikAún no hay calificaciones
- Universidad Central Del Ecuador: Fundamento ConceptualDocumento11 páginasUniversidad Central Del Ecuador: Fundamento Conceptualjoel toapantaAún no hay calificaciones
- Cuestionario DifusiónDocumento10 páginasCuestionario DifusiónKryz Robert GarciaAún no hay calificaciones
- 04 EnergiaDocumento70 páginas04 Energiaoctaviopozo andresauriaAún no hay calificaciones
- Reporte Láser He NeDocumento11 páginasReporte Láser He NeDante EscamillaAún no hay calificaciones
- Que Es La EnergiaDocumento1 páginaQue Es La EnergiaChristopher C-mAún no hay calificaciones
- Configuración ElectrónicaDocumento9 páginasConfiguración ElectrónicaCamila BotiaAún no hay calificaciones
- Pregunta 3 (CUESTIONARIO) MODELOS MOLECULARESDocumento1 páginaPregunta 3 (CUESTIONARIO) MODELOS MOLECULARESLesly Vilchez100% (1)
- Fuerza 3Documento23 páginasFuerza 3LOPEZ AVILA LAURA LEZETHAún no hay calificaciones
- Mapa Conceptual de La EnergiaDocumento1 páginaMapa Conceptual de La Energia1B Giovani Aragón SalazarAún no hay calificaciones
- EnergíaDocumento2 páginasEnergíaAbigail MartinezAún no hay calificaciones
- Tipos de Energí1Documento2 páginasTipos de Energí1narekbarsamianAún no hay calificaciones
- EspectrometriaDocumento3 páginasEspectrometriaoktaviusmasterAún no hay calificaciones
- Mapa Mental - Martínez Andres Eduardo Diego PDFDocumento2 páginasMapa Mental - Martínez Andres Eduardo Diego PDFDiego MartinezAún no hay calificaciones
- CuestionarioDocumento3 páginasCuestionarioNicole PorcayoAún no hay calificaciones
- FIS123 - Relatorio 01Documento7 páginasFIS123 - Relatorio 01Edson Luiz Ferreira SantosAún no hay calificaciones
- Trabajo 1 Mapa ConceptualDocumento1 páginaTrabajo 1 Mapa ConceptualPauliz EspitiaAún no hay calificaciones
- Ley Coulomb, Campo Eléctrico, Potencial EléctricoDocumento11 páginasLey Coulomb, Campo Eléctrico, Potencial EléctricoMARTINA JAZMIN BARRENECHEAún no hay calificaciones
- Informe Serie y ParaleloDocumento4 páginasInforme Serie y ParaleloddavigoAún no hay calificaciones
- 123456Documento2 páginas123456Anahi LaglaAún no hay calificaciones
- Propiedades PasivasDocumento11 páginasPropiedades PasivasJOSEAún no hay calificaciones
- Fisica I - Trabajo Final 2018Documento10 páginasFisica I - Trabajo Final 2018DanelAún no hay calificaciones
- Tecnicas de Modelado MolecularDocumento53 páginasTecnicas de Modelado MolecularMarletteMuñozAún no hay calificaciones
- ¿Qué Es La Ley de FaradayDocumento11 páginas¿Qué Es La Ley de FaradayYmary MB767Aún no hay calificaciones
- Informe Serie y ParaleloDocumento4 páginasInforme Serie y ParaleloddavigoAún no hay calificaciones
- Circuito Divisor de Voltaje EléctricoDocumento8 páginasCircuito Divisor de Voltaje EléctricoPamela LeivaAún no hay calificaciones
- Laboratorio Conservacion de La EnergiaDocumento3 páginasLaboratorio Conservacion de La Energiadanilo gutierrezAún no hay calificaciones
- Mapa-1842580-Alejandro AyalaDocumento1 páginaMapa-1842580-Alejandro AyalaAlex AyalaAún no hay calificaciones
- Definiciones de Los Diferentes Terminos ElectricosDocumento3 páginasDefiniciones de Los Diferentes Terminos ElectricosWilliam SolarteAún no hay calificaciones
- Tipos de EnergiaDocumento1 páginaTipos de Energiajuliana fernandezAún no hay calificaciones
- Ejercicio 3Documento2 páginasEjercicio 3Diego PrietoAún no hay calificaciones
- Laboratorio Rayos LaserDocumento8 páginasLaboratorio Rayos LaserFelipe ReyesAún no hay calificaciones
- DifusiónDocumento20 páginasDifusiónNeiver Castro JulioAún no hay calificaciones
- Enlaces QuimicosDocumento2 páginasEnlaces QuimicosCielo YadhiraAún no hay calificaciones
- Los Seres Vivos Dependen De La Mecánica CuánticaDe EverandLos Seres Vivos Dependen De La Mecánica CuánticaAún no hay calificaciones
- Generador SíncronoDocumento9 páginasGenerador SíncronoJorge VallejosAún no hay calificaciones
- Prueba Vectores 1Documento4 páginasPrueba Vectores 1Adonai RochaAún no hay calificaciones
- 2.02 Balizamiento 2019Documento19 páginas2.02 Balizamiento 2019Angel BarriaAún no hay calificaciones
- Preguntas de ClimaDocumento13 páginasPreguntas de ClimaHustonMaxPeñaAlagonAún no hay calificaciones
- Repaso Prueba 2-Quimica NM - Abril 2023Documento11 páginasRepaso Prueba 2-Quimica NM - Abril 2023GUIANCARLOS DAYNER ALBITES APAZA0% (1)
- Balanceo RedoxDocumento22 páginasBalanceo RedoxMARIANO ENRIQUE VARA ALMANZAAún no hay calificaciones
- Lab, Fisica Medica #1Documento2 páginasLab, Fisica Medica #1Pedro RodriguezAún no hay calificaciones
- Reporte de MecanismosDocumento16 páginasReporte de MecanismosDanielAún no hay calificaciones
- La Atmosfera para Segundo Grado de SecundariaDocumento5 páginasLa Atmosfera para Segundo Grado de SecundariaMax ParedesAún no hay calificaciones
- Informe de BiologíaDocumento7 páginasInforme de BiologíaKaren ReyesAún no hay calificaciones
- PEP 1 2do Sem 2023Documento6 páginasPEP 1 2do Sem 2023cesar.munoz.riAún no hay calificaciones
- PEC Geografía de España 2021 2022Documento15 páginasPEC Geografía de España 2021 2022abellanginerAún no hay calificaciones
- Biografia Isaac NewtonDocumento3 páginasBiografia Isaac NewtonNormanAún no hay calificaciones
- Examen Parcial (B) Electricidad - y - Magnetiso 2021-1Documento2 páginasExamen Parcial (B) Electricidad - y - Magnetiso 2021-1Andrea contrerasAún no hay calificaciones
- Movimiento Parabólico - Ejercicios Resueltos - Matemóvil-1-10Documento10 páginasMovimiento Parabólico - Ejercicios Resueltos - Matemóvil-1-10Benjamin PeñaAún no hay calificaciones
- Actividad#2Documento11 páginasActividad#2PabloAndresSr.Aún no hay calificaciones
- 3 Líneas Equipotenciales y Campo EléctricoDocumento10 páginas3 Líneas Equipotenciales y Campo EléctricoLaura Daniela Villar juvinaoAún no hay calificaciones
- Semana 10 Caf1Documento8 páginasSemana 10 Caf1RUBI GUILLERMO BARRERAAún no hay calificaciones
- Tangencias y EnlacesDocumento7 páginasTangencias y EnlacesAlejandro RiveraAún no hay calificaciones
- ELECTROMAGNETISMO-Electricidad - Cap. 4 (Potencial Eléctrico) - 2Documento16 páginasELECTROMAGNETISMO-Electricidad - Cap. 4 (Potencial Eléctrico) - 2Lucero AlarcónAún no hay calificaciones
- Transformador de Factor KDocumento18 páginasTransformador de Factor KJuan Manuel Camacho ZeaAún no hay calificaciones
- Teoria ElectromagneticaDocumento6 páginasTeoria ElectromagneticaDaniel Alberto Morales GarciaAún no hay calificaciones
- Evaluación Técnica de Máquina TérmicaDocumento46 páginasEvaluación Técnica de Máquina TérmicaRonald Pascual ParedesAún no hay calificaciones
- Carga y Descarga de CapasitoresDocumento7 páginasCarga y Descarga de CapasitoresZulmxtha PuherthoAún no hay calificaciones
- Momento de Una FuerzaDocumento31 páginasMomento de Una FuerzaXavier PinedaAún no hay calificaciones
- 8 Zaranda Simplicity 5x14Documento2 páginas8 Zaranda Simplicity 5x14rogerroman24Aún no hay calificaciones
- Horarios Apoyo y Mesas Marzo 2023Documento4 páginasHorarios Apoyo y Mesas Marzo 2023PaldiscordAún no hay calificaciones
- MRUV, Caída Libre y Movimiento ParabólicoDocumento19 páginasMRUV, Caída Libre y Movimiento ParabólicoLUIS ROBERTO EMANUEL BARRIOS TORRESAún no hay calificaciones
- Ensayo Gravimétrico y Ensayo de Cámara y Niebla SalinaDocumento4 páginasEnsayo Gravimétrico y Ensayo de Cámara y Niebla SalinaKELLY SUSANA MURGA OBISPOAún no hay calificaciones