Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Upl 607065be53001
Cargado por
Mirian Maribel Lima FloresDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Upl 607065be53001
Cargado por
Mirian Maribel Lima FloresCopyright:
Formatos disponibles
B0214605 B0214606
Cerebro Corazón Infusión
USO CARACTERÍSTICAS DEL PRODUCTO
Medio líquido altamente nutritivo que permite el desarrollo de mi- Medio de cultivo deshidratado: color beige claro, homogéneo, libre
croorganismos con escasos requerimientos nutricionales y nutri- deslizamiento.
cionalmente exigentes, aerobios y anaerobios. Medio de cultivo preparado: color ámbar claro, sin precipitado.
FUNDAMENTO ALMACENAMIENTO
Su alto valor nutritivo está dado por la infusión de cerebro de ter- Medio de cultivo deshidratado a 10-35 ºC.
nera, la infusión de corazón vacuno y la peptona que constituyen Medio de cultivo preparado a 2-8 ºC.
la fuente de carbono, nitrógeno, aminoácidos, péptidos y vitaminas
necesarias para el desarrollo de microorganismos. En el medio de PROCEDIMIENTO
cultivo, la glucosa es el hidrato de carbono fermentable, el cloruro Siembra
de sodio mantiene el balance osmótico y el fosfato disódico otorga Por inoculación directa de la muestra o del microorganismo en es-
capacidad buffer. tudio.
Esta infusión es apropiada para ser utilizada como base en la pre-
paración de hemocultivos debido a que pueden desarrollar todas Incubación
las especies de estreptococos excepto los tiol y piridoxal depen- En aerobiosis, a 33-37 ºC durante 18 a 24 horas. Algunos microor-
dientes. ganismos pueden requerir hasta 7 días de incubación.
Con el agregado de 20 Ul de Penicilina y 100 µg/ml de amicacina
se logra un medio selectivo para el cultivo de hongos patógenos INTERPRETACIÓN DE LOS RESULTADOS
porque estos antimicrobianos inhiben el desarrollo de la flora bac- Examinar los tubos para evaluar el crecimiento por turbiedad.
teriana que pudiera estar presente en la muestra.
CONTENIDO Y COMPOSICIÓN CONTROL DE CALIDAD
Código B0214605: envase x 100 g.
Código B0214606: envase x 500 g. MICROORGANISMOS CRECIMIENTO
Enterococcus faecalis
FÓRMULA (en gramos por litro) ATCC 29212 Satisfactorio
INFUSIÓN DE CEREBRO DE TERNERA.................................................. 200.0 Staphylococcus aureus
INFUSIÓN CORAZÓN VACUNO ........................................................................ 250.0 ATCC 25923 Satisfactorio
PEPTONA ....................................................................................................................................10.0 Streptococcus pyogenes
CLORURO DE SODIO......................................................................................................... 5.0 ATCC 19615 Satisfactorio
GLUCOSA ...................................................................................................................................... 2.0 Streptococcus pneumoniae
FOSFATO DISÓDICO ............................................................................................................ 2.5 ATCC 6305 Satisfactorio
pH FINAL: 7.4 ± 0.2 Streptococcus pneumoniae
ATCC 49619 Satisfactorio
INSTRUCCIONES Candida albicans
Suspender 37 g del polvo en 1 litro de agua purificada. Reposar 5 ATCC 10231 Satisfactorio
minutos. Calentar con agitación frecuente y llevar a ebullición hasta
disolver completamente. Distribuir en tubos o en otros recipientes
apropiados y esterilizar en autoclave a 121°C durante 15 minutos. CONTROL DE ESTERILIDAD RESULTADO
Medio sin inocular Sin cambios
MATERIALES NECESARIOS NO PROVISTOS - Las características del producto pueden alterarse si no se conser-
Equipos y material de laboratorio, microorganismos para control de va apropiadamente.
calidad, reactivos y medios de cultivo adicionales según requeri- - Descartar el producto que no ha sido utilizado y los desechos del
miento. mismo según reglamentaciones vigentes.
PRECAUCIONES REFERENCIAS
- Solamente para uso diagnóstico in vitro. Uso profesional exclu- - MacFaddin. 1985. Media for isolation-cultivation-identification-
sivo. maintenance of medical bacteria, volume 1. Williams & Wilkins, Bal-
- No utilizar el producto si al recibirlo su envase está abierto o da- timore, Md.
ñado. - Murray P.R., Baron, Pfaller, Tenover and Yolken. 1999. Manual of
- No utilizar el producto si existen signos de contaminación o dete- clinical microbiology, 7th ed. American Society for Microbiology,
rioro, así como tampoco si ha expirado su fecha de vencimiento. Washington, D.C.
- Utilizar guantes y ropa protectora cuando se manipula el produc-
to. INDICACIONES AL CONSUMIDOR
- Considerar las muestras como potencialmente infecciosas y ma- Utilizar el producto hasta su fecha de vencimiento.
nipularlas apropiadamente siguiendo las normas de bioseguridad Conservar el producto según las indicaciones del rótulo.
establecidadas por el laboratorio.
AUTORIZACIÓN ANMAT
PM -1292 - 22
Dir. Técnico: Bioq. Alejandro Rossi
02/2021 - REV .02
SÍMBOLOS UTILIZADOS
DIAGNÓSTICO CÓDIGO Nº ELABORADOR ESTÉRIL Nº DE LOTE Nº FECHA DE LÍMITE DE INSTRUCCIONES
IN VITRO DETERMINACIONES VENCIMIENTO TEMPERATURA DE USO
También podría gustarte
- b02146 Rev 01-Cerebro Corazon InfusionDocumento2 páginasb02146 Rev 01-Cerebro Corazon InfusionEdwin Aquino ApazaAún no hay calificaciones
- Agar Mac ConkeyDocumento2 páginasAgar Mac ConkeyHAROLD3 ILMAún no hay calificaciones
- Agar UreaDocumento2 páginasAgar Ureadaniel Barria UrriagaAún no hay calificaciones
- Upl 6054e95043249Documento2 páginasUpl 6054e95043249MARIA DE LA PAZ GRAJEDA PINEDAAún no hay calificaciones
- Urea MergedDocumento20 páginasUrea MergedncervantesnayhuaAún no hay calificaciones
- Upl 6054e95043249Documento2 páginasUpl 6054e95043249Jessica Yirnaldy Rodriguez JimenezAún no hay calificaciones
- Bilis Esculina PDFDocumento2 páginasBilis Esculina PDFOfelia Corrales DelgadilloAún no hay calificaciones
- Técnica. Agar CLEDDocumento2 páginasTécnica. Agar CLEDMarifer ArzolaAún no hay calificaciones
- Hoja de SeguridadDocumento2 páginasHoja de Seguridadlevimunozhdz27Aún no hay calificaciones
- Recuento en Placa AgarDocumento2 páginasRecuento en Placa AgarjjimenezveAún no hay calificaciones
- Medios de Cultivo DeshidratadosDocumento177 páginasMedios de Cultivo DeshidratadosGabriela SalinasAún no hay calificaciones
- Upl 60706bd879bdfDocumento2 páginasUpl 60706bd879bdfCesar Gustavo VillagraAún no hay calificaciones
- Agua PeptonadaDocumento2 páginasAgua PeptonadaalondraAún no hay calificaciones
- DnasaagarDocumento2 páginasDnasaagarEnrique GándaraAún no hay calificaciones
- b02147 Rev 01-Cerebro Corazon Infusion AgarDocumento2 páginasb02147 Rev 01-Cerebro Corazon Infusion Agarandent masonAún no hay calificaciones
- BHIDocumento2 páginasBHIsofía segundomontesAún no hay calificaciones
- Upl 5a281eacb5ee1Documento2 páginasUpl 5a281eacb5ee1DjjejeAún no hay calificaciones
- Cerebro PDFDocumento2 páginasCerebro PDFJuan VergaraAún no hay calificaciones
- Agar VBDocumento2 páginasAgar VBMichAún no hay calificaciones
- Mueller Hinton AgarDocumento3 páginasMueller Hinton AgarSantiago SalazarAún no hay calificaciones
- Agua Tamponada SalmonellaDocumento2 páginasAgua Tamponada SalmonellaMSc Penélope MeloAún no hay calificaciones
- Agar CetrimidaDocumento2 páginasAgar CetrimidaJacqueline González ManzoAún no hay calificaciones
- Agar NutritivoDocumento2 páginasAgar NutritivoDayana Michell Caucil GómezAún no hay calificaciones
- Agar TSADocumento2 páginasAgar TSAAnthuanet GonzalesAún no hay calificaciones
- SalmonellaDocumento2 páginasSalmonelladaniel quizaAún no hay calificaciones
- Agar TCBSDocumento3 páginasAgar TCBSana mariaAún no hay calificaciones
- Agar BrucellaDocumento2 páginasAgar BrucellaJorge HdezAún no hay calificaciones
- FICHASDocumento16 páginasFICHASKarla LdcmmsmaAún no hay calificaciones
- Upl 6054e713a290eDocumento2 páginasUpl 6054e713a290eCamilo Andres Barrios SanchezAún no hay calificaciones
- Bacillus Cereus Selectivo Agar (Según Mossel) : Hoja 1 de 2Documento2 páginasBacillus Cereus Selectivo Agar (Según Mossel) : Hoja 1 de 2DavidAún no hay calificaciones
- b23114 Rev 01-Mac Conkey AgarDocumento2 páginasb23114 Rev 01-Mac Conkey AgarYelsin Denis Fabian AmbrosioAún no hay calificaciones
- Sabouraud Glucosado Agar Con AntibioticoDocumento1 páginaSabouraud Glucosado Agar Con AntibioticoANGIE VALENTINA GARCÍA DÍAZAún no hay calificaciones
- B02123 Rev 01-Nutritivo Caldo PDFDocumento2 páginasB02123 Rev 01-Nutritivo Caldo PDFPadilla RodrigoAún no hay calificaciones
- Agar Verde BrillanteDocumento2 páginasAgar Verde Brillantegrecia ruiz azañeroAún no hay calificaciones
- b02114 Rev 01-Mac Conkey AgarDocumento2 páginasb02114 Rev 01-Mac Conkey AgarAide DueñasAún no hay calificaciones
- EmbDocumento3 páginasEmbana mariaAún no hay calificaciones
- Upl 5a281ad50f34aDocumento2 páginasUpl 5a281ad50f34aCamila BedoyaAún no hay calificaciones
- Upl 6092dd4f4357aDocumento2 páginasUpl 6092dd4f4357aLinus BraunAún no hay calificaciones
- 8-Ficha Tecnica MHDocumento3 páginas8-Ficha Tecnica MHBrenda GonzálezAún no hay calificaciones
- Medios de CultivoDocumento6 páginasMedios de CultivoDanny AndradeAún no hay calificaciones
- TDS - DRBC Agar - BK198 - BM142Documento3 páginasTDS - DRBC Agar - BK198 - BM142bajjuverAún no hay calificaciones
- AGAR NUTRITIVO 100mLDocumento1 páginaAGAR NUTRITIVO 100mLFATIMA EMILIANA CALDERON BARRIOSAún no hay calificaciones
- Agar Nutritivo PDFDocumento2 páginasAgar Nutritivo PDFEmanuel Pomacco100% (2)
- b23137 Rev 01-Mueller Hinton AgarDocumento3 páginasb23137 Rev 01-Mueller Hinton AgarMiriam Loreley Cahuantzi FloresAún no hay calificaciones
- Upl 5b5b1f0956365Documento2 páginasUpl 5b5b1f0956365Ryan Ken IlookatyouAún no hay calificaciones
- Procedimiento Análisis Micro BCDocumento8 páginasProcedimiento Análisis Micro BCAndrés EspinozaAún no hay calificaciones
- Bacillus. Samuel Mijares y Alexandra GarciaDocumento8 páginasBacillus. Samuel Mijares y Alexandra GarciaSamuel de jesus mijares villegasAún no hay calificaciones
- Agar Eosina-Azul de MetilenoDocumento15 páginasAgar Eosina-Azul de MetilenoGesús De La CruzAún no hay calificaciones
- Bacillus Cereus Selectivo AgarDocumento62 páginasBacillus Cereus Selectivo AgarJose Cesar MamaniAún no hay calificaciones
- 1508 Es 1Documento2 páginas1508 Es 1Nadia PerezAún no hay calificaciones
- Pseudomonas Agar P PDFDocumento2 páginasPseudomonas Agar P PDFDaniela Tovar AvilaAún no hay calificaciones
- Protocolo Microbiologico PDFDocumento35 páginasProtocolo Microbiologico PDFSantiago TovarAún no hay calificaciones
- Medios de Cultivo Apendice-FinalDocumento10 páginasMedios de Cultivo Apendice-FinaljorgeAún no hay calificaciones
- Agar Cromo UTIDocumento2 páginasAgar Cromo UTIDama GelvesAún no hay calificaciones
- Agar MrsDocumento2 páginasAgar MrsfaldridaAún no hay calificaciones
- Agar SoyaDocumento2 páginasAgar SoyaMichAún no hay calificaciones
- AGARESDocumento32 páginasAGARESYris Rosario100% (1)
- HT b04181 Rev 01-Orange Serum AgarDocumento2 páginasHT b04181 Rev 01-Orange Serum AgarCITROJUGO03Aún no hay calificaciones
- Manejo agroecológico de la mosca blanca en el cultivo de berenjenaDe EverandManejo agroecológico de la mosca blanca en el cultivo de berenjenaCalificación: 5 de 5 estrellas5/5 (1)
- Catalogo Cavalier 2018Documento5 páginasCatalogo Cavalier 2018Neylin Esteysi HGAún no hay calificaciones
- Resultado de AprendizajeDocumento8 páginasResultado de AprendizajeKarly StyAún no hay calificaciones
- Cursos de Arquitectura - EsoarchDocumento12 páginasCursos de Arquitectura - EsoarchTomy Daniel Ramirez AlvarezAún no hay calificaciones
- Trabajo ColaborativoDocumento9 páginasTrabajo ColaborativoAna María Garzón RamosAún no hay calificaciones
- Unidad 2-Actividad 3Documento9 páginasUnidad 2-Actividad 3Niris RojasAún no hay calificaciones
- Programa de Entrenamiento para Carreras de Medio FondoDocumento20 páginasPrograma de Entrenamiento para Carreras de Medio Fondoneubert martinez100% (1)
- Las Diferentes Sociedades ComercialesDocumento2 páginasLas Diferentes Sociedades Comercialeskatherine lirianoAún no hay calificaciones
- Cuadro Kraepelin 6ta y 8va Críticas de Los Franceses y BleulerDocumento6 páginasCuadro Kraepelin 6ta y 8va Críticas de Los Franceses y BleulerDaiana Ayelén100% (1)
- Unidad Ii FQDocumento56 páginasUnidad Ii FQSamuel BoltonAún no hay calificaciones
- Destreza 1Documento3 páginasDestreza 1Fernando CuaranAún no hay calificaciones
- R Auly0201mslglla0Documento1 páginaR Auly0201mslglla0cecilia palomarezAún no hay calificaciones
- Galletas Nutri HDocumento13 páginasGalletas Nutri Hmelissa ramos macedoAún no hay calificaciones
- 6 Teorema de Superposición - FINALDocumento6 páginas6 Teorema de Superposición - FINALCarmen BallestaAún no hay calificaciones
- WuvivoteruxepazawenokajoDocumento3 páginasWuvivoteruxepazawenokajoHabacuc LopezAún no hay calificaciones
- Autocad 3Documento3 páginasAutocad 3PABLO VILAÑEZAún no hay calificaciones
- Práctica 9 - Filtración Continua en Un Filtro de Tambor Rotatorio - 20131363Documento27 páginasPráctica 9 - Filtración Continua en Un Filtro de Tambor Rotatorio - 20131363Arlahe Salazar Luna-0086Aún no hay calificaciones
- Arreglos de ResistenciaDocumento6 páginasArreglos de ResistenciaEdgar AscencioAún no hay calificaciones
- Lab. Qaii Practica 3 Det. Bi en Fármaco Por ComplejometríaDocumento2 páginasLab. Qaii Practica 3 Det. Bi en Fármaco Por ComplejometríaToramaru Utsunomiya50% (2)
- Contrato de Venta Jeep LuisDocumento2 páginasContrato de Venta Jeep LuisWillysAún no hay calificaciones
- Sebastián Ibarra Mendieta: Guia de Trabajo No 3Documento3 páginasSebastián Ibarra Mendieta: Guia de Trabajo No 3Gilberto Ramirez SeguraAún no hay calificaciones
- Tecnica AmeuDocumento10 páginasTecnica Ameumanuel lopesAún no hay calificaciones
- Caracteristicas Constructivas de Los Captaciones Desde EmbalseDocumento10 páginasCaracteristicas Constructivas de Los Captaciones Desde Embalseanon_674787436Aún no hay calificaciones
- Ficha Tecnica k3 AdamaDocumento4 páginasFicha Tecnica k3 Adamanoe martinAún no hay calificaciones
- CURSO DE RECREADOR INFANTIL UltimoDocumento34 páginasCURSO DE RECREADOR INFANTIL UltimoAna Karina Brito DuqueAún no hay calificaciones
- Matriz LegalDocumento4 páginasMatriz LegalAnllela Lorena BlancoAún no hay calificaciones
- Historia de La CalidadDocumento2 páginasHistoria de La CalidadCrystell Aguilar CarballoAún no hay calificaciones
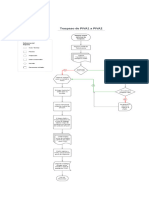
- Procesos de Envios de PIVA1 A PIVA2Documento1 páginaProcesos de Envios de PIVA1 A PIVA2casa.maravillas273Aún no hay calificaciones
- TESIS ALE Y EMI 2 CompletaDocumento27 páginasTESIS ALE Y EMI 2 CompletaalejandroAún no hay calificaciones
- Empujes 181026042004Documento25 páginasEmpujes 181026042004Antony Joel Santos VivancoAún no hay calificaciones
- Tarea 3 de Terapia Del AprendizajeDocumento10 páginasTarea 3 de Terapia Del AprendizajeEdwin Leon VasquezAún no hay calificaciones