Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Solución Guia de Quimica Orgánica
Cargado por
Yamelys Isabel Mercado De Los ReyesTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Solución Guia de Quimica Orgánica
Cargado por
Yamelys Isabel Mercado De Los ReyesCopyright:
Formatos disponibles
Indique si los siguientes compuestos son ORGÁNICOS O INORGÁNICOS
a. CH4 : orgánico
b. NH3 : inorgánico
c. H2O : inorgánico
d. CH3COOH: orgánico
e. CO2 : orgánico
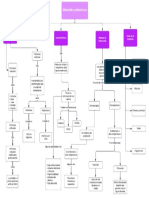
1. CARBONOS ALOTRÓPICOS: completa el siguiente esquema:
Diamante
Carbono
Grafito
Turba
Lignito
Amorfo natural
hulla
antracita
Carbono amorfo
Carbón coque
Amorfo artifial Carbón animal
Carbón vegetal
2. Teniendo en cuenta las diferencias entre los compuesto orgánicos y los inorgánicos completa el siguiente cuadro:
ASPECTOS COMPUESTOS INORGÁNICOS COMPUESTOS ORGÀNICOS
Tipos de elementos Todos los elementos de la tabla periódica. Básicos: C y H
Ocasionales: O, N, S, y halógenos.
Trazas: Fe, Co, P, Ca, Zn.
Tipo de enlace Enlace iónico, formado por iones y Enlace covalente, formado por pares
metálico formado por átomos. electrónicos compartidos.
Isómeros La isomería se limita a un reducido Exhiben isomería.
número de casos.
Formación de cadenas carbonadas La formación de cadenas no es común. Largas cadenas basadas en carbono.
Variedad Son menos variados. Son muy variados.
Solubilidad en agua solubles La mayoría son insolubles en agua.
Solubilidad en compuestos No solubles Solubles en solventes orgánicos.
orgánicos
Punto de fusión Es elevado Es bajo
Punto de ebullición Es elevado Es bajo
3. Teniendo en cuenta los tipos de carbono 1rio, 2rio, 3rio y 4nario, utiliza las siguientes figuras geométricas para indicar
respectivamente cada tipo de carbono: círculo, corazón, triángulo y cuadrado.
1rio
2rio
3rio
4nario
4. Identifica el tipo de enlace (sigma o pi) y de hibridación que presentan los siguientes compuestos:
Enlace sencillo (σ) y hibridación sp3
Enlace doble (σ y ᚂ) y hibridación sp2
Enlace sencillo (σ) y enlace doble (σ y ᚂ), hibridación sp3 y sp2
Enlace triple (σ y dos ᚂ) y hibridación sp
Enlace triple (σ y dos ᚂ) y enlace sencillo (σ), hibridación sp y sp3
5. Coloca en la casilla la información correcta:
a. En la hibridación sp2, se forman 3 orbitales hibridos y 1 Ppuros. Y forma enlace: doble.
b. En la hibridación sp3, se forman 4 orbitales hibridos y 0 Ppuros. Y forma enlace:sencillo.
c. En la hibridación sp, se forman 2 orbitales hibridos y 2 Ppuros. Y forma enlace: triple.
d. La distancia entre orbitales híbridos es de: 109,5°en la hibridación sp3.
e. La distancia entre orbitales híbridos es de: 120° en la hibridación sp2.
f. La distancia entre orbitales híbridos es de: 180° en la hibridación sp.
TRANSFERENCIA
1. En la siguiente figura se representa la forma en la que se disponen los orbitales de 2 átomos de
carbono en un compuesto orgánico
2. En una molécula orgánica, los átomos de carbono se clasifican de acuerdo con el número de átomos
de carbono a los que se encuentra enlazados. De acuerdo con lo anterior, es válido afirmar que existe
carbono de tipo terciario en la estructura
3. ¿Cuál de los siguientes compuestos orgánicos presenta hibridación sp?
4. Una de la características de los compuestos orgánicos es que poseen carbonos primarios (enlazados a un átomo
de carbono), secundarios (enlazados a dos átomos de carbono), terciarios (enlazados a 3 átomos de carbono) y
cuaternarios (enlazados a 4 átomos de carbono)
De acuerdo con esta información es válido afirmar que:
a. Z posee más carbonos terciarios y la misma cantidad de carbonos primarios que Y.
b. Z posee más carbonos secundarios y la misma cantidad de carbonos terciarios que Y.
c. Z y Y poseen la misma cantidad de carbonos terciarios y diferente cantidad de carbonos cuaternarios.
d. Z y Y poseen la misma cantidad de carbonos terciarios y secundarios.
Para contestar las preguntas 5 y 6 tenga presente la siguiente información:
En los compuestos orgánicos el carbono forma enlaces covalentes por lo cual tienen puntos de fusión y de
ebullición bajos. Son bastantes solubles en solventes orgánicos pero no en agua. Sus reacciones, por ser
moleculares son lentas y se realizan a temperaturas no muy elevadas. Por lo general son combustibles y la
mayor parte de estas sustancias se descomponen a temperaturas inferiores a los 300ºC. Están constituidos por
carbono, hidrógeno, oxígeno y nitrógeno, en menos proporción cloro, bromo, yodo, azufre y fósforo.
5. Teniendo en cuenta la electronegatividad cercana del carbono con los átomos de hidrógeno, oxígeno,
nitrógeno, azufre, fósforo, cloro bromo y yodo, sus enlaces se caracterizan por ser:
a. iónicos
b. inestables
c. covalentes
d. débiles
6. A partir del punto de ebullición y de fusión de los compuestos orgánicos se deduce que presentan gran
solubilidad en :
a. agua
b. solventes orgánicos
c. solventes inorgánicos
d. solventes neutros
Para contestar las preguntas 7 a 10 tenga presente la siguiente información: El átomo de Carbono posee 4
electrones de valencia, su número atómico es 6 (Z=6) y su configuración electrónica es: 6C 1S 2 2S2 2P2 o
también 1s 2s 2px 2py 2pz Para adquirir la estructura de gas noble gana o pierde 4 electrones. Generalmente el
carbono se comporta como electronegativo, adquiere la configuración de gas noble por compartición de
electrones con otros átomos.
Por el reducido volumen del átomo del carbono, los enlaces covalentes son fuertes y estables, lo cual permite la
formación de cadenas con un número de átomos de carbono ilimitado. Los cuatro enlaces se disponen
espacialmente en direcciones de los vértices de un tetraedro, en cuyo centro está el átomo de carbono.
7. El átomo de carbono tiene 6 electrones de valencia repartidos en:
a. 4 niveles de energía.
b. 2 niveles de energía.
c. 3 niveles de energía.
d. 5 niveles de energía.
8. Se deduce que los cuatro electrones de valencia del átomo de carbono en estado fundamental se encuentran
situados así:
a. 3 en el orbital 2s y 1 en el orbital 2px.
b. 2 en el orbital 2s y 2 en los orbitales px y py.
c. 1 en el orbital 2s y 3 en el orbital 2p.
d. 3 en el orbital 2s 1 en el orbital 2py.
9. Se concluye que el carbono generalmente se comporta como:
a. Electronegativo.
b. Electropositivo.
c. Metaloide.
d. Neutro.
10. Los cuatro enlaces que forma el átomo de carbono se disponen espacialmente en:
a. El centro de un tetraedro.
b. Los lados de un tetraedro.
c. Los vértices de un tetraedro.
d. La base de un tetraedro.
También podría gustarte
- Círculo Armónico Modal: Jónico, Lidio y Mixolidio: círculo armónico modal, #1De EverandCírculo Armónico Modal: Jónico, Lidio y Mixolidio: círculo armónico modal, #1Aún no hay calificaciones
- Quimica Organica-1Documento44 páginasQuimica Organica-1Percy Ignacio YzarraAún no hay calificaciones
- Quimica VDocumento47 páginasQuimica VLAURA100% (2)
- Quimica OrganicaDocumento100 páginasQuimica OrganicaSarIcoCanchariAún no hay calificaciones
- Clase 01 - Química Del CarbonoDocumento28 páginasClase 01 - Química Del CarbonoDANIELA ANGELLY APAZA RICRAAún no hay calificaciones
- Clase 19 Química Orgánica I Propiedades Del Carbono e Hidrocarburos 2016Documento32 páginasClase 19 Química Orgánica I Propiedades Del Carbono e Hidrocarburos 2016Gustavo GarridoAún no hay calificaciones
- 5º QuìmicaDocumento4 páginas5º QuìmicaSEBASTIANAún no hay calificaciones
- Pres Carb DamDocumento14 páginasPres Carb Damzack oligcvAún no hay calificaciones
- Guia 1 Quimica OrganicaDocumento11 páginasGuia 1 Quimica OrganicaCarlos GuardadoAún no hay calificaciones
- Quimica VDocumento46 páginasQuimica VLAURAAún no hay calificaciones
- S1 - El Átomo de Carbono - 230321Documento34 páginasS1 - El Átomo de Carbono - 230321Allison Guerrero diazAún no hay calificaciones
- Propiedades Del Carbono e HidrocarburosDocumento19 páginasPropiedades Del Carbono e Hidrocarburosthomas3pppAún no hay calificaciones
- Quimica OrgánicaDocumento38 páginasQuimica OrgánicaIbañezLinaAún no hay calificaciones
- Química OrgánicaDocumento35 páginasQuímica OrgánicaJennifer Nathaly Yáñez CifuentesAún no hay calificaciones
- Clase 01 - Quimica Del Carbono PDFDocumento29 páginasClase 01 - Quimica Del Carbono PDFhellenAún no hay calificaciones
- Átomo Del CarbonoDocumento22 páginasÁtomo Del CarbonoLOURDES QUENTA50% (2)
- s13 - El Átomo de Carbono - H SaturadosDocumento48 páginass13 - El Átomo de Carbono - H SaturadosIEP JOHN NASHAún no hay calificaciones
- Quimica Orgánica y Átomo de CarbonoDocumento13 páginasQuimica Orgánica y Átomo de CarbonoCarlos Alfonso Jara BenitesAún no hay calificaciones
- Clase 01 - Quimica Del CarbonoDocumento32 páginasClase 01 - Quimica Del CarbonoJaime Espinal Pichardo100% (1)
- Semana 15Documento23 páginasSemana 15josesito pañalitoAún no hay calificaciones
- Presentación 2 SemanaDocumento33 páginasPresentación 2 SemanaAnderson Harold Quispe RamosAún no hay calificaciones
- Clase 17 - Propiedades Del CarbonoDocumento28 páginasClase 17 - Propiedades Del CarbonoCarolina0% (1)
- Clase 19 Química Orgánica I Propiedades Del Carbono e Hidrocarburos 2016Documento27 páginasClase 19 Química Orgánica I Propiedades Del Carbono e Hidrocarburos 2016Jorge LuisAún no hay calificaciones
- Tema Quimicqa Organica SP, SP2, SP3 Enlace Sigmay Pi 2022 4toaño A, B, C, D, e 2022Documento33 páginasTema Quimicqa Organica SP, SP2, SP3 Enlace Sigmay Pi 2022 4toaño A, B, C, D, e 2022Juan Diego ArianoAún no hay calificaciones
- Copia de Nociones-QuimicaOrganicaDocumento101 páginasCopia de Nociones-QuimicaOrganicaCarlos Enrique Ortiz HerrnándezAún no hay calificaciones
- 15 Introduccion A La Quimica Organica 2019Documento43 páginas15 Introduccion A La Quimica Organica 2019Leandro PorrasAún no hay calificaciones
- Tema 11 Introducion Quimica OrganicaDocumento135 páginasTema 11 Introducion Quimica OrganicaJuan Pablo Hoyos TabaresAún no hay calificaciones
- Taller 1Documento2 páginasTaller 1Michael WongAún no hay calificaciones
- Guia #1 Conociendo Al Carbono 11° Segundo Periodo 2020Documento3 páginasGuia #1 Conociendo Al Carbono 11° Segundo Periodo 2020jose paterninaAún no hay calificaciones
- Introducción Química Orgánica Química Del CarbonoDocumento23 páginasIntroducción Química Orgánica Química Del CarbonoAlexandra Gómez LópezAún no hay calificaciones
- S1 - El Átomo de CarbonoDocumento29 páginasS1 - El Átomo de Carbonocaromi semAún no hay calificaciones
- QUÍMICA ORGANICA I - Semana 1Documento49 páginasQUÍMICA ORGANICA I - Semana 1Percy PaucarAún no hay calificaciones
- Saguilan Alpizar Irvin Eduardo Diego Roa Gómez Estrada Hernández Andrea Sanabria Roa ArmandoDocumento10 páginasSaguilan Alpizar Irvin Eduardo Diego Roa Gómez Estrada Hernández Andrea Sanabria Roa ArmandoIrvin Saguilan AlpizarAún no hay calificaciones
- QUIMICA ORGANICA Semana 1 TEORIADocumento14 páginasQUIMICA ORGANICA Semana 1 TEORIAJonatan IsaacAún no hay calificaciones
- Taller de Hibridacion Del CarbonoDocumento19 páginasTaller de Hibridacion Del CarbonoDaniel Rojas BolañosAún no hay calificaciones
- Introducción Química OrgánicaDocumento45 páginasIntroducción Química OrgánicaVale AcevedoAún no hay calificaciones
- Pizarra Química OrgánicaDocumento31 páginasPizarra Química OrgánicaMINNIEAún no hay calificaciones
- Taller El Carbono y Su HibridacionDocumento4 páginasTaller El Carbono y Su Hibridacionyolima vivasAún no hay calificaciones
- Quimica OrganicaDocumento24 páginasQuimica OrganicaPamela SalasAún no hay calificaciones
- Tema 11 Introducion Quimica OrganicaDocumento135 páginasTema 11 Introducion Quimica OrganicaApyOvalleAún no hay calificaciones
- Semana 01 - El Átomo Del CarbonoDocumento42 páginasSemana 01 - El Átomo Del CarbonoTatiana C. HerreraAún no hay calificaciones
- S1 - El Atomo de Carbono MejoradoDocumento28 páginasS1 - El Atomo de Carbono Mejoradoney.barbosaAún no hay calificaciones
- SEMANA N°10 - S hidrocarburos-RESUELTO.2Documento44 páginasSEMANA N°10 - S hidrocarburos-RESUELTO.2Angel LuisAún no hay calificaciones
- 4sec Qui - Org Hidroc (1b)Documento46 páginas4sec Qui - Org Hidroc (1b)Manueloncio Rojas ChalanAún no hay calificaciones
- El Carbono para Tercer Grado de SecundariaDocumento9 páginasEl Carbono para Tercer Grado de SecundariaArturo JaimeAún no hay calificaciones
- Quimica Organica y Tipos de Carbono para Quinto Grado de SecundariaDocumento5 páginasQuimica Organica y Tipos de Carbono para Quinto Grado de SecundariaAlejandra ValdiviaAún no hay calificaciones
- So Luci On Practica 2Documento45 páginasSo Luci On Practica 2Pablo BerrocalAún no hay calificaciones
- T1 Orgánica VazquezDocumento60 páginasT1 Orgánica VazquezMartina MaldonadoAún no hay calificaciones
- Química OrgánicaDocumento28 páginasQuímica OrgánicaNestor GutierrezAún no hay calificaciones
- s1 - El Átomo de CarbonoDocumento25 páginass1 - El Átomo de Carbonolesly RiosAún no hay calificaciones
- 4° Sec Química Orgánica PDFDocumento3 páginas4° Sec Química Orgánica PDFRomel Casafranca HuallparimachiAún no hay calificaciones
- El CarbonoDocumento4 páginasEl Carbonodjjms100% (2)
- S1 - El Átomo de CarbonoDocumento25 páginasS1 - El Átomo de Carbonojeyson100% (1)
- III. Química OrgánicaDocumento208 páginasIII. Química OrgánicaPaulina Diaz JimenezAún no hay calificaciones
- Círculo armónico diatónico artificial: Mayor artificial y doble mayor armónico: círculo armónico diatónico artificial, #1De EverandCírculo armónico diatónico artificial: Mayor artificial y doble mayor armónico: círculo armónico diatónico artificial, #1Aún no hay calificaciones
- Introducción a la química de los metales de transiciónDe EverandIntroducción a la química de los metales de transiciónAún no hay calificaciones
- Círculo armónico diatónico: Explorando la belleza y armonía de la música diatónica a través del círculo armónico: círculo armónico diatónico, #1De EverandCírculo armónico diatónico: Explorando la belleza y armonía de la música diatónica a través del círculo armónico: círculo armónico diatónico, #1Aún no hay calificaciones
- Química de los compuestos de coordinaciónDe EverandQuímica de los compuestos de coordinaciónAún no hay calificaciones
- TALLER DE FUNDAMENTOS DE MATEMÁTICA-maria Cabrera NavarroDocumento6 páginasTALLER DE FUNDAMENTOS DE MATEMÁTICA-maria Cabrera NavarroYamelys Isabel Mercado De Los ReyesAún no hay calificaciones
- TALLER DE MATEMÁTICAS-maria Cabrera NavarroDocumento7 páginasTALLER DE MATEMÁTICAS-maria Cabrera NavarroYamelys Isabel Mercado De Los ReyesAún no hay calificaciones
- Guia#8-Matematicas-Secciones Conicas-10°cDocumento3 páginasGuia#8-Matematicas-Secciones Conicas-10°cYamelys Isabel Mercado De Los Reyes100% (2)
- Guía#8 Matematicas 11°Documento3 páginasGuía#8 Matematicas 11°Yamelys Isabel Mercado De Los ReyesAún no hay calificaciones
- Procesos BiofisiologicosDocumento3 páginasProcesos BiofisiologicosStar JeanneAún no hay calificaciones
- Planta SXEW PeruDocumento102 páginasPlanta SXEW PerusalvadorAún no hay calificaciones
- Lab 6Documento10 páginasLab 6DIEGO FERNANDO CUERVO FAJARDOAún no hay calificaciones
- Tabla PeriódicaDocumento3 páginasTabla Periódicapaulreyes15pAún no hay calificaciones
- Ejercicios de NomenclaturaDocumento18 páginasEjercicios de NomenclaturaYolfrancisAún no hay calificaciones
- Fósforo en ColasDocumento15 páginasFósforo en ColasAaronAún no hay calificaciones
- AlquinosDocumento27 páginasAlquinosCHRISTIAN FELIPE JIMENEZ MURILLOAún no hay calificaciones
- Sesión 9. Producto de SolubilidadDocumento16 páginasSesión 9. Producto de SolubilidadAdrián Lume HuayllaniAún no hay calificaciones
- SolucionesDocumento5 páginasSolucionesAra OrueAún no hay calificaciones
- Investigación Previa - Formacion de CumarinasDocumento10 páginasInvestigación Previa - Formacion de CumarinasDaniel Granados JuárezAún no hay calificaciones
- Ejercicios Tema 4 Enlace Quc3admico 1Documento3 páginasEjercicios Tema 4 Enlace Quc3admico 1Yanela PFAún no hay calificaciones
- Aldehídos y CetonasDocumento5 páginasAldehídos y CetonasPaula Andrea Cuaran OrdoñezAún no hay calificaciones
- Mapa ConceptualDocumento1 páginaMapa Conceptualandrea456Aún no hay calificaciones
- Mota Antonio JoseDocumento60 páginasMota Antonio JoseGlagysDCarloAún no hay calificaciones
- Unidades Quimicas de ConcentraciónDocumento20 páginasUnidades Quimicas de ConcentraciónAnaika IsabelAún no hay calificaciones
- 4.1 Garcia Luis G11Documento6 páginas4.1 Garcia Luis G11Garcia Hernandez Luis EduardoAún no hay calificaciones
- Quimica InorganicaDocumento18 páginasQuimica InorganicamynorAún no hay calificaciones
- Pre-Informe 6 Lisseth FlorezDocumento16 páginasPre-Informe 6 Lisseth FlorezLisseth FlorezAún no hay calificaciones
- HidrocarburosDocumento3 páginasHidrocarburosJohn PoloAún no hay calificaciones
- BIOLOGIA RESUMEN FINAL 200 Pag..Documento206 páginasBIOLOGIA RESUMEN FINAL 200 Pag..Mario SantayAún no hay calificaciones
- Taller 1 Nivelatorio 2021-1Documento3 páginasTaller 1 Nivelatorio 2021-1Pablo ZapataAún no hay calificaciones
- Gas Como Materia Prima de La PetroquimicaDocumento33 páginasGas Como Materia Prima de La PetroquimicaMaricarmen CelisAún no hay calificaciones
- Dicson Rojas - Semana 8Documento9 páginasDicson Rojas - Semana 8dicsonAún no hay calificaciones
- Hidrodesulfuración PresentacionDocumento31 páginasHidrodesulfuración PresentacionFabricio NuňezAún no hay calificaciones
- Práctica 6: Determinación de Ni en Una Muestra Comercial Por Gravimetría.Documento18 páginasPráctica 6: Determinación de Ni en Una Muestra Comercial Por Gravimetría.Enrique DelgadoAún no hay calificaciones
- Examen de Medio Curso ResueltoDocumento5 páginasExamen de Medio Curso ResueltoPedro Tolentino OrnetaAún no hay calificaciones
- S06.s1 - Tarea CalificadaDocumento2 páginasS06.s1 - Tarea CalificadaMaria Caicedo CustodioAún no hay calificaciones
- Mediciones Hidrologicas 4Documento47 páginasMediciones Hidrologicas 4Fernando Elías Valderrama GómezAún no hay calificaciones
- Ev 3. Presentación de Las Vías y Procesos Metabólicos Identificados en El Metabolismo AeróbicoDocumento60 páginasEv 3. Presentación de Las Vías y Procesos Metabólicos Identificados en El Metabolismo AeróbicoAhovitAún no hay calificaciones
- Suelo en Huanuco-1Documento15 páginasSuelo en Huanuco-1Percy MasgoAún no hay calificaciones