Documentos de Académico
Documentos de Profesional
Documentos de Cultura
4° QUIM PD1 PPT Propiedades de La Tabla Periódica
Cargado por
jisunmacias0 calificaciones0% encontró este documento útil (0 votos)
8 vistas15 páginasTítulo original
4°-QUIM-PD1-PPT-Propiedades-de-la-tabla-periódica
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
8 vistas15 páginas4° QUIM PD1 PPT Propiedades de La Tabla Periódica
Cargado por
jisunmaciasCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 15
QUÍMICA
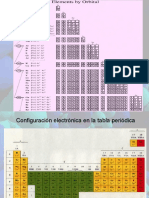
Propiedades de la tabla periódica
Obst. Daysi Chequer B.
Tabla periódica: Propuestapor Mendeleiev
La tabla periódica tiene 18 grupos y 7 periodos. Los grupos tienen la
misma valencia atómicay los periodostienenla cantidad de orbitales.
Los grupos se clasifican en:
Específicamente cada grupo que se encuentrandeforma
verticaly sellama:
• Grupo 1 (I A): los metales alcalinos
• Grupo 2 (II A): los metales alcalinotérreos
• Grupo 3 (III B): Familia del Escandio
• Grupo 4 (IV B): Familia del Titanio
• Grupo 5 (V B): Familia del Vanadio
• Grupo 6 (VI B): Familia del Cromo
• Grupo 7 (VII B): Familia del Manganeso
• Grupo 8 (VIII B): Familia del Hierro
• Grupo 9 (IX B): Familia del Cobalto
Específicamente cada grupo que se encuentrandeforma
verticaly sellama:
• Grupo 10 (X B): Familia del Níquel
• Grupo 11 (I B): Familia del Cobre
• Grupo 12 (II B): Familia del Zinc
• Grupo 13 (III A): los térreos
• Grupo 14 (IV A): los carbonoideos
• Grupo 15 (V A): los nitrogenoideos
• Grupo 16 (VI A): los calcógenos o anfígenos
• Grupo 17 (VII A): los halógenos
• Grupo 18 (VIII A): los gases nobles
PropiedadesPeriódicas
• RadioAtómico.
• VolumenAtómico.
• Potencial de Ionización.
• Electroafinidad.
• Electronegatividad.
Radioatómico
• Es la distancia entre el núcleo y el último electrón del átomo.
• En la tabla varía de la siguiente manera
• Grupos: Aumenta de arriba hacia abajo
• Periodos: Disminuye de izquierda a derecha
Volumen atómico
• Es el espacio que usa el átomo en el espacio, varía igual que el radio ( es proporcional a él)
• Volumen iónico: Depende de la carga del átomo
Potencialde ionización
• Cantidad de energía necesaria para retirar el último electrón de un átomo.
• Grupo: Aumenta de abajo hacia arriba.
• Periodo: Aumenta de izquierda a derecha.
Energía de ionización
También llamado potencial de ionización. “Es la
energía necesaria para extraer un e– de un
átomo neutro en estado gaseoso y formar un
catión”.
Afinidad electrónica o electroafinidad
“Es la energía intercambiada cuando un
átomo gaseoso captura un e– y forma un
anión”. Es difícil de medir y se suele hacer
por métodos indirectos. Puede ser positiva
o negativa aunque suele ser exotérmica.
Electronegatividad
Mide la tendencia de un átomo a atraer
los e– de otros átomos a los que está
enlazado. Es un compendio entre energía
de ionización (EI) y afinidad electrónica
(AE). La electronegatividad aumenta
hacia arriba en los grupos pues los e– son
más atraídos por el núcleo a menores
distancias y hacia la derecha en los
periodos ya que hay mayor número
atómico (Z) y una menor distancia.
Taller
1.- Indique cuales son las propiedades de la tabla periódica.
de química
2.- Unir con línea según corresponda.
-Periodo: Aumenta de izquierda a derecha.
Potencial de ionización
-Grupo: Aumenta de arriba hacia abajo.
-Periodo: Disminuye de izquierda a derecha.
Radio atómico
-Grupo: Aumenta de abajo hacia arriba.
3.- Complete los siguientes enunciados.
-Volumen atómico es el espacio que usa el …………………………en el espacio.
-Potencial de ionización es la …………………………………………………necesaria para retirar el último …………………………………….de un
átomo.
-Radio atómico es la distancia entre el …………………… y el último electrón del átomo
También podría gustarte
- 2.2 Propiedades Atómicas y Su Variación PeriódicaDocumento6 páginas2.2 Propiedades Atómicas y Su Variación PeriódicaJavi Armstrong HurtadoAún no hay calificaciones
- Química Apuntes 1 TrimestreDocumento12 páginasQuímica Apuntes 1 TrimestrePilar Martin VelezAún no hay calificaciones
- Qui MicaDocumento6 páginasQui MicaPeggi ProvosteAún no hay calificaciones
- 2 - Teor A at MicaDocumento19 páginas2 - Teor A at MicaCesar ValenzuelaAún no hay calificaciones
- Presentaciones FInal Periodicidad QuímicaDocumento47 páginasPresentaciones FInal Periodicidad QuímicaMr RobotAún no hay calificaciones
- Química 1º ParcialDocumento23 páginasQuímica 1º ParcialMaria Gil GarciaAún no hay calificaciones
- Tabla Periódica PDFDocumento25 páginasTabla Periódica PDFNatth Carolina VillegasAún no hay calificaciones
- Presentacion 6-Propiedades Periodicas - PpsDocumento14 páginasPresentacion 6-Propiedades Periodicas - PpsSauloRamosAún no hay calificaciones
- Propiedades PeriódicasDocumento5 páginasPropiedades PeriódicasLex_RenovatioAún no hay calificaciones
- Unidad 1 y 2 Estructura Atómica y Tabla PeriódicaDocumento46 páginasUnidad 1 y 2 Estructura Atómica y Tabla PeriódicaVeronica VilladaAún no hay calificaciones
- MARCO TEORICO Tabla PeriodicaDocumento11 páginasMARCO TEORICO Tabla PeriodicaCarlos Mario Barrios Ruiz100% (1)
- Guia 1 4to Periodo Quimica 8BDocumento6 páginasGuia 1 4to Periodo Quimica 8Blos 4 reveldesAún no hay calificaciones
- Tema 1 CompletoDocumento136 páginasTema 1 Completodb6j9v6znzAún no hay calificaciones
- Propiedades Periodicas Tema: Tabla PeriódicaDocumento1 páginaPropiedades Periodicas Tema: Tabla PeriódicaFabox BelloAún no hay calificaciones
- Propiedades PeriodicasDocumento6 páginasPropiedades PeriodicasLuis Castro50% (2)
- Tabla Periodica ApuntesDocumento2 páginasTabla Periodica Apuntesjulen casasAún no hay calificaciones
- MODELO ATOMICO Version CortaDocumento5 páginasMODELO ATOMICO Version Cortaamelotita100% (2)
- Propiedades PeriódicasDocumento12 páginasPropiedades PeriódicasPhill Jordan JacksonAún no hay calificaciones
- A Puntes Química Guia Ceneval 18Documento34 páginasA Puntes Química Guia Ceneval 18Luis Ochoa100% (1)
- Propiedades PeriodicasDocumento13 páginasPropiedades PeriodicasNay BautistaAún no hay calificaciones
- Propiedades Periodicas de La Tabla PeriodicaDocumento4 páginasPropiedades Periodicas de La Tabla PeriodicaDo not SleepAún no hay calificaciones
- El Tamaño de Los Átomos y Sus IonesDocumento2 páginasEl Tamaño de Los Átomos y Sus IonesEmili Vio KantutaAún no hay calificaciones
- Unidad 2-3 El Átomo y El Sistema Periódico. El Enlace Químico 4º ESO 2021-2022Documento18 páginasUnidad 2-3 El Átomo y El Sistema Periódico. El Enlace Químico 4º ESO 2021-2022Ainara SánchezAún no hay calificaciones
- Modelos AtomicosDocumento14 páginasModelos AtomicosMicaa FariasAún no hay calificaciones
- Propiedades Periodicas de La TPDocumento21 páginasPropiedades Periodicas de La TPcompartecienciaAún no hay calificaciones
- 3° Año-Teoría 12Documento2 páginas3° Año-Teoría 12Jackson López LaviAún no hay calificaciones
- Clase 8 Propiedades Periodicas TDocumento26 páginasClase 8 Propiedades Periodicas TCLASH OF CLANS Y MAS 12Aún no hay calificaciones
- Actividad5 Propiedades PeriódicasDocumento6 páginasActividad5 Propiedades PeriódicasSamir NasibAún no hay calificaciones
- El Atomo - Electricidad 2021Documento48 páginasEl Atomo - Electricidad 2021KATHERINE VERGARA LUIZAGAAún no hay calificaciones
- Clase 14Documento21 páginasClase 14GiaanBriamonteRuzakAún no hay calificaciones
- Instituto Educacional Juan Xxiii Valencia VenezuelaDocumento52 páginasInstituto Educacional Juan Xxiii Valencia VenezuelaAndrea TortoleroAún no hay calificaciones
- 3°1°-Química FotocopiarDocumento2 páginas3°1°-Química FotocopiarJoaco VillaAún no hay calificaciones
- Guía de Aprendizaje Semana 10 y 11 Grado 10 PDFDocumento6 páginasGuía de Aprendizaje Semana 10 y 11 Grado 10 PDFNathalia Andrea GutierrezAún no hay calificaciones
- 4 - Propiedades Periódicas - PPSDocumento13 páginas4 - Propiedades Periódicas - PPSMajoAún no hay calificaciones
- UD1 - El Átomo y La Tabla PeriódicaDocumento18 páginasUD1 - El Átomo y La Tabla PeriódicaLibertad Sanchez GonzalezAún no hay calificaciones
- Carga Nuclear EfectivaDocumento10 páginasCarga Nuclear EfectivaHilda Araceli Flores CabralAún no hay calificaciones
- Bloque 3Documento29 páginasBloque 3JOSE MANUEL ALVARADOAún no hay calificaciones
- Unidad Iii Sistema PeriódicoDocumento22 páginasUnidad Iii Sistema PeriódicoTamara AlfonsoAún no hay calificaciones
- ArtículoDocumento22 páginasArtículoOctaviusLopezVillanuevaAún no hay calificaciones
- Folleto Tabla PeriódicaDocumento3 páginasFolleto Tabla PeriódicaChacach Sol Melany RossemaryAún no hay calificaciones
- Propiedades PeriódicasDocumento6 páginasPropiedades PeriódicasYoshio AlarcónAún no hay calificaciones
- QuimicaDocumento5 páginasQuimicaYessi LizAún no hay calificaciones
- Cuestionario QuimicaDocumento6 páginasCuestionario QuimicaCristian EAún no hay calificaciones
- Diaporama Base Experimental Teoria Cuantica, Estructura Atomica, Periocidad Quimica, Clasificaciones Periodicas InicialesDocumento40 páginasDiaporama Base Experimental Teoria Cuantica, Estructura Atomica, Periocidad Quimica, Clasificaciones Periodicas InicialesFlorii Parker Gr100% (1)
- Estructura Atomica - Tabla Periodica 2019Documento50 páginasEstructura Atomica - Tabla Periodica 2019Nicolás BartoloméAún no hay calificaciones
- Tema 6Documento7 páginasTema 6marina.lpezzAún no hay calificaciones
- Teoría de DALTON.: Rayos CatódicosDocumento8 páginasTeoría de DALTON.: Rayos Catódicosvictor MarceloAún no hay calificaciones
- Presentacion Quimica ModificadoDocumento22 páginasPresentacion Quimica ModificadoNay BautistaAún no hay calificaciones
- Tabla PeriodicaDocumento10 páginasTabla PeriodicaNolan JuradoAún no hay calificaciones
- Duver Taller de Quimica TerminadoDocumento3 páginasDuver Taller de Quimica TerminadoENRIQUE MANJARRESAún no hay calificaciones
- Clase de C T Tema 20 - 3ro de SecundariaDocumento2 páginasClase de C T Tema 20 - 3ro de Secundariadayanis mamaniAún no hay calificaciones
- Periodicidad QuímicaDocumento41 páginasPeriodicidad QuímicaDaniel Santiago Ruiz SandovalAún no hay calificaciones
- Átomos AisladosDocumento4 páginasÁtomos AisladosdeivyAún no hay calificaciones
- Propiedades PeriódicasDocumento3 páginasPropiedades PeriódicasYuliana Castro HernándezAún no hay calificaciones
- Estructura Atómica y Tabla Periódica 4Documento2 páginasEstructura Atómica y Tabla Periódica 4Leonel NoyaAún no hay calificaciones
- Fisica 1º Bac Tema 1Documento6 páginasFisica 1º Bac Tema 1w4zv4t8fhnAún no hay calificaciones
- Propiedades PeriódicasDocumento2 páginasPropiedades PeriódicasDavid Francessco Marcilla VeraAún no hay calificaciones
- Teoría electromagnética para estudiantes de ingeniería: Notas de claseDe EverandTeoría electromagnética para estudiantes de ingeniería: Notas de claseCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Ejercicio Estadistica (Yuki)Documento2 páginasEjercicio Estadistica (Yuki)jisunmaciasAún no hay calificaciones
- VarianzaDocumento6 páginasVarianzajisunmaciasAún no hay calificaciones
- Preguntas Grupo#2Documento1 páginaPreguntas Grupo#2jisunmaciasAún no hay calificaciones
- Ejercicio Estadistica (Yuki)Documento2 páginasEjercicio Estadistica (Yuki)jisunmaciasAún no hay calificaciones
- Dictaduras en América LatinaDocumento1 páginaDictaduras en América LatinajisunmaciasAún no hay calificaciones
- El Texto CientíficoDocumento21 páginasEl Texto CientíficojisunmaciasAún no hay calificaciones
- Diapos SociedadDocumento2 páginasDiapos SociedadjisunmaciasAún no hay calificaciones
- SálvameDocumento16 páginasSálvamejisunmaciasAún no hay calificaciones
- Operaciones Con MatricesDocumento6 páginasOperaciones Con MatricesjisunmaciasAún no hay calificaciones
- 2BCT 01 Sistemas Por Gauss Ejercicios ResueltosDocumento14 páginas2BCT 01 Sistemas Por Gauss Ejercicios ResueltosGerardo DávilaAún no hay calificaciones
- LÍPIDOSDocumento49 páginasLÍPIDOSjisunmaciasAún no hay calificaciones
- Banco de PreguntasDocumento2 páginasBanco de PreguntasjisunmaciasAún no hay calificaciones
- Expo Accion Grupo1Documento8 páginasExpo Accion Grupo1jisunmaciasAún no hay calificaciones
- Trabajo Autonomo 1 Sociedad Faviana m12Documento11 páginasTrabajo Autonomo 1 Sociedad Faviana m12jisunmacias0% (2)
- TALLER 2 Sociedad m12 Grupo 1 NivelacionDocumento7 páginasTALLER 2 Sociedad m12 Grupo 1 Nivelacionjisunmacias100% (1)
- Modelo Entidad RelacionDocumento35 páginasModelo Entidad Relacioncarlos Palacio100% (2)
- Pat SextoDocumento15 páginasPat Sextoorlando rivasAún no hay calificaciones
- Retos y Promesas de La Inclusión Educativa en Venezuela.Documento220 páginasRetos y Promesas de La Inclusión Educativa en Venezuela.Maria Te Malvacias100% (1)
- Cartilla de Aacc y Tarifario FijaDocumento2 páginasCartilla de Aacc y Tarifario FijaEL PAKUSAún no hay calificaciones
- Inhibores Sintesis de LipidosDocumento56 páginasInhibores Sintesis de LipidosRobertoMuñoz100% (1)
- HISTORIADocumento1 páginaHISTORIADaniela PerezAún no hay calificaciones
- Unidad 6Documento18 páginasUnidad 6Artemiza RomaxAún no hay calificaciones
- Sal U3 A2 EdchDocumento14 páginasSal U3 A2 EdchAlejandra CervantesAún no hay calificaciones
- Efecto de La Concentración de Almidón de Almendra deDocumento69 páginasEfecto de La Concentración de Almidón de Almendra deANDREA MARIANA HERN�NDEZ MU�OZAún no hay calificaciones
- Flexibilidad Verbal y RendimientoDocumento5 páginasFlexibilidad Verbal y RendimientopmartinrAún no hay calificaciones
- Tif (Convertidor Boost)Documento20 páginasTif (Convertidor Boost)agallegosviAún no hay calificaciones
- Escala de MediciónDocumento4 páginasEscala de MediciónIvón CuevasAún no hay calificaciones
- Análisis Crítico Sobre La Película Pasante de ModaDocumento3 páginasAnálisis Crítico Sobre La Película Pasante de ModaJohanny MayoraAún no hay calificaciones
- Clase 7 - Recuperación de SueloDocumento37 páginasClase 7 - Recuperación de SueloJuan camiloAún no hay calificaciones
- Felipe Rocha OpinionesDocumento12 páginasFelipe Rocha OpinionesConejita MTAún no hay calificaciones
- Cerradura Electronic A Con PICDocumento68 páginasCerradura Electronic A Con PICJose Angel Peraza DominguezAún no hay calificaciones
- Documento Contable Importante HTDocumento6 páginasDocumento Contable Importante HTVincent Stiv0% (1)
- Taller 1 Presion Grupo 1 SJ NaukaryDocumento3 páginasTaller 1 Presion Grupo 1 SJ Naukaryjoluvasi58819Aún no hay calificaciones
- Análisis y Diseño de Una Solución para Uso de Servicios de BiDocumento7 páginasAnálisis y Diseño de Una Solución para Uso de Servicios de BiHugo Francisco Felipe CacerosAún no hay calificaciones
- Blavatsky, Helena - Isis Sin Velo (Completo)Documento886 páginasBlavatsky, Helena - Isis Sin Velo (Completo)Emir Asad100% (2)
- Informe de Practicas Avanzando.Documento16 páginasInforme de Practicas Avanzando.Katty Elizabeth Mejia NarroAún no hay calificaciones
- Usted Sera Rico - Bonomi Roberto PDFDocumento237 páginasUsted Sera Rico - Bonomi Roberto PDFAvilaLuisAún no hay calificaciones
- FO-UBP-08 Formulario de Registro de DistribuidoraDocumento1 páginaFO-UBP-08 Formulario de Registro de Distribuidorawlay2627gmailcom20% (5)
- Neuromarketing Digital Y Su Importancia para Desarrollar Contenido de Valor en Redes SocialesDocumento12 páginasNeuromarketing Digital Y Su Importancia para Desarrollar Contenido de Valor en Redes Socialesjesús escobar cacallicaAún no hay calificaciones
- Lanaseve PG 026 V.03Documento4 páginasLanaseve PG 026 V.03gabypadAún no hay calificaciones
- El Lugar de La Experiencia Estética en LaDocumento13 páginasEl Lugar de La Experiencia Estética en LaRodrigo Badillo LarragaAún no hay calificaciones
- LA Gestion Educativa y de Los AprendizajesDocumento13 páginasLA Gestion Educativa y de Los AprendizajesCilia Estilla MoralesAún no hay calificaciones
- Caso de Estudio Winnebago Industries Inc FinDocumento25 páginasCaso de Estudio Winnebago Industries Inc FinGustavo Lamiña100% (2)
- Parasitología Banco de Preguntas G-1Documento7 páginasParasitología Banco de Preguntas G-1Jonathan ValdiviezoAún no hay calificaciones
- El DescuentoDocumento7 páginasEl DescuentoMaria MartínAún no hay calificaciones