Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Compuestos Binarios Cuadro
Cargado por
Mariela X Lopez Camara100%(1)100% encontró este documento útil (1 voto)
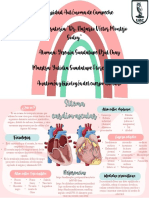
804 vistas1 páginaEl documento presenta una tabla que resume los principales tipos de compuestos químicos, incluyendo óxidos metálicos y no metálicos, hidruros metálicos y no metálicos, y sales binarias. Describe las reacciones químicas características de cada tipo de compuesto, como la formación de hidróxidos al reaccionar óxidos metálicos con agua o la formación de ácidos al reaccionar óxidos no metálicos con agua. También resume las valencias características de los metal
Descripción original:
cuadro de los compuestos binarios
Título original
Compuestos binarios cuadro
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoEl documento presenta una tabla que resume los principales tipos de compuestos químicos, incluyendo óxidos metálicos y no metálicos, hidruros metálicos y no metálicos, y sales binarias. Describe las reacciones químicas características de cada tipo de compuesto, como la formación de hidróxidos al reaccionar óxidos metálicos con agua o la formación de ácidos al reaccionar óxidos no metálicos con agua. También resume las valencias características de los metal
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
100%(1)100% encontró este documento útil (1 voto)
804 vistas1 páginaCompuestos Binarios Cuadro
Cargado por
Mariela X Lopez CamaraEl documento presenta una tabla que resume los principales tipos de compuestos químicos, incluyendo óxidos metálicos y no metálicos, hidruros metálicos y no metálicos, y sales binarias. Describe las reacciones químicas características de cada tipo de compuesto, como la formación de hidróxidos al reaccionar óxidos metálicos con agua o la formación de ácidos al reaccionar óxidos no metálicos con agua. También resume las valencias características de los metal
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 1
Al reaccionar Óxido potásico
Metal + Oxígeno → Óxido
con el agua Metal con u Óxido de Óxido de
Óxidos metálicos M/O K 2O K+1 Óxido de potasio metálico
producen Oxígeno potasio dipotasio
hidróxidos (valencia única) 4K + O2 → 2K2O
Al reaccionar Óxido de
Óxidos no No metal + Oxígeno →
con agua No metal con Anhídrido Óxido de cloro dicloro o
metálicos o NM/O CI2O CI: +1 +2 +5 +7 Anhídridos
producen Oxígeno hipocloroso (I) Monóxido de
anhídridos
acidos dicloro 2Cl2O → 2Cl2 + O2
Hidruro Metal + Hidrogeno →
“H” trabaja
Hidruros Metal con magnésico o Hidruro de Hidruro de Hidruro metálico
M/H MgH2 Mg +2 con valencia
metálicos Hidrogeno hidruro de magnesio magnesio
de “-1”
magnesio MgH2 → Mg + 2H
El no metal Inicia con Hidrogeno + No metal →
Hidruros no
siempre usa hidrogeno se Ácido Cloruro de Cloruro de Hidrácido
metálicos o H/NM HCI CI -1
su valencia acompaña con clorhídrico hidrogeno hidrogeno
hidrácidos
más pequeña no metal H2 + CI2 → 2 HCI
Sal binaria o
El no metal Hidracido + Hidroxido →
siempre usa Metal y no Agua + Sal haloidea
haloides M/NM LiCI Li +1 CI -1 Cloruro lítico Cloruro de litio Cloruro de litio
su valencia metal unidos
más pequeña Li + CI → LiCI
También podría gustarte
- Nomenclatura IUPACDocumento7 páginasNomenclatura IUPACAlejandro Ochoa Alvarez0% (1)
- 1314 FQ 3eso Correccion HidroxidosDocumento2 páginas1314 FQ 3eso Correccion HidroxidosDe La Puente FeerAún no hay calificaciones
- Cuadro Comparativo de Los Presidentes de 1940-1970 MéxicoDocumento2 páginasCuadro Comparativo de Los Presidentes de 1940-1970 MéxicoMariela X Lopez Camara83% (6)
- Calor y Temperatura Informe de Fisica IIIDocumento19 páginasCalor y Temperatura Informe de Fisica IIICharly Loor L Primos100% (3)
- Problem A RioDocumento3 páginasProblem A RioJaime LopezAún no hay calificaciones
- Clasificación de Los Elementos Químicos: Metales de Valencia Fija - Metaloides No MetalesDocumento1 páginaClasificación de Los Elementos Químicos: Metales de Valencia Fija - Metaloides No MetalesAntonella CuasquerAún no hay calificaciones
- 4º Química Compuestos SalinosDocumento11 páginas4º Química Compuestos SalinosTani Mar EstrellaAún no hay calificaciones
- INTRODUCCIÓN OxidosDocumento1 páginaINTRODUCCIÓN OxidosZWilfredo GonzalesAún no hay calificaciones
- Topic 1.2 Present Progressive Yes - No Questions and Short AnswersDocumento4 páginasTopic 1.2 Present Progressive Yes - No Questions and Short AnswersPablo CanoAún no hay calificaciones
- Importancia de Los Cinco ReinosDocumento6 páginasImportancia de Los Cinco ReinosSantiago SanchezAún no hay calificaciones
- INFOGRAFIADocumento1 páginaINFOGRAFIAEmma BautistaAún no hay calificaciones
- La LloviznaDocumento5 páginasLa LloviznaJhosen OrellanaAún no hay calificaciones
- Nombrar Las Siguientes SalesDocumento2 páginasNombrar Las Siguientes SalesCN KramAún no hay calificaciones
- Hidruros Ácidos Hidrácidos CationesDocumento4 páginasHidruros Ácidos Hidrácidos CationesYesenia FernándezAún no hay calificaciones
- ACTIVIDAD de Oxoácidos e HidróxidosDocumento1 páginaACTIVIDAD de Oxoácidos e HidróxidosJose Renato Pasapera CalderonAún no hay calificaciones
- Formulacion InorganicaDocumento7 páginasFormulacion Inorganicajmrgruiz844Aún no hay calificaciones
- NOMENCLATURADocumento1 páginaNOMENCLATURAjhoseptrading7Aún no hay calificaciones
- NOMENCLATURADocumento4 páginasNOMENCLATURAKarime KantúnAún no hay calificaciones
- Las Sales Hidratadas 2022Documento2 páginasLas Sales Hidratadas 2022Geovanna SuiraAún no hay calificaciones
- Formulario de QuimicaDocumento11 páginasFormulario de QuimicaDayanna Carolina Lopez MedinaAún no hay calificaciones
- Oxidos Básicos y Ácidos, Acidos Hidracidos y SalesDocumento3 páginasOxidos Básicos y Ácidos, Acidos Hidracidos y SalesAmnelys MejiasAún no hay calificaciones
- Uniones Químicas y Nomenclatura: Unidad 2Documento5 páginasUniones Químicas y Nomenclatura: Unidad 2Alan Wenceslao Quispe BordaAún no hay calificaciones
- Los Compuestos InorgánicosDocumento4 páginasLos Compuestos InorgánicosWilmer Guillermo Calderón SalazarAún no hay calificaciones
- Compuestos InorganicosDocumento2 páginasCompuestos InorganicosKaren Lia ColmenaresAún no hay calificaciones
- Complemento Química IADocumento13 páginasComplemento Química IAAngel DavidAún no hay calificaciones
- 8 M 1 A 2Documento10 páginas8 M 1 A 2valentina bedriñanaAún no hay calificaciones
- Los Compuestos InorgánicosDocumento6 páginasLos Compuestos InorgánicosAnshella LlaureAún no hay calificaciones
- TerDocumento10 páginasTerAndreaAún no hay calificaciones
- QuimicaDocumento7 páginasQuimicaMiguel ValleAún no hay calificaciones
- ClaseDocumento23 páginasClaseYuri PoblanoAún no hay calificaciones
- Laboratorio 3 Metales y No MetalesDocumento6 páginasLaboratorio 3 Metales y No MetalesluisAún no hay calificaciones
- Formulas QuimicasDocumento23 páginasFormulas QuimicasMilagros PereyraAún no hay calificaciones
- Hidróxidos PDFDocumento2 páginasHidróxidos PDFwebos100% (2)
- Taller No 1 Reacciones QuímicasDocumento4 páginasTaller No 1 Reacciones QuímicasFREDY FERNANDO CORTES VELANDIAAún no hay calificaciones
- Quimica InorganicaDocumento3 páginasQuimica InorganicaSarahi GalvanAún no hay calificaciones
- NomenclaturaDocumento2 páginasNomenclaturaJinett AvilaAún no hay calificaciones
- Hidruros Y ÁCIDOS HIDRÁCIDOSDocumento4 páginasHidruros Y ÁCIDOS HIDRÁCIDOSLuis Enrique Coca Ramirez50% (2)
- QUIMICADocumento6 páginasQUIMICAValeria MirelesAún no hay calificaciones
- S04.s1. Tarea de Quimica Grupo 05Documento3 páginasS04.s1. Tarea de Quimica Grupo 05Marianela VenturaAún no hay calificaciones
- Nomenclatura Resumen Quimica InorganicaDocumento1 páginaNomenclatura Resumen Quimica InorganicaCuartoASantaMaríadePaineAún no hay calificaciones
- FOLLETODocumento12 páginasFOLLETOJostin Alan PazmiñoAún no hay calificaciones
- HIDRUROSDocumento9 páginasHIDRUROSGenesis MancillaAún no hay calificaciones
- Quimica 2Documento1 páginaQuimica 2valentina carcamoAún no hay calificaciones
- Numeros de OxidacionDocumento2 páginasNumeros de OxidacionSamuel EliasAún no hay calificaciones
- ValenciasDocumento2 páginasValenciasFernanda ToapantaAún no hay calificaciones
- Química InorgánicaDocumento9 páginasQuímica InorgánicaMARIANA ZAPATA GILAún no hay calificaciones
- Reacción de Solución de CuSO4 Con Lana de AceroDocumento1 páginaReacción de Solución de CuSO4 Con Lana de AceroDominic CybillAún no hay calificaciones
- Hidroxidos 2022Documento2 páginasHidroxidos 2022ColdWeather IsFineAún no hay calificaciones
- 3 Quimica Hidroxidos 19 de JulioDocumento6 páginas3 Quimica Hidroxidos 19 de JulioVALERIA NICOLE MAMANI TITOAún no hay calificaciones
- Taller 3.3 Oxidos, Hidroxidos, Acidos y Sales IIP 2023Documento2 páginasTaller 3.3 Oxidos, Hidroxidos, Acidos y Sales IIP 2023TatianaAún no hay calificaciones
- 5º) Formación de Compuestos Binarios.Documento18 páginas5º) Formación de Compuestos Binarios.Jenna LouisAún no hay calificaciones
- 6-Funciones QuímicasDocumento23 páginas6-Funciones QuímicasFelipe AmadoAún no hay calificaciones
- Q Sem7Documento7 páginasQ Sem7Nils Quiña PomaAún no hay calificaciones
- Tarea 3Documento2 páginasTarea 3luis espinozaAún no hay calificaciones
- Formación de Sales Iem B 2022Documento18 páginasFormación de Sales Iem B 2022Pablo Ricardo PeressottiAún no hay calificaciones
- Química 5°Documento20 páginasQuímica 5°JAIRO ENRIQUEZ FLORESAún no hay calificaciones
- Nomenclatura Oral PARTE DOSDocumento27 páginasNomenclatura Oral PARTE DOSMonyAún no hay calificaciones
- Acidos HidracidosDocumento3 páginasAcidos HidracidosNidia Millán SalazarAún no hay calificaciones
- 1475 1485Documento11 páginas1475 1485cutdianAún no hay calificaciones
- NOMENCLATURASDocumento21 páginasNOMENCLATURASEnyo Eduardo SalasAún no hay calificaciones
- Ficha Hidróxidos-2do AñoDocumento4 páginasFicha Hidróxidos-2do AñoBrayhan MallaupomaAún no hay calificaciones
- Hidróxidos 2022Documento2 páginasHidróxidos 2022Geovanna SuiraAún no hay calificaciones
- Taller Nomenclatura Oxidos, HidroxidosDocumento3 páginasTaller Nomenclatura Oxidos, HidroxidosFreddy Mendez SarmientoAún no hay calificaciones
- PlatntillasDocumento26 páginasPlatntillasMariela X Lopez CamaraAún no hay calificaciones
- Infografia Sistema EndocrinoDocumento2 páginasInfografia Sistema EndocrinoMariela X Lopez CamaraAún no hay calificaciones
- ALBUM DIGITAL Sobre El RenacimientoDocumento25 páginasALBUM DIGITAL Sobre El RenacimientoMariela X Lopez Camara100% (4)
- Infografia Sistema CardiovascularDocumento2 páginasInfografia Sistema CardiovascularMariela X Lopez CamaraAún no hay calificaciones
- Desde La Antigüedad El Asombro Llevó Al Ser Humano Ha Intentar Dar Un Significado A La Realidad y A Cosas Que No Pueden Explicarse A Primera VistaDocumento2 páginasDesde La Antigüedad El Asombro Llevó Al Ser Humano Ha Intentar Dar Un Significado A La Realidad y A Cosas Que No Pueden Explicarse A Primera VistaMariela X Lopez CamaraAún no hay calificaciones
- MAPA CONCEPTUAL Sobre La OntologiaDocumento3 páginasMAPA CONCEPTUAL Sobre La OntologiaMariela X Lopez CamaraAún no hay calificaciones
- Ensayo Sobre La Cultura EmprendedoraDocumento4 páginasEnsayo Sobre La Cultura EmprendedoraMariela X Lopez CamaraAún no hay calificaciones
- Contrato Social y El NaturalismoDocumento9 páginasContrato Social y El NaturalismoMariela X Lopez CamaraAún no hay calificaciones
- MEMORAMA Del GriegoDocumento3 páginasMEMORAMA Del GriegoMariela X Lopez CamaraAún no hay calificaciones
- ETIMOLOGIA Mapa ConceptualDocumento1 páginaETIMOLOGIA Mapa ConceptualMariela X Lopez Camara100% (3)
- Cronología de Acontecimientos Sociopolíticos en MéxicoDocumento23 páginasCronología de Acontecimientos Sociopolíticos en MéxicoMariela X Lopez CamaraAún no hay calificaciones
- Cuadro Comparativo Los Gobiernos Post Revolucionarios de Los Problemas Sociales y PolíticosDocumento6 páginasCuadro Comparativo Los Gobiernos Post Revolucionarios de Los Problemas Sociales y PolíticosMariela X Lopez Camara100% (2)
- Ciencias Q Se Relacionan Con La EconomiaDocumento5 páginasCiencias Q Se Relacionan Con La EconomiaMariela X Lopez CamaraAún no hay calificaciones
- Compuestos TernariosDocumento22 páginasCompuestos TernariosMariela X Lopez CamaraAún no hay calificaciones
- Características Generales de Los AlquinosDocumento4 páginasCaracterísticas Generales de Los AlquinosPolette Sainz Espino100% (1)
- Interperismo, Erosion y SueloDocumento12 páginasInterperismo, Erosion y SueloJesus Apaez MartinezAún no hay calificaciones
- Distribucion de Electrones para Tercero de SecundariaDocumento7 páginasDistribucion de Electrones para Tercero de SecundariaNazareth Narvasta AntonioAún no hay calificaciones
- Examen Final y Solucionario de La Asignatura de MineralurgiaDocumento5 páginasExamen Final y Solucionario de La Asignatura de Mineralurgiatorner mercurioAún no hay calificaciones
- Físico Química 8° NEEDocumento4 páginasFísico Química 8° NEEVale MêrčädôAún no hay calificaciones
- Parcial de Quimica UnisangilDocumento2 páginasParcial de Quimica UnisangilManuelDavidAún no hay calificaciones
- Color 1Documento64 páginasColor 1Marcela Sanchez AAún no hay calificaciones
- OrmusDocumento22 páginasOrmusNanonano Nano50% (2)
- Filtración - Tecnología FarmaceutcaDocumento7 páginasFiltración - Tecnología FarmaceutcaLuis DuarteAún no hay calificaciones
- Informe de Física 5Documento14 páginasInforme de Física 5Adrián LuisAún no hay calificaciones
- 01 MovimientoDocumento9 páginas01 MovimientoRodolfo German Flores OyarceAún no hay calificaciones
- ColigativasDocumento33 páginasColigativasDiego ArriagadaAún no hay calificaciones
- Proceso de Fabricacion de Latas de CervezaDocumento17 páginasProceso de Fabricacion de Latas de CervezaVictor Eduardo Azero Patton100% (1)
- Anexo 5 Info Carga Combustible PDFDocumento13 páginasAnexo 5 Info Carga Combustible PDFCristian Muñoz PalmaAún no hay calificaciones
- Transferencia de Calor - Ley de PlanckDocumento8 páginasTransferencia de Calor - Ley de PlanckCesar Hdz LunaAún no hay calificaciones
- CatalizadorDocumento3 páginasCatalizadorlourdess100% (1)
- TAURO Una Impresionante ConstelaciónDocumento10 páginasTAURO Una Impresionante ConstelaciónjorgelynchAún no hay calificaciones
- Estructuras Cristalinas (FCC)Documento35 páginasEstructuras Cristalinas (FCC)lord_helix_hell666Aún no hay calificaciones
- Semana 16Documento8 páginasSemana 16zeppelinIVAún no hay calificaciones
- Aguas TermalesDocumento15 páginasAguas TermalesJuan KAAún no hay calificaciones
- Practica 1 EspejoDocumento4 páginasPractica 1 Espejoyuvan ramosAún no hay calificaciones
- Elaboracion de Detergente Limpiavidrios Lavandina y DesodoranteDocumento5 páginasElaboracion de Detergente Limpiavidrios Lavandina y DesodoranteMan GerAún no hay calificaciones
- Practica III - LIQ IIIDocumento13 páginasPractica III - LIQ IIIUriel OropezaAún no hay calificaciones
- Casos de Estudio CaDocumento3 páginasCasos de Estudio CaJORDY MAEL VELI MEDINAAún no hay calificaciones
- Mapa PRESIONES ANORMALESDocumento1 páginaMapa PRESIONES ANORMALESJesus Manuel MoralesAún no hay calificaciones
- Influencia de Varios Productos Inoculantes Sobre El Poder de NucleacionDocumento12 páginasInfluencia de Varios Productos Inoculantes Sobre El Poder de NucleacionEstuardo CalderònAún no hay calificaciones
- Norma Aridos PDFDocumento10 páginasNorma Aridos PDFClaudia CarhuaniAún no hay calificaciones
- Examen CIENCIAS NATURALES - Tercer TrimestreDocumento7 páginasExamen CIENCIAS NATURALES - Tercer TrimestreAbisai BazanAún no hay calificaciones