Documentos de Académico
Documentos de Profesional
Documentos de Cultura
800 937 1 PB
Cargado por
Jessi Geanina AnguloTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
800 937 1 PB
Cargado por
Jessi Geanina AnguloCopyright:
Formatos disponibles
Influencia de la conductividad y fuerza inica de
soluciones sintticas que simulan la fase acuosa
del hormign en el fenmeno de la corrosin
de armaduras (*) (1)
Influence of the conductivity and the Ionic strength
of synthetic solutions which simulate the aquouse
phase of concrete In the corrosion process
S. GONI, A. MORAGUES y C. ANDRADE
Dres. en Qumica
ICCET/CSIC
ESPAA
Fecha de recepcin: 12-VII-1989
RESUMEN ABSTRACT
Este trabajo presenta el estudio cuantitativo, mediante la Polarization Resistance (Rp) has been the electrochemical
tcnica de Resistencia de Polarizacin (Rp), de la technique employed to study quantitatively the influence
influencia de los iones C y OH' en la corrosin de of cr and OH' ions on the corrosion of steel reinforcing, in
armaduras de acero, en un medio acuoso sinttico de a synthetic aqueous medium of similar composition to
similar composicin al contenido en los poros del those of the concrete pore solution. Ionic strenght,
hormign. Fuerza inica, conductividad (resistividad) y sus resistibity and their variations in function of CI' and OH'
variaciones en funcin de la concentracin de dichos concentration have been chosen as more interesting
iones, han sido los parmetros de inters escogidos para solution parameters, together with intensity and potential
la evaluacin del proceso, adems de las medidas de corrosion measurements. The results showed the clear
intensidad y potenciales de corrosin. Los resultados antagonistic role played by CI' and OH' ions on the
muestran claramente el antagonismo de los iones C y corrosion process, which decreased as ionic strenght
OH', cuyo carcter agresivo o protector disminuye a increased.
medida que aumenta la fuerza inica del medio.
1. INTRODUCCIN 1. INTRODUCTION
El hormign es un material ptreo y poroso Concrete is a stonelike and porous nnaterial
que contiene en sus poros una solucin containing in its voids an alkaline solution with
alcalina de elevado pH (entre 12 y 14). Esta high pH (range 12-14). This alkalinity keeps the
alcalinidad mantiene pasivo al acero de las steel passivate in the reinforcements for
armaduras durante perodos de tiempo indefinite period of time.
indefinidos.
Las dos circustancias principales, que pueden The two major reasons which may produce the
provocar la corrosin del acero dentro del corrosion of steel within the concrete are the
hormign, son la presencia de iones Cl o la presence of CI ions or the material
carbonatacin del material por reaccin con el carbonation by reaction with atmospheric CO2.
(*) Reproduccin permitida mediante autorizacin del autor.
(1) Contribucin tcnica presentada en eM 1 SEMINARIO NACIONAL DE CORROSION DE ABRACO.
MATERIALES DE CONSTRUCCIN, Vol. 39, n. 215, julio/agosto/septlembre 1989 19
Consejo Superior de Investigaciones Cientficas http://materconstrucc.revistas.csic.es
Licencia Creative Commons 3.0 Espaa (by-nc)
CO2 atmosfrico. Tanto con la carbonatacin Both in carbonation as when the chlorides
como cuando los cloruros penetran desde el enter from an external medium, the work life of
exterior, en la vida til de una estructura que a corroding structure can be distinguished into
se corroe, se distinguen dos perodos (1): two periods: a) an initiation period which
a) un perodo de iniciacin que comprende el expresses the time the aggressive agent takes
tiempo que tarda el agresivo en llegar hasta la to reach the reinforcement, when the steel
armadura, momento en el que el acero se despassivate and b) a propagation period when
despasiva, y b) un perodo de propagacin en the steel is being actively corroded.
el que el acero se corroe activamente.
En el caso de los cloruros, hasta el presente, In the case of chlorides, at present, many
se han realizado muchos trabajos (2-4) studies have been carried out (2-4) concerning
relacionados con el potencial de ruptura (Er), o with the bondbreaking potential (Er) or the
con la cantidad de cloruros necesaria para amount of chloride required to despassivate
despasivar las armadurasen un medio tan the reinforcements_in a so alkaline medium
alcalino (lmite de Cl / O H ). Sin embargo, son (limit of [Cr]/[OH ]). However, there are many
mucho menos numerosos los trabajos que works intended to establish a relationship
tratan de relacionar la cantidad de cloruros y between the amount of chlorides and the
la velocidad de corrosin de las armaduras, corrosion rate in the reinforcements, i.e., its
esto es, su influencia en el perodo de influence on the propagation period of the
propagacin de la corrosin. corrosion.
La velocidad de corrosin del acero, en The corrosion velocity of a steel in concrete
hormign, depende fundamentalmente del depends majorly on its humidity content
contenido en humedad (que a su vez fija la (which, in turn, limits the O2 availability and
disponibilidad de O2 y la resistividad) y de la resistance) and its temperature. When
temperatura. Cuando la corrosin es debida a corrosion is due to chlorides, there are
los cloruros, existen evidencias experimentales experimental evidences (5-7) that these ions
(5-7) de que stos ejercen tambin una also affect the corrosion rate. However,
influencia en la velocidad de corrosin, pero quantitative' relationship has not yet been
sin que se hayan establecido unas relaciones established between them.
cuantitativas entre ambos.
Los autores, tratando de explorar The authors of this paper, by exploring
sistemticamente los parmetros que systematically the parametres affecting the
influencian la velocidad de corrosin del acero corrosion velocity of steel in concrete, give
en hormign, presentan en este trabajo here, the results derived from the
resultados de corrosin del acero en corrosion of steel in solutions which simulate
disoluciones que simulan la fase acuosa del the aqueous phase of a concrete containing
hormign, conteniendo cloruros. Para ello, han chlorides. For this goal, several solutions with
preparado soluciones de pH comprendido pH range 11,64 and 13,22 has been prepared
entre 11,64 y 13,22, con diversas adiciones de with different additions of NaCI and CaClg.
NaCI y CaCl2. Estas disoluciones han sido These solutions have been characterized by _
caracterizadas mediante su fuerza inica, their ionic strength, resistance and [Cl ]/[0H ]
resistividad y relacin [Cl ] / [ 0 H ], y se han ratio and then, these parametres have been
relacionado estos parmetros con la velocidad compared to the corrosion rate obtained
de corrosin obtenida de medidas de from measurements of Polarization Resistance.
Resistencia de Polarizacin.
2. EXPERIMENTAL 2. EXPERIMENTAL
Se han preparado 17 soluciones sintticas con Seventeen synthetic solutions have been
una matriz comn de Ca(0H)2 saturado (8 g.l"") prepared with a common matrix of saturated
en agua destilada. Sobre esta matriz se han Ca(0H)2 in destilled water. On this matrix, it
aadido iones Cl y O H ' en diferente has been added Cl and OH ions at different
concentraciones, obteniendo relaciones concentrations, obtaining [Cl ]/[0H ] ratio range
[Cl ] / [ 0 H ] en un rango comprendido entre O y around 0 and 71. All the reactives employed
7 1 . Todos los reactivos empleados han sido have been t\/lerck AR.
Merck AR.
Al principio y al final de cada experiencia se At the beginning and at the end of each
han realizado anlisis cuantitativos de los experiment, it has been carried out a
iones. El Ca^^ se ha valorado quantitative analysis of the ions. Ca^^ has been
20 MATERIALES DE CONSTRUCCIN, Vol. 39, n. 215, julio/agosto/septiembre 1 989
Consejo Superior de Investigaciones Cientficas http://materconstrucc.revistas.csic.es
Licencia Creative Commons 3.0 Espaa (by-nc)
complexomtricamente con soluciones de evaluated complexonrietrically with EDTA
EDTA 0,01 M empleando calcena como 0,01 M solutions employing calceine as
indicador. El ion OH", frente a HCI 0,01 M y indicator. OH ion, by HCI 0,01 M and
fenoftalena,_el Na+ y K^ por fotometra de fenoftaleine Na^ and K" by flame fotometry
llama y el Cl" por valoracin con AgNOg. Las and Cl by titration with AgNO^. The
medidas de pH se realizaron con un electrodo measurements of pH were carried out with a
combinado de vidrio empleando un pHmetro glass combined electrode employing a pH
Orion 9 0 1 . Las medidas de conductividad se metre Orion 901.
hicieron en un Conductmetro Crison 525 The measurements of conductivity were carried
mediante una clula conductimtrica de out by a conductiometre Crison 525 and
electrodos de platino. conductimetric cell of platinum electrodes.
En la Tabla I recogen los datos ms Table I shows the most significant data of the
significativos de todas las soluciones. Como se solutions tested. As it can be observed, there is
puede ver, existe una diferencia notable de los remarkable difference of pH values as a
valores de pH en funcin del NaCI o CaCl2 function of NaCI or CaCl2 added, where CaCl2
aadido, siendo ms bajos en el caso del has lower pH values due to the precipitation
CaClg debido a la reaccin de precipitacin del reaction of Ca(0H)2, which, in turn, is a
Ca(OH)2 que, a su vez, es funcin de su function of its concentration (See no. 15 in
concentracin (ver n." 15 en Tabla I). Table I).
TABLA I (TABLE I)
Caracterizacin de las soluciones sintticas (Characterization of synthetic pore solution)
KOH NaCI CaCIs [OH"], [Ca^'l Icorr, P
N." PH^ [cr]/[0H-] ( / x A c r n 2) f(M)
(N) (N) (N) (M) (M) {Clem)
1 0.5 12.36 0.06 0.03 8.3 1.6 18 0.6
2 - 0.75 - 12.36 0.06 0.03 12.3 1.6 13 0.8
3 0.2 - - 13.02 0.20 0.004 0 0.06 25 0.2
4 0.2 0.1 - 13.02 0.20 0.004 0.5 0.2 20 0.3
5 0.2 0.5 - 12.85 0.17 0.005 3.0 0.9 13 0.7
6 0.2 0.75 - 12.82 0.17 0.005 4.4 1.0 10 0.9
7 0.2 1.0 - 12.80 0.20 0.004 5.0 1.15 9 1.2
8 0.5 0.5 - 13.22 0.42 0.001 1.2 0.46 8 1.0
9 0.5 0.75 - 13.17 0.40 0.001 1.9 0.54 7 1.2
10 - - 0.5 11.96 0.04 0.23 13.5 1.8 21 0.7
11 - - 0.75 11.90 0.04 0.37 19.0 2.1 16 1.1
12 0.2 - 0.1 12.66 0.10 0.005 1.0 0.4 30 0.2
13 0.2 1 - 0.5 12.04 0.04 0.18 12.5 1.6 21 0.7
14 0.2 - 0.75 11.90 0.04 0.30 19.0 2.0 16 1.1
15 0.2 - 1.0 11.64 0.01 0.30 71.0 6.6 13 1.2
16 0.5 - 0.5 12.24 0.04 0.07 12.5 1.6 18 0.7
17 0.75 0.75 12.02 0.04 0.20 19.0 2.2 14 1.0
La clula de corrosin empleada es similar a la The corrosion cell employed is similar to the
descrita en un trabajo previo (8). Como one described in a previous paper (8). As
electrodos de trabajo se utilizan tres barras working electrodes, three identical steel rods of
idnticas (en cada clula) de acero de 5,4 mm 5.1 mm diametre, were employed (in each cell),
de dimetro, pulidas, desengrasadas y and a forth rod of carbon employed as a
pesadas; una cuarta barra de carbn se suplementary electrode. The area exposed to
emplea como electrodo auxiliar. El rea de electrochemical attack is 4.2 cm'i which is
exposicin al ataque electroqumico, de limited with isolating tape. The solutions are
4,2 cm^, se delimita con cinta aislante. Las kept in thermostated baths at 21 C along the
soluciones se mantienen en baos time the experiment lasts.
MATERIALES DE CONSTRUCCIN, Vol. 39, n." 21 5. julio/agosto/septiembre 1989 21
Consejo Superior de Investigaciones Cientficas http://materconstrucc.revistas.csic.es
Licencia Creative Commons 3.0 Espaa (by-nc)
termostatados a 21 C durante todo el tiempo
que dura la experiencia.
Tcnica de medida Techniques
La Resistencia de Polarizacin ha sido la The Polarization Resistance iias been tie
tcnica empleada para medir la evolucin de technique employed to evaluate the corrosion
la velocidad de corrosin con el tiempo, segn rate along time, according to the description
la forma descrita en anterior trabajo (8). La given in a previous paper (8). The corrosion
intensidad de corrosin se calcula a partir de intensity is calculated from Stern-Geary's
la ecuacin de Stern-Geary (9) empleando un equation (9) employing a constant B = 26 mV
valor de la cte. B de 26 mV o 52 mV, cuando el or 52 when the steel is actively corroding or
acero se corroe activamente o cuando el acero when the steel remains passive. The
se conserva pasivo. Las prdidas de peso electrochemical weight losses are compared to
electroqumicas se contrastan con las those obtained by weighing the steel prior and
obtenidas por pesada de los aceros after the experiments (Fig. 1).
antes y despus de la experimentacin (Fig. 1).
Los potenciales de corrosin se han medido
frente a un electrodo de referencia de
calomelanos saturados empleando un
Potenciostato Amel 551 con compensacin
electrnica de la cada hmica.
ELECTROCHEMICAL WEIGHT LOSS ( m g . c m ' ^ )
Fig. 1.Comparacin de las prdidas de peso calculadas
electroqumicamente y gravimtricamente.
Fig. 1.Comparison between electrochemical and
gravimetric weight loss.
Los datos de intensidad de corrosin que The corrosion potentials have been measured
aparecen en la Tabla I son unos valores employing a saturated calomel reference
medios obtenidos a partir de su integral en el electrode using a Potentiostate Amel 551 with
tiempo, dividida por el nmero de das de ohmic drop compensation. The data of
duracin de cada experimento. Esto se ha corrosion intensities shown in Table I, are the
hecho as a fines comparativos puesto que, por average values obtained from their integral
los general, la Icorr. instantnea aumentaba along time divided by the number of days of
bruscamente a partir de un cierto tiempo, sin each test. This has been made so in order to
conseguir obtener un equilibrio. establish a comparison, since, in general, the
instantaneous Icorr raises drasctically from a
certain period of time, without reaching an
equilibrium.
22 MATERIALES DE CONSTRUCCIN, Vol. 39, n. 215, julio/agosto/septiembre 1989
Consejo Superior de Investigaciones Cientficas http://materconstrucc.revistas.csic.es
Licencia Creative Commons 3.0 Espaa (by-nc)
3. RESULTADOS Y DISCUSIN 3. RESULTS AND DISCUSSION
Variacin de la Resistividad en funcin del Variation of the Resistivity as a function of
pH pH
Como puede verse en la figura 2, existe una As it can be observed in Fig. 2, there is a linear
relacin lineal entre la resistividad y el pH para relationship between the resistivity andjhe pH
cada una de las concentraciones de ion Cl for each one of the concentration of Cl ions
estudiadas, obteniendo un abanico de rectas tested, obtaining a range of rects that tend to
que tienden a confluir a valores altos de be equal at high pH value = 13,70. The
pH-13,70. La contribucin del ion Cl" a la contribution of the Cl ion to the solution
resistividad total de la solucin es ms acuosa resistivity is more remarkable at low pHs. The
a bajos pHs. La explicacin que se h a d a d o a explanation given to this point is based on the
este hecho, se basa en que el ion OH tiene fact that the OH ion has a value of equivalent
un valor de conductividad equivalente a at infinite dilution of 198 in comparison to Cl
dilucin infinita de 198 en comparacin con ion with 78,4. Thus,_ at high pHs, the
78,4 del ion Cl". Por lo tanto a altos pHs_ conductivity of OH will prevail over Cl in the
prevalecer la conductividad del ion O H ' sobre overall value of the specific conductivity (or its
el Cl en el valor global de la conductividad inverse, the resistivity).
especfica (o su inversa la resistividad). Sin
embargo, a bajos pHs la contribucin del ion However, at low pHs the contribution of Cl ion
Cl en funcin de su concentracin es bien as a function of its concentration is quite
diferenciada. differentiated.
NaCl A-NaOH
-CaCl2 x-NaOH+Ca(OH)2
13.5- A-KOH
\\ ^^ ^
13-
'*X "
pH
1^5-
\N rib)
^
\
12 -
(e) Vi \(d) \(c)
11.5- 1 1 I T-
(D 5 10 30 40 60 80 100
/(fl.cm)
Fig. 2.Variacin de la Resistividad en funcin del pH.
(a) O N en Cl", (b) 0,1 N, (c) 0,5, (d) 0,75 N y (e) 1 N.
Fig. 2.Variation of Resistivity in function of the pi-i value,
(a) 0 N en Cl'. (b) 0,1 N, (c) 0.5, (d) 0,75 N and (e) 1 N.
Comportamiento Electroqumico Electrochemical behaviour
En las figuras 3, 4 y 5 se representan los In fig. 3, 4 and 5, it has been represented the
valores instantneos de la Icorr. y la Ecorr. en instataneous values of the Icorr. and Ecorr. as
funcin del tiempo, siendo cada punto la functions of time, in which each point is the
media de tres resultados. La zona rayada en average of three results. The shaded area in
las grficas indica una frontera aproximada the charst show the approximate boundary
entre la Icorr. considerada significante y la bewteen significant Icorr. and unsignificant
Icorr. despreciable. ones.
La influencia de la concentracin del ion C f The influence of the Cl (NaCI) ion
(NaCl) para una cantidad cte. de KOH se concentration for a constant amount of KOH, is
MATERIALES DE CONSTRUCCIN, Vol. 39, n. 21 5, julio/aqosto/septiembre 1 989 23
Consejo Superior de Investigaciones Cientficas http://materconstrucc.revistas.csic.es
Licencia Creative Commons 3.0 Espaa (by-nc)
recoge en la Fig. 3. Como puede verse, en shown in Fig. 3. As it can be observed, in
ausencia de NaCI [curva (a) en Fig. 3] la Icorr. absence of NaCI (curve (a) in Fig. 3) the Icorr.
se mantiene prcticamente por debajo del remains essentially below the value 0,2 lA cm^
valor 0,2 juA y los Ecorr. correspondientes and the respective Ecorr. reach values
alcanzan valores de 100 mV. A medida que oMOO my. As the concentration of NaCI
aumenta la concentracin de NaCI, los valores increases, the Icorr. raises too, with a clear
de Icorr. tambin lo hacen, con una clara difference between those corresponding to a
diferencia entre ios correspondientes a la NaCI 0,1 N and 0,5-1 N concentration. On the
concentracin de NaCI de 0,1 N y 0,5-1 N. Por contrary, the Ecorr evolves towards more
el contrario, los Ecorr. evolucionan hacia negarive values. It must been pointed out that
valores ms negativos. Hay que destacar que the curve correponding to a NaCI 1 N
la curva correspondiente a una concentracin concentration does not reach the Icorr. that
1 N, en NaCI, no alcanza los valores de Icorr. would be expectable due to the high
que se experaran debido a su alta concentration of C. The explanation of this
concentracin en ion Cl . La explicacin a este phenomenom, as we shall see below, may be
fenmeno, como veremos ms adelante, puede found in the fact that the high ionic strength of
encontrarse en la elevada fuerza inica del the medium decreases ionic movility and
medio que resta m w i l i d a d inica y por lo tanto therefore, activity to the Cl ion.
actividad del ion Cl .
J-400-ff
>i(b)
^(e)
-I 1 1 1 1 1 1 1 1 1 r -
(e)[cr]=lN,pH=ll,64
-I 1 1 1 1 1 1 1 1 1 1 r- 10'-
(d)[cr]=0.75N,pH= 12.82
(c)[cr]0.5N.pH = 12,85
x
r--
d _c (d) [cr]=0.75N,pH=11,90
-A ^ ,
(c) [Cr]asN.pH =12,04
(b) [cr]=0.1N.pH=12.66
->^
pH = 13,02
(a)pH = 13.02-
T 1 1 1 1 1 1 1 1 1 1 1 1 r r r r-
10 20 30 40 50 60 70 80 90 0 10 20 30 40 50 60 70 80 90
t (days) t (days)
Fig. 3.Variacin de la Intensidad y Potencial de Corro- Fig. 4.Variacin de la Intensidad y Potenciales de
sin con el tiempo. Influencia de la concentracin del ion Corrosin con el tiempo. Influencia de la concentracin
c r (NaCI). del ion c r (CaClg).
Fig. 3.Variation of Corrosion Potential and instanta- Fig. 4.Variation of the Corrosion Potential and instanta-
neous Intensity in time. Influence of chloride concentra- neous Intensity with time. Influence of chloride concentra-
tion (NaCI). tion (CaCl2).
En el caso del CaCig (Fig. 4), los pHs bajan In the case CaCl2 (Fig. 4), the pHs fall
considerablemente en funcin de la remarkably as a function of the added
concentracin aadida, debido a la reaccin concentration, due to the precipitation reaction
de precipitacin del Ca(0H)2 antes of Ca(0H)2 formely mentioned, reaching,
24 MATERIALES DE CONSTRUCCIN, Vol. 39, n. 215, ulio/agosto/septiembre 1989
Consejo Superior de Investigaciones Cientficas http://materconstrucc.revistas.csic.es
Licencia Creative Commons 3.0 Espaa (by-nc)
mencionada, alcanzndose por lo tanto para la therefore for the same equivalent
misma concentracin equivalente de ion Cl corcentration of Cf ions, higher Icorr than
valores de Icorr. ms elevados que los those obtained with NaCI. Similarly, the Ecorr
obtenidos con NaCI. Asimismo los valores de are shifted to more negative zones.
Ecorr. se desplazan hacia zonas ms
negativas.
En cuanto a la influencia del pH (Fig. 5), y Regarding the influence of pH (Fig. 5), as it was
como era de esperar, para una concentracin expected, for a fixed concentration of CI, the
fija de C f la Icorr. menor se obtiene para el lowest Icorr is obtained for the highest pH
valor mayor de pH = 13,22, aunque en el caso value = 13,22. However, in the case of
de la concentracin 0,75 N de NaCI las curvas NaCI 0,75 N concentration, the curves
correspondientes a los pHs 12,36 y 12,82 se corresponding to pHs 12,36 and 12,82, are
entrecruzan prcticamente, desde el principio, crossed almost from the very beginning,
sin establecer una diferencia clara entre ellas. without a clear distiction between them. When
Cuando la concentracin de NaCI es 0,5 N a NaCI concentration is 0,5 at those pHs, the
dichos pHs, las curvas tambin se entrecruzan, curves also cross each other though after 20
pero a partir de 20 das, sin obtener valores days, without reaching stable value even after
estables an a los 50 das. 50 days.
En general, los valores de Icorr. disminuyen In general, the Icorr values fall drastically after
bruscamente al cabo del primer da, para the first day and then increase after 5 or 6
empezar a subir despus de 5 o 6 das sin days without reaching, almost in any case, a
llegar a alcanzar, casi en ningn caso, un stable equilibrium along time. For this reason
equilibrio estable con el tiempo. Debido a esto, and in order to evaluate quantitavely these
y para valorar cuantitativamente estos efectos, effects, it has been taken a average Icorr value
se ha considerado un valor medio de Icorr. en for each case (See Table II
cada caso (ver Tabla I).
-400 -400-
t(days) t(days)
Fig. 5.Variacin de la Intensidad y Potenciales de Corrosin con el tiempo. Influencia del pH.
Fig. 5.Variation of Corrosion Potential and instantaneous Intensity with time. Influence of the pH.
MATERIALES DE CONSTRUCCIN, Vol. 39, n. 21 5, julio/agosto/septiembre 1989 25
Consejo Superior de Investigaciones Cientficas http://materconstrucc.revistas.csic.es
Licencia Creative Commons 3.0 Espaa (by-nc)
Variacin de la Icorr. media en funcin de Variation of the average Icorr. as a function
la Fuerza inica of the Ionic Strength
Como se observa en la figura 6, cuando las As it can be observed in Fig. 6, when the
variaciones de la fuerza inica se deben a variations of the ionic strength are due to
cambios en la concentracin del NaCI (puntos changes in the NaCI concentration (points no.
n. 3, 4, 5, 6 y 7 en Fig. 6), la Icorr. media 3, 4, 5, 6 and 7 Fig. 6), the average Icorr.
aumenta considerablemente a valores bajos increases remarkably to low ionic strength
de fuerza inica, tendiendo a estabilizarse values, tending to reach an equilibrium at
para altos valores de sta. Lo mismo ocurre higher values of the latter ones. This also
cuando las variaciones de fuerza inica se happens when the variations of the ionic
deben a variacionesde pH (igual strength are due topH variations (equal
concentracin de C l ) [curvas (c) y (d) en Fig. concentration of Cl) (curves (c) and (d) in
6]; a bajos valores de fuerza inica, pequeas Fig. 6), at low ionic strength values, small
variaciones de sta producen grandes variations produce sharp changes in the Icorr.
cambios de Icorr., sin embargo, estos cambios However, these changes are lower at high ionic
se hacen menores a altos valores de fuerza strength values. In the case of CaCh^, the
inica. En el caso del CaCl2, el fenmeno es phenomenom is similar, excepting that the
parecido, con la excepcin del punto n. 15, point no. 15 does not suit to the general
que no se ajusta al comportamiento de los behaviour due probably to the solution low pH.
dems quiz debido al bajo pH de la solucin. Analysing this figure, we can imply that both
Del anlisis de esta figura se deduce que_ the aggresive character of_ Cl ions as the
tanto el carcter agresivo d e j o s iones Cl protector character of OH decrease as the
como el protector de los OH disminuye a ionic strength increases, due to the lower
medida que aumenta la fuerza inica, debido a movility of the ions that make fall their
la menor movilidad de los iones que hace aggressive or protector activity in the
disminuir su potencial actividad agresiva o corrosion.
protectora frente a la corrosin.
6.6H - NaCI
CaCIa
a) pH=11,64-12,66
b) pH12.80-13.02
c) [cr]=o,5N
E d) [cr]=o.75N
u
fi(Ionic strength)
Fig. 6.Variacin de la Intensidad de Corrosin en fun-
cin de la Fuerza inica.
Fig. 6.Variation of the Mean Corrosion Intensity in func-
tion of the toma strength.
Variacin de la Icorr. media en funcin de Variation of the average Icorr. as a function
la Resistividad of the Resistivity
Si enfrentamos los valores de Icorr. media con If we match the average Icorr values with those
los de resistividad (Fig. 7), obtenemos unas of the resistivity (fig. 7) it is obtained a linear
26 MATERIALES DE CONSTRUCCIN, Vol. 39, n. 21 5, jullo/agosto/septiembre 1989
Consejo Superior de Investigaciones Cientficas http://materconstrucc.revistas.csic.es
Licencia Creative Commons 3.0 Espaa (by-nc)
relaciones lineales (escala doble logartmica) relationship (double logaritlim scale) between
entre ellos. Como puede verse, para un pH them. As it can be observed, for a given pH, the
dado, la Icorr. disminuye al aumentar la Icorr. falls as the resistivity increases (due to a
resistividad (por una disminucin de la decrease in the Cl ion concentration) [See
concentracin del ion C l ) [ver rectas (a) y (b) lines (a) and (b) in Fig. 7]. However, for a fixed
en Fig. 7]. Sin embargo, para una Cl concentration, the icorr. increases with the
concentracin fija de Cl", la Icorr. aumenta con resistivity (pH decrease) [See lines (c) and (d)
la resistividad (disminucin del pH) [ver rectas in Fig. 7]. The shift between line (a) and (b) is
(c) y (d) en Fig. 7]. El desplazamiento entre las due to their different plHs and content of Ca^^
rectas (a) y (b) es debido al diferente pH y in the CaCl2 solutions.
contenido en Ca^^ de las disoluciones de
CaCIg.
De la observacin de esta figura se puede Analysing this figure we can imply the
deducir el papel antagnico que los iones Cl y antagonic role played by Cl and OH' ions in
OH juegan en el proceso de la corrosin. the corrosion process.
Por ltimo, si representamos la relacin Finally, if we represent the [C]/[0H']
[Cr]/[OH"l de concentraciones frente a la Icorr. concentration ratio against the average Icorr.
media (en escala doble logartmica) (Fig. 8) se (in double logaritm scale) (Fig. 8) it is obtained
obtiene una lnea recta de pendiente 0,6, a straight line with slope = 0,6 which suits all
donde se ajustan todos los puntos. the points.
10'
(d) [cr]=0.75N
-NaCI
/c) [cr]=0.5N
-CaCli
10'
f=n.64-12j66
-NaCI
-CaClz Titrated
10- 10 H
E
(a)pH=12.80-13.02
4.
10-4
{a) loglcorr.= 2 , 9 - 2 , 8 l o q / (r-C;96)
(b) log Icorr.s 3 , 3 - 2.4 log/ (r-0.88) log Icorc=-0,43+0.62 l o g [ c r ] / [ o H -
Ic) logIcorr.=-l,5 1.3ioq/ (r= 0 , 9 9 ) (r0,99)
Id) log Icorr.=-1,7+ 1.7 l o g / ( r 0,99)
10" I 1 11r 10"^ linn I I 1 l"l [
10 10* I
10-2 10-' 10<* 10' 10*
fia.cm) [cr]/[0H-]
Fig. 7.Variacin de la Intensidad media de Corrosin Fig. 8.Variacin de la Intensidad media de Corrosin
en funcin de la Resistividad. en funcin de la relacin de concentraciones [Cr]/[0H"1.
Fig. 7.Variation of the Mean Corrosion Intensity in func- Fig. 8.Variation of the IVIean Corrosion Intensity in func-
tion of the Resistivity. tion of the Icrj/lOH'j ratio.
4. CONCLUSIONES 4. CONCLUSIONS
De los resultados obtenidos pueden deducirse From the results obtained in this work, we can
las siguientes conclusiones: imply the following conclusions:
MATERIALES DE CONSTRUCCIN. Vol. 39, n. 215, julio/agosto/septiembre 1989 27
Consejo Superior de Investigaciones Cientficas http://materconstrucc.revistas.csic.es
Licencia Creative Commons 3.0 Espaa (by-nc)
1) El efecto antagnico de los iones C f y OH 1) The anatagonic effect of Cl and OH ions in
en el fenmeno de la corrosin se pone de tlie corrosion pfienomenom is indirectly
manifiesto indirectamente a travs de las shown out by the parameter variations of
variaciones de los parmetros de solucin, the solutions, ionic strength and resistivity
fuerza inica y resistividad a que estos that these ions give result.
iones dan lugar.
2) Altos valores de fuerza inica disminuyen la 2) High ionic strength values decrease ion
movilidad de los iones y, por lo tanto, su movility and therefore, decrease their
potencial actividad agresiva o inhibidora a aggressive or protector potential character
la corrosin. in the corrosion process.
3) El efecto de la conductividad del ion Cl , en 3) The conductivity effect of Cl ion in the
el valor global de la conductividad overall of the specific conductivity
especfica, va disminuyendo a medida que decreases as increases the pH, and it is
aumenta el pH, anulndose para un valor anulled for a pH limit value = 13,70
lmite de pH = 13,70 sea cual fuere su whatever the concentration may be.
concentracin.
4) Una relacin lineal (en escala doble 4) A linear relatioship (in double logarithm
logartmica) se obtiene entre la relacin de scale) is obtained between the [Cl ]/[0H ]
concentraciones [Cl ] / [ 0 H ] y la Icorr. ratio and the average Icorr. from which it
media, a partir de la cual se puede calcular can be evaluated the limit of the formers
el lmite de los primeros que originan which gives as results Icorr.
valores de Icorr. < 0,2 jLtA.cm-2. values < 0,2 lA. cm^.
5. BIBLIOGRAFA
(1) TUUTTI K.: Corrosion of Steel in Concrete, Swedish Cement and Concrete Research Institute Stockholm. Research
Report n.4; 289 (1982).
(2) HAUSMANN D. A.: Steel Corrosion in Concrete, Mater. Prot, Vol. 6: 19 (1967).
(3) GOUDA V. K.: Corrosion and Corrosion Inhibition of Reinforcing Steel, I. Immersed in Alkaline Solution, Br Corros. J.,
Vol.5: 198 (1970).
(4) HARROP D.: A Galvanostatic and Potentiodynamic Study of the Corrosion Behaviour of Mild Steel in Saturated Calcium
Hydroxide Solution and Embedded Mortar in the Presence of Chloride Ion, British Research Establishment Pub. n. 116
(1977).
(5) ANDRADE C. and PAGE C. L.: Pore Solution Chemistry and Corrosion in Hydrated Cement Systems Containing Chloride
Salts: A Study of Cation Specific Effects, Br. Corros. J., Vol. 21 (1): 49 (1986).
(6) ANDRADE C, ALONSO C, GOI S. y GONZALEZ J. A.: Corrosion de Armaduras en Hormigones en Contacto con Agua
de Mar: el Efecto de la Galvanizacin y el Uso de Nitrito con Inhividor, 7th Int. Congress on Marine Corrosion and
Fouling. Valencia (Spain) Nov. (1988).
(7) YONEZAWA T., ASHWORTH V. and PROCTER R. P.: Pore Solution Composition and Chloride Effects on the Corrosion of
Steel in Concrete, Corrosion engineering Vol. 44 (7): 489 (1988).
(8) ANDRADE C. and GONZALEZ J. A.: Quantitative Measurements of Corrosion Rate if Reinforcing Steels Embedded in
Concrete Using Polarization Resistance Measurements, Werkst. Korros. Vol. 29: 515, (1978).
(9) STERN M. and GEARY A. L.: A theohcal Analysis of the Shape of Polarization Curves J. of the Elect. Soc. Vol. 104 (1): 56
(1957).
28 MATERIALES DE CONSTRUCCIN, Vol. 39. n. 215, julio/agosto/septiembre 1989
Consejo Superior de Investigaciones Cientficas http://materconstrucc.revistas.csic.es
Licencia Creative Commons 3.0 Espaa (by-nc)
También podría gustarte
- Semana Intro 1-Reparto ProporcionalDocumento7 páginasSemana Intro 1-Reparto ProporcionalJessi Geanina AnguloAún no hay calificaciones
- Ficha Socios. Consideracio0nes Tecnicas de La Ley Del Plastico-1Documento2 páginasFicha Socios. Consideracio0nes Tecnicas de La Ley Del Plastico-1Jessi Geanina AnguloAún no hay calificaciones
- Screening-Geanina InformeDocumento12 páginasScreening-Geanina InformeJessi Geanina AnguloAún no hay calificaciones
- La MentaDocumento3 páginasLa MentaJessi Geanina AnguloAún no hay calificaciones
- Tecnica Analitica para Determinacion de Fenoles TotalesDocumento3 páginasTecnica Analitica para Determinacion de Fenoles TotalesJessi Geanina AnguloAún no hay calificaciones
- INTRODUCCIÓn RadioquimicaDocumento3 páginasINTRODUCCIÓn RadioquimicaJessi Geanina AnguloAún no hay calificaciones
- Goma Dextrano ResumenDocumento1 páginaGoma Dextrano ResumenJessi Geanina AnguloAún no hay calificaciones
- Método Patrón InternoDocumento8 páginasMétodo Patrón InternoJessi Geanina AnguloAún no hay calificaciones
- Tecnica Analitica para Determinacion de Fenoles TotalesDocumento3 páginasTecnica Analitica para Determinacion de Fenoles TotalesJessi Geanina AnguloAún no hay calificaciones
- Omegas 3,6,9Documento1 páginaOmegas 3,6,9Jessi Geanina AnguloAún no hay calificaciones
- FuranoDocumento4 páginasFuranoJessi Geanina AnguloAún no hay calificaciones
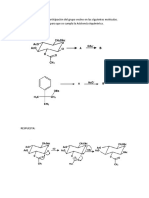
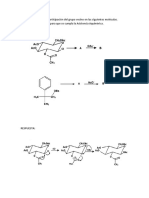
- Problema de Asistencia AnquimericaDocumento2 páginasProblema de Asistencia AnquimericaJessi Geanina AnguloAún no hay calificaciones
- Mecanismo de Acción de Los AnticuerposDocumento10 páginasMecanismo de Acción de Los AnticuerposJessi Geanina Angulo0% (2)
- Info ExpoDocumento37 páginasInfo ExpoAndrea IncháusteguiAún no hay calificaciones
- Física Nuclear Acceso A La Universidad PDFDocumento77 páginasFísica Nuclear Acceso A La Universidad PDFJessi Geanina Angulo100% (2)
- Problema de Asistencia AnquimericaDocumento2 páginasProblema de Asistencia AnquimericaJessi Geanina AnguloAún no hay calificaciones
- Cuestionario Materia y MediciónDocumento4 páginasCuestionario Materia y MediciónFREDDY SOBERANOAún no hay calificaciones
- Syllabus Q1001.3 2010 13Documento10 páginasSyllabus Q1001.3 2010 13Miguel Leyva EscobarAún no hay calificaciones
- Termodinamica IDocumento4 páginasTermodinamica IINGENIERÍA OrfeoAún no hay calificaciones
- Eficiencia Volumetrica Informe 02 Ponce Motores de Combustion Interna FIM UNIDocumento30 páginasEficiencia Volumetrica Informe 02 Ponce Motores de Combustion Interna FIM UNIJosePeñaTorres0% (1)
- Biologia Celular UVM - 9na Practica LaboratorioDocumento6 páginasBiologia Celular UVM - 9na Practica LaboratorioEdgarAún no hay calificaciones
- Electrodinamica Notas y EjerciciosDocumento131 páginasElectrodinamica Notas y EjerciciosMiguel Angel Dìaz CastañedaAún no hay calificaciones
- 910 Preparacion Superficial y Aplicacion de PinturaDocumento9 páginas910 Preparacion Superficial y Aplicacion de PinturaPamela CcahuanaAún no hay calificaciones
- Átomo de CarbonoDocumento29 páginasÁtomo de Carbonomanrey48100% (1)
- Campo Eléctrico Generado Por Una Distribución Continua Lineal de Carga - WikilibrosDocumento4 páginasCampo Eléctrico Generado Por Una Distribución Continua Lineal de Carga - WikilibrosXavier Blanco PonsAún no hay calificaciones
- MasDocumento2 páginasMasDarwin Nestor Arapa QuispeAún no hay calificaciones
- Informe y Cuestionario de Textura de SueloDocumento14 páginasInforme y Cuestionario de Textura de SueloLoui PérezAún no hay calificaciones
- Laboratorio Dos SolubilidadDocumento13 páginasLaboratorio Dos Solubilidadmaryori jennifer ramos ollachicaAún no hay calificaciones
- Tipoas de RocasDocumento15 páginasTipoas de RocasELIBETH MALDONADOAún no hay calificaciones
- Ficha Resumen Sobre Lectura Del Paisaje Marino CosteroDocumento5 páginasFicha Resumen Sobre Lectura Del Paisaje Marino CosteroAnonymous EVoCffsF9RAún no hay calificaciones
- Stonclad Ur - Poliol PDFDocumento8 páginasStonclad Ur - Poliol PDFAndres OsorioAún no hay calificaciones
- Diseno de Desarenador para Ptar NinaquiroDocumento3 páginasDiseno de Desarenador para Ptar NinaquiroAli KWAún no hay calificaciones
- Apuntes de Corriente Eléctrica (Parte 1)Documento3 páginasApuntes de Corriente Eléctrica (Parte 1)ALVARO ARIEL TORREZ CALLEAún no hay calificaciones
- Actividad 1 - El Carbón y El PetróleoDocumento11 páginasActividad 1 - El Carbón y El PetróleoDAVID JIMENEZ ORTIZAún no hay calificaciones
- Trabajo - de - Tubo - de - Venturi M.FDocumento17 páginasTrabajo - de - Tubo - de - Venturi M.FEleaZar Kyofet InediToAún no hay calificaciones
- Informe 8, Analisis de Mezclas BinariasDocumento10 páginasInforme 8, Analisis de Mezclas BinariasAndres Fernando Silvestre SuarezAún no hay calificaciones
- EJEMPLo de Doble TuboDocumento13 páginasEJEMPLo de Doble TuboMilagros Villena AvilaAún no hay calificaciones
- Pca Quimica de TerceroDocumento5 páginasPca Quimica de TerceroPatricio OrellanaAún no hay calificaciones
- 2 Estructura de PolimerosDocumento24 páginas2 Estructura de PolimerosCami CamilongaAún no hay calificaciones
- Tensión SuperficialDocumento3 páginasTensión Superficialsilvera123Aún no hay calificaciones
- Semana 2Documento2 páginasSemana 2Fisica Octavo NovenoAún no hay calificaciones
- Mecanica de FluidosDocumento18 páginasMecanica de FluidosTyrone CruzAún no hay calificaciones
- PLANIFICACIÓN ANUAL 4 U Ciencias 2023Documento2 páginasPLANIFICACIÓN ANUAL 4 U Ciencias 2023Ingrid ValdebenitoAún no hay calificaciones
- Cometa Halley BoppDocumento1 páginaCometa Halley Boppmerry lindaAún no hay calificaciones
- Balanza ElectromagneticaDocumento3 páginasBalanza ElectromagneticaCristtian Martinez100% (1)
- Problemas CIII Ocw Tema2Documento4 páginasProblemas CIII Ocw Tema2registradoresAún no hay calificaciones