Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Coorrosion Yhoel
Cargado por
denissa0 calificaciones0% encontró este documento útil (0 votos)
8 vistas7 páginasTítulo original
COORROSION-YHOEL.docx
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
8 vistas7 páginasCoorrosion Yhoel
Cargado por
denissaCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 7
7.3.
CORROSION GALVANICA
La corrosin galvnica ocurre cuando dos metales con diferentes potenciales
electroqumicos o con diferentes tendencias a corroerse en contacto al
metal-metal en un medio electroltico corrosivo. Los tres componentes
esenciales son:
Materiales que poseen diferentes potenciales superficiales.
Un electrolito comn.
Un conductor elctrico comn.
La unin de dos metales o aleaciones en un mismo medio, pero que estn
elctricamente aislados no experimentaran corrosin galvnica, como
producto de la unin galvnica, la corrosin del metal ms activo se
incrementa y su superficie se tomara andica, mientras que la corrosin, del
metal ms noble disminuye y su superficie se tomara catdica. La fuerza
impulsora de la corrosin es el potencial y la velocidad de corrosin, como
resultado de la unin galvnica
7.3.1. SERIE GALVANICA
Una serie galvnica de metales y aleaciones es til para predecir el
comportamiento galvnico, tal serie de metales es un arreglo de mtales y
aleaciones de acuerdo con su potenciales de corrosin, esto permitir
determinar que el metal o aleacin es ms activo en una unin galvnica.
El potencial de corrosin de un metal o aleacin es afectado por factores del
medio, dependiendo del tipo de medio donde pueden o no formarse una
pelcula de productos de corrosin sobre la superficie. Por lo comn la serie
galvnica ha sido realizada mediante mediciones en agua de mar, tabla 7.11
y figura 7.11
Tabla 7.11. Serie galvnica en agua de mar a 25C
Figura 7.11.potenciales de corrosin y aleaciones de agua de mar a 10
25C
LA TEORIA DEL POTENCIAL MIXTO Y LA CORROSION GALVANICA
Los conceptos de la teora de potenciales mixtas, que ya han sido discutidos
en el captulo 4 y analizados en relacin a la corrosin galvnica en las
secciones 4.7.1 y 4.7.3, hacen posibles hacer ciertas afirmaciones respecto al
efecto de la unin de dos metales dmeles.
a.- La serie galvnica predice que una unin metlica el metal ms activo
llega a ser el nodo de la celda de corrosin, mientras que el metal ms
noble llega ser el ctodo.
b.- La velocidad de corrosin del metal ms activo es acelerado mientras que
para el metal ms noble es retardado.
Para analizar una unin galvnica imaginemos el sigt: Zn/NaCl(IN)/Fe, que en
la prctica podra encontrarse en una proteccin catdica, el Zn se comporta
como nodo y el Fe como ctodo.
En el Zn (nodo) ZnZn+2 +2e
En el hierro (ctodo) O2 + 2H2O + 2e
Los resultados experimentados obtenidos, para el caso anterior, son
mostrados en la figura 7.12
Diagrama de potencial mixto E vs log para el par galvanizado Zn - Fe
Fig.7.13 curvas de polarizacin para el acero al carbono
Fig.7.14 curvas de polarizacin para metales disimiles M y N bajo diferentes
situaciones de. a) curvas catdicas
7.3.3. INFLUENCIA DEL AREA Y DISTANCIA DE LOS ELEMENTOS QUE
CONFORMAN LA UNION GALVANICA
a. El efecto del rea
Es un factor importante en la corrosin galvnica y puede ser evaluada en
funcin de la relacin del rea superficial del ctodo.
Una relacin de reas desfavorable consiste de un gran ctodo y un pequeo
nodo, por lo que la unin estara bajo control catdico.
La figura 7.15(a) muestra un nodo pequeo, que corresponde un tornillo de
acero recubierto con zinc, en contacto con un gran ctodo.
La figura 7.15(b) muestra un ctodo pequeo, en contacto con un gran nodo
7.15(a) 7.15 (b)
b. Efecto de la distancia
La corrosin acelerada debido a efectos galvnicos es generalmente mucho
mayor cerca de la unin galvnica, y el ataque disminuir conforme
incrementa la distancia a este punto.
La figura 7.16 donde la corrosin es ms severa alrededor de la periferia de
las cabezas de los pernos de acero recubiertos con cadmio que estuvieron en
contacto con la plancha de aluminio.
También podría gustarte
- Como Se Forman Los FósilesDocumento2 páginasComo Se Forman Los FósilesVickyLegorrAún no hay calificaciones
- Informe de LaboratorioDocumento8 páginasInforme de LaboratorioGabriel RomeroAún no hay calificaciones
- Sikaguard 70Documento4 páginasSikaguard 70alfonsodavilamontesAún no hay calificaciones
- Tarea3 G33Documento42 páginasTarea3 G33jairoAún no hay calificaciones
- Nociones Basicas Sobre Control de IncendiosDocumento22 páginasNociones Basicas Sobre Control de Incendiosacv2cordero83% (6)
- PRAC.#1 Reacciones de Reconocimientos de CarbohidratosDocumento4 páginasPRAC.#1 Reacciones de Reconocimientos de CarbohidratosGLORIA MARGARITA GUERRERO REYAún no hay calificaciones
- Historia de La FarmaciaDocumento17 páginasHistoria de La FarmaciaCentro de Internet R&RAún no hay calificaciones
- Toda Estabilidad - En.esDocumento20 páginasToda Estabilidad - En.esBad Gal Riri BrunoAún no hay calificaciones
- Características Principales Aplicaciones Típicas: Acero Dulce, Celulósico - AWS E6011Documento2 páginasCaracterísticas Principales Aplicaciones Típicas: Acero Dulce, Celulósico - AWS E6011jhosser andres jojoa calderonAún no hay calificaciones
- Diapositivas Válvulas AlivioDocumento66 páginasDiapositivas Válvulas AlivioJesus100% (1)
- Bioquimica Practica ReninaDocumento7 páginasBioquimica Practica ReninaArianna Lizeth Gonzalez AlmanzaAún no hay calificaciones
- Metanol Hoja de SeguridadDocumento6 páginasMetanol Hoja de SeguridadjosestalinmsAún no hay calificaciones
- Tarea Sintesis Inorganica 1 2020Documento4 páginasTarea Sintesis Inorganica 1 2020irvin aguirre floresAún no hay calificaciones
- Bufalos CriaDocumento2 páginasBufalos CriaMilitza GonzalezAún no hay calificaciones
- Guía de Ejercicios 2bDocumento9 páginasGuía de Ejercicios 2bEdgardo TabiloAún no hay calificaciones
- Termodinámica EjerciciosDocumento17 páginasTermodinámica EjerciciosJosé Alejandro Monge CruzAún no hay calificaciones
- Preinforme 3 FinalDocumento7 páginasPreinforme 3 FinalMónica Martínez PoloAún no hay calificaciones
- Concentración de Las Disoluciones - Colorimetría - InformeDocumento4 páginasConcentración de Las Disoluciones - Colorimetría - InformeMiguel Angel Chavez SilvaAún no hay calificaciones
- Práctica Calor Específico SólidoDocumento6 páginasPráctica Calor Específico SólidoAna CorsiniAún no hay calificaciones
- Practica 7 InorganicaDocumento6 páginasPractica 7 InorganicaVíctor JímenezAún no hay calificaciones
- Multipro 3000Documento2 páginasMultipro 3000RICARDO DONOSOAún no hay calificaciones
- Materiales Ceramicos, Polimericos y CompuestosDocumento27 páginasMateriales Ceramicos, Polimericos y CompuestosOliver MartinezAún no hay calificaciones
- Estequiometría. Meteorización QuímicaDocumento4 páginasEstequiometría. Meteorización QuímicaLuisaFernandaLeonOrtizAún no hay calificaciones
- Preparacion OftalmicaDocumento5 páginasPreparacion OftalmicalalolitoAún no hay calificaciones
- 2.5 Principios de Funcionamiento Del ConductímetroDocumento2 páginas2.5 Principios de Funcionamiento Del ConductímetroDiana RidderAún no hay calificaciones
- Flujograma de Procedimiento de Preparación de Un JarabeDocumento4 páginasFlujograma de Procedimiento de Preparación de Un JarabeLidia Escobar100% (1)
- Norma Covenin Ventilacion - 2250-2000 PDFDocumento14 páginasNorma Covenin Ventilacion - 2250-2000 PDFJose Molero50% (2)
- Evaluacion Final - Escenario 8 - Primer Bloque-Ciencias Basicas - Virtual - Fluidos y Termodinámica - (Grupo b03)Documento7 páginasEvaluacion Final - Escenario 8 - Primer Bloque-Ciencias Basicas - Virtual - Fluidos y Termodinámica - (Grupo b03)Yojan Mateo Rojas PulidoAún no hay calificaciones
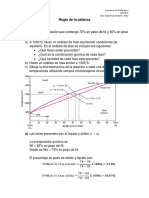
- Regla de La Palanca 2Documento3 páginasRegla de La Palanca 2josSAN.6262Aún no hay calificaciones
- 2) Refinacion de MetalesDocumento84 páginas2) Refinacion de MetalesJonatan Zero-Wu Zepeda100% (1)