Documentos de Académico
Documentos de Profesional
Documentos de Cultura
RLMM Art 02v22n2 p40
Cargado por
Rene Ccolque HuillcaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
RLMM Art 02v22n2 p40
Cargado por
Rene Ccolque HuillcaCopyright:
Formatos disponibles
Revista Latinoamericana de Metalurgia y Materiales, Vol.
22, N 2,2002,40
- 51
EVIDENCIAS ESPECTROSCOPICAS DE LA DEGRADACIN HIDROLTICA DE LA POLI(p-DIOXANONA) M. A. Sabino
1,
O. Nuez
2,
A. J. Mller
1. Grupo de Polmeros USB, Departamento Ciencia de los Materiales; 2. Departamento de Procesos y Sistemas. Universidad Simn Bolvar, Apartado 89000, Caracas 1080-A, Venezuela
Resumen En este trabajo se estudi la degradacin hidroltica de un polmero biodegradable y bioabsorbible, la Poli (p-Dioxanona) o PPDX. La PPDX es un polister-ter aliftico con gran potencial biomdico, debido a su estructura molecular y propiedades adecuadas para utilizarse como material de osteosntesis. La PPDX se degrada hidrolticamente originando subproductos de degradacin de bajo peso molecular, atxicos que pueden ser metabolizados o bioabsorbidos por el organismo. Se utilizaron monofilamentos de PPDX que se degradaron hidrolticamente en una solucin buffer fosfato yagua a 37C durante 12 semanas, y se utilizaron tcnicas de caracterizacin como Espectroscopia Infrarrojo por Transformada de Fourier (FfIR) y Espectrometra de masa (EM). A travs de FTIR, se demostr que durante el perodo de degradacin se evidencia la disminucin de grupos 0H libres, producto de la posible asociacin de estos grupos a los productos resultantes de las rupturas de enlaces. Tambin se evidenci la posible formacin de estructuras intermediarias o complejas, mediante asociacin de grupos, donde pueden intervenir los grupos fosfatos presentes en el medio de hidrlisis. Adems, como consecuencia de los rompimientos del grupo ster presente en la estructura de la PPDX, se observan variaciones de absorbancia de las bandas asociadas a los grupos carbonilos dada la aparicin del grupo cido carboxlico. Estas evidencias fueron verificadas mediante Espectrometra de Masas donde se determin que uno de los subproductos de la degradacin de la PPDX corresponde al cido 2-hidroxi-etoxi- etanoico. Palabras claves: Poli (p-dioxanona), Abstract In this work, the hydrolytic degradation of a biodegradable and bioabsorbable polymer, Poly(p-dioxanone) or PPDX, was studied. PPDX is an alifatic polyester-ether with potential for biomedical applications since its molecular structure and properties are adequate to be used as osteosynthesis material. PPDX degrades hydrolytically originating byproducts of low molecular weight that are non-toxic and that can be metabolize or bioabsorbed by the body. PPDX monofilaments were hydrolytically degraded in a phosphate buffer solution and in water at 37C during 12 weeks, Fourier Transform Infrared Spectroscopy (FTIR) and Mass spectrometry (MS) were employed to characterize the degradation products. FTIR results showed that during the degradation period a decrease in the number of free O-H groups was recorded, a possible product of the association of these groups to tbose produced by degradation. It was also found that intermediary or complex structures were formed by group association where a contribution of the phosphate groups present in the hydrolysis medium is probable. Furthermore, as a consequence of the ester bond cleavage present in PPDX, a variation in the absorbance of bands associated to carbonyl groups are observed in view of the formation of carboxylic acid groups. These evidences were verified by Mass Spectrometry, whose results indicated that one of the degradation byproducts of PPDX is 2-hydroxy-etoxi-ethanoic acid. Keywords: Polytp-dioxanone), degradation, hydrolysis, spectroscopy, biomaterials degradacin, hidrlisis, espectroscopia, biomateriales
1. Introduccin El medio fisiolgico humano (H20 extracelular) rene las condiciones apropiadas para que se puedan producir con facilidad los procesos hidrolticos. Para ello el polmero debe poseer enlaces hidrolticamente inestables para que el proceso de biodegradacin se produzca en un tiempo razonable y el-mismo pueda llevarse a cabo en condiciones de pHfisiolgico (entre 7 y 7.4) [1]. LaPPDX se ha utilizado
ampliamente como material biodegradable. Si este polmero se compara con otros polisteres biodegradables como el Poli(cido Gliclico) PGA Yel Poli(cido L-lctico) PLLA, se puede concluir que la presencia de un enlace ter y de un CH2- adicional le confieren gran flexibilidad. Adicionalmente, y debido a que presenta menor concentracin de grupos ster debe presentar una menor velocidad de degradacin va hidrlisis, 16 cual conducira a una mayor retencin de sus propiedades en funcin del tiempo [2-5]. Es por lo tanto
M. A. Sabina y col. /Revista Latinoamericana de Metalurgia y Materiales
de gran importancia prctica el poder determinar las evidencias de la ocurrencia del proceso de degradacin hidroltica, siendo ste el momento a partir del cual el material presentar una modificacin (o deterioro) importante de sus propiedades iniciales. 2. Metodologa Experimental 2.1. Materiales En la experiencia se trabaj con un monofilamento de Poli(p-Dioxanona) PPDX Johnson & Johnson (marca Ethicon), con un dimetro promedio de 1 mm. La muestra se encontraba esterilizada y empacada al vaco. Para el proceso de degradacin in vitro de las muestras, se utiliz como medio de hidrlisis agua destilada la cual present un pH inicial de 7.2 Ytranscurridas las dos primeras semanas el pH descendi hasta un valor de 4.5 donde se mantuvo durante el resto del tiempo para una duracin total de 16 semanas. El otro medio de hidrlisis utilizado fue una solucin buffer fostato 0.2 M (a base de fosfato de sodio hidrogenado Na2HP04y fosfato de potasio di-hidrogenado-Kf.Ptj.) la cual present un pH inicial de 7.4, donde otro grupo de monofilamentos fueron colocados. 2.2. Espectroscopia Infrarroja. FTIR La experiencia consisti en preparar pelculas por evaporacin de solvente realizando la disolucin de las muestras en una solucin fenol/tetracloroetano (2:3) y garantizando el proceso de evaporacin dentro de un horno al vaco a temperatura ambiente. Para los ensayos se utiliz
un Espectrofotmetro Infrarrojo por Transformadas Fourier FTIR marca Nicolet, modelo Magna 750. La resol empleada fue de 4 cm', el nmero de barridos igual a 30 y detector DTGS KBr con beamsplitter de KBr. Para determinacin de la constante de velocidad k, de acu con el mtodo de velocidades iniciales [6] se obtuvi espectros infrarrojos para muestras extradas da a da d la primera semana de degradacin en ambos medi Previamente, se obtuvo una curva de calibracin co finalidad de establecer la relacin [-COO-]/ Absorbancia, importante recalcar que la determinacin de la absorb estuvo centrada en la banda de 1750 cm' atribuible ~ absorcin de los steres alifticosf-Ce=O); y con el fin evitar los problemas de espesor entre las diferentes pel se estableci la relacin entre la banda atribuible al carbonilo y la banda atribuible a la vibracin de alargami del grupo C-O-C, que en el caso de teres alifticos encuentra alrededor de 1125-1150 cm:' debido al alargamieac asimtrico. 2.3. Espectrometra de Masas Para poder realizar los anlisis por la tcnica GC-MS Chromatoghaphy-Mass Spectrometry") fue nece ari derivatizacin de los subproductos de la degrada hidroltica del polmero, para as garantizar que los mi:smes no fuesen retenidos en la columna del espectrmetro de [7]. En base a esto, se emple N-t-butildimetilsililimi (TBD MSIM), cuya formula molecular y su estructura qumi::z es: C(CH3)3-Si(CH3)2NCH=NCH=CH (Figura 1), y cuya acci ~ derivatizante se esquematiza en la Figura 2.
CH]
Muestra
~o: +
H
CH1- C-CH1
s+CH1 N
I
CH1-Si-N(d
/ -
I
CH1
----. I
Ir
I
CH &J
Muestra
~6H
Si-X CH1
CH]
I
CH3- C-CH]
1
CH1
I I
CH3
/ -
CHJ-Si-NU
Muestra
~O-S-CHJ
+HX
I
CH1
Fig. 2. Esquema de la reaccin de derivatizacin
Fig. 1. Estructura molecular de TBDMSIM
42
Revista Latinoamericana de Metalurgia y Materiales, Vol. 22, N 2, 2002.
En un ambiente estril las muestras de PPDX virgen, en forma de discos con dimetro de 20 mm y un espesor aproximado de 0.5 rnm (obtenidos a partir de moldeo por comprensin de los monofilamentos desde el fundido y enfriadas bruscamente), fueron introducidas en tubos de ensayo que contenan 50 rnL de la solucin buffer fosfato, y dichos tubos se introdujeron en un bao termostatizado a una temperatura de 37C durante un periodo de 16 semanas. La solucin buffer fue filtrada (004 um) antes de ser usada, y se tomaron alcuotas durante perodos de 4 semanas, los cuales fueron subsecuentemente analizadas, con el fin de hacer seguimiento a los productos de degradacin que se presentan en funcin del tiempo. Sin embargo, este seguimiento no pudo ser posible debido a que las alcuotas correspondientes a la 4ta, 8va y 12va semana no presentaron indicios detectables por el equipo de los subproductos de degradacin de bajo peso molecular, pero si se obtuvo una buena resolucin para las alcuotas tomadas al final, es decir, luego de 16 semanas de degradacin donde se haban formado las especies de ms bajo peso molecular. Derivatizacin Las muestras o alcuotas tomadas luego del tiempo referido (16 semanas) se emple para realizar su derivatizacin en presencia del reactivo TBDMSIM. La muestra tomada (1 rnL) de la solucin buffer, contenedora de los subproductos de la degradacin hidroltica de la PPDX, fue puesta en un tubo de ensayo, se le aadi 1 mg de cido ascrbico con el fin de evitar la oxidacin de los cidos orgnicos presentes en la solucin; luego fue acidificada a pH 2-3 con 50 ul, de HCL, luego fue extrada tres veces con acetato de etilo (grado anlisis 99.9% Merck). Seguidamente se aadi sulfato de sodio como desecante para recoger el agua presente. El extracto fue combinado y posteriormente evaporado con Nitrgeno (gas)" El sustrato en forma de polvo que qued en el fondo del tubo, fue secado en una estufa al vaco a temperatura ambiente por 4 horas, en espera de su derivatizacin. Para determinar las condiciones ptimas de la derivatizacin, se procedi de la siguiente manera: en viales con capacidad de 1 rnL se aadieron 0.10 rnL de iso-octano y diferentes proporciones (entre 5-50 ul.) del reactivo TBDMSIM, y se evaluaron las siguientes condiciones de
tiempo y temperatura, 30 minutos a 60C. Al inyectar las diferentes mezclas de iso-octano y TBDMSIM, se encontr que con 20 ul. del derivatizante fue posible elucidar los cidos formados. Una vez determinado que las condiciones ptimas para la derivatizacin corresponden a 20 ul. de TBDMSIM, y 30 min a 60C, se procedi a mezclar 1 mg de los subproductos de la degradacin de la PPDX previamente secos con la cantidad correspondiente del derivatizante y 0.1 rnL de iso-octano. La Figura 3, muestra la formacin del derivatizado terbutil-dimetilsilil (TBDMS) de los grupos cidos y alcohol obtenidos de la hidrlisis. La mezcla mencionada fue inyectada automticamente en un Cromatografo de Gases (HP 5890, serie-2) acoplado a un Espectrmetro de Masa (HP 5972) (GC-MS), el cual cuenta con un inyector en modo split-splitless, y una columna capilar WCOTdeslica(CP-Sil-19CB,Chrompack,25mx0.32rnmI.D.). Se utiliz Helio como gas de arrastre. Las muestras fueron introducidas en el inyector split a 250C; para esto, la temperatura inicial delhomo fue 40C por un tiempo de 1 min, luego fue llevada hasta 200C a una velocidad de 10CI min y mantenida a esa temperatura por 8 minutos, para luego alcanzar la temperatura final. La fragmentacin de las especies se realiz a travs de impacto electrnico. El resto de las condiciones operacionales fueron las siguientes: el tiempo de corrida fue de 68 minutos; inyeccin/masa: 20-500 .tU min; segundos por barrido: 1.0; voltaje 1600 V; temperatura de transferencia 250C; defecto de masa 30 rnmu/1 OOamu;y el modo sean: full. El mtodo de adquisicin de datos fue a travs del programa HP CHEM 5890 column flow control. 3. Resultados 3.1. EspectroscODia lnfrarroia. FTIR El anlisis infrarrojo es una herramienta importante para identificar los cambios en la composicin qumica luego de estar sometida la PPDX a una degradacin hidroltica, manifestndose dichos cambios en variaciones en las regiones donde se presenta la absorcin de bandas atribuibles a grupos hidrxi, carbonilos, teres o steres (Figura 4). La Espectroscopia Infrarrojo no slo puede ser satisfactoriamente aplicada para caracterizar compuestos
o //,
OH -R- C-OH
CH3 CH]
CH] C~
2 TBDMSIM
---+-
I
CH)- C-
1
Si - O - R-
11
CO-
I
S-
I
C-CH]
CH3 CH]
CH3 CH3
Fig. 3. Derivatizacin de cidos y alcoholes productos de la degradacin hidroltica de un polister aliftico.
M. A. Sabino y col. /Revista Latinoamericana de Metalurgia y Materiales
43
orgnicos o para detectar interacciones entre polmeros en mezclas a travs de los cambios que sufren determinadas bandas en los espectros infrarrojos de dichas mezclas, sino tambin para determinar las posibles vas de degradacin que ha sufrido un polmero sometido. a un proceso hidroltico [8]. Entonces, la tcnica no slo permite caracterizar las muestras de polmeros sometidas a procesos de degradacin, sino que tambin da indicios de cual es el posible mecanismo de degradacin que sufren dichas muestras a las
condiciones experimentales a las que han sido sometidas (vase Figura 5), tomando como referencia las diferencias que se puedan observar entre los espectros infrarrojos de los componentes que no han sido sometidos a ningn proceso degradativo y aquellos obtenidos una vez realizada la degradacin. Tales cambios incluyen desplazamientos en la frecuencia de absorcin de la seal, incremento en el ancho de la banda, y cambios en la absorbancia o aparicin de bandas atribuibles a los posibles subgrupos o especies de degradacin [8,9].
Fig. 4. Esquema del proceso de hidrlisis de un polister aliftico como la PPPDX en medio acuoso.
CH2-CH2-0-CH2-C-O-
11
o
H20
:; __::==te.~
OH
-O-CH2-C-OOH
I I
Ir
OH . + OH-C-CH2-
p+ OH-P_ .. 1---
Fig. 5. Esquema del proceso de hidrlisis de un polister aliftico como la PPDX en una solucin buffer fosfato [9]. En algunas investigaciones realizadas [10,11], se observa la variacin de las absorbancias en la zona de 3330 cm", lo cual indica la formacin o el aumento de grupos hidroxi en las muestras hidrolizadas. As mismo, se evidencian variaciones en la banda de absorcin ubicada alrededor de 1736 cm', atribuyndose estos eambios a que dichos grupos se encuentran en un ambiente qumico diferente, es decir, pueden indicar que el grupo carbonilo perteneciente a un grupo funcional ster, pasara a formar parte de grupos funcionales cetonas, cidos carboxlicos, etc., como producto de los cambios ocurridos en la composicin qumica del polrnero, luego de haber sido sometido a una degradacin hidroltica. El estudio de los espectros de las muestras de PPDX se fundament bsicamente en las muestras hidrolizadas en la solucin buffer fosfato ya que en todos los casos las variaciones sufridas fueron similares. De este modo se limit al anlisis de las zonas de nmero de onda entre 3800---3400, 3050---2850,1800-1600, 1300---1100y 1080-1020 cm'; debido a que en dichas zonas se evidencian cambios apreciables en lbs espectros. Las bandas caractersticas para la PPDX se presentan en la Tabla 1.
44
Revista Latinoamericana de Metalurgia y Materiales, Vol. 22, N 2, 2002.
Tabla l. Bandas de absorbancia IR caractersticas para la PPDX. N onda (cm") Grupo Observaciones
3620-3610 3460 2960 2920 l740 1135 1060
-OH -OH -CH3 -CHTCHT -C=O -CO-C-CO-
Alargamiento de grupos -OH libre y asociados Alargamiento de enlaces O-H Oscilacin de grupos metilos terminales Oscilacin de grupos etilenos Alargamiento del grupo carbonilo asociado al ster Vibracin antisimtrica asociada a teres alifticos Alargamiento de los grupos asociados a un ster
Al apreciar la Figura 6, de manera general se evidencia, al incrementarse el tiempo de degradacin, un engrosamiento de la banda entre 3700- 3400 cm:', lo cual es caracterstico a la presencia de grupos hidroxi -OH pertenecientes a cidos carboxlicos y alcoholes, sta banda tambin podra indicar la presencia de hidroperxidos debido a que se ha reportado que estos son relativamente estables a temperaturas moderadas [12]. En esta misma Figura, en la regin alrededor de 3615 crn', atribuible a los grupos O-H libres, se tiene que dicha banda muestra una tendencia a su desaparicin, lo cual puede ser producto del proceso degradativo y de la posible asociacin de estos grupos a los productos resultantes de las rupturas de enlace debido a la degradacin hidroltica, por lo que los O-H libres pueden pasar a formar parte de carbonos terciarios o carbonos asociados. Este argumento es corroborado por el incremento de la banda de absorbancia en 3460 cm:', que de acuerdo a la literatura corresponde a impedimentos del grupo O-H [13]. As mismo, en la Figura 7, la banda ubicada hacia 1240 cm' muestra un comportamiento similar al visto para la banda de 3615 cm", en donde para la muestra virgen se observa la presencia de un pico intenso y agudo, el cual se va debilitando en el tiempo debido a que, como se expres anteriormente, durante el proceso degradativo se promueven interacciones entre cadenas ms fuertes que las iniciales, disminuyendo dicha banda. De acuerdo a la literatura [13], la presencia de una banda hacia 1240 cm' se debe a la disposicin ecuatorial del R-OH en acetatos, ya que, si la configuracin fuese axial se presentaran mltiples bandas en dicha regin. Con relacin a lo expresado, se ha encontrado en la literatura [9], que la desaparicin de esta banda ubicada en 1240 crrr' se debe al
acoplamiento en el plano del grupo O-H enlazado al carbonilo y sus homlogos, pudindose formar estructuras como la mostrada en la Figura 5 anterior, y lo cual se evidencia en la Figura 7. Lo anteriormente expuesto se aprecia adicionalmente por el desdoblamiento que sufre el pico ubicado en 1050 cm:' en dos bandas bien diferenciadas como se muestra en la Figura 8. Como es sabido, la banda que seala el alargamiento del C-O en alcoholes primarios se presenta entre 1064-1030 cm', y la correspondiente a los steres de los alcoholes secundarios se presenta entre 1070-1100 cm': por lo que se podra pensar que la banda de absorbancia a 1050 cm' corresponde a grupos O-H primarios, mientras que la banda ubicada a 1070 cm', es atribuida a O-H secundarios, lo cual parece indicar que se debe a la ruptura al azar de enlaces inducida por la hidrlisis, siendo entonces posible que se origine este tipo de sustitucin secundaria [13]. La disminucin de grupos terminales libres se pudo determinar cuantitativamente mediante la relacin de absorbancias relativas entre los picos en 3615 cm:' correspondientes a O-H libres y 1135 cm', correspondiente al grupo ter (R-O-R'), obtenindose que el valor disminuye con el tiempo de degradacin, debido a la desaparicin de los grupos O-H libres a medida que transcurre el tiempo de hidrlisis (vase Tabla 2). La misma tendencia se obtiene para las muestras hidrolizadas en agua y en la solucin buffer fosfato. Parece posible que durante el proceso de degradacin y de ruptura al azar de enlaces va hidrlisis, se obtengan estructuras intermediarias o complejas, las cuales se forman por la asociacin de grupos (puentes de hidrgeno, etc.).
M. A. Sabino y col. /Revista Latinoamericana de Metalurgia y Materiales
45
A b s o r b a n e i a
3800
3700
3600 N de Onda (cm")
3500
3400
Fig. 6. Espectros FTIR, regin 3800-3400cm', correspondientes a las muestras de PPDX degradadas en una solucin buffer para perodos de (a) O sem, (b) 2 sem, (c) 4 sem, (d) 6 sem, (e) 8 sem y (f) 12 sem.
A b s o r b a n e
i
1300
1250
1200
1150
1100
N de Onda (cm")
Fig. 7. Espectros FTIR, regin 1300-1100cm", correspondientes a las muestras de PPDX degradadas en una solucin buffer para perodos de (a) O sem, (b) 2sem, (e) 4 sem, (d) 6 sem, (e) 8 sem y (f) 12 sem.
A b s
o
r b
i:I
n e i a
[al 1080 1060 1040 1020
ND de Onda (cm")
Fig. 8. Espectros FTIR, regin 1080-1020cm-1, correspondientes a las muestras de PPDX degradadas en una solucin buffer para perodos de (a) O sem, (b) 2 sem, (e) 4 sem, (d) 6 sem, (e) 8 sem y (f) 12 sem.
46
Revista Latinoamericana de Metalurgia y Materiales, Vol. 22, N 2,2002.
Tabla 2. Relacin de absorbancias relativas para los picos registrados en 3615 cm' (O-H libres) y 1100 crn' (R-O-R').
Tiempo de hidrlisis (semanas)
Relacin de Absorbancias (-OH I R-O-R') 0,983 0,964 0,930 0,725 0,684 0,559 0,553
o
2
4
6
8 10 12
Estas estructuras pueden ser evidenciadas por el paso de grupos O-H primarios a posibles grupos O-H secundarios y terciarios atribuidos a la banda hacia 1070 cm' de la Figura 8 anterior; lo cual adicionalmente se pudiese constatar en la Figura 7 anterior, al observar como en la semana 4 y 6 se presenta la formacin de una banda muy ancha alrededor de 1152 cm", atribuida a grupos O-H terciarios y 1110 cm" atribuida a grupos secundarios [13]. En la Figura 9, se puede observar como la banda para la PPDX virgen ubicada hacia 1740 cm:' asignada al grupo carbonilo proveniente del grupo ster, se presenta bien definida y va sufriendo un desdoblamiento hacia 1754 cm' y 1732 cm', durante-el proceso de hidrlisis, presentando el inicio de diferencias ms pronunciadas a partir de la sexta semana, donde el pico a menor nmero de onda y atribuido al carbonilo proveniente de los cidos carboxlicos formados se incrementa. Especficamente, en el espectro de la sexta semana se observa que la poblacin de grupos carbonilos provenientes del cido carboxlico s maxirniza, lo cual parece indicar que el proceso de hidrlisis hasta esta semana corresponde bsicamente a la ruptura va hidrlisis del grupo ster, y que a partir de all la presencia de una mayor concentracin de grupos -COOH podran estar interviniendo como catalizadores en el proceso de degradacin. Esta afirmacin puede ser ms claramente evidenciada en la Figura 10, para las muestras de PPDX degradadas en agua, donde se aprecia igualmente una disminucin de la banda atribuible a los grupos carbonilos provenientes del grupo ster a medida que transcurre el tiempo de hidrlisis, y al mismo tiempo un aumento temprano de la banda de absorcin correspondiente .a los grupos carboxlicos provenientes de la formacin de grupos cidos carboxlicos producto de la reaccin de hidrlisis. Como se ve en la Figura 11 en el espectro correspondiente a la cuarta semana, se observa una diferencia debido a la aparicin de un pico alrededor de 1760-1768 cm' y a un ensanchamiento pronunciado de la banda con la aparicin
de un pequeo lomo hacia 1720-1690 cm' (sealado con una flecha) visto ms claramente a travs de la Deconvolucin por Transformada de Fourier (seal en 1695 cm"), realizada en la zona de inters en el espectro original de la cuarta semana; estos ltimos aspectos, refuerzan la idea de la formacin de posibles estructuras intermedias entre el polmero y los componentes de la solucin buffer (vase Figura 5 anterior), lo cual es atribuido a la posible formacin de estructuras cclicas conjugadas a grupos carbonilos provenientes del grupo ster o de los grupos cidos formados durante el proceso de degradacin, y posiblemente dichas estructuras fomenten interacciones entre las cadenas de menor peso molecular, lo cual parece cobrar importancia debido a la aparicin de las bandas hacia 1152 y 1110 cm'! (vase Figura 7) [14-16]. Finalmente, en las Figuras 12 y 13 se aprecia el desplazamiento de la banda de absorcin ubicada en 2981 cm:', hacia longitudes de onda mayores 2985 cm:', este hecho se atribuye a la formacin de cidos carboxlicos dmeros, evidenciado por el aumento de esta banda a medida que el tiempo de hidrlisis transcurre. As, la posible formacin de estructuras intermediarias mencionadas anterior-mente podra contribuir al pronunciamiento y desplazamiento de dicha banda [17].
A b
o
r b
a n e a
f
e
b a
1820 1800 1780 1760 1740 1720 1700 1680
N de Onda (cm-1) Fig. 9. Espectros de infrarrojo entre 1800 cm' y 1500 cm', correspondientes a las muestras de PPDX degradadas en una solucin buffer para perodos de (a) O sem, (b) 2 sem, (e) 4 sem, (d) 6 se m, (e) 8 sem y (f) 12 sem.
M. A. Sabino y col. /Revista Latinoamericana de Metalurgia y Materiales
47
A
b s o
r
A b s
o d e b
b a
D
r b a n
i
a
Jf
Deconvoludn
e
a
FT
a
18101&101100 11&11110 1181 111114() 1T.lCJ1120 1110 111X11SQD 16&1
a
Y'lCI 1B<1D
1Bla
lID!
118D
111!C1 1740
112D
1100
111BD 111BD 184(J
N de Onda (eDIl)
Fig. 10. Espectros FTIR, regin 1800-1500 cm", correspondientes a las muestras de PPDX degradadas en agua para perodos de degradacin de (a) O sem, (b) 4 sem, (e) 8 sem, y (d) 12 sem.
N de Onda (cnr')
Fig.l1. Espectros FTIR, regin 1640 - 1850 cm', correspondientes a las muestras de PPDX degradadas en agua para perodos de degradacin de (a) Osem; (b) 4 sem. El espectro intermedio es una Deconvolucin FT del espectro (b).
t\ h s
.\
o
if,
iE!'1
b s
Q
h
'11
b
idi
b'l
i"
3100
3050
3000 2950 \0 de Onda (cm .1)
2000
N<'
lIl'
onda
(l'Ill,I)
Fig. 12. Espectros de infrarrojo entre 3100 cm'! y 2850 cm', correspondientes a las muestras de PPDX degradadas en una solucin buffer para perodos de (a) O sem, (b) 2 sem, (c) 4 sem, (d) 6 sem, (e) 8 sem y {f) 12 sem.
Fig. 13. Espectros FTIR, regin 3100-2850 cm" correspondientes a las muestras de PPDX degradadas en agua para perodos de degradacin de (a) O sem, (b) 4 sem, (e) 8 sem y (f) 12 sem.
3.2. Esvectrometra
de Masas
Cuando un compuesto tiene baja volatilidad o cuando su . masa padre no puede determinarse, podra existir la posibilidad de preparar un derivado adecuado. El derivado seleccionado debe proporcionar una volatilidad mejorada, un modo
predecible simplificado
de escisin, un modelo de fragmentacin o la estabilidad incrementada del in padre.
Los compuestos que contienen varios grupos polares, pueden tener una volatilidad bastante baja, por ejemplo, arninocidos, cidos carboxlicos, etc., es por ello que estos compuestos son selecciones evidentes
efectivas
para ser
48
Revista Latinoamericana de [etahirvia -~ tueriales, Vol. 22, N 2, 2002.
tratados qumicamente con el fin de aumentar su volatilidad y que puedan as proporcionar picos caractersticos. Seguramente el uso de los derivados de Trimetilsilil con el fin de enmascarar los grupos OH y -COOH provenientes de la hidrlisis de la PPDX son lo suficientemente voltiles para pasar a travs de las columnas del cromatgrafo de gases (sin quedar atrapadas en las paredes de la misma) y dar seales caractersticas de los productos que se han formado. Es importante considerar que para el caso de los derivatizados, el pico del in molecular [M]+7podra no estar siempre presente, pero el pico [M-15]+ debido a la escisin de uno de los enlaces Si-CH3 siempre resultar notable. La columna de slica utilizada en el experimento presenta una alta capacidad de separar los compuestos polares, debido a la intensidad de los picos determinados por el detector, sin embargo parte de los compuestos no derivatizados pudieron bien ser absorbidos durante la lnea de inyeccin, o bien, por la columna una vez que fueron transferidos a la misma. Es por ello que las alcuotas provenientes de las soluciones donde se realiz la degradacin in vitro de la PPDX fueron debidamente derivatizadas de manera de mejorar la separacin y evitar la retencin de las especies en el sistema GC-MS. El compuesto TBDMSIM fue seleccionado para hacer la derivatizacin debido a que este compuesto puede ser aplicado para todos aquellos compuestos que tienen la capacidad de donar protones (como por ejemplo, cidos decarboxlicos, hidroxi-cidos, etc.) y que el producto obtenido al reaccionar el TBDMSIM con la muestra, es decir, el derivatizado terbutildimetil-silil (TBDMS) tiene una alta estabilidad hidroltica y excelentes propiedades para los anlisis GC-MS [8, 18, 19]. Un pico cromatogrfico simple sin cola, generalmente se obtiene para los derivatizados TBDMS separados en columnas como la utilizada en este tipo de experimento. Como se sealo al principio, una caracterstica de los derivatizados es que no presentan iones moleculares y que el in [M-15]+ se debe a la perdida del grupo terbutil, el cual es, sin embargo, muy intenso, y entonces permite la fcil identificacin de los grupos cidos. Asimismo, el in con rn/z=73 (siendo rn/z la relacin masa/carga del in) correspondiente al grupo _(CH3)3Si+es de una alta intensidad, y tambin proviene del derivatizado, Otros iones prominentes que sern apreciados a valores rn/z 75, 115, 147 Y 189 corresponden a los grupos: (a) (b) (e) (d) HO+=Si(C~)2 [(C~\C](C~)2Si+ (C~)3SiO+=Si(C~)2 [(C~\C](C~)2SiO+=Si(C~)2
retencin para los productos de la degradacin de la PPDX hidrolizada en la solucin buffer fosfato, vemos que los picos intensos alrededor de 13 y 16 min., corresponden a las especies que se forman a partir de los iones provenientes del derivatizante y de los grupos fosfatos, como por ejemplo: Silanol, trimetil-fosfato; como se aprecia en la Figura 14. Es importante destacar que las muestras de PPDX en forma de discos sometidas a la degradacin hidroltica en la solucin buffer, fueron preparadas de esa manera con el fin de garantizar el mayor porcentaje de fase amorfa y que la degradacin ocurriera casi en su totalidad, a pesar de ello la intensidad de los picos para las primeras semanas de degradacin no permitieron obtener cromatogramas con buena resolucin, sino hasta la semana 16 donde se presentaron especies de bajo peso molecular detectables por el equipo. El proceso de degradacin a tiempos prolongados permite una mejor definicin de los grupos cidos que se van formando, y es por ello que en esta Figura 14, se puede apreciar que despus de la semana 16, la intensidad de los picos alrededor de 6, 23 Y 39 minutos de retencin son pronunciados. Como se seal anteriormente, los picos observados a 13.5 y 15.8 minutos corresponden a las especies que se forman a partir de los iones provenientes del derivatizante.
15.84
11 U N D
A
-13:90 ! 38.95
N I ,\
rr-~~
5.95
23.60
I .. -
..
10 20 30 40
50
tiempo
Fig. 14. Cromatogramas GC- MS para los productos de degradacin de la PPDX derivatizados en funcin del tiempo de hidrlisis, luego de 16 semanas del proceso degradativo.
formados respectivamente. Asimismo, si observamos el cromatograma general GC- MS en funcin de los tiempos de
En la Figura 15, se presenta el esquema de la reaccin de formacin de la principal especie hidroxi-cida que resulta de la hidrlisis de la PPDX, y que de acuerdo a los resultados obtenidos en el cromatograma de la Figura 14 anterior, corresponde al pico ubicado a los 38.928 minutos de retencin en el GC-MS, y cuyo espectro de masas se mostrar ms adelante en la Figura 16.
M. A. Sabina y col. /Revista Latinoamericana de Metalurgia y Materiales
49
r _ J HOlO&O~OyO[H---"
n
Hidrlisis
O~O~H
PPDX
cido-2-hidroxi-etoxi-etanoico
- _ 15. Reaccin de ataque hidroltico que sufre la PPDX sometida a un proceso de degradacin y principal producto resultante de la hidrlisis.
7]
8000
6000
147
4000
]32-
2000
117 45 1]] 205 44~
O O
50
100
150
200
250
300
350
400
450
500
mh
Fig. 16. Espectro de masas para el compuesto derivatizado TBDMS (con t(eluSin) de 38.928 min), el cual es producto de la degradacin bidroltica de la PPDX despus de 16 semanas de hidrlisis en una solucin buffer fosfato a 37C. Compuesto: cido 2-hidroxi-etoxi-etanoico. 2000
73 73
1750 ]000 1500
1250
750
1000 500 750
45 59
IDI
500 250 250
OL....l.---L...&.....LJ.ULJ.JL.I.....t.J.LLL....LL.I
45
.59
o~~~~~~~~.w~~~~~~~~
70 80 90 JOO JJO J21 20 30 40 50 60 70 80 90 100 Jl O 120
20
30
40
50
60
mlz
Fig. 17. Espectro de masas del compuesto con t(retencin): 26.983 mino
m/z
Fig. 18. Espectro de masas del compuesto con t(retencin) : 5.850 mino
50
Revista Latinoamericana de Metalurgia y Materiales, Vol. 22, N 2, 2002.
Haciendo un seguimiento, al pico alrededor de los 39 min., al aumentar el tiempo de degradacin se incrementa la concentracin del cido formado en el medio dehidrlisis y por lo tanto la intensidad de la banda. Asimismo, se identificaron otros picos, los cuales se corresponden a otros grupos cidos que tambin se forman a partir del progreso de la degradacin de los productos inicialmente formados, lo cual conduce a la posterior obtencin de especies de ms bajo peso molecular. Entonces, el espectro de masas del principal compuesto derivado de la degradacin hidroltica de laPPDX se mostr en la Figura 16 anterior, y los espectros de masa de los diferentes compuestos y su correspondiente asignacin mlz e intensidad, pueden ser vistos en las Figuras 17 y 18. La abundancia relativa de estos compuestos y los iones provenientes de las fragmentaciones sufridas (mlz), se resumen en la Tabla 3.
Un esquema de las posibles fragmentaciones que podra sufrir la molcula de la PPDX, se presenta esquemticamente en la Figura 19, Yall mismo se muestran los fragmentos mlz que resultaran de dicha fragmentacin y que aparecen en los espectros de masa sealados en las Figuras 16-18. Es importante destacar, que la Figura 16, muestra claramente que los fragmentos originados a partir de la degradacin hidroltica de la PPDX conduce mayormente a la formacin del cido-2 hidroxi- etoxi-etanoico, y que ste compuesto al seguirse degradando va hidrlisis, induce a la generacin de especies de muy bajo peso molecular entre las que se encuentra el monmero, como 10 manifiesta la Figura 18, donde losfragmentosparecen corresponder a la fragmentacin del compuesto dioxano.
Fragmento
(mlz) 1)(119,103)
2 ~ 4 6 1
2) (205, 17)
+
n
4. Conclusiones Los biomateriales polimricos presentan una serie de ventajas (sobre otros materiales como los metales o las biocermicas) que suponen la fabricacin de dispositivos y aparatos ortopdicos que sustituyan parcial o totalmente a los miembros del aparato locomotor o simplemente permitan servir de sostn en la reparacin de fracturas seas. En este sentido, la posibilidad de que el polmero sea degradado, ofrece la oportunidad de que pueda conseguirse un proceso de curacin ptimo, con la recuperacin de la funcionalidad del sistema fisiolgico y por ende del tejido afectado, mientras el polmero se degrada mediante un mecanismo puramente hidroltico, el cual da lugar a la fragmentacin del polmero en cadenas macromoleculares (debido a que el polmero posee un enlace hidrolticaraente inestable), originando productos de degradacin de bajo peso molecular, atxicos y que pueden ser metabolizados o bioabsorbidos por el organismo. A travs de FTIR, se demostr que durante el perodo de
3) (191,31) 4)(177,45) 5) (161,61) 6)(133,89) 7) (147,75) 8) (163,59)
9) = 2) (205,17) Fig. 19. Diagrama de las posibles fragmentaciones que puede sufrir la PPDX o un oligmero producto de la degradacin hidroltica del polmero. degradacin se evidencia la disminucin de grupos Q-H libres, producto de la posible asociacin de estos grupos a los productos resultantes de las rupturas de enlaces; y la posible formacin de estructuras intermediarias o complejas, mediante asociacin de grupos, donde pueden intervenir los grupos fosfatos presentes en el medio de hidrlisis. Adems, como consecuencia de los rompimientos del grupo ster presente en la estructura de la PPDX, se observan variaciones de absorbancia de las bandas asociadas a los grupos carbonilos dada la aparicin del grupo cido carboxlico. Estas evidencias fueron verificadas mediante Espectrometra de Masas donde se determin que uno de los subprouctos de la degradacin de la PPDX corresponde al cido 2-hidroxi-etoxi- etanoico. A travs de.FTIR,se. demostr que durante el perodo de degradacin se evidencia la disminucin de grupos Q-H libres, producto de la posible asociacin de estos grupos a los productos resultantes de las rupturas de enlaces; y la
M. A. Sabina y col. /Revista Latinoamericana de Metalurgia y Materiales
51
Tabla 3. Tiempos de retencin e iones.prominentes obtenidos de los espectros de masa de los derivatizados (Figuras 16, 17 Y 18) de la hidrlisis de la PPDX. Tempo de..
m/z
retencion (min) 45 5g 73 89
103
Intensidad relativa (%)
13 4
cadena, las terminaciones de cadena libres, y las cadenas plegadas son degradadas en fragmentos; por lo que a medida que la degradacin procede, el peso molecular disminuye, y sufre una cada considerable una vez que la mayor cantidad de zona amorfa ha sido degradada hidrolticamente y se ha dado comienzo al ataque a las zonas cristalinas.
100
2 5
Referencias
P. Craig, J.A. Williams, K.W.Davis, A.D. Magoun.,Surgery. Gynecology & Obstetrics, 141, (1975) 1 2. P. Tormala, J. Vasenius, S. Vainionpaa, J. Laiho, T. Pohjonen, P. Rokkanen, J. Biomedical Material Research, 21, (1991) 1 3. J. Schitz, J.O. Hollinger, Clinic. Orthopedics & Related Research,237,(1988)245 4. J.A. Ray, N. Doddi, D. Regula, J.A. Wiliams, A. Melveger, Surgery Gynecology Obstetrics, 153, (1981) 497 5. J. San Roman, Rev. Plst. Mod., 413, (1990) 689. 6. W. Jencks, Catalysis in Chemistry and Enzymology, Me Graw-Hill, Inc, New York (1969) 45 7. T. Iwata, Y. Doi, F. Kokubu, Sh. Teramachi, Macromolecules, 32, (1999) 8325. 8. 1.Rehman, E. Andrews, R. Smith, J. of Materials Science, 7,(1996) 17 9. L. Lu, C. Garcia, A.G. Mikos, J. Biomed. Mat. Res., 46, (1999)236 10. C.e. Chu, N.D. Campbell, J. of Biomedical Materials Research, 16, (1982) 417 11. G. Farrow, D. Ravens, Polymer, 3, (1962) 17 12. B.J. PoI, P. Wachem, L. Van der Does, A. Bantjes, J. Biomed. Mat. Res., 32, (1996) 321 13. K. Nakanissi, H.S. Fhilippa, Infrared absorption spectroscopy, Holden-Day, 2da. Edition, San Francisco, (1977) 17 14. G. Grimandi, P. Weiss, F. Millot, N. Passuti, J. Biomed. Mater. Res., 39, (1998) 660 15. P. Weiss, M. Lapkowski, R. Legeros, J. Bouler, J. Mater. Sci. Mater Med., 10, (1997) 621 16. G. Meijs, S. McCarthy, E. Rizzardo, Y. Chen, J. Biomed. Mat. Res. 27 ,(1993) 345 17. U. Edlmund, A.C.Albertsson, J. Polym. Sci. A. Polym Chem., 37, (1999) 1877 18. E. King, S. Robinson, R. Cameron, Polym. Int., 48, (1995) 915 19. X. Qu, A. Wirsen, A.e. Albertsson, J. Appl. Polym. Sci., 74, (1999) 3186 20. M.A. Sabino, J.L. Feijoo, AJ. Mller, Macromol. Chem. Phys.,201 (2000) 2687 21. M.A. Sabino, S. Gonzalez, L. Mrquez, J.L. Feijoo;Polym. Deg. & Stab., 69, (2000)-209 22. M.A. Sabino, J.L. Feijoo, A.J. Mller, Polym. Deg. & Stab., 73, (2001) 541 23. M.A. Sabino, G. Ronca, L. Sabater, A.J. Mller, Polym. Bulletin, 48, (2002) 291 1.
117
133 147
20
11
44
1 2 1 14 3 1 3 2 39 3
38.928
157 169 189 205 215 243
259 304 332
345 359 374 405
449
3 2
1 2 36 4 30
45 52
26.983 59 67
73
87
3 100 5
28
101 45 50
5.850 59-' 66
51
10
16
7
73 88 93 102
100
8 7
posible formacin de estructuras intermediarias o complejas, mediante asociacin de grupos, donde pueden intervenir los grupos fosfatos presentes en el medio de hidrlisis. Adems, como consecuencia de los rompimientos del grupo ster presente en la estructura de la PPDX, se observan variaciones de absorbancia de las bandas asociadas a los grupos carbonilos dada la aparicin del grupo cido carboxlico. Estas evidencias fueron verificadas mediante Espectrometra de Masas donde se determin que uno de los subproductos de la degradacin de la PPDX corresponde al cido 2-hidroxi-etoxi- etanoico. Adicionalmente, se ha reportado en publicaciones anteriores [20-23], que el peso molecular viscosimtrieo decrece linealmente en funcin del tiempo de hidrlisis, debido a que la degradacin hidroltica comienza en las regiones amorfas, en donde los segmentos de enlaces de
También podría gustarte
- Exel Practico 2019Documento4 páginasExel Practico 2019Rene Ccolque HuillcaAún no hay calificaciones
- Coaching y Liderazgo - Modulo IDocumento2 páginasCoaching y Liderazgo - Modulo IRene Ccolque HuillcaAún no hay calificaciones
- Solver EjercicioDocumento4 páginasSolver EjercicioRene Ccolque HuillcaAún no hay calificaciones
- Solver EjercicioDocumento4 páginasSolver EjercicioRene Ccolque HuillcaAún no hay calificaciones
- 5.nuevas Quimicas y Sus AplicacionesDocumento44 páginas5.nuevas Quimicas y Sus AplicacionesRene Ccolque HuillcaAún no hay calificaciones
- Diseño de Árboles y EjesDocumento13 páginasDiseño de Árboles y EjesJose Ulises Cabrera Martinez100% (1)
- Cap 08Documento20 páginasCap 08Nicolas FernandoAún no hay calificaciones
- Espiritu SantoDocumento2 páginasEspiritu Santolaprofedereli100% (28)
- Cuestionario de Repaso - 2da. Evaluación Parcial - EVA - Art - III - 2020 - 2Documento10 páginasCuestionario de Repaso - 2da. Evaluación Parcial - EVA - Art - III - 2020 - 2Katherine De La Cruz NuñezAún no hay calificaciones
- Arquitectura NacionalistaDocumento18 páginasArquitectura NacionalistaErika Lira RangelAún no hay calificaciones
- Unidad 1. Corpus Teórico-Crítico. 2021. AbrilDocumento164 páginasUnidad 1. Corpus Teórico-Crítico. 2021. AbrilEl pepeAún no hay calificaciones
- S Principios Quimicos 780Documento28 páginasS Principios Quimicos 780Peter Johan Jaime HernándezAún no hay calificaciones
- Rivera La Revolución Es Un Sueño EternoDocumento19 páginasRivera La Revolución Es Un Sueño EternoAndrea PortugalAún no hay calificaciones
- Femme FataleDocumento2 páginasFemme FataleAjelet Sahar Cabrera RuizAún no hay calificaciones
- Algunas Glándulas Endocrinas y Sus HormonasDocumento5 páginasAlgunas Glándulas Endocrinas y Sus HormonasAlessandra18960% (1)
- ABC Campus Virtual ESI Tutorial Capacitandos Subir Archivo 4Documento7 páginasABC Campus Virtual ESI Tutorial Capacitandos Subir Archivo 4Luis ChimentiAún no hay calificaciones
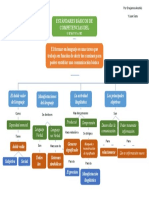
- Mapa Conceptual CompetenciasDocumento1 páginaMapa Conceptual CompetenciasSofi SotoAún no hay calificaciones
- Informe - Huachipa - Mecánica de SuelosDocumento99 páginasInforme - Huachipa - Mecánica de SuelosIrwin Cubas LlatasAún no hay calificaciones
- Kathy Charmaz - La Pérdida Del YoDocumento24 páginasKathy Charmaz - La Pérdida Del YoJimena MunicoyAún no hay calificaciones
- Abdomen Agudo HemorrágicoDocumento11 páginasAbdomen Agudo HemorrágicoValentina RicoAún no hay calificaciones
- Literaturagauchesca 131218131300 Phpapp02 PDFDocumento9 páginasLiteraturagauchesca 131218131300 Phpapp02 PDFMelisa BenelliAún no hay calificaciones
- Móvil: Línea: 620615714Documento1 páginaMóvil: Línea: 620615714Seth Rollings GeorgeAún no hay calificaciones
- Tecnicas de Atencion Al ClienteDocumento6 páginasTecnicas de Atencion Al ClienteBELKI ARELY SOSA RIVASAún no hay calificaciones
- WHR Elfos OscurosDocumento71 páginasWHR Elfos OscurosCristianAún no hay calificaciones
- 2 Sistemas de Propulsion de Cohetes PDFDocumento73 páginas2 Sistemas de Propulsion de Cohetes PDFTiare AntunezAún no hay calificaciones
- Tipologia de CuencasDocumento49 páginasTipologia de CuencasEstefany M CHAún no hay calificaciones
- Luis Ricaurte LOOKUMIDocumento31 páginasLuis Ricaurte LOOKUMILuis RicaurteAún no hay calificaciones
- Texto Gestión Logística PDFDocumento191 páginasTexto Gestión Logística PDFKevin Vazques OlazabalAún no hay calificaciones
- PR BK Taster With Cover Page v2Documento69 páginasPR BK Taster With Cover Page v2Marlon Ivanok Franco carpioAún no hay calificaciones
- Formato de Ficha TecnicaDocumento5 páginasFormato de Ficha TecnicacyberdeyAún no hay calificaciones
- TP 4Documento2 páginasTP 4martinbanfiAún no hay calificaciones
- Planeacion Docente U2 - AnálisisDocumento12 páginasPlaneacion Docente U2 - AnálisisOzkar GdoAún no hay calificaciones
- Manual de Normativas de DibujoDocumento8 páginasManual de Normativas de Dibujoivan chavezAún no hay calificaciones
- Proyecto de Asocie Peru 06-12Documento142 páginasProyecto de Asocie Peru 06-12tiaret yasminAún no hay calificaciones
- Nota GovernatoriDocumento2 páginasNota GovernatoriMartín MengarelliAún no hay calificaciones