Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Equipo y Materiales de Parasitología
Equipo y Materiales de Parasitología
Cargado por
Alicia MoralesTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Equipo y Materiales de Parasitología
Equipo y Materiales de Parasitología
Cargado por
Alicia MoralesCopyright:
Formatos disponibles
EQUIPO Y MATERIALES DE PARASITOLOGA.
FACILIDADES ADECUADAS E EN EL LABORATORIO. EQUIPO DE MICROSCOPIA. DEBE HABER UN BUEN MICROSCOPIO BINOCULAR PARA CADA PERSONA QUE HACE EL DIAGNOSTICOS PARASITLOGICOS. ESTE DEBE ESTAR EQUIPADO CON UN OBJETIVO SECO DEBIL, UNO SECO FUERTE Y OTRO DE INMERSION EN EXCELENTE CONDICION, CON OCULARES X Y 10X , CON PLATINA MECANICA Y CONDENSADOR POR DEBVAJ DE LA MISMA. PARA CADA MICROSCOPIO DEBE HABER UNA BUENA LAM PARA ELECTRICA CON FILTRO LUZ DE DIA. EL EQUIPO MACROSCOPICO ADICIONAL DEBE INCLUIR UN MICROMETRO OCULAR U UN MICROMETRO OBJETIVO PARA CALIBRAR CUALQUIER MICROSCOPIO EN PARTICULAR CON LOS OBJETIVOS Y OCULARES QUE SE EMPLEAN.
OTRO MATERIAL. DEBE HABER AL MENOS UNA INCUBADORA SEGURA, UNA
ESTUFA DE SECAR Y UNA O MAS CENTRIFUGADDORAS CLINICAS INTERNATIONAL. TAMBIEN SE REQUIEREN UN ESTERILIZADOR DE VAPOR Y UN MICROTOMO DE PRESION PARA CORTES SERIADOS.
VIDIRERIA. FRASCOS PARA REACTIVOS, CAJAS DE PETRI, VASOS DE
PRECIPITADO TIP PYREX, MATRACES, EMBUDOS Y PIPETAS DE DISTINTOS TAMAOS, TUBOS, PROBETAS GRADUADAS, PORTA OBJETOS Y CUBREOBJETOS ABUNDANTES. LOS PORTAOBJETOS DEBEN SER DE VIDRIO DURO Y TRANSPARENTE, NO EMPAABLES, CON BORDES ROMOS. EL GROSOR NUMERO 2 SE ACONSEJA PARA EXAMEN DE HACES FRESCAS, PUESTO QUE SE ROMPE MENOS FACILMENTE QUE EL NUMERO 1, EL CUAL SE EMPLEA PARA PREPARACINES PERMANENTES DE FROTISY CORTES TEIDOS. TUBOS DE PRUEBAS, PREFERENTEMENTE DE PYREX, SON TUBO DE WASSERMANN (12X100 MM) PARA LA CONCENTRACION DE PARASITOS PRESENTES EN LAS HECES, 14 X 150MM Y 25 X 200 MM PARA EL CULTIVO DE PROTOZOARIOS, Y PEQUEOS TUBOS SEROLOGICOS PARA PRUEBAS INMUNOLOGICAS. SE REQUIEREN CAJAS DE TINCION PARA PREPARACIONES TEIDAS DE FROTIS DE MATERIAS FECALES. FROTIS SANGUINEOS, PARASITOS EN PRODUCTOS DE SONDEO O EN CULTIVOS PARA CORTES DE TEJIDOS. DEBE HABER DOS OTRES JUEGOS DE 10 A 12 CAJAS, HABRA ASIMISMO CAJAS DE KOPLI MAS PEQUEAS PARA TENIR PREPARACIONES EN CUBREOBJETOS.
RECIPIENTES PARA MUESTRAS. UN RECIPIENTE ADECUADO PARA
MUESTRAS ES UN FRASCO DE VIDRIO DE 2 ONZAS (56,7 ML) CON TAPO DE ROSCA DE ALUMINIO O PLASTICO, QUE PUEDE USARSE PARA MUESTRAS DE HECES, ORINA O ESPUTO. CUANDO SE TRATA DE ESPECMENES DE GRAN TAMAO O TEJIDOS GRUESOS SON MAS ADECUADOS LOS FRASCOS RECTANGULARES O REDONDOS DE MUSEO.
OTROS MATERIALES. APLICADOES Y ABATELENGUAS DE MADERA, GASA O
GUATA QUIRURGICAS, INSTRUMENTOS DE DISECCIN Y AUTOPSIA Y MUCHOS OTROS MATERIALES MENORES SON NECESARIOS PARA EFECTUAR ADECUADAMENTE EXAMENES PARASITOLOGICOS. PARA PREPARACIONE DE FROTIS DE MATERIAS FECALES FRESCAS DE RUTINO CADA OPERADOR REQUIERE FRASCOS CUENTAGOTAS DE SOLUCION SALINA FISIOLOGICA Y YODO COLOCADOS EN LUGAR ADECUADO (YODO SATURADO FILTRADO EN YODURO DE POTASIO AL 1%) PARA TECNICAS DE CONCENTRACION DEBE HABER A MANO GRASCOS GRANDES DE SOLUCION DE SULFATO DE ZINC (SP.GR. 1.180) FORMOL Y SOLUCION SALINA SATURADA. PARA TEIR FROTIS FECALES, LA TECNICA MAS SATISFACTORIA ES LA DE LA HEMATOXILINA FERRICA; PERO HAY ADEMAS OTRAS TECNICAS EXCELENTES PARA LA FIJACION Y TINCION DE LAS HECES TANTO EN MASA COMO EN EXTENSIONES SOBRE PORTAOBJETOS. EL LABORATORIO DEBE TENER SUFICIENTES PROVISION DE ALCOHOL ETILICO, ALCOHOL ETILICO ABSOLUTO, XILOL, ETER, GLICEROL, MEDIO NEUTRO DE MONTAJE PARA PREPARACIONES MICROSCOPIAS PERMANENTES, AGUA DESTILADA Y MUCHOS OTROS REACTIVOS QUE SON UTILIZADOS EN LOS PROCEDIMEINTOS DIAGNOSTICOS HABITUALES U OCASIONALES.
EXAMEN COPROPARASITOSCOPICO. TOMA
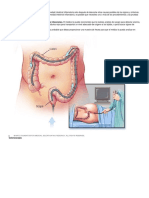
UNA EACUACION NORMAL CONSTA CASI EXLUSIVAMENTE DE HECES, PERO CUANDO EL INTESTINO ESTA ENFERMO SE PUEDE ENCONTRAR TAMBIEN MOCO, SANGRE Y CANTIDADES CONSIDERABLES DE TEJIDOS DESPRENDIDOS., ASIMISMO, PUEDE SER EXPULSAOS ASCARIS, ENTEROBIUS Y PROGLOTIDES DE TAENIA Y DIPYLIDIUM SIN LA PRESENCIA DE HUEVOS EN LA PORCION FECAL DE MUESTRAS. EL EXAMENTE MACROSCOPICO DE LA MUESTRA DEBE PRECEDER SIEMPRE AL ESTUDIO MICROSCOPICO. LA RECOGIDA SE HARA EN UN RECIPIENTE LIMIO, SIN
DE
MUESTRAS.
COMBINACIONES CON LA ORINA DEL PACIENTE U OBJETOS EXTRINSECOS MICROSCOPICOS DE LA MUESTRA DEBE PRECEDER SIEMPRE AL ESTUDIO MICROSCOPICO. LA RECOGIDA SE HARA EN UN RECIPIENTE LIMPIO, SIN COMBINACIONES CON LA ORINA DEL PACIENTE U BOJETOS EXTRINSECOS MICROSCOPICOS. LA MUESTRA DEBE ESTAR LIBRE DE GOTAS DE ACEITE, MAGNESIO, SALES DE ALUMINIO EN POLVO, BARIO O BISMUTO. LAS HECES FORMADAS, SIN SEAS DE GRAN PUTREFACCIN, PUEDEN A VECES DEJARSE DURANTE LA NOCHE A LA TEMPERATURA DEL LABORATORIO, SIN QUE SE PIENDAN LAS CARACTERISTICAS DIGNOSTICAS DE LOS PARASITOS QUE PUEDA HABER EN ELLAS, SIN EMBARGO ES PREFERIBLE GUARDARLAS EN EL REFRIGERADOR.
PROCESO DE LA MUESTRA PARA SU EXAMEN. ANTES DE HACER EL
FROTIS DE LAS MATERIAS FECALES DEBEN EXAMINARSE MACDROSCOPICAMENTE LEESPECIMEN Y ELEMENTOS (HECES, MOCO, SANGRE, ELEMENTOS DE TEJIDOS Y ALIMENTOS NO DIGERIDOS) Y PARA BUSCAR PARASITOS MACROSCOPICOS TALES COMO GUSANOS REDONDOS Y ROGLOTIDES DE CESTODOS, ETC.. SEPARADOS APROXIMADAEMTNE POR 1MM, Y SE ESPARCEN 1 2 MG DE MATERIAL EN UNA O DOS GOTAS DE SOLUCION SALINA ISOTONICA EN EL LADO IZQUIERDO Y EL OTRO TANTO EN LA SOLUCIN DE YODO, Y FILTRADA DE YODO EN KI AL 1%; NO EN LE LUGOL, QU ES DEMASIADO FUETE PARA LOS ELEMENTOS PARASITOARIOS, EN EL LADO DERECHO. LAS PREPARACINES NO TEIDAS SON DE ESPECIAOL VALOR PARA EL ESTUDIO DE PARASITOS VIVOS, COMO TROFOZIITOS DE PROTOZOARIOS MOVILE, HUEVOS DE HELMINTOS Y LARVAR DE NEMATODOS. EL FROTIS DE YODO SE EMPLEA PRINCIPALEMTNE PARA ESTUDIR LAS CARACTERISTICAS DIAGNOSTICADA DE QUISTES DE PROTOZOARIOS. FORTIS GRUESO DE KATO FUE DESARROLLADA EN EL JAPOR POR KATO Y MIURA (1954) ES ADECUADA PARA EXAMEN DE HECES EN GRAN ESCALA PARA TODO TIPO DE HUEVOS. EL UNICO MATERIAL ESPECIAL QUE SE REQUIERE ES CELOFAN HUMEDECIBLE DE MEDOIANO ESPESOR, CORTADO EN TIRAS DE 22 X 30 MM Y MANTENIDAS DURANTE 24 HORAS O MAS EN UNA MEZCLA DE 100 PARTES DE GLICEROL, 100 PARTES DE AGUA U UNA PARTE DE SOLUCION ACUOSA DE VERDE MALAQUITA AL 3%. EL PROCEDIMIENTO ES EL SIGUIENTE. SE ONEN DE 50 A 60 MG DE
MATERIALS FECHAS (4MM3) EN UN PORTAOBJETOS LIMPIO, SE CUBRE CON UNA TIRA DE CELOFAN, SE COLOCA HACIA ABAJO SOBRE UNA TOALLA DE PALEL, SE PREIONA PARA EXTENDER LAS HECESEN FORMA HOMOGENEA HASTA EL MARGEN O MAS ALLA, SE VUELVE EL PORTAOBJETOS Y SE DEJA SECAR A TEMPERARURA AMBIENTE DURANTE UNA HORA O EN INCUBADORA APROXIMADAMENTE A 40. C DURANTE 20 30 MINUTOS Y LUEGO SE EXAMINA AL MICROSCOPIO, PARA IDENTIFICAR LOS HUEVOS, SI ES NECESARIO SE PUEDE USAR MAYOR AUMENTO, A MEDIDA QUE SE SECA EL FROTIS SE VAN ACLARANDO LOS HECES MAS RAPIDAMENTE QUE LO HUEVOS, PERO ESTOS TAMBIEN SE ACLARAN.
FROTIS TEIDO CON PRESEVATIVO. LA MUESTRA DE HECES HA SIDO
PRESERVADA POR LA TECNICA MIF, SE TOMAN CON PIPETSA UNA O DOS GOTAS DE LA SUSPENSIUON BIEN AGITADA Y SE COLOCA EN UN PORTAOBJETOS LIMPIO, SE PONE AL MICROSCOPIO. CON EL METODO PVA LOS PREPARACION SUELE FIJARSE EN EL PORTAOBJETOS AL TIEMPO DESER OBTENIDA Y TRATA Y TIE PARAEL EXAMEN CUANDO CONVENGA. LSO FROTIS TEIDOS PERMANTENTES PARA EL ESTUDIO DE PROTOZOARIOS INTESTINALES SE PREPARAN HACIENDO UN FROTIS DE UNA PORSION REPRESENTATIVA DE LAS HACES EN UN PORTAOBJETOS ABSOLUTAMENTEL IMPIO Y SE TRATAN CON UN LIQUIDO FIJADOR ANTES DE QUE EL FROTIS SE SEQUE POR EJEMPLO, LA SOLUCION SE SCHAUDINN. 1.- LAS TECNICAS SIGUIENTES. DE TINCION EMPLEADAS COMUNENTE SON LAS
2.- HEMATOXILINA FERRICA DE FAUST. 3.- FIJADOR PVA 4.- CLORACION TRICOMICA 5.- MIF A) FROTIS DIRECTO B) TOMA Y PREVENCION DE MUESTRAS. 6.- LIQUIDO FIJADOR DE TURDYEV.
TECNICAS DE CONCENTRACION. LA RAZON DE SU CONCENTRACION A
PARTIR DE LAS MATERIAS FECALES ES SEPARARLOS DE LA MASA DE AMTERIAL DE LA MUESTRA FORMADA POR BASTERIAS, ALIMENTO NO DIGERIDO, ETC. I.- SEDIMENTAICON. SE LLEA A ACABO SUSPENDIENDO LAS HACES EN AGUA CORRIENTE Y DEJANDO QUE SE VERIFICQUE UN ASENTAMIENTO NATURAL, O BIEN SE PUEDE ACELERAR EL PROCESO MECANICAMENTE POR MEDIO DE CENTRIFIGACION. ESTA TECNICA ES PRINCIPALEMTNE UTIL PARA EL CONCENTRACIN DE QUISTES DE PROTOZOARIOS Y HUEVOS DE HELMINTOS, PERO, SUSTITUYENDO LA SOLUCION SALINA FISIOLOGICA POR EL AGUA, SE PUEDE CONCENTRAR TROZOITOS DE AMEGASP OR MEDIO DE CENTRIFUGACION CONSERVANDO SU DIABILIDAD. II.- FLOTACION. AL CONTRARIO QUE EN LA SEIMENTACION, EN LA CUAL OSPARASITOS IMICROSCOPICOS, QUE SON MAS PESADOS QUE LAS BACTERIAS, Y LAS PARTICULAS DE ALIMENTOS NO DIGERIDAS VAN AL FONDO DEL RECIPIENTE, LA FLOTACION UTILIZA UN MEDIO LIQUIDO DE SUSPENCION MAS PESADO QUE LOS PARASITOS Y ESTOS SUBEN A LA SUPERFICIE Y PUEDEN SER RECOGIDOS DE LAPELICULA SUPERFICIAL. III.- FLOTACION CENTRIFUGACION. ESTE METODO COMBINA LOS PRINCIPIOS DE LA GRAVITACION Y DE LA FLOTACION. SE SUSPENDE UNA MUESTRA FECAL EN APROXIMADAMENTE 10 VECES SU VOLUMEN AGUA, SE FILTRA POR GASAS PARA QUITAR LAS PARTICULAS MAS GRANDES, SE COLOCA EN UN TUBO DE CENTRIFUGACION Y POR MEDIO DE 2 3 CENTRIFUGACINES SUCESIVAS, DECANTACIONES DEL SOBRENADANTE Y RESUSPENSIONES DE ELIMINAN LAS PARTICULAS FINAS. DESPUES DE LA ULTIMA CENTRIFUGACION SE DECANTA TODO EL SOBRENADANTE, SE VUELVE A SUSPENDER EL DEDIMENTO EN LE MEDIO FLOTANTE, SE CENTRIFUGA Y DESPUDE DE DEJAR REPOSAR EL TUBO DE CENTRIFUGACION DURANTE 5 MINUTOS APROXIMADAMENTE SE RETIRA LA P0ELCIULA SUPERFICIAL CON UN ASA BACTERIOLOGICA O ADHIRIENDOLA A UN PORTAOBJETOS. ESTA TECNICA PRODUCE ALTAS CONCENTRACIONES DE PARACITOS PRACTICAMENTE LIBRE DE DETRITOS. LA MAYOR O MENOR FACILIDAD CON QUE RECONOCEN LOS PARASITOS DEPENDEN DEL MEDIO DE FLOTACION EMPLEADO Y DE LA ESPECIE DE PARASITOS DE QUE SE TRATE. TECNICAS CUANTITATIVAS PARA HUEVOS. LAS DIVERSAS TECNICAS ARRIBA DESCRITAS DAN OPORTUNIDAD PARA LA RECUPERACION EFICAZ E IDENTIFICACION PRECISA DE LA MAYORIA DE LOS ELEMENTOS PARASITARIOS EN LAS HECES, AUNQUE NO DEJA DE RECONOCERSE LA NECESIDA DE TCNICAS
QUE PERMITAN CUALCULAR EL GRADO DE PARA SITACIN DEL PACIENTE, SE HAN DESARROLLADO METODOS PARA EL CALCULO RELATIVAMENTE PRECISO DEL GRADO DE PASASITACION DE UNCINARIAS, ASCARIS Y, EN MENOR GRADO TRICHURIS. POR MEDIO DEL RECUENTO DE HUEVOS PRESENTES EN LAS HECES.
CULTIVO DE UNCINARIAS.
HECES
PARA
DIGNOSTICO
DE
LARVAS
DE
LOS HUEVOS DE UNCINARIAS Y LOS HUEVOS QUE SE ASEMJAN A ELLOS ON A MENUDO DIFICILES O INCLUSO IMPOSIBLE DE IDENTIFICAR, MIENTRAS QUE LAS LARVAS DEL ESTUDIO INFECTANTE QUE SE DESARROLLAN DEL HUEVO SON MAS FACILMENTE RECONOCIBLES. UN PROBLEMA COMUNES LA DIFERENCIA ENTRE LAS INFECCIONES POR NECATIS Y ANCYLOSTOMA, UN METODO SENCILLO EN EL TUBO DE ENSAYO USANDO MATERIALES FACILMENTE OBTENINBLES FUE IDEADO POR HARANDA Y NORI (1955) Y MODIFICADO POR OTROS INVESTIGADORES., HA SIDO COMPROBADA. LOS CULTIVOS EN TUBO SE HACEN EXTENDIENDO UN FROTIS DELGADO 1 A 2MM DE HECES EN EL TERCIO MEDIO UN SOLO LADO UNA TIRA DE PAPEL FILTRO DE 13 X 120MM LA CUAL SE INTRODUCE EN UN TUBO DECENTRIFUGACION DE EXTREMO CONICO QUE CONTENGA APROXIMADAMENTE 3 MLDE AGUA DESTILADA HASTA 1 CM DEL FONDO, CON EL LADO LIMPIO ADHERIUDO AL TUBO. EL CULTIVOSEGUARDA A TEMPERATURA AMBIENTE EN LA OBSCURIDAD SE AADE DURANTE 7 A 10 DIAS, Y DIARIAMENTE SE AADE AGUA PARA MANTENER EL NIVEL POR ENCIMA DEL EXTREMO INFERIOR DEL PAPEL. EL FLUJO CAPILAR DEAUGA HACIA ARRIBA. POR EL PAPEL Y FROTIS FECAL MANTIENE HUMEDAS LA HECES Y LLEVA ELEMENTOS SOLUBLES DE LAS HECES AL PUNTO SUPERIOR DEL PALEL DONDE SE VOLATIZAN O ACUMULAN EN UNA MANCHA OSCURA. AL LEGAR AL ESTADIO INFECTANTE LAS LARVAS MIGRAN AL AGUA, DONDE SE LAS PUEDE OBERSERVAR CON UNA LUPA, SIENDO POSIBLE EXTRAERLAS CON UNA PIPETA PARASU EXAMEN MICROSCOPICO. VARIACIONES MENORES EN EL TUBO Y TIRA DE PAPEL NO SON CRTICAS.
BIBLIOGRAFIA.
Bailenger. J., and Neuzil E. 1953 Nouvelles techniques dexamen des helminthes. Fixation, coloratios, montage. Ann. Parasitol., 28, 392-398
Baroody, B. J and Mos, H. 1946. The Relative Efficiency of Water Centrifugal Sedimentation and Other Methods of Stool Examination for Diagnosis of Schistosomaiasis Japonica. J. Lab & Clin. Med., 31, 815-823 Beaver, P C. 1949 A Nephelometric Method of Calibrating the Photoelectric Meter for Making Egg-counts by direc Fecal Smear. J Parasito., 35 8sec. 2) 13 1950 The Standardization of Fecal Smears for Estimating Egg Production and Worm Burden. J. Parasito., 36, 451-456
1953. Persistence of Hookworm Larvae in Soil. Amer J. Trop . Med & Hyg., 2, 102-108
También podría gustarte
- Ensayo Condicionamiento OperanteDocumento6 páginasEnsayo Condicionamiento OperanteAngela Carolina Moreno Madrigal100% (1)
- Guía para La Desinfección y Esterilización en Centros de SaludDocumento133 páginasGuía para La Desinfección y Esterilización en Centros de SaludJair Humberto Angulo Perez0% (1)
- Pretest - Postest Refuerzo PresencialDocumento2 páginasPretest - Postest Refuerzo PresencialCLAUDIA PATRICIAAún no hay calificaciones
- Resultados Convocatoria 702445 PDFDocumento2 páginasResultados Convocatoria 702445 PDFOswaldo TiconaAún no hay calificaciones
- Folleto Primeros AuxiliosDocumento2 páginasFolleto Primeros AuxiliosGrupo EliotAún no hay calificaciones
- GAFA Probióticos DigitalDocumento39 páginasGAFA Probióticos DigitalMarina Martínez ZapataAún no hay calificaciones
- Circuitos AnestesicosDocumento20 páginasCircuitos AnestesicosFARMACIA SIMILARESAún no hay calificaciones
- Seminario de Vias Venosas Como Lo Hago Prof. Dr. Luis Del Rio DiezDocumento48 páginasSeminario de Vias Venosas Como Lo Hago Prof. Dr. Luis Del Rio DiezLUIS DEL RIO DIEZAún no hay calificaciones
- Técnica Aséptica.Documento2 páginasTécnica Aséptica.CINTHIA ALEJANDRA MENDOZA HERNANDEZAún no hay calificaciones
- Concepto de AnestesiaDocumento9 páginasConcepto de AnestesiaJefry Ortiz NuñezAún no hay calificaciones
- Sistema RespiratorioDocumento5 páginasSistema RespiratoriomiriamAún no hay calificaciones
- Accesorios PM2000MDocumento11 páginasAccesorios PM2000MFrida Mis LeonAún no hay calificaciones
- Termorregulacion PresentacionDocumento31 páginasTermorregulacion PresentacionJacob Alván100% (1)
- 6.medicina IslámicaDocumento37 páginas6.medicina IslámicaYaffett LombardoAún no hay calificaciones
- Cuidados Del Sistema DigestivoDocumento2 páginasCuidados Del Sistema DigestivoElvis Hermes33% (3)
- TestaDocumento13 páginasTestaSonia LidinskiAún no hay calificaciones
- Ic ArgDocumento8 páginasIc ArggustavokeilholdAún no hay calificaciones
- CubetasDocumento11 páginasCubetasRosaAún no hay calificaciones
- Agenesia PulmonarDocumento3 páginasAgenesia PulmonarSantiago Vargas100% (1)
- Resumo História MedicinaDocumento16 páginasResumo História MedicinaDébora MartinsAún no hay calificaciones
- MU - Analizador Marcapasos Externo PG 3077Documento22 páginasMU - Analizador Marcapasos Externo PG 3077Javi Payá HerrerosAún no hay calificaciones
- Bioqumica Def2Documento31 páginasBioqumica Def2DanielAún no hay calificaciones
- Dolor de BarrigaDocumento3 páginasDolor de BarrigaDahiana CárdenasAún no hay calificaciones
- Reporte ECGDocumento12 páginasReporte ECGSalvador ZarAún no hay calificaciones
- Óxido NitrosoDocumento9 páginasÓxido Nitrosoantonio rodriguezAún no hay calificaciones
- Norma Técnica de Atención Integral Al NiñoDocumento9 páginasNorma Técnica de Atención Integral Al NiñoMariSole SanchezAún no hay calificaciones
- Actividad de Aprendizaje 1 Evidencia LeinnyDocumento2 páginasActividad de Aprendizaje 1 Evidencia LeinnyNanis RemolinaAún no hay calificaciones
- Asisa Zaragoza PDFDocumento146 páginasAsisa Zaragoza PDFpinkybisAún no hay calificaciones
- Instalación de Las Prótesis TotalesDocumento35 páginasInstalación de Las Prótesis TotalesXavier AltamiranoAún no hay calificaciones
- GingivitisDocumento2 páginasGingivitisSalvador Diaz RomeroAún no hay calificaciones