Documentos de Académico
Documentos de Profesional
Documentos de Cultura
4ta-Sem-Dilatacion, Calorimetria y Termodinamica (Alumnos)
4ta-Sem-Dilatacion, Calorimetria y Termodinamica (Alumnos)
Cargado por
Yuber Alex PanccaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
4ta-Sem-Dilatacion, Calorimetria y Termodinamica (Alumnos)
4ta-Sem-Dilatacion, Calorimetria y Termodinamica (Alumnos)
Cargado por
Yuber Alex PanccaCopyright:
Formatos disponibles
-1-
Ciclo Enero - Marzo 2012
DILATACIN Y CALORIMETRIA
1. Temperatura: La temperatura mide el
grado de agitacin molecular promedio
que en su interior tiene un objeto, es decir
mide la energa cintica promedio de
traslacin de sus molculas.
2. Cero absoluto: Estado ideal en el que se
supone las molculas que constituyen un
cuerpo o sustancia, dejan de vibrar
(termina el movimiento molecular).
3. Escalas de temperatura:
RELATIVAS: Centgrada (C) y
Fahrenheit (F), se caracterizan por
aceptar valores negativos.
ABSOLUTAS: Kelvin (K) y Rankine
(R) en estas escalas no existen valores
negativos.
Frmula prctica para conversiones
entre escalas
32 273 492
= = =
5 9 5 5
C F K R - - -
5 9 5 5
C F K R D D D D
= = =
Para precisiones mayores tenemos:
273.15 K C = +
4. Dilatacin lineal: Aumento en la
longitud.
0
=
f
L L L D -
0
= L L T a D D
0
(1 )
f
L L T a = + D
Donde: T: temperatura
L: longitud
5. Dilatacin superficial: Es cuando hay
aumento en el rea (A).
=
f o
A A A D - =
o
A A T b D D
0
= (1 )
f
A A T b + D
6. Dilatacin volumtrica: Es cuando hay
aumento en el volumen (V).
=
f o
V V V D - =
o
V V T g D D
0
= (1 )
f
V V T g + D
Donde: a , b y g se denominan
coeficientes de dilatacin lineal, superficial
y volumtrico respectivamente. Y se
relacionan mediante:
2 2
b g
a = =
7. Calor (Q): El calor es la energa que se
transmite de un cuerpo a otro, solamente
a causa de una diferencia de
temperaturas. Siempre se transmite del
ms caliente al mas fri. Tal flujo
energtico cesa cuando ambos cuerpos
alcanzan una misma temperatura
(temperatura de equilibrio).
8. Calor sensible: Se usa para cambiar de
temperatura en una misma fase:
Q Ce m T = D
9. Calor de transformacin: Se usa para
cambiar de fase, durante este cambio la
temperatura se mantiene
constante: Q L m =
Para recipientes, se usa el calor: Q K T = D
Donde: Ce : calor especfico
-2-
m : masa
L : calor latente
K : capacidad calorfica
MAGNITUD
UNIDAD MAS
USUAL
UNIDAD EN S.I.
Q caloras (Cal) Joule (J)
m gramos (g) Kilogramo (kg)
T D
grados centgrados
(C)
Kelvin (K)
Ce
1 -1
Cal C g
-
1 1
J K kg
- -
L
1
Cal g
-
1
J kg
-
K
1
Cal C
-
1
J K
-
10. Equivalente mecnico de calor:
1cal 4,18J = ; 1J 0, 24cal =
11. Equilibrio trmico o ley cero de la
termodinmica: Si dos cuerpos A y B
estn en equilibrio trmico (igual
temperatura i.e. no hay intercambio de
energa interna) con un tercer cuerpo C,
entonces A y B estn en equilibrio
trmico entre s. Esto quiere decir
que dos cuerpos que estn en equilibrio
trmico, tienen la misma temperatura.
Algunos valores de uso frecuente para el
agua:
Cal
1
g C
Ce =
en fase liquida.
Cal
0, 5
g C
Ce =
en fase slida o gaseosa.
cal
80
g
L = (+) para derretir y () para
congelar.
cal
540
g
L = (+) para vaporizar y ()para
condensar.
EJERCICIOS.
1. Un termmetro en escala C, por error de
fabricacin, su escala marca 150 C para
ebullicin del agua y -10 C para la
congelacin de la misma. Cul ser el
valor en que este termmetro malogrado
marque una lectura correcta?
A) 16.7C B) 16.0C C) 16.5C
D) 14.6C E) 15C
2. Se crea una nueva escala relativa al que
llamaremos escala altiplano (A), que
registra la ebullicin del agua a 180 A, y
el de congelacin a 20 A. Cuntos
altiplanos (A) se registra para 30 C?
A) 70A B) 68A C) 65A
D) 66A E) 68A
3. Si la lectura de una temperatura en grados
Fahrenheit excede en 40 a la lectura en
grados Celsius, determinar la temperatura
en Kelvin.
212 100
32 0
F C
A) 283
B) 238
C) 383
D) 183
E) 338
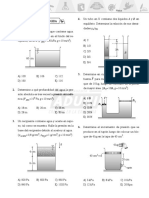
4. La lectura de la columna de mercurio de
un termmetro es 4 cm cuando el
termmetro se sumerge en agua con
hielo, y de 24 cm cuando el termmetro
se sumerge en vapor de agua hirviendo a
condiciones normales. Qu longitud
tendr en una habitacin a 22 C?
24 100
4
0
Hg(cm)
C
x
22
A) 10.4 cm
B) 8.4 cm
C) 9.4 cm
D) 18.4 cm
E) 14.4 cm
5. A qu temperatura en C el valor en la
escala Fahrenheit excede en 22 al doble
del valor en la escala Celsius?
-3-
A) 30C B) 40C C) 50C
D) 60C E) 55C
6. El dimetro de un agujero en una placa
de aluminio
5 1
2, 4 10 C a
- -
= es de 50
mm a 20C. Cul es el nuevo dimetro
cuando la placa se calienta a la
temperatura de 220C?
A) 50.24mm B) 50.25mm C) 25.24mm
D) 50.20mm E) 25.50mm
7. Un tanque de acero
5 1
1, 2 10 C a
- -
= de
100L se llena completamente con
gasolina
4 1
10, 8 10 C g
- -
= a 10C. Si la
temperatura aumenta a 50C. Qu
volumen de gasolina se derrama?
A) 2.176L B) 3.176L C) 4.176L
D) 5L E) 5.176L
8. Qu cantidad de masa de aluminio
( 0, 22cal / c g C = ) a 100C debe
aadirse a 220 g de agua a 10C, de
manera que la temperatura de equilibrio
sea de 40C?
A) 400 g B) 450 g C) 550 g
D) 600 g E) 500 g
9. Desde qu altura se debe dejar en
libertad un trozo de plomo de 10 g
( 0, 031cal / c g C = ), para que, por
motivo del impacto con el piso, su
temperatura se ele en 2C? Considerando
que el plomo no rebota y que absorbe
todo el calor generado. (
2
10 / g m s = )
A) 20 m B) 25.9 m C) 26.9 m
D) 28.7 m E) 30 m
10. Tiene un bloque de hielo a 0C. Luego
se le entrega 200 caloras. Qu cantidad
de hielo se descongela?
A) 2.7 g B) 2.5 g C) 2.6 g
D) 3.1 g E) 2.8 g
11. Ana y Diego construyen dos escalas
termomtricas. Para Ana el punto de
ebullicin del agua es 110A y el punto
de congelacin 10A. Para Diego el
punto de ebullicin es de 200D y el
punto de congelacin 20D. Si la escala
de Ana marca 35A, Cunto marca la
escala de Diego?
A) 53D B) 65D C) 54D
D) 66D E) 61D
12. Calcular la cantidad de calor que debe
ganar un trozo de hielo de 20 g a -30C
para convertirlo en agua a 80C de masa
A) 3500 cal B) 3300 cal C) 3000 cal
D) 3600 cal E) 2900 cal
13. Desde 20 m de altura se deja caer una
pelota de 1 kg de masa, determinar la
cantidad de calor que absorbi, siendo la
gravedad 10 m/s
2
A) 48 cal B) 46 cal C) 44 cal
D) 42 cal E) 40 cal
14. Las varillas mostradas se encuentran
inicialmente a 10C. Determinar a qu
temperatura ambas varilla logran unirse.
3 3
6 10 , 1 10
A B
C C a a
- -
= = .
40cm
10cm
5cm
A B
A) 15 C
B) 20 C
C) 25 C
D) 30 C
E) 40 C
15. Se tienen 40 g de agua a 10C, y se
mezcla con 60 g de agua a 90C, todo en
un recipiente de capacidad calorfica
despreciable. Cul es la temperatura
final de la mezcla?
A) 45 C B) 86 C C) 58 C
D) 78 C E) 69 C
16. Un cubito de hielo de 30g que estn a
-40C, si se requiere transformar en agua
a la temperatura de 50C, Cunto es la
cantidad de calor que se requiere?.
A) 5600 cal B) 4500 cal C) 4000 cal
D) 4550 cal E) 1460 cal
17. A qu temperatura se hallar una barra
de aluminio de 200.12cm de largo, si al
-4-
reducir la temperatura en la mitad, su
longitud disminuye en 0,12cm.
6 1
24 10
Al
C a
- -
=
A) 40 C B) 42 C C) 50 C
D) 45 C E) 50 C
18. Los rieles de un ferrocarril tienen 10 m
de longitud a 41 F. Calcular la dilatacin
para una temperatura de 378 K.
6 1
12 10
Fe
C a
- -
=
A) 10 mm B) 9 mm C) 8 mm
D) 12 mm E) 14 mm
19. Se quiere vaporizar 20 gr de agua que
esta a temperatura ambiente de 15C.
Calcular la cantidad de calor necesaria.
A) 12.0 KCal B) 12.6.9 KCal C) 12.4 KCal
D) 12.5 KCal E) 12.8 KCal
20. En una nevera (heladera) se colocan 40
gr de agua de 30 C y se obtienen cubitos
de hielo a 0 C. Qu cantidad de calor se
extrajo del agua?
A) 4.4 KCal B) 4.2 KCal C) -4.4 KCal
D) -3.8 KCal E) -4.0 KCal
21. Un vasija de vidrio contiene 1000 cm
3
de mercurio lleno hasta el borde, si se
aumenta la temperatura en 100C y el
recipiente alcanza un volumen de 1010
cm
3
(coeficiente de dilatacin
volumtrica del mercurio es de
4 1
1,8 10 C
- -
). Cunto de mercurio se
derrama?
A) 3
3
cm
B) 5
3
cm
C) 18
3
cm
D) 8
3
cm
E) 20
3
cm
22. En un calormetro de equivalente en
agua 10 gramos, se encuentra 20 gramos
de agua a 20 C, si se introduce un cuerpo
de 40 gramos de a 50 C, la temperatura
de equilibrio se logra a 40 C. Determinar
el calor especfico del cuerpo en
(cal/gC).
A) 1.5 B) 3.5 C) 4.5
D) 11.5 E) 13
23. En un recipiente de capacidad
calorfica despreciable se encuentran M
gramos de hielo a 0C. Se introducen en
el 120 gramos de agua a 60C, que
permiten fundir exactamente todo el
hielo. Qu cantidad de hielo haba en el
recipiente?
A) 80 g B) 120 g C) 90 g
D) 95 g E) 100 g
24. Se tienen dos varillas, una de hierro y
la otra de zinc, que miden 30.5cm y 30cm
a 0C. a qu temperatura deben
calentarse ambas varillas para que tengan
la misma longitud?
(
6 -1
Fe
12 10 C a
-
=
;
6 -1
Zn
26 10 C a
-
=
)
A) 1300C B) 1540C C) 1207.7C
D) 1200C E) 1304.4C
25. Un recipiente de capacidad calorfica
despreciable contiene cierta cantidad de
mercurio a 15C. Si se introduce una
esfera de platino a 120C se alcanza una
temperatura equilibrio de 40C. En un
segundo caso con los mismos elementos,
si el mercurio est a 20C la temperatura
de equilibrio es 50C. Hallar la
temperatura inicial del platino en este
caso
A) 125C B) 158C C) 146C
D) 152C E) 130C
26. Un alambre de 1m se dilata en 2mm
cuando su temperatura se incrementa en
100C Cul es el valor de su coeficiente
de dilatacin en 1/C?
A)
5
2 10
-
B)
5
3 10
-
C)
5
4 10
-
D)
5
5 10
-
E)
5
6 10
-
-5-
Ciclo Enero - Marzo 2012
TERMODINAMICA
1. Termodinmica: Ciencia que se
encarga solamente del estudio de las
transformaciones del calor en trabajo
mecnico.
2. Gas ideal: Llamado tambin gas
perfecto, sus molculas tienen
dimensiones propias despreciables, sus
molculas no interactan entre si, sus
molculas chocan elsticamente contra
las paredes del recipiente.
3. Estado termodinmico: Situacin
especfica del gas definida por sus
propiedades termodinmicas: presin
absoluta P (en Pa), volumen V (en m
3
) y
temperatura absoluta T (en Kelvin K).
4. Ecuacin de estado de los gases ideales:
PV nRT =
Donde: P: Presin absoluta, en Pa
V: Volumen del gas, en
3
m
n: nmero de moles, en mol
T: temperatura absoluta, en K
R: constante universal de los gases
J cal
8.314 1.986
mol K mol K
R = =
5. Proceso termodinmico: Es el paso de
un estado inicial P
1
, V
1
, T
1
a otro estado
final P
2
, V
2
, T
2
Si en un proceso la masa
permanece constante:
1 1 2 2
1 2
conste
PV PV
T T
= =
6. Principales procesos termodinmicos:
Iscoro o
isovolumtrico
volumen constante:
cte
P
T
=
Isobrico
presin constante:
cte
V
T
=
Isotrmico
temperatura
constante:
cte PV =
Adiabtico
el gas ni recibe ni
cede calor al
exterior
7. Trabajo realizado por un gas: Es el
rea debajo de la curva al granear P
versus V.
No hay rea
0 W =
2 1
( ) W P V V
P V
= -
= D
2
1
ln
V
W n R T
V
=
-6-
2 2 1 1
1
PV PV
W
g
-
=
-
g :coeficiente
adiabtico
Tambin se puede definir una relacin
entre: /
P V
C C g =
Donde Cp y Cv son los calores especficos
del gas a presin y volumen constante
respectivamente [Cal/mol.K]
Gas
V
C
P
C
g
Monoatmico 3 5 1,666
Diatmico 5 7 1,4
Calor a volumen constante:
V
Q n C T = D
Calor a presin constante:
P
Q n C T = D
n(mol) ; ,
V P
C C (
cal
mol K
); T D (Kelvin K)
8. Primera ley de la termodinmica: Para
todo sistema termodinmico:
Q W U = + D , Donde Q y W son el calor
y trabajo netos, respectivamente; U D es
la variacin de la energa interna que
depende nicamente de la temperatura.
9. En cualquier proceso la variacin de la
energa interna se calcula con
=
V
U n C T D D
3
=
2
U R n T D D para gases
monoatmicos y
5
=
2
U R n T D D para gases biatmicos
10. Mquina trmica (M.T.): Dispositivo
que transforma el calor en trabajo
mecnico
Q
A
: calor que se le d a la M.T.
Q
B
: calor que pierde la M.T.
W: trabajo que realiza la M.T.
T
A
: temperatura alta.
T
B
: temperatura baja.
A B
W Q Q = -
11. Eficiencia: Para cualquier M.T. se
define: = =1
B
A A
Q W
Q Q
h -
Para M.T. reversibles o ideales, es vlida la
relacin de Kelvin:
B B
A A
T Q
T Q
=
12. Mquinas trmicas de Carnot: Son
M.T. reversibles o ideales de mxima
eficiencia.
13. Segunda ley de la termodinmica:
Es imposible construir una mquina
trmica 100% eficiente
No es posible convertir todo el calor que
se entrega a una M.T. en trabajo.
14. Entropa (S): Microscpicamente:
Expresa la capacidad de la energa a
sufrir cambios (a mayor entropa la
transformacin energtica en difcil).
Microscpicamente: Expresa la medida
del desorden molecular. La entropa es
muy usual para analizar
cuantitativamente la segunda ley de la
termodinmica. La variacin AS en un
proceso termodinmico reversible se
calcula con:
Q
S
T
D
D = ; Q D : es la variacin de calor
-7-
EJERCICIOS.
1. Cinco litros de gas a una presin absoluta
de 200 kPa y a una temperatura de 200 K
se calientan uniformemente hasta 500 K
y la presin absoluta se reduce a 150 kPa.
Qu volumen ocupar el gas en esas
condiciones?
A) 14 L B) 15 L C) 16 L
D) 15.7 L E) 16.7 L
2. En un sistema se sabe que 160 g de
oxgeno siguen el proceso mostrado.
Determine el trabajo efectuado por el
sistema. (
1
127 T C = )
P
V
0
2V
0
V
(1)
(2)
A) 16 620 J
B) 862 J
C) 20 620 J
D) 12 620 J
E) 420 J
3. Halle el calor suministrado a un gas ideal
en cierto proceso, si la tercera parte de
este calor fue transformado en trabajo y
la energa interna del gas aument en 80
J.
A) 100 J B) 110 J C) 120 J
D) 130 J E) 140 J
4. Diez moles de cierto gas ideal se
expanden isotrmicamente, a la
temperatura de 100 K, hasta triplicar su
volumen. Calcule el trabajo del gas,
ln3 1.1 = y 8.31J /(mol K) R =
A) 0 J B) 8141 J C) 11141 J
D) 10141 J E) 9141 J
5. Calcular la cantidad de calor necesaria
para elevar la temperatura de 200 g de
aluminio de -70 C a -40 C
A) 1360 cal B) 1340 cal C) 1320 cal
D) 1310 cal E) 1300 cal
6. En un comportamiento la presin
absoluta es de 831 KPa, en el se
encuentra 5 moles de gas a 7C, calcule
el volumen del comportamiento, en m
3
A) 0.010 B) 0.011 C) 0.012
D) 0.013 E) 0.014
7. Un gas se ha comprimido a temperatura
constante desde un volumen de 8L hasta
el volumen de 6L. El aumento de presin
ha sido de 40 KPa. Halle la presin
absoluta inicial del gas
A) 100 KPa B) 120 KPa C) 140 KPa
D) 160 KPa E) 180 KPa
8. Se muestra un proceso de expansin que
cambia de 1 a 2 en el siguiente esquema.
Hallar el trabajo producido por el gas.
A) 560 J
B) 640 J
C) 420 J
D) 120 J
E) 603 J
9. Una mquina trmica para funcionar
absorbe 1200J y expulsa 400J en cada
ciclo. Luego su eficiencia es de:
A) 33.3% B) 66.6% C) 44%
D) 30% E) 47%
10. En la figura mostramos un cilindro
vertical cerrado por un pistn liso de piso
despreciable cuya seccin es de 0,5 m
2
.
Si el volumen del gas se expande
lentamente hasta que el pistn ascienda
20 cm, halle el trabajo que produce el
gas. La presin atmosfrica es: 10
5
N/m
2
.
gas
A) 20 KJ
B) 5 KJ
C) 10 KJ
D) 25 KJ
E) 30 KJ
11. La figura muestra un cilindro cerrado
por un pistn que carece de friccin, de
0,6 m
2
de seccin y peso despreciable
sobre el cual hay un bloque de peso 24
KN. Halle el trabajo que desarrolla el gas
cuando el pistn sube lentamente 10 cm.
Presin atmosfrica (P
O
= 10
5
N/m
2
)
gas
A) 8400 J
B) 4800 J
C) 840 J
D) 480 J
E) 500 J
-8-
12. En un cilindro vertical cerrado por un
pistn de 1 m
2
de rea transversal y peso
despreciable (friccin despreciable).
Sobre el pistn se coloca un cuerpo de
15000 N, calcule el trabajo que se realiza
cuando el pistn cae lentamente 10 cm.
(P
O
= 10
5
Pa).
A) 11200 J B) 12000 J C) 11500 J
D) 11000 J E) 10500 J
13. En un cilindro horizontal se tiene un
gas ideal encerrado por un pistn de peso
despreciable. Si el gas se comprime
lentamente mediante una fuerza F,
disipando 80 J de energa calorfica,
determine la variacin de la energa
interna que experimenta el gas. Si el
trabajo externo total realizado sobre el
gas fue 150 J. (considere la capacidad
calorfica del recipiente despreciable)
A) 82 J B) 75 J C) 40 J
D) 70 J E) 230 J
14. Un recipiente contiene 200 g de nen,
ocupando un volumen de 20 lt. a una
presin de 8 atmsferas. Se le expande
isotrmicamente, hasta que ocupa un
volumen cuatro veces de la inicial.
Calcule; la presin final y la variacin de
la energa interna.
A) 2 atm; 2 J B) 2 atm; 4 J C) 8 atm; 2 J
D) 2 atm; -2 J E) 2 atm, 0
15. Dentro de un recipiente cilndrico de
paredes aislantes trmicos y seccin
transversal 625cm
2
, se encuentra un gas
ideal tal como se muestra. Determine el
trabajo que desarrolla el gas
5
gas
2 10 Pa P = , si el pistn se deja
deslizar lentamente de (1) hasta (2) a
presin constante.
0.4m
Vacio
0.4m
(1) (2) A) 5000 J
B) 2000 J
C) 3000 J
D) 4000 J
E) 5000 KJ
16. Si en cada uno de los balones de gas la
energa interna es igual a 900R
(R=constante universal de los gases)
donde T
1
=300K T
2
=450K T
3
=900K,
Cul es el numero de moles en cada
caso?
A) 1, 3, 4 B) 2, 4, 6 C) 6, 4, 2
D) 5, 4, 6 E) 6, 4, 1
17. Un gas ideal se lleva por el ciclo
reversible, tal como se muestra.
Determine el trabajo realizado por el gas
en un ciclo.
a
b
c
(KPa) P
-3 3
(10 m ) V
20 80
100
150
A) 1.5 KJ
B) 4 KJ
C) 4.5 KJ
D) 3.5 KJ
E) 2 KJ
18. Si una maquina trmica trabaja entre
27C y 227C absorbiendo 600J de calor
y cediendo al exterior 420J de calor
Cul es su eficiencia?
A) 30% B) 25% C) 19%
D) 20% E) 17%
19. Una esfera de plata de 200 g se
encuentra a la temperatura de 200C, y se
sumerge completamente en un lquido.
Luego de un cierto tiempo se extrae la
esfera, verificndose que su temperatura
descendi hasta 70C. Cunto calor
cedi la esfera al lquido durante su
permanencia en ella? Ce plata = 0,056
cal/g.C
A) -1456 cal B) 1456 cal C) -1556 cal
D) 1556 cal E) 1656 cal
20. Un camin que viaja a razn de 36
km/h frena hasta detenerse. Calcular la
cantidad de caloras producidas por el
camin hasta detenerse. (Masa del
camin 5000 kg)
A) 50 Kcal B) 55 Kcal C) 60 Kcal
D) 65 Kcal E) 70 Kcal
También podría gustarte
- Produccion Transp Electrica-AnayaDocumento18 páginasProduccion Transp Electrica-AnayaCesar Huamani MaytaAún no hay calificaciones
- IVB - FISI - 4to. Año - Guía 3 - Potencial EléctricoDocumento7 páginasIVB - FISI - 4to. Año - Guía 3 - Potencial EléctricoYuber Alex PanccaAún no hay calificaciones
- Administracion Por ExcepcionDocumento41 páginasAdministracion Por ExcepcionDiany Bermejo40% (5)
- III BIM - HP - 3ER AÑO - Guia 2 - El Primer MilitarismoDocumento11 páginasIII BIM - HP - 3ER AÑO - Guia 2 - El Primer Militarismopsycho_lito22Aún no hay calificaciones
- 30 CalorimetriaDocumento14 páginas30 CalorimetriaMarcelo GuzmánAún no hay calificaciones
- F - S10 - Calorimetría - Cambio de FaseDocumento9 páginasF - S10 - Calorimetría - Cambio de FaseRicardoAún no hay calificaciones
- Fisica Ii - Quinto - (Termodinamica I) 8va SesiónDocumento2 páginasFisica Ii - Quinto - (Termodinamica I) 8va SesiónMinas YuberAún no hay calificaciones
- Miscelanea - FisicaDocumento3 páginasMiscelanea - FisicaDeisy rosioAún no hay calificaciones
- 4º Trigonometria - PitagorasDocumento91 páginas4º Trigonometria - Pitagorashector100% (1)
- Tema 5 Caida LibreDocumento3 páginasTema 5 Caida LibreNora OliveroAún no hay calificaciones
- TERMOMETRIADocumento4 páginasTERMOMETRIAErning YHAún no hay calificaciones
- Momento de Una FuerzaDocumento6 páginasMomento de Una FuerzaJHOJAN ANTONI COTRINA JUIPAAún no hay calificaciones
- FisicaDocumento2 páginasFisicapichanaqui mendez palaciosAún no hay calificaciones
- 1 - A - Seminario - Solucionario Uns - 2017 Ii - 2018 IDocumento4 páginas1 - A - Seminario - Solucionario Uns - 2017 Ii - 2018 IADMINISTRADOR CEPUNS50% (2)
- Movimiento de Caida Libre EjerciciosDocumento6 páginasMovimiento de Caida Libre EjerciciosAnonymous au6UvN92kBAún no hay calificaciones
- 2-Circuitos Corriente ContinuaDocumento10 páginas2-Circuitos Corriente Continuamariola2000Aún no hay calificaciones
- Aritmética 9Documento13 páginasAritmética 9Juan Carlos Pérez PérezAún no hay calificaciones
- Semana N°1Documento6 páginasSemana N°1Jose Luis Ferre PeresAún no hay calificaciones
- 004 Termometria y Dilatacion RptasDocumento1 página004 Termometria y Dilatacion RptascrexgAún no hay calificaciones
- Semana 9Documento3 páginasSemana 9Percy AlaniaAún no hay calificaciones
- Cantidad de Movimientoimpulso y ChoquesDocumento7 páginasCantidad de Movimientoimpulso y ChoquesFidel Cumpa ZarpánAún no hay calificaciones
- EstaticaDocumento7 páginasEstaticagrogeryAún no hay calificaciones
- Física Semestral Uni - Ejercicios de Estática de FluidosDocumento2 páginasFísica Semestral Uni - Ejercicios de Estática de FluidosLennin Brayan Diaz HerreraAún no hay calificaciones
- Poligonos - 2021-2Documento4 páginasPoligonos - 2021-2Carlos Atuncar ParejaAún no hay calificaciones
- Problemas de Segunda Condicion de Equilibrio 43862Documento2 páginasProblemas de Segunda Condicion de Equilibrio 43862Cristhian ChumaceroAún no hay calificaciones
- FISICSDocumento2 páginasFISICSLuis Alejandro Chuquipoma MarínAún no hay calificaciones
- 1.UPeU Sis Medición AngularDocumento2 páginas1.UPeU Sis Medición AngularBraulio Gutierrez PariAún no hay calificaciones
- 1er Material Ciencias-PreDocumento271 páginas1er Material Ciencias-PreKevin MirandaAún no hay calificaciones
- Fisica Pre CadeteDocumento2 páginasFisica Pre Cadeteوقف بوري كاجوAún no hay calificaciones
- Ades SullanaDocumento4 páginasAdes SullanaRosa Melva Vera RuedaAún no hay calificaciones
- ELECTROSTATICADocumento2 páginasELECTROSTATICAChristian Tello LlamojaAún no hay calificaciones
- Sem6 - Termometría - Dilatación TérmicaDocumento5 páginasSem6 - Termometría - Dilatación TérmicaPanchitoPQ21Aún no hay calificaciones
- Magnitudes Reparto 2Documento9 páginasMagnitudes Reparto 2Jaime Oros Gamarra100% (1)
- Boletin 3º JULIODocumento209 páginasBoletin 3º JULIOCésar Francisco Tuya Gamarra50% (2)
- Angulo Trigonometrico Sistema de Medicion AngularDocumento296 páginasAngulo Trigonometrico Sistema de Medicion Angularraul victor velasquez jaqueAún no hay calificaciones
- Práctica de Termometría - Virtual Mañana 1Documento2 páginasPráctica de Termometría - Virtual Mañana 1ImDreamAún no hay calificaciones
- Física Formulario 2021 - II FaseDocumento3 páginasFísica Formulario 2021 - II FaseDANIELA DLS100% (1)
- Semana 4 Estática II Fisica I IAg 2021 2Documento3 páginasSemana 4 Estática II Fisica I IAg 2021 2Christian TipismanaAún no hay calificaciones
- Libro Tareas PDFDocumento112 páginasLibro Tareas PDFJulio BarbozaAún no hay calificaciones
- Examen 01Documento1 páginaExamen 01Maria LazarteAún no hay calificaciones
- FisicaDocumento3 páginasFisicaElmo Jaime SALAS YAÑEZAún no hay calificaciones
- Guia de FisicaDocumento3 páginasGuia de FisicaHassler M CasafrancaAún no hay calificaciones
- Balota Academia Estatica IDocumento3 páginasBalota Academia Estatica Iestofa100% (1)
- Sistema de Racionales Jose Marco EJERCICIOS 2013Documento7 páginasSistema de Racionales Jose Marco EJERCICIOS 2013Piero ArequeAún no hay calificaciones
- Física - Análisis DimensionalDocumento3 páginasFísica - Análisis DimensionalPiero Giovanni Martin Berrospi VegaAún no hay calificaciones
- EstaticaDocumento2 páginasEstaticaNueva GeneracionAún no hay calificaciones
- 03 AritmeticaDocumento14 páginas03 AritmeticaBautista Gomez Dionisio0% (1)
- Practica TermometriaDocumento2 páginasPractica TermometriaDenisse CondoriAún no hay calificaciones
- Termometria y Calor Basico 1Documento8 páginasTermometria y Calor Basico 1Reisell Martin Rojas PilcoAún no hay calificaciones
- Hidrostatica-Tema 9Documento4 páginasHidrostatica-Tema 9RobertAún no hay calificaciones
- Tiro HorizontalDocumento2 páginasTiro HorizontalGianella PaezAún no hay calificaciones
- Fisica 4toDocumento7 páginasFisica 4toAntonela Garibay RubioAún no hay calificaciones
- Segunda Ley de Newton LABORATORIODocumento5 páginasSegunda Ley de Newton LABORATORIOAxl Camilo LopezAún no hay calificaciones
- Problemas EstaticaDocumento2 páginasProblemas Estaticaorlan2_rAún no hay calificaciones
- Cepuns 2013-II Semana 03Documento8 páginasCepuns 2013-II Semana 03boc_55Aún no hay calificaciones
- Tema 07 - MCUV PDFDocumento4 páginasTema 07 - MCUV PDFRonald Alexis Benites PeñaAún no hay calificaciones
- FISICA I Sem 3Documento4 páginasFISICA I Sem 3José Alberto MendozaAún no hay calificaciones
- PC3 (Fisica)Documento2 páginasPC3 (Fisica)Rodolfo Castro MirandaAún no hay calificaciones
- Repaso ElectrostaticaDocumento5 páginasRepaso ElectrostaticaCarlos MorenoAún no hay calificaciones
- Examen Parcial 01Documento1 páginaExamen Parcial 01ETHEL ANDREA AREVALO PINEDOAún no hay calificaciones
- Fisica 5to - Campo Electrico RepasoDocumento2 páginasFisica 5to - Campo Electrico RepasoFranky Tello Buitrón0% (1)
- Term Odin A MicaDocumento2 páginasTerm Odin A MicaDavid Daniel Ramirez CornejoAún no hay calificaciones
- Ejercicios Calorimetría Dilatación y TermodinámicaDocumento9 páginasEjercicios Calorimetría Dilatación y TermodinámicaJeff Huckleberry50% (2)
- Ctfisi 5ºs IiipDocumento12 páginasCtfisi 5ºs IiipAnfer Galindo Tunqui0% (1)
- Lenguaje y Literatura 06 EL VERBO Y LIT. NARRATIV CONTEMPORANEADocumento8 páginasLenguaje y Literatura 06 EL VERBO Y LIT. NARRATIV CONTEMPORANEAYuber Alex PanccaAún no hay calificaciones
- Hoja de AsistenciasDocumento5 páginasHoja de AsistenciasYuber Alex PanccaAún no hay calificaciones
- Preguntas Historia Geografia RespDocumento12 páginasPreguntas Historia Geografia RespYuber Alex PanccaAún no hay calificaciones
- Examen Diario Ultimo 23 de JulioDocumento1 páginaExamen Diario Ultimo 23 de JulioYuber Alex PanccaAún no hay calificaciones
- IV Bim. 1er. Año - RV - Guia #4 - Textos NarrativosDocumento12 páginasIV Bim. 1er. Año - RV - Guia #4 - Textos NarrativosYuber Alex PanccaAún no hay calificaciones
- Trabajo Energia, Hidrost Tica (Claves)Documento8 páginasTrabajo Energia, Hidrost Tica (Claves)Yuber Alex Pancca100% (1)
- II BIM - 4to. Año - ALG - Guía 7 - RacionalizaciónDocumento5 páginasII BIM - 4to. Año - ALG - Guía 7 - RacionalizaciónYuber Alex PanccaAún no hay calificaciones
- IV BIM - 3er. Año - Bio - Guía 8 - Aparato Reproductor HumanDocumento5 páginasIV BIM - 3er. Año - Bio - Guía 8 - Aparato Reproductor HumanYuber Alex PanccaAún no hay calificaciones
- IV BIM - 3er. Año - Bio - Guía 7 - Sistema Endocrino IIDocumento6 páginasIV BIM - 3er. Año - Bio - Guía 7 - Sistema Endocrino IIYuber Alex PanccaAún no hay calificaciones
- IV Bim - 5to. Año - Guía 7 - Petroleo y Contaminacion AmbienDocumento7 páginasIV Bim - 5to. Año - Guía 7 - Petroleo y Contaminacion AmbienÓscar Cárdenas TorresAún no hay calificaciones
- Informe Venezuela Potencia Productiva Clase 1Documento13 páginasInforme Venezuela Potencia Productiva Clase 1Rubén FernándezAún no hay calificaciones
- Manual Dumper CaterpillarDocumento118 páginasManual Dumper CaterpillarAndreis Dario Paez AlvaradoAún no hay calificaciones
- Estudios Económicos - Ministerio de Producción - Piura 2023Documento3 páginasEstudios Económicos - Ministerio de Producción - Piura 2023gustavo.payetAún no hay calificaciones
- Como Escoger Una Imagen SatelitalDocumento5 páginasComo Escoger Una Imagen SatelitalGherly Yadira Morales AlfaroAún no hay calificaciones
- 300 Problemas Que Te Ayudaran A Comprender El MundoDocumento35 páginas300 Problemas Que Te Ayudaran A Comprender El MundoLuis Daniel Fernández QuintanaAún no hay calificaciones
- Deber 1 Alex Uquillas Dibujo Tecnico JhvyfytiDocumento3 páginasDeber 1 Alex Uquillas Dibujo Tecnico JhvyfytiFernando UquillasAún no hay calificaciones
- Clase Modelo. Mezclas y DisolucionesDocumento9 páginasClase Modelo. Mezclas y Disolucionesjaguillermo4205Aún no hay calificaciones
- Marco Histórico Del Profeta DanielDocumento8 páginasMarco Histórico Del Profeta Danieloxemiro100% (3)
- El Proceso CreativoDocumento56 páginasEl Proceso CreativoGlorig2Aún no hay calificaciones
- Tukas IndividualDocumento17 páginasTukas IndividualInha Carvalho NamorjesAún no hay calificaciones
- Tratamiento de Las Fracturas No-UniónDocumento6 páginasTratamiento de Las Fracturas No-UniónPablo Gonzalez RivielloAún no hay calificaciones
- Diseño de Una Smart Grid para Un Sistema Híbrido de EnergíaDocumento8 páginasDiseño de Una Smart Grid para Un Sistema Híbrido de Energíarubio111Aún no hay calificaciones
- Plan Global Análisis Numérico IIIDocumento5 páginasPlan Global Análisis Numérico IIIHans Müller Santa CruzAún no hay calificaciones
- EdafizaciónDocumento16 páginasEdafizaciónANA YULI MEDINA TAPIAAún no hay calificaciones
- El Modelo de PickmanDocumento9 páginasEl Modelo de PickmanEVDgraphicsAún no hay calificaciones
- Presupesto PlantillaDocumento100 páginasPresupesto PlantillaMaira AragonAún no hay calificaciones
- Trabajo de ColpasDocumento28 páginasTrabajo de ColpasDiana Alvarez leonAún no hay calificaciones
- Itinerarios Semana Santa Almuñécar 2019 PDFDocumento32 páginasItinerarios Semana Santa Almuñécar 2019 PDFAntonio García RuizAún no hay calificaciones
- C.S.Udima EQPMTO-SEGUNDA PLANTA 2°Documento1 páginaC.S.Udima EQPMTO-SEGUNDA PLANTA 2°George Guevara GuerreroAún no hay calificaciones
- Hoteles Sostenibles y Responsables.Documento24 páginasHoteles Sostenibles y Responsables.eavaAún no hay calificaciones
- Quipus Arturo Ruiz EstradaDocumento3 páginasQuipus Arturo Ruiz EstradaGalindomarcosAún no hay calificaciones
- Modulo 1 Cosechadora 1206Documento34 páginasModulo 1 Cosechadora 1206Isai OrtizAún no hay calificaciones
- Estudio de Caracterización de Residuos Solidos Del Distrito ChachapoyasDocumento79 páginasEstudio de Caracterización de Residuos Solidos Del Distrito ChachapoyasNilton HAún no hay calificaciones
- Modulo SAP 1Documento54 páginasModulo SAP 1Katy GatiAún no hay calificaciones
- 7 Guia Informatica PrimeroDocumento3 páginas7 Guia Informatica PrimeroTatiana SalasAún no hay calificaciones
- PDF Isla de Zapatera Idolos DDDocumento48 páginasPDF Isla de Zapatera Idolos DDedgardAún no hay calificaciones
- El Padre Pio PDFDocumento46 páginasEl Padre Pio PDFGonzalez JorgeAún no hay calificaciones