Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Electrolisis Ayudantia
Cargado por
grupo de ciencias0 calificaciones0% encontró este documento útil (0 votos)
7 vistas13 páginaselectrolisis ayudantia
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PPT, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoelectrolisis ayudantia
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPT, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
7 vistas13 páginasElectrolisis Ayudantia
Cargado por
grupo de cienciaselectrolisis ayudantia
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPT, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 13
Electrolisis
Natalia Sepúlveda Letelier
Electrolisis
LaElectrólisis es un proceso para
separar un compuesto en los
elementos que lo conforman, usando
para ello la electricidad. La palabra
Electrólisis viene de las raíces
electro, electricidad y lisis,
separación.
Experimento
Se funde o se disuelve el electrólito en un determinado
solvente, con el fin de que dicha sustancia se separe en
iones (ionización).
Se aplica una corriente eléctrica continua mediante un
par de electrodos conectados a una fuente de
alimentación eléctrica y sumergidos en la disolución.
El electrodo conectado al polo positivo se conoce como
ánodo, y el conectado al negativo como cátodo.
Cada electrodo atrae a los iones de carga opuesta. Así,
los iones negativos, o aniones, son atraídos y se desplazan
hacia el ánodo, mientras que los iones positivos, o
cationes, son atraídos y se desplazan hacia el cátodo.
Conclusiones
La energía necesaria para separar a los iones e
incrementar su concentración en los electrodos es
aportada por la fuente de alimentación eléctrica.
En los electrodos se produce una transferencia de
electrones entre éstos y los iones, produciéndose
nuevas sustancias. Los iones negativos o aniones ceden
electrones al ánodo (+) y los iones positivos o cationes
toman electrones del cátodo (-).
En definitiva lo que ocurre es una reacción de
oxidación-reducción, donde la fuente de alimentación
eléctrica se encarga de aportar la energía necesaria.
Electrolisis del Agua
Laelectrolisis del agua si no es agua
destilada, la electrólisis no sólo separara
el oxígeno y el hidrógeno, sino los demás
componentes que estén presentes como
sales, metales y algunos otros minerales.
Precauciones
Nunca deben unirse los electrodos, ya que la corriente eléctrica no va
a conseguir el proceso y la batería se sobrecalentará y quemará.
Debe utilizarse siempre corriente continua (energía de baterías o de
adaptadores de corriente), NUNCA corriente alterna (energía del
enchufe de la red)
La electrólisis debe hacerse de tal manera que los dos gases
desprendidos no entren en contacto, de lo contrario producirían una
mezcla peligrosamente explosiva.
Una manera de producir agua otra vez es mediante la exposición a un
catalizador. El más comúnmente es el calor; otro es el platino en forma
de lana fina o polvo. El segundo caso debe hacerse con mucho cuidado,
incorporando cantidades pequeñas de hidrógeno en presencia de
oxigeno y el catalizador, de manera que el hidrógeno se queme
suavemente, produciendo una llama tenue. Lo contrario nunca debe
hacerse.
Aplicaciones
Producción de aluminio, litio, sodio, potasio y magnesio.
Producción de hidrógeno con múltiples usos en la industria: como
combustible, en soldaduras, etc. Ver más en hidrógeno diatómico.
Producción de cloro, hidróxido de sodio, clorato de sodio y
clorato de potasio.
La electrometalurgia es un proceso para separar el metal puro de
compuestos usando la electrólisis. Por ejemplo, el hidróxido de
sodio es separado en sodio puro, oxígeno puro y agua.
La anodización es usada para proteger los metales de la
corrosión.
La galvanoplastia, también usada para evitar la corrosión de
metales, crea una película delgada de un metal menos corrosible
sobre otro metal.
Galvanoplastia
Es la rama tecnológica que agrupa a aquellos
procesos en los que se logra depositar una capa
metálica continua y adherente, sobre la
superficie de un conductor inmerso en un
electrólito, con el uso de la corriente eléctrica.
Al proceso de deposición en particular se le
denomina recubrimiento electrólitico.
Los recubrimientos electrolíticos pueden ser
de metales puros o de aleaciones.
Objetivos de la Galvanoplastia
Aumentar la resistencia a la corrosión;
depositando un material mas resistente, a la
agresividad del medio en el que se encontrará
la pieza durante el uso. Es común en estos
casos encontrar, capas de níquel, cromo,
estaño o cinc sobre piezas de acero.
Aumentar la dureza superficial; depositando
una capa con cualidades de alta dureza. Se
pueden encontrar en la práctica con este
objetivo, capas de cromo duro sobre el filo de
herramientas de acero.
Aumentar la resistencia al desgaste; depositando
una capa especialmente elaborada de algún material
con propiedades elevadas de resistencia al desgaste,
bajo coeficiente de fricción y buena retención del
lubricante. Este caso encuentra aplicación frecuente
en el recubrimiento con cromo de la superficie de
rozamiento de los anillos de pistón de los
motores de combustión interna.
Dar una mejor apariencia a la pieza; depositando
una capa de apariencia lustrosa, mate u otra deseada,
o bien de determinado color o textura. Con esta
aplicación tropezamos a diario, y es muy común su uso
para recubrir con materiales vistosos como oro, plata,
níquel, cromo, cadmio, platino, latón etc. a piezas de
material base barato.
Restaurar dimensiones desgastadas;
depositando capas de hierro o cromo sobre
piezas que han sufrido desgaste durante el
trabajo. Este tipo de recubrimiento se usa
para restaurar algunas piezas en los procesos
de reparación de máquinas.
Base para la adherencia posterior de otros
materiales; La adherencia de ciertos
materiales no metálicos como las gomas, o las
capas de cromo decorativo, a las piezas de
acero se mejora mucho si esta se recubre
previamente con una capa de cobre.
Modificar el coeficiente de fricción; Es común en las
máquinas el uso de capas superficiales de materiales
blandos depositados electrolíticamente en los
cojinetes de deslizamiento para facilitar el
asentamiento correcto de la unión árbol-cojinete en el
período inicial de trabajo. También ciertas texturas
de capas de cromo y otros materiales sobre piezas de
acero logradas electrolíticamente puede mejorar la
resistencia al rozamiento de las uniones deslizantes.
Mejorar el contacto entre conectores eléctricos; en
el mundo de las máquinas eléctricas y electrónicas
actualmente, las partes de los conectores que realizan
el acople conductor están recubiertas
electrolíticamente de materiales que garantizan un
buen contacto. Especialmente en aparatos
electrónicos de alta fiabilidad se usan
frecuentemente los recubrimientos con oro.
Tipos de recubrimiento
Nombre Material Campo de Aplicación
Cobreado Cobre Recubrimiento decorativo de
piezas de materiales no
metálicos.
Cromado Cromo Recubrimiento anticorrosivo y
decorativo.
Acerado Hierro Material de relleno en zonas
desgastadas en acero
Niquelado Niquel Recubrimiento anticorrosivo y
decorativo.
Capa base para el cromado.
Cadmiado Cadmio Para facilitar la soldadura
blanda en componente
eléctricos.
Recubrimiento de contactos
eléctricos en conectores
comunes.
Galvanizado Cinc Recubrimiento anticorrosivo del
acero.
Estañado Estaño Recubrimiento anticorrosivo
temporal del acero.
Dorado Oro Recubrimiento protector y
decorativo
Plateado Plata Recubrimiento protector y
decorativo
Latonado Latón Recubrimiento protector y
decorativo
También podría gustarte
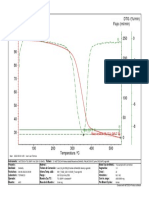
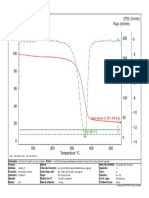
- TG /% Flujo / (Ml/min) DTG / (%/min) : Pico: 357.5 °CDocumento1 páginaTG /% Flujo / (Ml/min) DTG / (%/min) : Pico: 357.5 °Cgrupo de cienciasAún no hay calificaciones
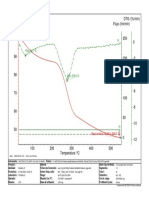
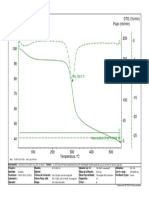
- TG /% Flujo / (Ml/min) DTG / (%/min) : Pico: 64.7 °CDocumento1 páginaTG /% Flujo / (Ml/min) DTG / (%/min) : Pico: 64.7 °Cgrupo de cienciasAún no hay calificaciones
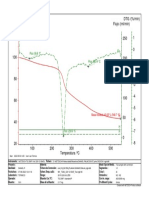
- TG /% Flujo / (Ml/min) DTG / (%/min) : Pico: 62.0 °CDocumento1 páginaTG /% Flujo / (Ml/min) DTG / (%/min) : Pico: 62.0 °Cgrupo de cienciasAún no hay calificaciones
- TG /% Flujo / (Ml/min) DTG / (%/min) : Pico: 64.7 °CDocumento1 páginaTG /% Flujo / (Ml/min) DTG / (%/min) : Pico: 64.7 °Cgrupo de cienciasAún no hay calificaciones
- TG /% Flujo / (Ml/min) DTG / (%/min) : Pico: 86.6 °CDocumento1 páginaTG /% Flujo / (Ml/min) DTG / (%/min) : Pico: 86.6 °Cgrupo de cienciasAún no hay calificaciones
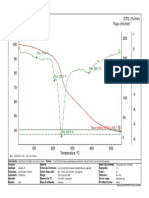
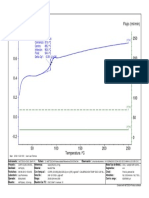
- TG /% Flujo / (Ml/min) 1 DTG / (%/min) : Pico: 114.8 °CDocumento1 páginaTG /% Flujo / (Ml/min) 1 DTG / (%/min) : Pico: 114.8 °Cgrupo de cienciasAún no hay calificaciones
- TG /% Flujo / (Ml/min) DTG / (%/min) : Pico: 64.7 °CDocumento1 páginaTG /% Flujo / (Ml/min) DTG / (%/min) : Pico: 64.7 °Cgrupo de cienciasAún no hay calificaciones
- Hdpe (DSC)Documento1 páginaHdpe (DSC)grupo de cienciasAún no hay calificaciones
- Hdpe (DSC)Documento1 páginaHdpe (DSC)grupo de cienciasAún no hay calificaciones
- PS (DSC)Documento1 páginaPS (DSC)grupo de cienciasAún no hay calificaciones
- Uniones Entre Atomos IIDocumento25 páginasUniones Entre Atomos IIgrupo de cienciasAún no hay calificaciones
- Ldpe (Tga)Documento1 páginaLdpe (Tga)grupo de cienciasAún no hay calificaciones
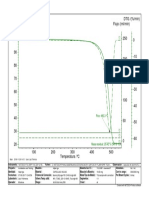
- TG /% Flujo / (Ml/min) DTG / (%/min) : Masa Residual: 21.38 % (548.6 °C)Documento1 páginaTG /% Flujo / (Ml/min) DTG / (%/min) : Masa Residual: 21.38 % (548.6 °C)grupo de cienciasAún no hay calificaciones
- Qto Des eDocumento1 páginaQto Des egrupo de cienciasAún no hay calificaciones
- Enlace QuimicoDocumento17 páginasEnlace Quimicogrupo de cienciasAún no hay calificaciones
- Hdpe (Tga)Documento1 páginaHdpe (Tga)grupo de cienciasAún no hay calificaciones
- Re Suelto en Laces MDocumento30 páginasRe Suelto en Laces Mgrupo de cienciasAún no hay calificaciones
- Enlaces EsquemasDocumento14 páginasEnlaces Esquemasgrupo de cienciasAún no hay calificaciones
- Enlace QuímicoDocumento2 páginasEnlace QuímicoFrancisca Belen VillafrancaAún no hay calificaciones
- TEMA 8 EnlaceDocumento25 páginasTEMA 8 EnlaceInma Artiaga Redondo100% (1)
- Enlace Quimico 2Documento25 páginasEnlace Quimico 2grupo de cienciasAún no hay calificaciones
- Guía Características de Los FascismosDocumento4 páginasGuía Características de Los Fascismosgrupo de cienciasAún no hay calificaciones
- ECONOMIADocumento4 páginasECONOMIAgrupo de cienciasAún no hay calificaciones
- Guía #7 Probabilidad 3° Medio MatemáticaDocumento4 páginasGuía #7 Probabilidad 3° Medio Matemáticagrupo de cienciasAún no hay calificaciones
- LincomicinaDocumento2 páginasLincomicinaMaria AlvarezAún no hay calificaciones
- Esta Di SticaDocumento72 páginasEsta Di SticaLiseth QuinteroAún no hay calificaciones
- ElectrolisisDocumento11 páginasElectrolisisgrupo de cienciasAún no hay calificaciones
- Clase 9Documento7 páginasClase 9grupo de cienciasAún no hay calificaciones
- Evaluación de administración de medicamentos IMDocumento1 páginaEvaluación de administración de medicamentos IMgrupo de ciencias0% (1)
- Practica 6 POTENCIADocumento5 páginasPractica 6 POTENCIAJuan MuñozAún no hay calificaciones
- Informe Torca2Documento5 páginasInforme Torca2Giovanni Lopez PachonAún no hay calificaciones
- ElectricidadDocumento7 páginasElectricidadNicol GuevaraAún no hay calificaciones
- Informe de Fisica 3 N 4Documento16 páginasInforme de Fisica 3 N 4Daniel Aquiño ApolinarioAún no hay calificaciones
- Precaucionesdeinstalacion PDFDocumento11 páginasPrecaucionesdeinstalacion PDFYoedri GarciaAún no hay calificaciones
- Medida Del GAPDocumento3 páginasMedida Del GAPManu de La CruzAún no hay calificaciones
- Fibras ópticas y evolución de las comunicaciones ópticasDocumento14 páginasFibras ópticas y evolución de las comunicaciones ópticasNico PerezAún no hay calificaciones
- Metodos de Localizacion de Fallas en Cables de PotenciaDocumento13 páginasMetodos de Localizacion de Fallas en Cables de PotenciasusanaAún no hay calificaciones
- Modelo Memoria ElectricasDocumento7 páginasModelo Memoria ElectricasFranco Diaz VasquezAún no hay calificaciones
- Circuitos DC en Serie y Paralelo: Simulación y Análisis TeóricoDocumento17 páginasCircuitos DC en Serie y Paralelo: Simulación y Análisis TeóricoGabriela GAún no hay calificaciones
- 740 Automatizado de Inodoros de Bano Con AmbientadorDocumento1 página740 Automatizado de Inodoros de Bano Con AmbientadorPijermanAún no hay calificaciones
- Presupuesto Electrico 12 PostesDocumento4 páginasPresupuesto Electrico 12 PostesMARIO BERAZAAún no hay calificaciones
- Informe Filtro Paso-BandaDocumento11 páginasInforme Filtro Paso-BandaOscar CunalataAún no hay calificaciones
- Problemas de Circuitos SEP. 2017Documento8 páginasProblemas de Circuitos SEP. 2017juan gomezAún no hay calificaciones
- Examen 3 Antenas NRC4223Documento9 páginasExamen 3 Antenas NRC4223Santiago ErickAún no hay calificaciones
- Campos Electrostáticos en Medios MaterialesDocumento8 páginasCampos Electrostáticos en Medios MaterialesAldo David Silva MartinezAún no hay calificaciones
- Ganancia antenaDocumento3 páginasGanancia antenaAaron GerardoAún no hay calificaciones
- P#5 Configuracion Darlington y CascadaDocumento10 páginasP#5 Configuracion Darlington y CascadaJavier VeintimillaAún no hay calificaciones
- Problemas Propuestos Lineas de TransmisionDocumento6 páginasProblemas Propuestos Lineas de TransmisionJosé S. BernalAún no hay calificaciones
- MedidaPotenciaActivaLabElectricasDocumento4 páginasMedidaPotenciaActivaLabElectricasMary Isabel EspinoAún no hay calificaciones
- Rele Wikipedia La Enciclopedia Libre PDFDocumento3 páginasRele Wikipedia La Enciclopedia Libre PDFAB Francisco JuanAún no hay calificaciones
- Prueba 1 - Revisión Del IntentoDocumento5 páginasPrueba 1 - Revisión Del IntentoKevin Torres SilvaAún no hay calificaciones
- 2 Electro - 2020-1 - Unlocked PDFDocumento108 páginas2 Electro - 2020-1 - Unlocked PDFMaximiliano Tomas VAGLIENTIAún no hay calificaciones
- S04 S2 MaterialDocumento19 páginasS04 S2 MaterialAntonio Napa AriasAún no hay calificaciones
- Interacción magnética 40Documento8 páginasInteracción magnética 40Marianitaa SilvanAún no hay calificaciones
- Circuito Electricos 2 - POTENCIADocumento4 páginasCircuito Electricos 2 - POTENCIADarwin Dario Uscacchi ValenciaAún no hay calificaciones
- 41-1 - Medicion de Temperatura PDFDocumento45 páginas41-1 - Medicion de Temperatura PDFlive PazheAún no hay calificaciones
- Informe 4 Circuitos Electronicos 1Documento8 páginasInforme 4 Circuitos Electronicos 1Ricardo D. Alca MejiaAún no hay calificaciones