Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Problem A 707
Cargado por
GontanjimT.Jiménez0 calificaciones0% encontró este documento útil (0 votos)
7 vistas1 páginaEste documento presenta los pasos para ajustar la reacción redox entre permanganato de potasio (KMnO4), sulfato de hierro (II) (FeSO4) y ácido sulfúrico (H2SO4) en medio ácido. Primero identifica los números de oxidación que cambian y escribe las semirreacciones de oxidación y reducción. Luego ajusta los elementos, oxígeno, hidrógeno y carga eléctrica para igualar los electrones transferidos y obtener la ecuación balanceada completa de la reacción.
Descripción original:
3
Título original
Problem a 707
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoEste documento presenta los pasos para ajustar la reacción redox entre permanganato de potasio (KMnO4), sulfato de hierro (II) (FeSO4) y ácido sulfúrico (H2SO4) en medio ácido. Primero identifica los números de oxidación que cambian y escribe las semirreacciones de oxidación y reducción. Luego ajusta los elementos, oxígeno, hidrógeno y carga eléctrica para igualar los electrones transferidos y obtener la ecuación balanceada completa de la reacción.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
7 vistas1 páginaProblem A 707
Cargado por
GontanjimT.JiménezEste documento presenta los pasos para ajustar la reacción redox entre permanganato de potasio (KMnO4), sulfato de hierro (II) (FeSO4) y ácido sulfúrico (H2SO4) en medio ácido. Primero identifica los números de oxidación que cambian y escribe las semirreacciones de oxidación y reducción. Luego ajusta los elementos, oxígeno, hidrógeno y carga eléctrica para igualar los electrones transferidos y obtener la ecuación balanceada completa de la reacción.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 1
PROBLEMAS DE QUÍMICA
ELECTROQUÍMICA
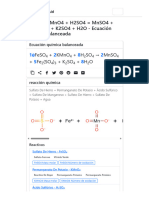
Problema707: Ajusta la siguiente reacción redox en medio ácido:
KMnO4 + FeSO4 + H2SO4 → MnSO4 + Fe2(SO4)3 + K2SO4
KMnO4 + FeSO4 + H2SO4 → MnSO4 + Fe2(SO4)3 + K2SO4
Números de oxidación que cambian: +7 +2
K+ + MnO4− + Fe2+ + SO42− +2H+ + SO42− →
+2 +3
→ Mn2+ + SO42− + 2Fe3+ + 3SO42− + 2K+ + SO42−
+7 +2 +2 +3
MnO4− + Fe2+ → Mn2+ + Fe3+
Semirreacciones: Fe2+ → Fe3+ oxidación
MnO4− → Mn2+ reducción
Ajustar elementos: Fe2+ → Fe3+
MnO4− → Mn2+
Ajustar oxígeno: Fe2+ → Fe3+
MnO4− → Mn2+ + 4 H2O
Ajustar hidrógeno: Fe2+ → Fe3+
MnO4− + 8 H+ → Mn2+ + 4 H2O
Ajustar carga: Fe2+ → Fe3+ + e−
MnO4− + 8 H+ + 5e− → Mn2+ + 4 H2O
Igualar e−: 5 Fe2+ → 5 Fe3+ + 5 e−
MnO4− + 8 H+ + 5e− → Mn2+ + 4 H2O
Sumar y añadir iones de MnO4− + 5 Fe2+ + 8 H+ → Mn2+ + 5 Fe3+ + 4 H2O
acompañamiento: 2 KMnO4 + 10 FeSO4 + 8 H2SO4 → 2 MnSO4 + 5 Fe2(SO4)3 +
K2SO4 + 8 H2O
www.alonsoformula.com Carlos Alonso
También podría gustarte
- Redos Kmno4 Feso4 PDFDocumento1 páginaRedos Kmno4 Feso4 PDFmangora7Aún no hay calificaciones
- Guía de Balanceo Ion Electron en Medio Acido y BasicoDocumento26 páginasGuía de Balanceo Ion Electron en Medio Acido y BasicodayanaAún no hay calificaciones
- QuímicaDocumento56 páginasQuímicaLuisa Adriana Ríos CandilaAún no hay calificaciones
- CUESTIONARIO Docxinforme6Documento4 páginasCUESTIONARIO Docxinforme6Bianca LeyvaAún no hay calificaciones
- Can Bang Oxh KH H63Documento2 páginasCan Bang Oxh KH H63Hưng Nguyễn TuấnAún no hay calificaciones
- Reaccion RedoxDocumento6 páginasReaccion RedoxArreceygor AmoblamientosAún no hay calificaciones
- Guia RedoxDocumento3 páginasGuia RedoxDaxter Del Canto FábilaAún no hay calificaciones
- G 2020-B Profeso Eneral Ii R: Dr. Diego A. Lomelí Rosales: I/Departamento de Química/Academia de Química GeneralDocumento10 páginasG 2020-B Profeso Eneral Ii R: Dr. Diego A. Lomelí Rosales: I/Departamento de Química/Academia de Química GeneralMoMoAún no hay calificaciones
- Quim2 Soluciones Tema 6.oxido ReduccionDocumento43 páginasQuim2 Soluciones Tema 6.oxido ReduccionAndy LilaAún no hay calificaciones
- Método Ion ElectrónDocumento2 páginasMétodo Ion ElectrónAndrés AhumadaAún no hay calificaciones
- Oxidación-Reducción. Soluciones EjerciciosDocumento31 páginasOxidación-Reducción. Soluciones EjerciciosDaniel RMAún no hay calificaciones
- Capitulo V - Volumetría Oxido-Reducción FIQ-2023-IDocumento6 páginasCapitulo V - Volumetría Oxido-Reducción FIQ-2023-IWilinster ReateguiAún no hay calificaciones
- Unidad 10 Ejercicios Con SolucionesDocumento64 páginasUnidad 10 Ejercicios Con Solucionesja.quintana.cillerueloAún no hay calificaciones
- Actividades Equipo 5Documento15 páginasActividades Equipo 5Fanne Ortíz100% (1)
- Balanceo Tanteo-RedoxDocumento2 páginasBalanceo Tanteo-RedoxCliver Adriano Velarde SoteloAún no hay calificaciones
- Unidad IV - Ejercicios de RedoxDocumento11 páginasUnidad IV - Ejercicios de RedoxEmilio FerroAún no hay calificaciones
- Hóa học 10 - Cân bằng phản ứng oxi hóa khửDocumento2 páginasHóa học 10 - Cân bằng phản ứng oxi hóa khửquanganh123.qanAún no hay calificaciones
- Volumetria REDXDocumento35 páginasVolumetria REDXEsthefany Aguilar GomezAún no hay calificaciones
- CUESTIONARIO Titulacion RedoxDocumento3 páginasCUESTIONARIO Titulacion RedoxDiego MontenegroAún no hay calificaciones
- Método RedoxDocumento2 páginasMétodo RedoxAndrés AhumadaAún no hay calificaciones
- Tarea 12 Valoraciones Redox y Aplicaciones PotenciométricasDocumento3 páginasTarea 12 Valoraciones Redox y Aplicaciones PotenciométricasDanielaAún no hay calificaciones
- Ejercicios de Reacciones y BalanceoDocumento1 páginaEjercicios de Reacciones y BalanceoLost Generation100% (1)
- RedoxDocumento14 páginasRedoxJavy EspíndolaAún no hay calificaciones
- Tarea: Balance de Ecuaciones Químicas: Química de Las Sustancias Puras Valerio Gallardo Pamela Joselyn Grupo: 1IM25Documento4 páginasTarea: Balance de Ecuaciones Químicas: Química de Las Sustancias Puras Valerio Gallardo Pamela Joselyn Grupo: 1IM25Joselyn GLAún no hay calificaciones
- EXAMENDocumento6 páginasEXAMENLis VeraAún no hay calificaciones
- KMN O4Documento8 páginasKMN O4Israel NarvastaAún no hay calificaciones
- 1) Completar Y Ajustar Las Siguientes Reacciones:: Hcns + 3Br + 4H O + 6H + 6E H So + 6Hbr + HCN + 6H + 6EDocumento4 páginas1) Completar Y Ajustar Las Siguientes Reacciones:: Hcns + 3Br + 4H O + 6H + 6E H So + 6Hbr + HCN + 6H + 6EShery Dayanira Mendoza VeraAún no hay calificaciones
- 05 - Motafawik.com - تمارين في موازنة المعادلات الكيميائية مع الحلولDocumento9 páginas05 - Motafawik.com - تمارين في موازنة المعادلات الكيميائية مع الحلولbig bossAún no hay calificaciones
- Budget de Formation Des Quations de Raction ChimiqueDocumento9 páginasBudget de Formation Des Quations de Raction Chimiquebig bossAún no hay calificaciones
- NeutralizacionDocumento1 páginaNeutralizacionMateowright13Aún no hay calificaciones
- Sexto UrgenteDocumento5 páginasSexto UrgenteFisicastiyopAún no hay calificaciones
- Def QuimicaDocumento5 páginasDef QuimicaCastillo Cabos ChristianAún no hay calificaciones
- Balanceo Ion Electron-2Documento2 páginasBalanceo Ion Electron-2Ivan Olaya100% (1)
- Re Acci OnesDocumento4 páginasRe Acci OnesCarlos MeraAún no hay calificaciones
- Igualacion de Ecuaciones-1Documento14 páginasIgualacion de Ecuaciones-1La belleza no es universal100% (1)
- 7 Diagrama de Flujo BiolixiviacionDocumento1 página7 Diagrama de Flujo BiolixiviacionAlexis Chunga Reupo100% (1)
- Unidad 7 Reacciones de Transferencia de Protones. Oxidacion ReduccionDocumento11 páginasUnidad 7 Reacciones de Transferencia de Protones. Oxidacion ReduccionoficinadirectaAún no hay calificaciones
- Balanceo de Ecuaciones Quimicas Por TanteoDocumento2 páginasBalanceo de Ecuaciones Quimicas Por Tanteo7teachercarlos100% (2)
- Bloque 4 Primera ParteDocumento25 páginasBloque 4 Primera PartejaiderAún no hay calificaciones
- Redox y La Aplicación de La Estequiometría PDFDocumento35 páginasRedox y La Aplicación de La Estequiometría PDFwilmer vargasAún no hay calificaciones
- SEMANA 4 - Reacciones QuímicasDocumento21 páginasSEMANA 4 - Reacciones QuímicasAnthony Ramirez DavilaAún no hay calificaciones
- ReactiiredoxDocumento1 páginaReactiiredoxDiana LucaciAún no hay calificaciones
- 05 - Método Ión-ElectrónDocumento19 páginas05 - Método Ión-ElectrónHANNAH CAMILA MELECIO CALVOAún no hay calificaciones
- Tema 11Documento55 páginasTema 11Diana Diez PrietoAún no hay calificaciones
- 2do Ejercicio RedoxDocumento22 páginas2do Ejercicio Redoxchems pana cheemsAún no hay calificaciones
- cân bằng ptDocumento16 páginascân bằng ptTra GiangAún no hay calificaciones
- Problemas de Oxido-Reducción PDFDocumento11 páginasProblemas de Oxido-Reducción PDFmitzyanaAún no hay calificaciones
- FeSO4 + KMnO4 + H2SO4 MnSO4 + Fe2 (SO4) 3 + K2SO4 + H2O - Ecuación Química BalanceadaDocumento5 páginasFeSO4 + KMnO4 + H2SO4 MnSO4 + Fe2 (SO4) 3 + K2SO4 + H2O - Ecuación Química BalanceadaGontanjimT.JiménezAún no hay calificaciones
- Bai Tap Can Bang Phuong Trinh Hoa Hoc Lop 8Documento5 páginasBai Tap Can Bang Phuong Trinh Hoa Hoc Lop 8Nguyễn Vĩnh MạnhAún no hay calificaciones
- Trabajo de Clase 3Documento17 páginasTrabajo de Clase 3Jose Arnaldo Lupaca QuispeAún no hay calificaciones
- Trabajo de Clase 3Documento17 páginasTrabajo de Clase 3Jose Arnaldo Lupaca QuispeAún no hay calificaciones
- Práctica #8Documento13 páginasPráctica #8ROSMERY TATIANA ORTEGA MUÑOZAún no hay calificaciones
- Annotated-Informe 8Documento8 páginasAnnotated-Informe 8Ivan David Silva MoscolAún no hay calificaciones
- Balanceom RedoxDocumento5 páginasBalanceom RedoxFrancisco MestanzaAún no hay calificaciones
- Tarea Balanceo Ion Electron BDocumento1 páginaTarea Balanceo Ion Electron BBrayan YoseftAún no hay calificaciones
- Tarea 2 KATHERINEDocumento9 páginasTarea 2 KATHERINEktrncrvjlAún no hay calificaciones
- Balanceo de Ecuaciones RedoxDocumento2 páginasBalanceo de Ecuaciones Redoxjosuedavidnarvaezjaimes5Aún no hay calificaciones
- 2 BalanceoDocumento3 páginas2 BalanceoBethy NicasioAún no hay calificaciones
- 3 Balanceo PDFDocumento3 páginas3 Balanceo PDFYadiraAún no hay calificaciones
- Grandes Filosofos ImagnesestudiosDocumento1 páginaGrandes Filosofos ImagnesestudiosGontanjimT.JiménezAún no hay calificaciones
- Materia Biología 1 Trime 2 (2) YADocumento2 páginasMateria Biología 1 Trime 2 (2) YAGontanjimT.JiménezAún no hay calificaciones
- Materia Bilogia 1Documento5 páginasMateria Bilogia 1GontanjimT.JiménezAún no hay calificaciones
- Materia Biología 1 Trime 2 (1) YADocumento6 páginasMateria Biología 1 Trime 2 (1) YAGontanjimT.JiménezAún no hay calificaciones
- Catequesis de La Unidad Educativa Fiscomisional La DolorosaDocumento1 páginaCatequesis de La Unidad Educativa Fiscomisional La DolorosaGontanjimT.JiménezAún no hay calificaciones
- Formulario 3RA MTRICULADocumento12 páginasFormulario 3RA MTRICULAGontanjimT.JiménezAún no hay calificaciones