Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Linea de Tiempo Sofía Soto 10A
Cargado por
sofiahaydar17Descripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Linea de Tiempo Sofía Soto 10A
Cargado por
sofiahaydar17Copyright:
Formatos disponibles
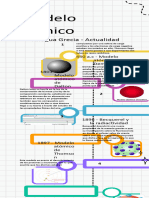
LÍNEA DE TIEMPO
- LOS MODELOS ATÓMICOS -
Teoría Cuántica de Planck
(1900):
Propuso la teoría cuántica al explicar el
fenómeno de la radiación del cuerpo
negro mediante cuantos de energía.
Introdujo el concepto de cuantización,
donde la energía no es continua, sino
que está cuantizada en unidades
Siglo X a.C Democrito discretas llamadas "cuantos".
Propuso la idea de que la materia
está compuesta por partículas
indivisibles llamadas átomos.
Aunque sus ideas no se basaban
en evidencia experimental,
sentaron las bases conceptuales
para la teoría atómica.
Experimento de la Lámina
delgada de Oro (Rutherford,
1909):
Llevó a cabo un experimento que
reveló la estructura interna del átomo,
descubriendo que la mayor parte de la
masa se encuentra en un núcleo denso
en el centro, desafiando el modelo de
Ley de Conservación de Thomson.
la Masa (Lavoisier, 1789):
Antoine Lavoisier enunció la ley que
establece que la masa total en un
sistema cerrado se conserva durante
las reacciones químicas.
Modelo Atómico de Bohr
(1913):
Propuso un modelo en el que los
electrones se mueven en órbitas
cuantizadas alrededor del núcleo,
explicando de manera exitosa el espectro
de líneas del hidrógeno y aportando a la
comprensión de la cuantización en el
Leyes de las Proporciones átomo.
Definidas y Múltiples (Proust,
1799):
Joseph Proust formuló las leyes que
afirmaban que los elementos se
combinan en proporciones definidas y
múltiples para formar compuestos.
Modelo de Ondas de
Schrödinger (1926):
Desarrolló la mecánica cuántica,
describiendo los electrones como
ondas de probabilidad, eliminando la
idea de órbitas fijas y proporcionando
una visión más precisa de la ubicación
Modelo Atómico de de los electrones en el átomo.
Dalton (1803):
John Dalton propuso que los átomos
son partículas indivisibles y que los
elementos se combinan en
proporciones fijas para formar
compuestos.
SOFÍA SOTO HAYDAR 10A
También podría gustarte
- Modelo AtomicoDocumento4 páginasModelo AtomicoRoberto Lopez HernándezAún no hay calificaciones
- Actividad de Aprendizaje Biii Modelo Atomico-1Documento3 páginasActividad de Aprendizaje Biii Modelo Atomico-1Angie OchoaAún no hay calificaciones
- INFOGRAFÍADocumento1 páginaINFOGRAFÍAcarreradiego175Aún no hay calificaciones
- Línea de Tiempo Modelos Atomicos 1 23Documento5 páginasLínea de Tiempo Modelos Atomicos 1 23Vazquez RogelioAún no hay calificaciones
- Historia de Los Modelos Atómicosy Modelo Mecanico CuanticoDocumento20 páginasHistoria de Los Modelos Atómicosy Modelo Mecanico CuanticoDELMY ISABEL ÁLVAREZ VILLAFRANCOAún no hay calificaciones
- Atomos y Enlaces QuimicoDocumento5 páginasAtomos y Enlaces Quimicogevipo7855Aún no hay calificaciones
- Modelos AtomicosDocumento14 páginasModelos AtomicosFLAVIA VALENTINAAún no hay calificaciones
- Mapa de Tiempo Del Átomo - QuímicaDocumento5 páginasMapa de Tiempo Del Átomo - QuímicaDavid FarinangoAún no hay calificaciones
- 3ºA Carazas Linea de Tiempo AtomoDocumento26 páginas3ºA Carazas Linea de Tiempo AtomoAmparo Rodriguez0% (1)
- Modulo - 3 - Teorias AtómicasDocumento4 páginasModulo - 3 - Teorias Atómicasrideroy0105Aún no hay calificaciones
- Modelos AtómicosDocumento1 páginaModelos AtómicosSolano Torres SaraAún no hay calificaciones
- Línea de Tiempo Modelos Atomicos - Velasco SantiagoDocumento3 páginasLínea de Tiempo Modelos Atomicos - Velasco SantiagoSantiago Vs100% (1)
- Modelo AtómicoDocumento7 páginasModelo AtómicoLópez Pérez DanielAún no hay calificaciones
- 6 Modelos Atomicos IlustradosDocumento6 páginas6 Modelos Atomicos IlustradosGiovanni CruzAún no hay calificaciones
- Tríptico Modelos AtómicosDocumento2 páginasTríptico Modelos AtómicosEtian JaraAún no hay calificaciones
- Linea Del Tiempo Modelos AtómicosDocumento2 páginasLinea Del Tiempo Modelos AtómicosLore DLAún no hay calificaciones
- Personal BestDocumento5 páginasPersonal BestNachoo SosaaaAún no hay calificaciones
- Tarea 2 Historia Del Modelo AtomicoDocumento3 páginasTarea 2 Historia Del Modelo AtomicoJacqueline Trinidad EvangelistaAún no hay calificaciones
- Modelos AtómicosDocumento4 páginasModelos AtómicosRaulZorrillaAún no hay calificaciones
- Linea de Tiempo de Las Teorías AtómicasDocumento1 páginaLinea de Tiempo de Las Teorías Atómicasmjocabed2004Aún no hay calificaciones
- Atomos y Modelos Atomicos PDFDocumento2 páginasAtomos y Modelos Atomicos PDFjessica ardila100% (1)
- Resumen Modelos AtómicosDocumento6 páginasResumen Modelos Atómicosyour.worst.nightmare79417873Aún no hay calificaciones
- Modulo 3 Teorias AtómicasDocumento4 páginasModulo 3 Teorias AtómicasAnghela Robles CotrinaAún no hay calificaciones
- Expo de Quimica Modelo AtomicoDocumento34 páginasExpo de Quimica Modelo AtomicoLedezma MaciasAún no hay calificaciones
- 1.-Modelos AtomicosDocumento23 páginas1.-Modelos Atomicosalanalambre2607Aún no hay calificaciones
- Modelos AtomicosDocumento6 páginasModelos AtomicosBy Miguel - clash royal y másAún no hay calificaciones
- Linea Del Tiempo Modelos AtómicosDocumento1 páginaLinea Del Tiempo Modelos AtómicosBEIDA ISABEL PEREZ MIRANDAAún no hay calificaciones
- Modelos AtomicosDocumento10 páginasModelos AtomicosDana JardonAún no hay calificaciones
- Unidad 2 Estructura Atómica PDFDocumento16 páginasUnidad 2 Estructura Atómica PDFmynoa rinetteAún no hay calificaciones
- Modelos AtomicosDocumento5 páginasModelos AtomicosDiter VazquezAún no hay calificaciones
- Modelos Atómicos - PPTX 1Documento9 páginasModelos Atómicos - PPTX 1wilmerAún no hay calificaciones
- Modelos AtómicosDocumento7 páginasModelos AtómicosNelson-black-master130Aún no hay calificaciones
- Sumativa 1, Teoria Atomica, Giovanni RodriguezDocumento13 páginasSumativa 1, Teoria Atomica, Giovanni RodriguezGiovanni RodriguezAún no hay calificaciones
- TI-2 Teoría AtómicaDocumento10 páginasTI-2 Teoría AtómicaMax Perez LealAún no hay calificaciones
- Modelos AtómicosDocumento7 páginasModelos AtómicosJulia Peralta MeloAún no hay calificaciones
- Modelos AtomicosDocumento6 páginasModelos AtomicosJESSICA LIZETTE HERNANDEZ DIAZAún no hay calificaciones
- Qui MicaDocumento235 páginasQui MicaJupiter GonzalezAún no hay calificaciones
- Espo de Linea Del TiempoDocumento5 páginasEspo de Linea Del TiempoMiguel AleAún no hay calificaciones
- MÓDULO 2 - Fundamentos de QuímicaDocumento52 páginasMÓDULO 2 - Fundamentos de Químicajose.torres1Aún no hay calificaciones
- Modelos AtómicosDocumento5 páginasModelos Atómicosleydimar0% (1)
- Tarea Evidencias de Estructura AtómicaDocumento5 páginasTarea Evidencias de Estructura Atómicaalanntorres09ctrlAún no hay calificaciones
- Modelo Atomico de RutherfordDocumento7 páginasModelo Atomico de RutherfordAlejandro122009Aún no hay calificaciones
- La Materia y Los ÁtomosDocumento3 páginasLa Materia y Los ÁtomosAMBAR SUÁREZAún no hay calificaciones
- Teorias AtomicasDocumento2 páginasTeorias AtomicasEl RISASAún no hay calificaciones
- Modelos AtómicosDocumento8 páginasModelos AtómicosLuciano Pizaña ZamoraAún no hay calificaciones
- Investigación 1 - Química BásicaDocumento8 páginasInvestigación 1 - Química BásicaJosafat S. TapiaAún no hay calificaciones
- Mat QuímicaDocumento11 páginasMat QuímicaJessica García LópezAún no hay calificaciones
- Los Modelos Atomicos y Su HistoriaDocumento5 páginasLos Modelos Atomicos y Su HistoriaKennia Rivera GuapulemaAún no hay calificaciones
- Modelos Atomicos 8 BasicoDocumento17 páginasModelos Atomicos 8 BasicoPao Veliz GonzalezAún no hay calificaciones
- Deberes de QuimicaDocumento3 páginasDeberes de QuimicaDeyviss CzzAún no hay calificaciones
- Los Modelos Atómicos ResumenDocumento2 páginasLos Modelos Atómicos Resumenhaxlolog044Aún no hay calificaciones
- Actividades Química 4Documento10 páginasActividades Química 4valentinauruenaaAún no hay calificaciones
- Lectura 7 Modelos Atómicos.Documento5 páginasLectura 7 Modelos Atómicos.pablinlopezlarra04Aún no hay calificaciones
- La Mecánica CuánticaDocumento7 páginasLa Mecánica CuánticaDYLAN DAVID SALAZAR HERRERAAún no hay calificaciones
- Modelos AtomicosDocumento24 páginasModelos Atomicosjimezas100% (3)
- Modelos AtómicosDocumento2 páginasModelos AtómicosCamila GomezAún no hay calificaciones
- Modelo Satomi CosDocumento20 páginasModelo Satomi CosMay MartinezAún no hay calificaciones
- Modelos AtómicosDocumento2 páginasModelos AtómicosSo VAún no hay calificaciones