Documentos de Académico
Documentos de Profesional
Documentos de Cultura
El Tío Tungsteno, Una Luz Brillante
Cargado por
MARÍA JOSÉ ROJAS RIVASDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
El Tío Tungsteno, Una Luz Brillante
Cargado por
MARÍA JOSÉ ROJAS RIVASCopyright:
Formatos disponibles
En 1815 se conocían cincuenta y pico átomos
William Prout conjeturó que el hidrógeno era de
hecho el elemento primordial, y que todos los demás
elementos habían sido construidos a partir de él.
Átomos
condensación natural
masas atómicas fraccionarias
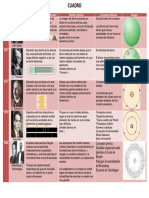
Mendeléiev hizo la tabla periódica.
Tabla Periódica Vio que el incremento de la frecuencia mostraba
saltos bruscos y discretos al pasar de un elemento a
otro.
En 1913, Henry Moseley, comenzó a investigar
átomos con la técnica recién desarrollada de la
espectroscopia de rayos X.
Moseley pensó que eso tenía que reflejar una El descubrimiento de Moseley le permitió «pasar
Si había un hueco, significaba que faltaba un
propiedad atómica fundamental, y que ésa sólo podía lista» de los elementos. En la secuencia no podía Faltaban siete elementos aun por descubrir
elemento.
ser la carga nuclear. haber ningún hueco.
Las «anomalías» que acompañaban a las masas
atómicas se resolvieron
Los números atómicos se habían utilizado El número atómico indicaba la carga nuclear, indicaba
anteriormente para indicar la secuencia ordinal de los Moseléy les dio auténtico significado la identidad del elemento, su identidad química, de
Anomalías de las masa atómicas elementos clasificados por su masa atómica una manera absoluta y segura.
Fallaba el modelo de átomo de Rutherford por los
Rutherford y Moseley se habían interesado electrones
principalmente por el núcleo del átomo, su masa y sus
El tío tungsteno, una luz unidades de carga eléctrica. Según la física clásica maxwelliana, un átomo basado
en el modelo de sistema solar no podía funcionar.
brillante
En 1913, unifico el modelo atómico de Rutherford y
la teoría cuántica de Planck.
Consideró que todos los elementos podían La posición de cada elemento en la tabla periódica
construirse de manera sistemática, y, de manera representaba el número de electrones de sus
Niels Bohr
natural, ocuparían los lugares que les correspondían átomos, y la reactividad y unión de cada elemento
en la tabla periódica. podían verse en términos electrónicos
Sugería los elementos de transición.
Bohr, Einstein y Moseley Había utilizado la idea en relación con los efectos
Einstein fotoeléctricos, la teoría cuántica y su potencial
revolucionario había sido
Moseley y Bohr habían dejado claro que la tabla
periódica se basaba en una serie numérica
Moseley
fundamental que determinaba el número de
elementos de cada período
La de que los átomos de los elementos ligeros,
Surgió una nueva idea dadas las prodigiosas temperaturas y presiones que
había en el interior de una estrella,
1929
la famosa fórmula de Einstein e = mc2
En las estrelllas
Bohr había imaginado una Aufbau, una construcción
de todos los elementos comenzando por el
hidrógeno, pero resultaba que tal Aufbau tenía lugar
en las estrellas.
También podría gustarte
- ModelosDocumento3 páginasModelosricky hernandezAún no hay calificaciones
- Quimica DanielDocumento13 páginasQuimica DanielDannySalcedoAún no hay calificaciones
- Tarea Evidencias de Estructura AtómicaDocumento5 páginasTarea Evidencias de Estructura Atómicaalanntorres09ctrlAún no hay calificaciones
- Estructura Del Atomo - Linea de TiempoDocumento3 páginasEstructura Del Atomo - Linea de TiempopotterheadAún no hay calificaciones
- Ventajas y Desventajas de Los Modelos AtomicosDocumento7 páginasVentajas y Desventajas de Los Modelos AtomicosDanelys FranklinAún no hay calificaciones
- Quimica - 4 ToDocumento5 páginasQuimica - 4 ToVictor Huerta RojasAún no hay calificaciones
- Teorias AtomicasDocumento5 páginasTeorias AtomicasIñaki Cancino SanchezAún no hay calificaciones
- Mode AtomicoDocumento8 páginasMode AtomicoSolanlly Araujo MaestreAún no hay calificaciones
- Modelos AtomicosDocumento20 páginasModelos AtomicosElkin Javier RodriguezAún no hay calificaciones
- Estructura Atómica Parte 1Documento1 páginaEstructura Atómica Parte 1fuamencioAún no hay calificaciones
- Modelos HistoricosDocumento10 páginasModelos HistoricosSusana ChicasAún no hay calificaciones
- Atomos y Enlaces QuimicoDocumento5 páginasAtomos y Enlaces Quimicogevipo7855Aún no hay calificaciones
- La Lectura AtómicaDocumento20 páginasLa Lectura AtómicaGabriel MarinAún no hay calificaciones
- Quà Mica I BQ UD 2 PDFDocumento107 páginasQuà Mica I BQ UD 2 PDFPaulaAún no hay calificaciones
- Infografía CronológicaDocumento3 páginasInfografía Cronológicaandy08mdzAún no hay calificaciones
- Teorías AtómicasDocumento5 páginasTeorías AtómicasAlejandro SegoviaAún no hay calificaciones
- AtomosDocumento1 páginaAtomosMariana Jimenez San MiguelAún no hay calificaciones
- Estructura de La Materia 2018Documento82 páginasEstructura de La Materia 2018samioAún no hay calificaciones
- Química PREDocumento4 páginasQuímica PREVictor Huerta RojasAún no hay calificaciones
- Teoría Atómica y Estructura de La Materia Equipo 3Documento23 páginasTeoría Atómica y Estructura de La Materia Equipo 3lesliemartinezAún no hay calificaciones
- Modelos AtomicosDocumento3 páginasModelos AtomicosFrancia GonzalezAún no hay calificaciones
- Cuadro Comparativo de Los Modelos AtomicosDocumento1 páginaCuadro Comparativo de Los Modelos Atomicoslautarobre10Aún no hay calificaciones
- Modelos AtómicosDocumento15 páginasModelos AtómicosCarlosAún no hay calificaciones
- CONFORMACION DE LA MATERIA - PPT (Autoguardado)Documento35 páginasCONFORMACION DE LA MATERIA - PPT (Autoguardado)ABISAI BENITEZ CRUZAún no hay calificaciones
- Actividad 03 U1 Cuadro Comparativo - Gustavo Rubio RafaelDocumento3 páginasActividad 03 U1 Cuadro Comparativo - Gustavo Rubio RafaelGustavo RubioAún no hay calificaciones
- XX - Copia de 4 - Quimica II 1roDocumento29 páginasXX - Copia de 4 - Quimica II 1roRenzo AntonioAún no hay calificaciones
- Linea de Tiempo - Estructura MolecularDocumento3 páginasLinea de Tiempo - Estructura MolecularDeyanira GonzalezAún no hay calificaciones
- 1 Modelo Atómico PDFDocumento25 páginas1 Modelo Atómico PDFISRAELAún no hay calificaciones
- Historia Del ÁtomoDocumento5 páginasHistoria Del ÁtomoEnrique MedinaAún no hay calificaciones
- Teoría AtómicaDocumento6 páginasTeoría AtómicaAngello MolinaAún no hay calificaciones
- 3 Semana Q - BQ - 2023 - 1Documento66 páginas3 Semana Q - BQ - 2023 - 1EilynAún no hay calificaciones
- Cuadro Comparativos de Los Modelos AtomicosDocumento1 páginaCuadro Comparativos de Los Modelos AtomicosJuan Cruz EmmaAún no hay calificaciones
- Historia Del AtomoDocumento9 páginasHistoria Del Atomokaren diazAún no hay calificaciones
- Quimica Linea de TiempoDocumento1 páginaQuimica Linea de TiempoAngel Ricardo Medina De La CruzAún no hay calificaciones
- Clase 2 Estructura AtomicaDocumento128 páginasClase 2 Estructura AtomicaDaniela Sierra Quiroz50% (2)
- Experimentos de ÁtomosDocumento3 páginasExperimentos de ÁtomosViviana LascanoAún no hay calificaciones
- Apuntes QI UNIDAD II RAP 1Documento10 páginasApuntes QI UNIDAD II RAP 1Akiriz MostazaAún no hay calificaciones
- Teoria AtomicaDocumento5 páginasTeoria Atomicaalejandra garciaAún no hay calificaciones
- Atomo Historia Actualidad y PerspectivasDocumento7 páginasAtomo Historia Actualidad y PerspectivasPaco MartinezAún no hay calificaciones
- Demócrito y Leucipo Fueron Dos Filósofos Griegos PreDocumento3 páginasDemócrito y Leucipo Fueron Dos Filósofos Griegos Prersaenzmercado18Aún no hay calificaciones
- La Teoría Atómica Unidad 2Documento3 páginasLa Teoría Atómica Unidad 2Luis Manuel Garcia de la CruzAún no hay calificaciones
- Actividad 2Documento10 páginasActividad 2Marcos Atilano Alan EduardoAún no hay calificaciones
- Quimica Sem 04Documento4 páginasQuimica Sem 04Jordan G.SAún no hay calificaciones
- Infografía Modelos AtómicosDocumento1 páginaInfografía Modelos AtómicosRoberto Ramírez86% (14)
- Cuadro Comparativos de Los Modelos AtomicosDocumento1 páginaCuadro Comparativos de Los Modelos AtomicosSamuel Fernando Delgado67% (3)
- Particulasfundamentales y Los Usos de La Energia NuclearDocumento2 páginasParticulasfundamentales y Los Usos de La Energia Nuclearnorma riveraAún no hay calificaciones
- Excelente Estructura Atómica, Modelos, Tabla y Prop PeriodicasDocumento21 páginasExcelente Estructura Atómica, Modelos, Tabla y Prop PeriodicasJuan Ignacio FabregasAún no hay calificaciones
- Quimica BasicaDocumento2 páginasQuimica BasicaGuillermo Montero HerreraAún no hay calificaciones
- Guía N°3 - Módelo y Estructura AtómicaDocumento5 páginasGuía N°3 - Módelo y Estructura AtómicaAngrySquirl 24Aún no hay calificaciones
- Quimica 4 - La Sinfonia de La Tabla PeriodicaDocumento10 páginasQuimica 4 - La Sinfonia de La Tabla Periodicasabrina permigianiAún no hay calificaciones
- Estructura de La MateriaDocumento3 páginasEstructura de La MateriaOmar Cubillas LuyoAún no hay calificaciones
- Morado y Verde Animado Patrón Abstracto Proyecto de Grupo Presentación de EducaciónDocumento16 páginasMorado y Verde Animado Patrón Abstracto Proyecto de Grupo Presentación de EducaciónIVANNA VERA HUERTAAún no hay calificaciones
- Cuadro Comparativo de Los Modelos AtómicosDocumento4 páginasCuadro Comparativo de Los Modelos AtómicosedinsonatmAún no hay calificaciones
- 711 Guia 1 Modelos AtómicosDocumento2 páginas711 Guia 1 Modelos AtómicosMaria CarrilloAún no hay calificaciones
- Cuadro Comparativo, Ortiz Rondón Rogger Joaquín, C.I 28.650.780, Sección 01Documento3 páginasCuadro Comparativo, Ortiz Rondón Rogger Joaquín, C.I 28.650.780, Sección 01Rogger Rjor100% (1)
- Modelos AtómicosDocumento1 páginaModelos AtómicosIgnacio HerreroAún no hay calificaciones
- Teoria Del Modelo Atomico - Udem Sem1Documento8 páginasTeoria Del Modelo Atomico - Udem Sem1sandyAún no hay calificaciones
- Infografia Línea Del Tiempo Historia Timeline Doodle MulticolorDocumento1 páginaInfografia Línea Del Tiempo Historia Timeline Doodle MulticolorPatricia HernándezAún no hay calificaciones
- Modelos Atómicos INGRID PAMELA.Documento3 páginasModelos Atómicos INGRID PAMELA.Juan Abel RochaAún no hay calificaciones
- Batería 4.4: Nombre Del Alumno: - Número de Lista: - Fecha: 27/03/23 Grado: 2 GrupoDocumento1 páginaBatería 4.4: Nombre Del Alumno: - Número de Lista: - Fecha: 27/03/23 Grado: 2 GrupoMARÍA JOSÉ ROJAS RIVASAún no hay calificaciones
- Planeación Crónica PDFDocumento3 páginasPlaneación Crónica PDFMARÍA JOSÉ ROJAS RIVASAún no hay calificaciones
- Cronología de La Invasión Francesa A España (Con Memes)Documento7 páginasCronología de La Invasión Francesa A España (Con Memes)MARÍA JOSÉ ROJAS RIVASAún no hay calificaciones
- Riesgos de La TecnologíaDocumento1 páginaRiesgos de La TecnologíaMARÍA JOSÉ ROJAS RIVASAún no hay calificaciones
- Bateria 4.1 Números de Oxidación 2022-2023Documento1 páginaBateria 4.1 Números de Oxidación 2022-2023MARÍA JOSÉ ROJAS RIVASAún no hay calificaciones
- Artículo 12Documento1 páginaArtículo 12MARÍA JOSÉ ROJAS RIVASAún no hay calificaciones
- El Pasado Indígena 2Documento1 páginaEl Pasado Indígena 2MARÍA JOSÉ ROJAS RIVASAún no hay calificaciones
- CV Victor Rojas - VFDocumento2 páginasCV Victor Rojas - VFMARÍA JOSÉ ROJAS RIVASAún no hay calificaciones
- El Combate Al Narcotráfico en México y en El Mundo.Documento1 páginaEl Combate Al Narcotráfico en México y en El Mundo.MARÍA JOSÉ ROJAS RIVASAún no hay calificaciones
- RobertDocumento14 páginasRobertAlbert Romero AquinoAún no hay calificaciones
- Solucionario-1era SeparataDocumento23 páginasSolucionario-1era Separatayekuz100% (9)
- Materia y ComposicionDocumento2 páginasMateria y ComposicionAses de la MatematicaAún no hay calificaciones
- Números CuánticosDocumento4 páginasNúmeros CuánticosMtra Sofy ChaconAún no hay calificaciones
- Trabajo Creativo CiclotrónDocumento6 páginasTrabajo Creativo CiclotrónAlexandra Ocampo CamargoAún no hay calificaciones
- Efectos Cuanticos Y Relativistas en El GrafenoDocumento5 páginasEfectos Cuanticos Y Relativistas en El GrafenoRubenAún no hay calificaciones
- PROBLEMARIO 1er DEP CyD A20Documento4 páginasPROBLEMARIO 1er DEP CyD A20Ivan Carpio VilchisAún no hay calificaciones
- Prueba Química Modelos AtómicosDocumento6 páginasPrueba Química Modelos AtómicosIvonneAedoGonzálezAún no hay calificaciones
- Capitulo 1 Motores Jaula de ArdillaDocumento52 páginasCapitulo 1 Motores Jaula de Ardillaronald javierAún no hay calificaciones
- Ejercicios: ContenidoDocumento17 páginasEjercicios: ContenidoReyes RbcAún no hay calificaciones
- Prueba BimestralDocumento2 páginasPrueba BimestralCRISTIAN ESNEIDER PINZON TOPALAún no hay calificaciones
- Radiologia MenorDocumento20 páginasRadiologia Menorfrancisca conchaAún no hay calificaciones
- Taller Fisica III Efectos CuánticosDocumento4 páginasTaller Fisica III Efectos CuánticosLeo Quintero Pérez0% (1)
- Cobalto-60 en CD Juarez Rev 3Documento6 páginasCobalto-60 en CD Juarez Rev 3CARMEN ALICIA FARPON RUIZAún no hay calificaciones
- Generadores de Radiación ClínicosDocumento14 páginasGeneradores de Radiación ClínicosCesia ArgüellesAún no hay calificaciones
- Resolucion Practica 2Documento5 páginasResolucion Practica 2Enrique AlbertoAún no hay calificaciones
- Electroterapia 1Documento140 páginasElectroterapia 1andres raul Bruno SaraviaAún no hay calificaciones
- Las Teorias AtomistasDocumento5 páginasLas Teorias AtomistasOscar MartínezAún no hay calificaciones
- Configuracion Electronica EjemplosDocumento19 páginasConfiguracion Electronica EjemplosCielo GarcíaAún no hay calificaciones
- Tarea 2 Problemas de Campo Electrico - Sears 12va Cap 21 FBTFI02Documento5 páginasTarea 2 Problemas de Campo Electrico - Sears 12va Cap 21 FBTFI02Hector TorcattAún no hay calificaciones
- Efecto Fotoeléctrico: PAU ULL Septiembre 2007Documento10 páginasEfecto Fotoeléctrico: PAU ULL Septiembre 2007MOISESAún no hay calificaciones
- Taller Atomos y MoleculasDocumento4 páginasTaller Atomos y MoleculasCastro Duarte Danna AlejandraAún no hay calificaciones
- Practica de Quimica 1 Reporte de Practica Equipo 8Documento8 páginasPractica de Quimica 1 Reporte de Practica Equipo 8Shamed AngelAún no hay calificaciones
- Detjun 2010Documento5 páginasDetjun 2010Sarah Jayne BurlinghamAún no hay calificaciones
- TK9001 2018-1923Documento107 páginasTK9001 2018-1923Chucho LopezAún no hay calificaciones
- Prueba FormativaDocumento4 páginasPrueba FormativaNatalia Arias FigueroaAún no hay calificaciones
- Fis Cua 2do 1T AlumnoDocumento60 páginasFis Cua 2do 1T AlumnoJustinAún no hay calificaciones
- Autoevaluación 5Documento7 páginasAutoevaluación 5Luis David Ortiz AnguloAún no hay calificaciones
- Album de Química (Gases Nobles)Documento7 páginasAlbum de Química (Gases Nobles)manuel jose sandoval urizarAún no hay calificaciones
- Segundo Examen de Física ModernaDocumento2 páginasSegundo Examen de Física ModernajuanchoAún no hay calificaciones