Documentos de Académico
Documentos de Profesional
Documentos de Cultura
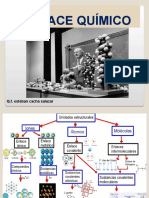
Mapa Conceptual
Cargado por
Fer Ángeles0 calificaciones0% encontró este documento útil (0 votos)
38 vistas1 páginaTítulo original
Mapa conceptual (1)
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
38 vistas1 páginaMapa Conceptual
Cargado por
Fer ÁngelesCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 1
ANGELES CEDEÑO MARIA FERNANDA 3IM41
ENLACES QUI MI COS
los át omos est án t rat ando de alcanzar el est ado más est able (de menor energía) posible. Muchos át omos se vuelven est ables cuando su orbit al de valencia
est á lleno de elect rones o cuando sat isfacen la regla del oct et o (al t ener ocho elect rones de valencia). Si los át omos no t ienen est e arreglo, "desearán"
lograrlo al ganar, perder o compart ir elect rones mediant e los enlaces.
ENLACE ENLACE ENLACE ENLACE POLAR CON
ENLACE
I ONI CO COORDI NADO DOBLE COVAl ENCI A
COVALENTE POLAR METALI CO
Y NO POLAR
El enlace iónico o electr ovalente es un
enlace que se for ma por la tr ansfer encia En tipo de unión química que se
de uno o más electr ones de un átomo o Hay dos tipos pr incipales de pr oduce únicamente entr e los
gr upo de átomos a otr o. Los enlaces enlaces covalentes: polar y no átomos de un mismo elemento
iónicos se for man con mayor facilidad polar . En un enlace covalente metálico. Gr acias a este tipo de
cuando r eaccionan elementos con ener gía polar , los electr ones se compar ten enlace los metales logr an estr uctur as
de ionización pequeña (metales) con de for ma no equitativa entr e los molecular es sumamente compactas,
elementos de elevadas átomos y pasan más tiempo cer ca sólidas y r esistentes, dado que los
electr onegatividades y afinidad de un átomo que del otr o. Debido a núcleos de sus átomos se juntan a tal
electr ónica (no metales). Los pr imer os la distr ibución desigual de extr emo, que compar ten sus
pier den fácilmente electr ones y los electr ones de valencia.
electr ones entr e los átomos de
últimos los ganan con igual facilidad. difer entes elementos, apar ecen
car gas liger amente positivas (?+) y
liger amente negativas (??) en
distintas par tes de la molécula.
Los enlaces covalentes no
polar es se for man entr e Un enlace doble en química es un
Se denomina enlace covalente coor dinado o dativo al dos átomos del mismo enlace covalente entr e dos átomos
enlace químico que se for ma cuando dos átomos elemento o entr e átomos que implica cuatr o electr ones de
compar ten un par de electr ones, per o este par pr ocede de difer entes elementos enlace en lugar de dos en un enlace
sólo de uno de los átomos. Este tipo de enlace se que compar ten electr ones simple. Los enlaces dobles ocur r en
pr esenta cuando un átomo no metálico compar te un de maner a más o menos con mayor fr ecuencia entr e dos
par de electr ones con otr os átomos. Par a que se equitativa. átomos de car bono, por ejemplo, en
pr esente este tipo de enlace, se r equier e que el átomo los alquenos
dador tenga un par de electr ones libr es en un or bital
exter ior y el átomo aceptor tenga capacidad par a
r ecibir ese par de electr ones en su última capa de
valencia.
También podría gustarte
- Teoría electromagnética para estudiantes de ingeniería: Notas de claseDe EverandTeoría electromagnética para estudiantes de ingeniería: Notas de claseCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Triptico de Quimica IDocumento3 páginasTriptico de Quimica INaomi Artica56% (9)
- Curso de Orientacion Con BrujulaDocumento45 páginasCurso de Orientacion Con BrujulaJean Carlos BritoAún no hay calificaciones
- Enlaces Quimicos 190502210922 PDFDocumento19 páginasEnlaces Quimicos 190502210922 PDFCarlos Araneda MelladoAún no hay calificaciones
- Sesion 06 - Enlace QuimicoDocumento74 páginasSesion 06 - Enlace QuimicoDANY HANCCOAún no hay calificaciones
- Calculo de Cargas Térmicas de ClimatizacionDocumento53 páginasCalculo de Cargas Térmicas de ClimatizacionsurflowersAún no hay calificaciones
- ENLACE QUÍMICO 1 (Lewis y Tipos de EnlacesDocumento48 páginasENLACE QUÍMICO 1 (Lewis y Tipos de EnlacescatalinaAún no hay calificaciones
- Enlace Quimico - OK PDFDocumento35 páginasEnlace Quimico - OK PDFYves Olivier Brard AracenaAún no hay calificaciones
- Guia ERADocumento34 páginasGuia ERAGaspar a secasAún no hay calificaciones
- AUTORROTACIÓNDocumento7 páginasAUTORROTACIÓNsantoyo70Aún no hay calificaciones
- Bloque VDocumento40 páginasBloque VMafer SolanoAún no hay calificaciones
- Cim Tareas1 GonzalezsolisjaimeDocumento3 páginasCim Tareas1 GonzalezsolisjaimepedroAún no hay calificaciones
- En LacesDocumento46 páginasEn LacesMiriam Noemi Arenas PobleteAún no hay calificaciones
- Enlaces Ionicos y Nomenclatura QuimicaDocumento9 páginasEnlaces Ionicos y Nomenclatura QuimicaIsabel Palacios NoleAún no hay calificaciones
- Diapositivas de ENLACE QUIMICODocumento30 páginasDiapositivas de ENLACE QUIMICOMax Percy Carhuamaca RojasAún no hay calificaciones
- Enlaces Quimicos y Soluciones QuímicasDocumento35 páginasEnlaces Quimicos y Soluciones QuímicasBrenda HernandezAún no hay calificaciones
- Enlace Químico - 2 - 2020Documento13 páginasEnlace Químico - 2 - 2020Bárbara López HerediaAún no hay calificaciones
- ENLACES QUÍMICOS PresentacionDocumento19 páginasENLACES QUÍMICOS PresentacionElizabeth JimenezAún no hay calificaciones
- Enlace Químico Iónico y CovalenteDocumento51 páginasEnlace Químico Iónico y CovalenteDiego Giraldo BoteroAún no hay calificaciones
- Enlaces Químicos P II 2020Documento30 páginasEnlaces Químicos P II 2020LilithAún no hay calificaciones
- Unidad2 Tarea 2 Enlace Quimico y Estructura MolecularDocumento4 páginasUnidad2 Tarea 2 Enlace Quimico y Estructura MolecularBrayan Bareño FerroAún no hay calificaciones
- QI ENLACES QUÍMICOS Lectura con cuestionario Sem. 21-1Documento9 páginasQI ENLACES QUÍMICOS Lectura con cuestionario Sem. 21-1Kaled Emiliano Viveros HernándezAún no hay calificaciones
- Enlaces QuímicosDocumento8 páginasEnlaces QuímicosAlexis MuñozAún no hay calificaciones
- Enlaces QuimicosDocumento2 páginasEnlaces QuimicosCielo YadhiraAún no hay calificaciones
- Enlaces QuimicosDocumento8 páginasEnlaces QuimicosCHAMORRO SAAVEDRA ELIOT RICARDOAún no hay calificaciones
- Enlace - Químico - Parte IDocumento24 páginasEnlace - Químico - Parte Idania muñozAún no hay calificaciones
- Unutr0100 s5 Ordinario IIDocumento22 páginasUnutr0100 s5 Ordinario IIMILENA DANIELA TUTIVEN VELIZAún no hay calificaciones
- QuimicaDocumento4 páginasQuimicaTalia Veronica ReyesAún no hay calificaciones
- Presentación Enlaces Químicos Iónico, Covalente y Metálico Ilustrativo Verde NaranjaDocumento10 páginasPresentación Enlaces Químicos Iónico, Covalente y Metálico Ilustrativo Verde NaranjaNicole SolanoAún no hay calificaciones
- Unidad 3 - Clasificación Del Enlace CovalenteDocumento21 páginasUnidad 3 - Clasificación Del Enlace Covalentealexis ortegaAún no hay calificaciones
- Tipos de enlace covalenteDocumento19 páginasTipos de enlace covalenteEdu Vallejo GaiborAún no hay calificaciones
- 5-Estructura MolecularDocumento35 páginas5-Estructura Molecularivan carvajalAún no hay calificaciones
- Ciencia y Mecánica de MaterialesDocumento20 páginasCiencia y Mecánica de MaterialesAna Maria PerezAún no hay calificaciones
- Clase Semana 2 y 3 Completo PDFDocumento20 páginasClase Semana 2 y 3 Completo PDFSawyer Baldwin Katny AdonisAún no hay calificaciones
- Tema 4Documento18 páginasTema 4alejasp1708Aún no hay calificaciones
- Quimica General Enlaces QuimicosDocumento3 páginasQuimica General Enlaces QuimicosFederico David FloresAún no hay calificaciones
- QuímicaDocumento3 páginasQuímicaValentino MorosiniAún no hay calificaciones
- Mapa Mental Enlace QuimicoDocumento2 páginasMapa Mental Enlace QuimicoYamilAún no hay calificaciones
- Enlaces químicos y tipos de enlaceDocumento8 páginasEnlaces químicos y tipos de enlaceDanielAún no hay calificaciones
- Taller#1 Enlace QuimicoDocumento5 páginasTaller#1 Enlace QuimicoJulian Camilo CantorAún no hay calificaciones
- Enlace Covalente (Tipos) - Enlace MetalicoDocumento3 páginasEnlace Covalente (Tipos) - Enlace MetalicoLuciana DomeAún no hay calificaciones
- Clase 2Documento11 páginasClase 2Varinnia TamaraAún no hay calificaciones
- Enlaces Químicos y Estructuras de LewisDocumento54 páginasEnlaces Químicos y Estructuras de LewisMiguelAngelCaviedesAún no hay calificaciones
- Tipos de Enlace QuímicoDocumento4 páginasTipos de Enlace Químico5IM9- Corona Guzmán Ingrid AnahiAún no hay calificaciones
- Enlace QuímicoDocumento11 páginasEnlace QuímicoMARIA ALEXANDRA PACHON ARANDIAAún no hay calificaciones
- CLASE 7-Enlace QuímicoDocumento59 páginasCLASE 7-Enlace Químicojhonnatan loyolaAún no hay calificaciones
- Enlace QuimicoDocumento2 páginasEnlace QuimicoChristian Malagón100% (1)
- 6_Enlace químicoDocumento16 páginas6_Enlace químicoFranco AgustínAún no hay calificaciones
- Mapa ConceptualDocumento1 páginaMapa Conceptualhumberto tapia gonzalesAún no hay calificaciones
- Clase Enlace QuímicoDocumento2 páginasClase Enlace QuímicoDaniel Morales MartinezAún no hay calificaciones
- 3ro Abl Enlace Quimico-Estructura de LewisDocumento3 páginas3ro Abl Enlace Quimico-Estructura de Lewisrokiquino5Aún no hay calificaciones
- Enlace Covalente Ii Parte Clase 14 Octavo BasicoDocumento23 páginasEnlace Covalente Ii Parte Clase 14 Octavo Basicotpp 11100% (1)
- Clase 7 - U3 (Enlace Químico-Enlace Iónico-Covalente)Documento50 páginasClase 7 - U3 (Enlace Químico-Enlace Iónico-Covalente)BrunoAún no hay calificaciones
- Act 9Documento2 páginasAct 9duranximena96Aún no hay calificaciones
- Cuadro SinopticoDocumento2 páginasCuadro SinopticoLore DLAún no hay calificaciones
- Guia Nº 03 - ENLACE QUIMICODocumento5 páginasGuia Nº 03 - ENLACE QUIMICOAriana RodriguezAún no hay calificaciones
- Enlace IonicoDocumento18 páginasEnlace IonicoCarlos BadillaAún no hay calificaciones
- Apuntes-Enlaces SolidosDocumento16 páginasApuntes-Enlaces Solidososielvalentin14Aún no hay calificaciones
- Enlaces Químicos: Tipos y PropiedadesDocumento33 páginasEnlaces Químicos: Tipos y PropiedadesCarlos Flib WilliamsAún no hay calificaciones
- Unidad 2 - EnlacesDocumento55 páginasUnidad 2 - EnlacesrichmindAún no hay calificaciones
- Guia 03 QuimicaDocumento9 páginasGuia 03 QuimicaLesmes Hidalgo CamposAún no hay calificaciones
- Tipos de enlace químico: iónico, covalente y metálicoDocumento13 páginasTipos de enlace químico: iónico, covalente y metálicoCARLA LUCÍA DÍEZ TORRESAún no hay calificaciones
- Capitulo 1Documento26 páginasCapitulo 1lisseth calleAún no hay calificaciones
- 3. Enlaces Químicos Intramoleculares, Enlaces Químicos Intermoleculares, Hibridaciones, Resonancia y Ruptura de EnlaceDocumento69 páginas3. Enlaces Químicos Intramoleculares, Enlaces Químicos Intermoleculares, Hibridaciones, Resonancia y Ruptura de EnlaceJahayda PaulaAún no hay calificaciones
- Propiedades Periódicas de Los ElementosDocumento3 páginasPropiedades Periódicas de Los ElementosFer ÁngelesAún no hay calificaciones
- Triptico, SeguridadDocumento2 páginasTriptico, SeguridadFer ÁngelesAún no hay calificaciones
- Estado Benefactor y NeoliberalismoDocumento1 páginaEstado Benefactor y NeoliberalismoFer ÁngelesAún no hay calificaciones
- Poster Científico Llamativo Periódico Vintage MarrónDocumento1 páginaPoster Científico Llamativo Periódico Vintage MarrónFer ÁngelesAún no hay calificaciones
- Guia de Aprendizaje No.3Documento20 páginasGuia de Aprendizaje No.3David Romero FerreiraAún no hay calificaciones
- Práctica Camisa y SerpentinDocumento10 páginasPráctica Camisa y SerpentinNicolle MoysAún no hay calificaciones
- Tpe#5 Julissa ParedesDocumento7 páginasTpe#5 Julissa ParedesGuillermo NoriegaAún no hay calificaciones
- Essa - 581761Documento2 páginasEssa - 581761David MurallaAún no hay calificaciones
- Formación de martensita y perfiles de dureza en aceros templadosDocumento10 páginasFormación de martensita y perfiles de dureza en aceros templados̶M̶a̶u̶r̶i̶c̶i̶o̶ B̶e̶c̶e̶r̶r̶a̶ P̶e̶ñ̶a̶l̶o̶z̶a̶Aún no hay calificaciones
- ElectrodinámicaDocumento10 páginasElectrodinámicaCristhian Vivanco EstradaAún no hay calificaciones
- Memorias SincelejoDocumento48 páginasMemorias SincelejoGerson ChamorroAún no hay calificaciones
- Especiificaciones PanelesDocumento9 páginasEspeciificaciones PanelesDenis ArevaloAún no hay calificaciones
- Polymobil Plus Brochure Español PDFDocumento8 páginasPolymobil Plus Brochure Español PDFMonica FajardoAún no hay calificaciones
- 0-II - Probl Resueltos EFE JLR 231015Documento118 páginas0-II - Probl Resueltos EFE JLR 231015Frailyn VerasAún no hay calificaciones
- Mapa de Pendientes I.E. TarcaDocumento1 páginaMapa de Pendientes I.E. TarcaCarlos GDAún no hay calificaciones
- Funciones matemáticas 2o ESODocumento3 páginasFunciones matemáticas 2o ESORichard ArizaAún no hay calificaciones
- 8.2 Variación de La Presión Con La Profundidad y Principio de PascalDocumento20 páginas8.2 Variación de La Presión Con La Profundidad y Principio de PascalJuan Alberto FLOR CORAZIAún no hay calificaciones
- Requeriemiento de Equipos TOPO IIDocumento4 páginasRequeriemiento de Equipos TOPO IIGABRIELA GUERREROSAún no hay calificaciones
- Descargable Información ProyectosDocumento24 páginasDescargable Información ProyectosDiego LunaAún no hay calificaciones
- Concesiones Mineras en AndahuaylasDocumento36 páginasConcesiones Mineras en AndahuaylasLuz Clarita Avalos DuranAún no hay calificaciones
- Metodo de Thiem Theis y JacobDocumento7 páginasMetodo de Thiem Theis y JacobAndrea YepezAún no hay calificaciones
- Pud-1-Física Gral.-2do BachilleratoDocumento4 páginasPud-1-Física Gral.-2do BachilleratoDavid Alberto BustillosAún no hay calificaciones
- EJEMPLO - 6 - LaminadoDocumento4 páginasEJEMPLO - 6 - Laminadodiego bgAún no hay calificaciones
- Escalares y Vectores, MRU y MRUV 2020Documento43 páginasEscalares y Vectores, MRU y MRUV 2020Diana Valeria EscobarAún no hay calificaciones
- Barranquillita - Memoria RetilapDocumento24 páginasBarranquillita - Memoria RetilapelcuesAún no hay calificaciones
- Principios de LubricaciónDocumento189 páginasPrincipios de LubricaciónJose Angel MelendezAún no hay calificaciones
- Cómo obtienen energía los seres vivosDocumento1 páginaCómo obtienen energía los seres vivosLuis ArredondoAún no hay calificaciones
- Acero Plata Dureza Alta HerramientasDocumento1 páginaAcero Plata Dureza Alta HerramientasAngel AlbanAún no hay calificaciones
- Informe FisicoquímicaDocumento8 páginasInforme FisicoquímicaDánery CAAún no hay calificaciones
- Medidas eléctricas UNNE corrientes Foucault medidores energíaDocumento9 páginasMedidas eléctricas UNNE corrientes Foucault medidores energíarogelio de oliveraAún no hay calificaciones