Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Material de Apoyo Vacunas
Cargado por
Fisio Sport Brasil BrasilTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Material de Apoyo Vacunas
Cargado por
Fisio Sport Brasil BrasilCopyright:
Formatos disponibles
CBCC6
Actividad
1:
La
vacunación
como
acto
comunitario
Material
de
apoyo
Setiembre
2020
-‐
Por
Mariana
Rivera,
Amy
Mónaco
&
María
Moreno
Depto.
Desarrollo
Biotecnológico
–
Instituto
de
Higiene
Facultad
de
Medicina
.
Universidad
de
la
República
Qué son las vacunas – Introducción
Una
vacuna
es
una
preparación
biológica
que
confiere
inmunidad
adquirida
activa
frente
a
una
enfermedad
particular.
Típicamente,
consiste
en
un
agente
que
se
asemeja
al
agente
causal
de
la
enfermedad,
que
estimula
al
sistema
inmune
del
organismo
vacunado
a
reconocerlo
como
amenaza,
destruirlo
y
a
reconocer
y
destruir
cualquier
microorganismo
asociado
con
ese
agente
que
pueda
encontrar
en
el
futuro.
Las
vacunas
profilácticas
son
aquellas
que
tienen
como
objetivo
proteger
a
los
individuos
de
las
enfermedades.
Se
administran
a
individuos
sanos
para
prevenir
o
reducir
los
efectos
de
una
futura
infección
por
un
patógeno,
o
para
prevenir
que
se
establezca
una
infección
en
el
futuro.
Las
vacunas
terapéuticas
tienen
como
objetivo
tratar
una
enfermedad
ya
existente
en
un
individuo
dado.
Se
administran
a
los
individuos
para
tratar
o
reducir
los
efectos
de
una
enfermedad
ya
existente.
La
vacunación
(administración
de
una
vacuna)
es
el
método
más
costo-‐efectivo
para
prevenir
enfermedades
infecciosas.
La
inmunidad
adquirida
y
extendida
a
la
población
debido
a
la
vacunación
es
ampliamente
responsable
de
la
erradicación
de
la
viruela,
y
a
la
drástica
disminución
de
la
incidencia
de
enfermedades
infecciosas,
tales
como
poliomielitis,
sarampión,
tétanos,
entre
otras,
en
gran
parte
del
mundo.
La
eficacia
de
la
vacunación
ha
sido
científica
y
ampliamente
estudiada
y
verificada;
las
vacunas
disponibles
en
el
mercado
han
demostrado
ser
seguras
y
eficaces.
Los
términos
“vacuna”
y
“vacunación”
derivan
de
Variolae
vaccinae,
el
término
que
designó
Edward
Jenner
en
1796
para
la
varicela
vacuna,
en
el
título
del
trabajo
en
el
que
describía
los
efectos
protectivos
de
la
varicela
vacuna
(cowpox)
frente
a
la
viruela
(en
humanos).
En
1881,
Louis
Pasteur
en
honor
a
Jenner,
propuso
que
se
extendiera
el
término
"vacuna"
a
todas
las
formulaciones
protectivas
que
se
desarrollaran.
Las
vacunas
han
revolucionado
la
salud
durante
el
siglo
XX,
ya
que
ha
sido
una
de
las
estrategias
más
efectivas
para
disminuir
la
tasa
de
mortalidad
y
morbilidad
debido
a
enfermedades
infecciosas
a
lo
largo
de
la
historia.
Luego
de
la
implementación
del
agua
potable,
se
cree
que
son
el
invento
que
ha
salvado
más
vidas
en
la
historia
de
la
humanidad.
Sin
embargo,
las
enfermedades
infecciosas
aún
afectan
muchas
vidas
humanas
y
animales.
Esto
se
debe
principalmente
a
que
aún
no
se
ha
logrado
alcanzar
el
máximo
potencial
de
las
vacunas,
por
varias
razones.
En
primer
lugar,
aún
no
se
ha
logrado
que
las
vacunas
efectivas
estén
disponibles
para
la
población
de
todos
los
países,
principalmente
en
los
países
subdesarrollados.
La
Alianza
Mundial
para
las
Vacunas
e
Inmunizaciones
(GAVI,
por
sus
siglas
en
inglés
de
Global
Alliance
for
Vaccines
and
Immunizations)
estima
que
más
de
1,5
millones
de
personas,
incluyendo
600.000
niños
menores
de
5
años,
mueren
por
año
de
enfermedades
prevenibles
por
vacunación.
Además,
aún
no
se
cuenta
con
vacunas
efectivas
contra
todas
las
enfermedades,
incluyendo
HIV,
tuberculosis
y
malaria,
que
provocan
más
de
5
millones
de
muertes
en
todo
el
mundo
anualmente.
La
vacunación
utiliza
la
memoria
inmunológica
del
sistema
inmune
adaptativo,
de
forma
tal
que
la
exposición
a
una
vacuna
genera
un
pool
de
linfocitos
B
y
T,
que,
frente
a
una
nueva
exposición
al
agente
infeccioso,
son
activados
y
logran
la
eliminación
de
ese
agente
infeccioso.
La
vacunación
prepara
al
sistema
inmune
para
defenderse
frente
a
los
agentes
infecciosos.
Los
objetivos
de
la
vacunación
son:
lograr
la
protección
del
individuo
vacunado
y
lograr
la
protección
colectiva
mediante
la
inmunidad
de
rebaño,
limitando
la
circulación
del
patógeno,
y
en
consecuencia,
disminuyendo
el
riesgo
de
infección
de
los
individuos
no
vacunados.
La
inmunidad
de
rebaño
es
muy
Página 1 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
importante para prevenir infecciones tales como el sarampión. Vacunarse significa decidir tomar un
tratamiento sin estar enfermo, y sin tener certeza de si sería necesario. Dado que todo tipo de tratamiento
tiene riesgos asociados, la decisión de la vacunación debe hacerse basándose en un análisis de
riesgo/beneficio, que demuestra que el beneficio que se obtiene de la vacunación es mucho mayor que el
riesgo que trae asociado. Este análisis es muy fácil de hacer cuando se tiene la amenaza muy cercana de
contraer una enfermedad grave, que cuando la enfermedad no es grave, o la posibilidad de contraerla es
remota o rara. Estos casos, dan lugar a escepticismo respecto a las vacunas, también conocido como
"vacilación frente a las vacunas" ("vaccine hesitancy" en inglés). Estas dudas respecto al funcionamiento de
las vacunas han ocurrido desde los principios de la vacunación, con los primeros experimentos de Jenner
en el siglo XVIII. Sin embargo, hoy en día hay mucho más conocimiento sobre el funcionamiento de las
vacunas de lo que había en la época de Jenner, y aún así hay fuertes grupos de personas organizadas como
anti-‐vacunas, con conceptos equivocados o desinformación, que ponen en riesgo la inmunidad de rebaño,
ya que disminuyen la cobertura vacunal, y dejan expuestos a individuos que por diferentes razones no
pueden vacunarse o no responden a la vacunación.
Breve historia de la vacunación
En
el
último
siglo
las
vacunas
demostraron
ser
una
de
las
intervenciones
médicas
más
exitosas
y
efectivas,
siendo
una
de
las
aplicaciones
médicas
más
importantes
para
prevenir
enfermedades
infecciosas.
El
experimento
realizado
en
Inglaterra
por
Edward
Jenner
en
1796
es
un
hito
de
la
inmunología,
ya
que
demostró
que
la
inoculación
con
pus
de
lesiones
de
varicela
vacuna
(cowpox),
confería
protección
a
las
personas
frente
a
una
infección
de
viruela,
contribuyendo
de
esta
manera
a
entender
el
concepto
de
"inmunización",
y
a
la
posterior
erradicación
de
la
viruela,
muchos
años
después.
La
viruela
era
una
de
las
enfermedades
humanas
más
severas,
y
provocaba,
solo
en
Europa,
la
muerte
de
más
de
400.000
personas
por
año.
En
1979,
luego
de
un
arduo
trabajo
de
coordinación
mundial
para
la
inmunización
de
la
población,
se
logró
la
erradicación
de
la
enfermedad.
El
trabajo
de
Jenner
fue
continuado
y
refinado
por
el
francés
Louis
Pasteur,
que
logró
atenuar
microorganismos
en
su
laboratorio,
y
en
1885
desarrolló
la
primer
vacuna
contra
la
rabia
para
humanos.
El
trabajo
de
Pasteur
significó
un
gran
avance
en
la
comprensión,
la
prevención
y
el
tratamiento
de
las
enfermedades
infecciosas,
ya
que
estableció
las
bases
de
la
vacunación,
es
decir,
el
principio
de:
aislamiento,
inactivación
y
administración
de
estos
patógenos
que
previo
a
la
inactivación,
causaban
enfermedad.
Los
principios
de
Pasteur
permitieron
el
desarrollo
de
lo
que
hoy
conocemos
como
"vacunas
de
primera
generación",
que
están
basadas
en
microorganismos
enteros,
ya
sea
muertos,
o
vivos
y
atenuados
(por
ejemplo,
el
Bacilo
de
Calmette-‐Guerin
contra
la
tuberculosis,
plaga,
pertussis,
y
viruela).
En
la
segunda
mitad
del
siglo
XX,
las
innovaciones
y
las
nuevas
tecnologías
que
permitieron
el
cultivo
de
líneas
celulares
de
mamífero
dieron
lugar
a
las
vacunas
"de
segunda
generación",
tales
como
polio
(vacuna
oral
de
Sabin),
sarampión,
rubeola,
paperas,
y
varicela.
Más
recientemente,
el
uso
de
la
vacuna
de
la
polio
inactivada
(vacuna
de
Salk),
junto
con
la
vacuna
oral
de
Sabin,
implementadas
en
planes
de
vacunación
mundial,
han
permitido
que
se
esté
muy
cerca
de
la
erradicación
de
esta
enfermedad.
En
los
países
desarrollados,
los
programas
nacionales
de
inmunización
han
disminuido
drásticamente
la
incidencia
de
enfermedades
infecciosas
bacterianas
y
virales,
que
previo
a
la
implementación
de
éstos
solían
afectar
a
los
niños.
En
mayo
de
2012,
194
estados
miembros
de
la
Organización
Mundial
de
la
Salud
(OMS)
promovieron
y
aprobaron
el
"plan
de
acción
de
vacunación
mundial"
(GVAP
por
sus
siglas
en
inglés
de
Global
Vaccine
Action
Plan),
con
la
visión
de
brindar
acceso
universal
a
la
vacunación,
lo
que
debía
resultar
en
2
a
3
millones
de
vidas
salvadas
por
año
a
nivel
mundial
(http://www.who.int/immunization/global_
vaccine_action_plan/).
Aunque
las
vacunas
desarrolladas
en
el
último
siglo
han
sido
de
incuestionable
valor,
ya
que
se
estima
que
han
evitado
más
de
700
millones
de
enfermedades
y
más
de
150
millones
de
muertes,
los
métodos
convencionales
de
diseño
de
vacunas
tienen
varias
limitaciones.
Por
ejemplo,
no
se
pueden
utilizar
para
desarrollar
vacunas
contra
microorganismos
que
no
crezcan
in
vitro
(por
ejemplo:
Mycobacterium
leper,
virus
del
papilloma
humano
tipos
16
y
18).
No
confieren
protección
frente
a
patógenos
con
hipervariabilidad
antigénica
(por
ejemplo
menigococcus
serogrupo
B,
HIV,
HCV),
o
contra
Página 2 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
patógenos con fase intracelular, que causan infecciones que deben ser controladas por células T, tales como
tuberculosis o malaria. Por último, el enfoque tradicional del desarrollo de vacunas es muy lento y consume
mucho tiempo, impidiendo lograr respuestas rápidas frente a la necesidad de una nueva vacuna, por
ejemplo, en el caso de una pandemia de influenza. Para superar todas estas limitaciones, durante los
últimos 30 años, se han aplicado nuevas biotecnologías al desarrollo de vacunas, tales como: el ADN
recombinante, la química de polisacáridos, y más recientemente vacunología reversa (RV), vacunología
estructural, y vacunas de ARN sintético, han permitido diseñar y desarrollar vacunas "de tercera
generación", que previamente se creía que no eran posibles de lograr.
Cómo funcionan las vacunas?
El objetivo de la vacunación es simular la infección por el patógeno, desencadenar una respuesta inmune,
e inducir memoria inmunológica, para poder eliminar dicho patógeno en un encuentro futuro. Para que una
vacuna desencadene una respuesta inmune, el primer requerimiento es que los antígenos sean
transportados desde el sitio de inoculación a los órganos linfoides secundarios, donde residen las APCs, las
células T y las B. Los antígenos pueden drenar hacia los órganos linfoides (tales como el bazo y los ganglios
linfáticos (LN)), a través del fluido intersticial y de los vasos linfoides aferentes. Además, las vacunas
particuladas pueden ser internalizadas por APCs en el sitio de inoculación y subsecuentemente viajar por el
sistema linfático para interaccionar con las células B y T en los LN.
La respuesta de células B, o respuesta humoral es uno de los dos brazos del sistema inmune adaptativo. Es
realizado por los linfocitos B, que defienden el individuo de patógenos mediante la liberación de
anticuerpos en los fluidos corporales. Los anticuerpos son importantes para la defensa frente a patógenos
en el medio extracelular o en las mucosas. Pueden evitar la colonización de las mucosas, la entrada de
patógenos al organismo, y que los patógenos se diseminen en la sangre y otros tejidos. También pueden
interceptar ciertos patógenos intracelulares, al migrar entre las células. Las respuestas de células B, pueden
ser de dos tipos, dependiendo si requieren de la ayuda de las células T o no. El tipo de célula B que responde
está fuertemente influenciado por el antígeno con que se realice la inmunización.
Las
respuestas
de
células
B
timo-‐independientes
(TI)
ocurren
sin
la
ayuda
de
células
T.
Son
inducidas
por
y
dirigidas
contra
antígenos
polivalentes
con
epitopes
repetitivos
tales
como
estructuras
lipídicas
o
polisacarídicas
de
los
patógenos.
Las
respuestas
TI
generalmente
tienen
lugar
en
etapas
tempranas
de
la
infección
y
son
mediadas
por
células
B
especializadas,
incluyendo
las
de
la
zona
marginal
y
las
células
B1.
Estas
células
B
dan
lugar
a
células
plasmáticas
que
secretan
anticuerpos
de
baja
afinidad,
y
no
generan
células
B
de
memoria.
Sin
embargo,
las
respuestas
de
anticuerpos
TI
son
más
rápidas
que
las
T-‐
dependientes,
y
por
lo
tanto
cumplen
un
rol
fundamental
en
disminuir
la
carga
microbiana
en
etapas
tempranas
de
la
infección.
Las
respuestas
de
células
B
timo-‐dependientes
(TD)
dependen
estrictamente
de
la
ayuda
de
células
T.
Las
respuestas
TD
tienen
lugar
a
tiempos
más
tardíos
de
la
infección/inmunización,
debido
a
que
se
necesita
tiempo
para
que
ocurra
la
activación
de
células
T-‐helper
antígeno-‐específicas.
Las
respuestas
de
células
B
TD
están
mediadas
por
el
mayor
subset
de
células
B
denominadas
células
B
foliculares
o
B2,
y
dan
lugar
a
células
plasmáticas
que
secretan
anticuerpos
de
alta
afinidad
así
como
también
a
células
de
memoria.
La
respuesta
de
células
T
es
el
otro
gran
brazo
de
la
respuesta
inmune
adaptativa.
Está
mediada
por
linfocitos
T
que
son
importantes
en
la
protección
de
patógenos
tanto
intracelulares
como
extracelulares.
Los
linfocitos
T
comprenden
los
linfocitos
T
citotóxicos,
y
las
células
T-‐helper.
La
función
de
los
linfocitos
T
citotóxicos
es
eliminar
células
infectadas
con
virus
u
otros
patógeno
intracelulares.
Se
caracterizan
por
la
expresión
de
una
proteína
de
superficie
denominada
CD8.
Las
células
T-‐helper
están
diseñadas
para
liberar
citoquinas
que
estimulan
la
actividad
de
otras
células
inmunes
que
son
las
que
van
a
actuar
directamente
sobre
la
causa
de
infección/o
antígeno
vacunal,
tales
como
células
B
y
macrófagos.
Se
caracterizan
por
la
expresión
del
co-‐receptor
de
superficie
CD4.
Antes
de
que
una
célula
citotóxica
pueda
eliminar
una
célula
infectada,
o
una
célula
T-‐helper
pueda
secretar
citoquinas,
debe
ser
activada
por
un
antígeno
específico.
Una típica respuesta de células T comprende las siguiente fases:
Página 3 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
• Fase de inducción: las células T reconocen su antígeno y son activadas para proliferar y
diferenciarse en células T efectoras. Esta fase no ocurre en sitio de inoculación, sino en los órganos
linfoides secundarios, a donde el antígeno es transportado por las APCs.
• Fase efectora: las céluals T diferenciadas son estimuladas para ejercer su función, luego de un re-‐
encuentro con el antígeno. Esta fase tiene lugar en el sitio de entrada del patógeno o de
inoculación del antígeno. Esto implica que una vez diferenciadas, las células T abandonan los
órganos linfoides secundarios donde habían sido activadas, y migran al sitio donde se encuentra el
antígeno.
• Fase de contracción: luego que se elimina el antígeno, la mayoría de los linfocitos efectores muere
por apoptosis, dejando una población pequeña y estable de células T de memoria de larga vida,
resultando en un aumento de la frecuencia de células específicas contra ese antígeno.
En
caso
de
que
el
antígeno
persista,
las
células
T-‐antígeno
específicas
no
pasan
por
esta
fase
de
contracción
clásica,
sino
que
entran
en
un
estado
de
"agotamiento"
caracterizado
por
una
disminución
de
sus
funciones
efectoras.
Las vacunas más exitosas se basan en la generación de anticuerpos neutralizantes. La generación de
respuestas T de memoria es, sin embargo, una meta fundamental de las vacunas contra HIV, malaria y
tuberculosis, para las que la inmunidad humoral no es suficiente, y para las que se cuenta con fuerte
evidencia preclínica del rol de las células T en controlar ese tipo de infecciones. Se ha tenido poco éxito al
intentar inducir inmunidad protectiva de células T por medio de la vacunación, lo que podría implicar que
se requiere que el antígeno esté disponible por más tiempo para mantener la memoria de células T, y
además, ésta decae poco tiempo después del procesamiento de los antígenos relacionados con la
vacunación. Además, las vacunas que emplean microorganismos inactivados, o proteínas recombinantes
pueden ser poco efectivas en la inducción de respuestas T protectivas. Se requiere avanzar en el
conocimiento para poder entender los factores que lideran y mantienen la inmunidad de células T, para
poder mejorar las estrategias en el diseño de vacunas.
Duración de la inmunidad inducida por la vacunación
Aunque
las
infecciones
naturales
generalmente
confieren
inmunidad
para
toda
la
vida,
casi
todas
las
vacunas
disponibles
requieren
de
más
de
una
dosis
(booster)
para
lograr
respuestas
inmunes
humorales
duraderas,
sin
importar
si
la
vacuna
es
viva-‐atenuada,
vacunas
no-‐replicantes,
o
de
subunidades.
Las
respuestas
de
anticuerpos
anti-‐virales
son
extremadamente
estables,
con
vidas
medias
que
van
desde
los
50
años
para
el
virus
de
varicela-‐zoster,
hasta
más
de
200
años
para
otros
virus
tales
como
el
sarampión
y
las
paperas.
Las
respuestas
de
anticuerpos
contra
antígenos
de
difteria
y
tétanos
decaen
más
rápidamente,
con
vidas
medias
estimadas
en
11
y
19
años
respectivamente.
La
memoria
de
células
B
es
de
larga
duración,
pero
no
existen
correlaciones
significativas
entre
los
números
de
células
B
de
memoria
y
los
niveles
de
anticuerpos.
Las
vidas
medias
de
los
anticuerpos
contra
los
siguientes
antígenos
y
virus
son:
tétanos:
11
años
<
varicela-‐zoster
virus:
50
años
<
rubeola:
114
años<
sarampión:
3014
años.
El
antígeno
vacunal
(ej:
soluble
o
particulado/agregado)
juega
un
rol
importante
en
la
determinación
de
la
inmunogenicidad
y
en
las
interacciones
con
las
DCs,
las
células
B
y
T
son
las
que
dictan
la
magnitud
y
la
duración
de
la
respuesta
inmune
en
los
centros
germinales.
Si
aprendemos
cómo
optimizar
estas
interacciones,
vamos
a
ser
capaces
de
desencadenar
respuestas
inmunes
más
efectivas
y
duraderas
con
menos
vacunaciones.
Vías de inoculación de las vacunas
Las
vacunas
pueden
ser
inoculadas
mediante
inyección
o
mediante
una
vía
natural.
En
la
práctica,
la
mayoría
de
las
vacunas
son
inyectadas
por
vía
intramuscular
(IM)
o
sub-‐cutánea
(SC),
y
pocas
vacunas
se
aplican
por
otras
rutas.
La
vía
oral
es
utilizada
para
dos
vacunas
vivas
virales
(polio
y
rotavirus),
y
para
la
vacuna
contra
cólera
(basada
en
la
bacteria
inactivada).
Las
vacunas
de
influenza
estacional
son
administradas
por
vía
IM
Página 4 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
o SC, pero también existe una diseñada específicamente para administrar por vía intradérmica (ID). También
existe una vacuna atenuada que se administra por vía intransal (IN). Al momento de diseñar una vacuna, se
debe considerar también la vía de inoculación, ya que ésta puede modificar el tipo de respuesta que se
desencadene, o puede presentar desafíos adicionales para el antígeno vacunal (por ejemplo: vía oral vs vía
SC).
Tipos de vacunas
Hay diversas maneras de clasificar los diferentes tipos de vacunas, dependiendo del criterio que se utilice.
A continuación se detalla dos maneras de clasificación. La primera, según si son vacunas de primera,
segunda o tercera generación, en función de cómo han sido desarrolladas (a medida que se fue avanzando
en herramientas biotecnológicas). Y luego se detalla una clasificación según cómo se administra el antígeno:
es decir, si se administra el antígeno directamente para que el sistema inmune lo reconozca y se
desencadene una respuesta, o si se administra la información genética para que la maquinaria celular del
individuo inmunizado produzca ese antígeno y luego desencadene una respuesta contra éste.
De primera, segunda y tercera generación:
Vacunas con organismos enteros
Las vacunas de primera generación son vacunas con organismos enteros, ya sea inactivados (muertos) o
vivos y atenuados. Las vacunas con microorganismos vivos y atenuados, tales como las de viruela, polio o
tuberculosis (BCG), son capaces de inducir respuestas celulares citotóxicas (CTL), respuestas de células T-‐
helper (TH), y altos títulos de anticuerpos. Sin embargo, los patógenos atenuados pueden potencialmente
revertir su virulencia hacia una forma peligrosa, y pueden causar enfermedad en individuos que hayan
recibido la vacuna que estén inmunocomprometidos.
Las vacunas con microorganismos inactivados (o muertos) no presentan este riesgo de reversión de
virulencia. Sin embargo, no todas son capaces de generar respuestas CTL, y pueden no funcionar para
algunas enfermedades. Además, contienen gran cantidad de PAMPs, lo que puede derivar en una respuesta
inmune exacerbada, causando efectos adversos no deseados.
Vacunas de subunidades
También conocidas como vacunas de segunda generación, se desarrollaron para disminuir el riesgo de las
vacunas hechas con microorganismos enteros (ya sea inactivados o vivos y atenuados). Éstas son vacunas
de subunidades, y consisten en antígenos específicos, que pueden ser proteicos, polisacarídicos, o de otro
tipo. Las subunidades usadas para producir vacunas pueden obtenerse mediante el cultivo del
microorganismo y posterior purificación del antígeno, o de forma recombinante. Pueden generar repuestas
TH y de anticuerpos, pero no respuestas citotóxicas, y en general requieren la adición de adyuvantes para
lograr una respuesta adecuada. Dentro de las vacunas de subunidades, se encuentran las vacunas de
subunidades proteicas, las vacunas de toxoides, las vacunas de polisacáridos, las vacunas conjugadas.
® Vacunas
de
toxoides:
Se
basan
en
una
o
más
toxinas
que
han
sido
detoxificadas
por
métodos
químicos,
físicos
o
genéticos.
® Vacunas
de
polisacáridos:
están
constituidas
por
polisacáridos
bacterianos
purificados.
® Vacunas
conjugadas:
están
constituidas
por
los
mismos
polisacáridos
bacterianos
purificados,
pero
conjugados
químicamente
a
una
proteína
carrier
(del
inglés:
"transportadora").
Estas
vacunas
fueron
desarrolladas
luego
de
constatar
que
las
vacunas
de
polisacáridos
generaban
respuestas
de
anticuerpos
de
pero
no
generaban
memoria.
La
causa
de
esta
falla
en
las
vacunas
de
polisacáridos
se
debía
a
que
los
polisacáridos
son
antígenos
T-‐independientes,
por
lo
que
esta
falta
de
estimulación
de
células
T,
era
lo
que
derivaba
en
que
la
respuesta
inmune
fuera
muy
débil
o
ni
siquiera
ocurriera.
Por
el
contrario,
los
antígenos
T-‐dependientes,
tales
como
los
toxoides
de
tétanos
o
difteria
sí
lograban
generar
respuestas
inmunes
robustas.
Luego
se
demostró
que
la
co-‐
Página 5 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
administración de antígenos T-‐dependientes (tales como proteínas) junto con
inmunógenos más "pobres", resultaba en una respuesta T-‐dependiente también contra
el componente que inicialmente generaba una respuesta T-‐independiente (ej: el
polisacárido). Una vacuna conjugada se crea mediante la unión covalente de un antígeno
poco inmunogénico (ej: polisacárido), a una proteína carrier (preferentemente del mismo
microorganismo), logrando así conferir los atributos inmunológico del carrier al antígeno
que tiene unido. Esta técnica se aplica generalmente a polisacáridos bacterianos para
prevenir enfermedades bacterianas invasivas (por ejemplo contra Streptococcus
pneumoniae).
® VLPs: del inglés "Virus Like Particles". Están compuestas por proteinas de la cápside viral
que tienen la capacidad de auto-‐ensamblarse y conformar una estructura tridimensional
similar a una partícula viral, pero sin su material genético, por lo que no son infecciosas.
La tecnología de las VLPs tiene grandes ventajas: son estructuras muy estables,
estructural y antigénicamente son prácticamente indistinguibles de los virus de los que se
derivan, pero al no contener material genético, no son infectivas, por lo que son más
seguras y son capaces de estimular una fuerte respuesta inmune, tanto humoral como
celular. Como se muestra en la Figura 1, hay varios tipos de VLPs, dependiendo si sólo
contienen componentes proteicos, o si también tienen componentes lipídicos, simulando
la estructura de virus envueltos.
Página 6 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
Figura
1.
Tipos
de
Virus
Like
PArticles
(VLPs).
Adaptado
de
J.
Bárcena
&
E.
Blanco,
Subcell
Biochem.
2013;68:631-‐65
Vacunas de ácidos nucleicos (ADN o ARN)
Las vacunas de ADN/ARN son de tercera generación. Contienen material genético que codifica para
proteínas específicas (antígenos) de un patógeno. El material genético (ADN o ARN) se inocula en el
organismo y es internalizado por células, cuyo metabolismo normal sintetiza proteínas basadas en el código
genético del plásmido que han internalizado. Debido a que estas proteínas contienen regiones de
aminoácidos que son características de bacterias o virus, son reconocidas como extrañas, y por consiguiente
son procesadas por células del hospedero y expuestas en su superficie. El sistema inmune se activa,
desencadenando una respuesta inmune. Alternativamente, el ADN puede encapsularse en proteínas para
facilitar el ingreso a las células. Si se incluye esta cápside proteica al ADN, la vacuna resultante puede
combinar la potencia de una vacuna viva y atenuada, sin riesgo de reversión de la virulencia. En 1983,
investigadores del Depto de Salud de Nueva York desarrollaron una estrategia para producir vacunas de
ADN recombinante utilizando ingeniería genética para transformar la vacuna ordinaria contra la varicela en
vacunas que fueran capaces de prevenir otras enfermedades. Alteraron el virus de la varicela vacuna
(cowpox) mediante la inserción de un gen de otros virus (por ejemplo virus de Herpes simplex, hepatitis B
e influenza).
Página 7 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
Clasificación según el origen de los antígenos:
Otra
forma
de
clasificar
las
vacunas,
es
dependiendo
del
origen
de
los
antígenos
protectivos.
En
este
sentido,
se
pueden
distinguir
dos
grandes
categorías:
Vacunas
basadas
en
el/los
antígeno/s:
estas
vacunas
ya
contienen
el
antígeno
propiamente
dicho,
y
comprenden
las
vacunas
de
microorganismos
inactivados
y
a
las
vacunas
de
subunidades.
Vacunas
basadas
en
información
codificante
del
antígeno:
Estas
vacunas
contienen
la
información
necesaria
para
que
las
células
del
individuo
vacunado
produzca
el
antígeno.
De
hecho,
el
antígeno
con
que
se
inmuniza
es
producido
in
vivo
luego
de
la
administración
de
la
vacuna.
Dentro
de
esta
categoría
encontramos
las
siguientes
vacunas:
• Vacunas
vivas
y
atenuadas:
generalmente
son
virales,
pero
también
hay
ejemplos
bacterianos,
como
en
el
caso
de
la
BCG.
Están
constituidas
por
versiones
atenuadas
del
patógeno
contra
el
que
se
quiere
inducir
una
respuesta
inmune
protectiva.
Históricamente
fueron
las
primeras
vacunas
en
ser
desarrolladas.
• Vacunas
de
vectores:
se
basan
en
un
microorganismo
inocuo
(que
es
capaz
de
infectar,
pero
no
causar
enfermedad
o
causar
una
enfermedad
muy
leve)
que
ha
sido
modificado
para
expresar
el
antígeno
de
interés.
Generalmente
son
virales.
Aún
no
existe
ninguna
vacuna
de
este
tipo
licenciada
para
uso
en
humanos.
• Vacunas
quiméricas:
consisten
en
una
combinación
de
2
virus,
generalmente
basados
en
un
virus
atenuado
al
que
se
le
ha
reemplazado
la
glicoproteina
de
la
envoltura
por
la
de
otro
virus.
Una
quimera
exitosa
debe
replicarse
con
alto
título
en
cultivo
celular,
y
ser
segura
para
la
administración
a
humanos.
Una
vacuna
de
este
tipo
ya
fue
aprobada
para
uso
humano
(2010),
y
otras
están
siendo
evaluadas.
• Vacunas
de
ácidos
nucleicos:
pueden
estar
compuestas
de
ADN
o
ARN.
Cuando
se
usan
"desnudas"
consisten
únicamente
en
información
genética.
Cuando
se
formulan
con
lípidos
catiónicos
o
en
emulsiones,
se
asemejan
más
a
las
vacunas
vivas
atenuadas.
Adyuvantes
A
pesar
del
éxito
de
las
vacunas
de
primera
generación,
surgieron
algunos
problemas
con
su
uso.
En
primer
lugar,
presentan
riesgo
de
intercambios
genéticos
con
otros
virus,
lo
que
podría
resultar
en
la
reversión
de
la
virulencia
de
las
vacunas
con
microorganismos
vivos
y
atenuados,
y
causar
enfermedad
al
individuo
vacunado.
En
segundo
lugar,
debido
a
su
complejidad
en
cuanto
al
contenido
antigénico,
estas
vacunas
pueden
inducir
efectos
adversos,
tales
como
fiebre,
o
toxicidad,
entre
otros.
Para
evitar
estos
efectos,
las
vacunas
más
utilizadas
son
las
vacunas
de
subunidades,
ya
que
contienen
sólo
el
antígeno
purificado,
contra
el
que
se
espera
que
reaccione
el
sistema
inmune,
confiriendo
protección
al
individuo.
Con
este
tipo
de
vacunas
se
logró
alcanzar
perfiles
de
seguridad
superiores,
a
expensas
de
una
disminución
de
la
inmunogenicidad,
debido
a
la
falta
de
PAMPs.
Por
esta
razón,
estas
vacunas
requerían
el
uso
de
"adyuvantes".
El
término
"adyuvante"
deriva
de
la
palabra
latina
"adyuvare"
que
significa
"ayudar".
Los
adyuvantes
pueden
ser
definidos
como
un
conjunto
de
aditivos
sumamente
heterogéneos,
que
aumentan
la
inmunogenicidad
de
los
antígenos,
y
modulan
la
respuesta
inducida
por
la
inmunización.
Aunque
los
adyuvantes
se
utilizan
desde
hace
décadas,
poco
se
sabe
acerca
de
su
mecanismo
de
acción.
No
obstante,
gracias
a
los
avances
en
el
conocimiento
del
sistema
inmune
se
ha
propuesto
que
los
adyuvantes
actúan
formando
depósito,
reclutando
células
del
sistema
inmune
al
sitio
de
inyección,
promoviendo
una
leve
inflamación
local
(secreción
de
citoquinas
y
quemoquinas)
que
lleva
a
la
inducción
de
una
respuesta
inmune
rápida
y
robusta
que
se
correlaciona
con
una
mayor
protección.
El
descubrimiento
de
los
adyuvantes,
como
de
tantos
otros
hallazgos
médicos
relevantes,
fue
por
casualidad.
A
principios
del
siglo
XX,
el
veterinario
francés
Gastón
Ramón
observó
que
el
rendimiento
del
anti-‐suero
de
caballo
anti-‐tétano
y
anti-‐difteria,
era
mayor
en
los
animales
que
tenían
un
absceso
en
el
sitio
de
inoculación.
Mediante
la
inyección
de
almidón,
tapioca,
u
otras
sustancias,
indujo
abscesos
estériles
en
el
sitio
de
inoculación
junto
con
la
toxina
inactivada,
Página 8 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
y de esa manera, aumentó la producción de anti-‐suero, confirmando la hipótesis de que las sustancias
capaces de promover una mayor inflamación local en el sitio de inoculación también eran capaces de
promover un mayor rendimiento del anti-‐suero. Por la misma época, el inglés Alexander Glenny descubrió
los efectos de las sales de aluminio de promover respuestas inmunes. Estas sales de aluminio fueron
utilizadas en vacunas para humanos por primera vez en 1932, y fueron los únicos adyuvantes licenciados
para uso en humanos durante más de 70 años. A pesar de su uso extensivo y continuo, el mecanismo por
el cual las sales de aluminio funcionan como adyuvantes, aún no ha sido completamente dilucidado. Por
esta razón, Janeway describía a los adyuvantes como "el pequeño secreto sucio de los inmunólogos".
Aunque existe un gran número de sustancias con capacidad adyuvante, debido a que no se conoce su
mecanismo de acción, y por ende los efectos secundarios a corto y largo plazo, en la actualidad existen muy
pocos adyuvantes autorizados para uso en humanos. Dado que las regulaciones tendían a ser más flexibles
para vacunas veterinarias, en estas vacunas es posible encontrar una mayor diversidad de adyuvantes.
Las sales de aluminio actúan principalmente aumentando la producción de anticuerpos, y por lo tanto son
útiles para vacunas cuyo objetivo son patógenos que pueden ser eliminados mediante anticuerpos. Las
vacunas adyuvantizadas con aluminio no son eficaces a la hora de combatir patógenos intracelulares, para
los que se necesita una respuesta citotóxica, de tipo Th1. Los adyuvantes se han utilizado durante más de
90 años, y actualmente son componentes fundamentales de más de 30 vacunas licenciadas para uso en
humanos.
En la actualidad, muchos compuestos de origen orgánico, inorgánico, natural, o sintético han demostrado
que son capaces de promover respuestas inmunes y tienen propiedades de potentes adyuvantes. Estas
sustancias se pueden dividir en dos grupos: inmunoestimulantes (entre los que se encuentran las saponinas,
los agonistas de TLRs, y las citoquinas), y agentes de entrega (delivery agents, tales como emulsiones, micro
y nanopartículas, sales minerales). Los inmunoestimulantes estimulan las células presentadoras de antígeno
(APCs) y promueven la secreción de varias citoquinas. Por otro lado, los agentes de entrega ayudan a
preservar la conformación de los antígenos para que puedan ser presentados de forma adecuada a las APCs,
y promueven una liberación lenta de los antígenos, promoviendo una estimulación del sistema inmune
continua. Por ejemplo, los agonistas de TLRs y otros inmunoestimulantes pueden estimular el reclutamiento
de células inmunes y la secreción de citoquinas, mientras que las emulsiones y las sales minerales pueden
producir un efecto depósito en el sitio de inoculación con liberación prolongada del antígeno y la
estimulación continua de células inmunes.
Página 9 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
Figura
2.
Respuesta
inmune
a
la
vacunación
con
y
sin
adyuvante.
Adaptado
de
Pasquale
et.
al.
Vaccines
2015,
3,
320-‐343;
doi:10.3390/vaccines3020320.
Los
adyuvantes
han
sido
fundamentales
para
lograr
el
éxito
de
muchas
vacunas,
incluyendo
vacunas
terapéuticas
y
vacunas
contra
cáncer.
El
uso
de
adyuvantes
puede
implicar
la
reducción
en
la
cantidad
de
antígeno
necesario
en
la
vacuna
(efecto
dose-‐sparing),
disminuyendo
costos
y
acelerando
los
procesos
de
producción
de
vacunas.
Esto
último
es
muy
importante
cuando
surge
un
brote
de
una
nueva
infección,
o
por
ejemplo,
en
el
caso
de
la
pandemia
de
influenza
en
el
2009/2010,
donde
contar
rápidamente
con
una
vacuna
contra
el
virus
pandémico
era
fundamental
para
proteger
a
la
población.
A
pesar
de
la
importancia
en
el
desarrollo
de
vacunas,
sólo
unos
pocos
adyuvantes
han
sido
licenciados
para
uso
clínico
y
el
desarrollo
de
nuevos
adyuvantes
que
sean
seguros,
efectivos
es
fundamental
para
el
desarrollo
de
nuevas
vacunas.
La
seguridad
de
los
adyuvantes
es
evaluada
en
el
contexto
de
la
vacuna
con
la
que
será
utilizado.
Es
decir,
mientras
los
componentes
de
una
vacuna
son
evaluados
individualmente
en
etapas
pre-‐clínicas,
la
evaluación
de
seguridad
que
se
debe
realizar
para
cualquier
vacuna,
debe
considerar
el
producto
final,
con
todos
sus
componentes,
y
no
se
aprueba
el
uso
de
un
adyuvante
determinado,
si
no
que
se
aprueba
el
adyuvante
en
el
contexto
de
una
formulación
particular.
Una
nueva
estrategia
para
mejorar
la
eficacia
de
las
vacunas,
es
lograr
formulaciones
de
adyuvantes
mediante
la
combinación
de
dos
o
más
de
ellos,
que,
al
combinarse,
actúan
de
manera
sinérgica,
activando
varios
mecanismos
inmunes.
Estos
"adyuvantes
combinados"
o
Sistemas
de
Adyuvantes
(AS,
del
inglés
Adjuvant
systems™,
GlaxoSmithKline
(GSK))
son
combinaciones
de
adyuvantes
clásicos
e
inmunoestimulantes
específicamente
diseñados
para
dirigir
la
respuesta
inmune
adaptativa
contra
patógenos
específicos
en
una
población
determinada,
incluyendo
niños,
adultos
mayores,
e
individuos
inmunocomprometidos.
Ya
han
sido
registrados
en
varias
vacunas
humanas
y
veterinarias,
y
nuevas
combinaciones
de
adyuvantes
se
encuentran
en
vacunas
en
ensayos
clínicos.
A
medida
que
se
mejora
el
entendimiento
sobre
el
tipo
de
respuesta
necesaria
para
inducir
protección
frente
a
distintas
enfermedades
mediante
vacunación,
la
combinación
de
adyuvantes
surge
como
una
buena
estrategia,
ya
que
no
sólo
logran
aumentar
la
intensidad
de
la
respuesta
inmune
generada,
sino
dirigir
la
respuesta
desencadenada
hacia
el
perfil
deseado,
ya
sea
hacia
Th1,
Th2,
o
Th17.
Ya
se
están
utilizando
varios
AS
en
vacunas
ya
aprobadas,
y
otros
aún
están
en
formulaciones
en
ensayos
clínicos.
AS01
(MPL
+
QS-‐21)
forma
parte
de
la
vacuna
contra
malaria
recientemente
licenciada,
AS03
fue
aprobado
para
vacunas
contra
influenza
pre-‐
pandémica
y
pandémica,
y
AS04
para
la
vacuna
contra
el
HPV
(Cervarix™)
y
contra
el
virus
de
la
hepatitis
B
(HBV)
(Fendrix®).
Página 10 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
Los aspectos prácticos del aumento de la respuesta inmune pueden ser varios: los adyuvantes pueden
promover reducciones en la cantidad de antígeno necesaria por dosis de vacuna. Una mejora en la calidad
de la respuesta inmune puede implicar que se requieran menos dosis para lograr la protección. La
combinación de la reducción de la cantidad de antígeno por dosis y de la cantidad de dosis puede tener
importantes implicancias en el suministro y el acceso de las vacunas a nivel mundial. Los adyuvantes
también pueden mejorar las respuestas inmunes en poblaciones que generalmente no responden
eficazmente frente a la vacunación, tales como niños, adultos mayores, e individuos
inmunocomprometidos. Dependiendo de la señal inicial que se active del sistema inmune innato, la elección
del adyuvante puede direccionar el tipo de respuesta adaptativa que se desencadenará contra el antígeno
administrado, preferentemente activando respuestas de células T específicas. El aumento del
entendimiento del rol potencial de los adyuvantes ha significado rápidos avances en el desarrollo de
vacunas. Nuevas vacunas adyuvantizadas que están en desarrollo tienen como blanco patógenos muy
desafiantes tales como el virus del dengue, cytomegalovirus, HIV, enfermedades malignas tales como
melanoma y cáncer de pulmón, y poblaciones desafiantes, tales como los adultos mayores. A pesar del
rápido progreso en el diseño de antígenos y adyuvantes, aún tenemos brechas de conocimiento que no nos
permiten terminar de entender el sistema inmune, tales como la contribución relativa de las respuestas
inmunes innatas y adaptativas en la protección frente a patógenos específicos, y el modo de acción
específico de adyuvantes particulares. Nueva información, derivada de distintas disciplinas, tales como
biología de sistemas, vaccinómica, transcriptómica, y epigenética, sin dudas va a contribuir al
entendimiento de la vacunación y del sistema inmune. Un mayor entendimiento del modo de acción de los
adyuvantes también va a facilitar la evaluación del perfil de seguridad de nuevas vacunas adyuvantizadas.
Esquema de Vacunación
El actual Plan Nacional de Vacunación (PNV) se crea en el año 1982. Mediante la Ley 15.272, se establece
la obligatoriedad de la vacunación contra ocho enfermedades prioritarias (tuberculosis, poliomielitis,
difteria, tétanos, tos ferina, sarampión, rubeola y paperas). La vacunación es universal, gratuita y
obligatoria, y es un programa prioritario para el Ministerio de Salud Pública (MSP).
El esquema inicial pautado incluía las vacunas BCG (contra la tuberculosis), triple bacteriana (difteria,
tétanos y tos ferina), OPV (vacuna poliomielítica oral), y triple viral (sarampión, rubeola y paperas) (ver tabla
1).
Desde entonces el Esquema de Vacunación ha tenido múltiples incorporaciones:
Ø En el año 1992 se introduce una segunda dosis de vacuna anti-‐sarampión a los 5 años de edad.
Ø En el año 1994 se introduce la vacuna anti-‐Haemophilus influenzae tipo b (Hib).
Ø En el año 1999 se introduce la vacuna anti-‐varicela y la pentavalente (que incluye combina la vacuna
triple viral con Hib y Hepatitis B), agregando además una dosis de vacuna anti-‐hepatitis B en adolescentes
(12 años).
Ø En el año 2008 se introducen las vacunas anti-‐hepatitis A y la vacuna anti-‐neumocóccica 7 valente, que
en el año 2010 es sustituida por la vacuna anti-‐neumocóccica conjugada 13 valente.
Ø En el año 2012 se incorpora el componente anti-‐pertussis (como componente acelular) a la vacuna doble
bacteriana de los 12 años (vacuna dpaT) y se sustituye la vacuna anti-‐poliomelítica vía oral (OPV, Vacuna
Sabin) por la inactivada vía i.m. (IPV, Vacuna Salk).
Ø En el año 2013 se incorpora la vacuna tetravalente contra el HPV (tipos 6,11, 16 y 18) para todas aquellas
adolescentes al cumplir los 12 años en esquema de tres dosis.
Ø En el año 2014 se incorpora la segunda dosis de vacuna anti-‐varicela a los 5 años de edad.
Ø En el año 2015 se introduce la vacuna dpaT, por su componente de B. pertussis, a todas las embarazadas
(en cada gestación).
Ø En el año 2017 se modifica el esquema de vacunación anti-‐VPH, pasando de tres dosis a dos dosis en
menores de 15 años. Se suprime la dosis de IPV de los 15 meses de edad (que pasará a darse a partir de
2021 a los 5 años de edad).
Ø En el año 2019 se incorpora la vacuna anti-‐VPH en varones de 11 y 12 años de edad o que estén cursando
6to año escolar.
Página 11 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
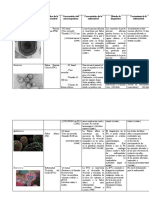
Tabla 1: Vacunas incluidas en el actual esquema nacional de vacunación.
Vacuna Agente etiológico Descripción del componente – Vacuna basada en:
BCG Micobacterium tuberculosis Bacterias atenuadas: bacilo de Calmette-‐Guerin (M. bovis)
Clostridium tetani Subunidades: toxoide
Corynebacterium diphtheriae Subunidades: toxoide
Pentavalente Bordetella pertussis Bacteria muerta (vacuna celular)
Haemofilus Influenza del tipo B Subunidades: oligosacaridos conjugados
Virus de la Hepatitis B Subunidades: proteina recombinante
IPV Polio virus Virus inactivado (vacuna Salk)
Virus del Sarampión Virus atenuado
S.R.P Virus de la Rubéola Virus atenuado
(triple viral) Mixovirus parotiditis Virus atenuado
Varicela Virus varicela zóster Virus atenuado
Neumococco 13V Streptococcus pneumoniae Subunidades: polisacaridos conjugados (13 valente)
Hepatitis A Virus de la Hepatitis A Virus inactivado
HPV Papiloma virus humano VLP (virus like particle): tetravalente
Clostridium tetani Subunidades: toxoide
Triple bacteriana Corynebacterium diphtheriae Subunidades: toxoide
(DPT) Bordetella pertussis Bacteria muerta (vacuna celular)
Clostridium tetani Subunidades: toxoide
Triple bacteriana Corynebacterium diphtheriae Subunidades: toxoide
acelular (dpaT) Bordetella pertussis Subunidades: proteínas (vacuna acelular)
Doble bacteriana Clostridium tetani Subunidades: toxoide
(dT) Corynebacterium diphtheriae Subunidades: toxoide
Queda así establecido el actual Esquema Nacional de Vacunaciones (Figura 3) que asegura el acceso
universal y gratuito a diversas vacunas para prevenir enfermedades infectocontagiosas.
Figura 3: Esquema de Vacunación vigente en Uruguay.
Página 12 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
Además, en forma de campaña se administran las vacunas antigripal y anti-‐neumocócica 23 valente.
También, desde el año 2005, la vacunación anti-‐hepatitis, se administra en forma obligatoria a personal de
salud.
La vacunación como acto comunitario
El principal objetivo de la vacunación es prevenir la infección o enfermedad en un individuo mediante la
vacunación del mismo. Sin embargo, la vacunación también permite alcanzar otros objetivos:
- Control o eliminación, y hasta erradicación de enfermedades.
- Protección de individuos no vacunados.
- Protección frente a patógenos no relacionados con la vacuna
1) Control, eliminación y erradicación de enfermedades prevenibles con vacunas.
El control o eliminación de una enfermedad causada por un agente especifico implica la reducción
permanente de la incidencia de ésta en un área geográfica dada como resultados de esfuerzos deliberados
(principalmente, vacunación y vigilancia epidemiológica). Requiere mantenimiento de medidas de
intervención continuas. Se logra por la interrupción de la transmisión interpersonal (circulación del agente,
como polio o sarampión) o por una alta protección ante enfermedades de riesgo continuo (tétanos
neonatal).
En estos casos, existe riesgo permanente de reingreso, por lo que deben mantenerse altas coberturas,
entendiéndose por COBERTURA VACUNAL al porcentaje de individuos vacunados de la cohorte a vacunar y
evitar BOLSILLOS DE BAJA COBERTURA, e intensificar la vigilancia epidemiológica para permitir la detección
temprana de un reingreso.
En caso de reingreso o brote, existen distintas estrategias como pueden ser las campañas de vacunación de
la población susceptible o mediante vacunación en anillo, que implica la vacunación de personas/población
alrededor del individuo o lugar donde surge el brote para contener la transmisión interpersonal (Ej. Ébola,
meningitis).
La erradicación implica la reducción permanente a 0 de la incidencia mundial de la infección causada por
un agente especifico como resultado de esfuerzos deliberados. Hasta la fecha, la viruela ha sido la única
enfermedad erradicada gracias a la vacunación, mientras que la poliomielitis está en camino de ello.
Una vez que se logra erradicar una enfermedad, las medidas de intervención ya no son necesarias, porque
hay eliminación mundial de la circulación del agente.
Los criterios de enfermedad erradicable son:
• No existe reservorio animal.
• El hombre es crítico en la transmisión.
• Existe una vacuna y una estrategia de vacunación efectiva y segura.
• Existe estrategias de vigilancia.
Existen varias enfermedades que se encuentran transitando de la fase de control a erradicación, como la
poliomielitis, Sarampión, Rubeola y Hepatitis A.
2) Protección de individuos no vacunados
Existen algunas estrategias que permiten proteger a individuos no vacunados, ya sea porque no quieren
vacunarse o porque no pueden.
ESTRATEGIA
CAPULLO
O
NIDO:
implica
la
vacunación
de
todo
el
entorno
cercano
al
individuo
a
proteger.
Como
ejemplo,
esta
estrategia
se
aplica
para
proteger
a
los
recién
nacidos
de
la
tos
ferina
mediante
la
vacunación
de
la
madre
en
el
último
semestre
de
gestación
y
a
todos
los
individuos
adultos
en
estrecho
contacto
con
el
niño
al
nacer.
EFECTO
REBAÑO:
se
obtiene
cuando
se
genera
una
alta
INMUNIDAD
DE
REBAÑO,
es
decir
que
una
proporción
de
individuos
desarrolla
inmunidad,
ya
sea
natural
o
adquirida,
en
una
población
dada,
permitiendo
la
reducción
de
la
circulación
del
agente
causante
de
la
enfermedad.
Efecto
rebaño
solo
es
aplicable
cuando
la
persona
participa
en
la
transmisión
del
agente
y
cuando
la
inmunización
confiere
algo
de
protección
a
la
infección
(no
solo
a
la
enfermedad).
La
inmunidad
de
rebaño
conlleva
a
una
perturbación
Página 13 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
de la incidencia de la infección o la enfermedad en el segmento no inmunizado (no vacunado) de la
población, lo que es conocido como EFECTO REBAÑO. En general, está perturbación conlleva a la reducción
de la incidencia. Ocasionalmente puede generar un aumento de la incidencia o de la severidad de la
enfermedad, por ejemplo, por corrimiento de la edad de infección en los no inmunizados (ej. Hepatitis A,
varicela).
El
efecto
rebaño
es
un
elemento
clave
en
los
programas
de
inmunización,
ya
que
permite
el
control
o
eliminación,
y
hasta
la
erradicación
de
enfermedades.
Para
ello
es
necesario
considerar
el
número
básico
de
reproducción
(R0)
que
es
el
promedio
del
número
de
casos
secundarios
que
surgen
del
promedio
del
número
de
casos
primarios
en
una
población
susceptible.
Si
R0≥1
existe
transmisión
y
propagación
de
la
enfermedad,
mientras
que
si
Si
R0<1
puede
permitir
la
erradicación
de
la
enfermedad.
La
fracción
susceptible
de
la
población
es
1/R0,
entonces
1-‐
1/R0
es
la
fracción
de
la
población
a
ser
vacunados
para
obtener
un
efecto
de
rebaño.
Por
ejemplo,
para
un
R0=2,
la
población
susceptible
es
1/R0=
0,5.
Y
por
tanto,
para
controlar
la
enfermedad,
la
fracción
de
la
población
a
vacunar
o
inmunizar
tiene
que
ser
≥
0.5,
o
sea
que
el
50
%
de
la
población
tiene
que
tener
inmunidad.
Figura
4:
Graficas
de
correlación
entre
el
umbral
de
inmunidad
de
rebaño
en
función
del
R0,
asumiendo
una
vacuna
100%
efectiva.
3) Protección
frente
a
patógenos
no
relacionados
con
la
vacuna
(protección
no-‐específica).
Algunas
vacunas
han
demostrado
proteger
frente
a
cepas
o
tipos
no
vacunales
a
través
de
la
generación
de
PROTECCIÓN
CRUZADA.
Por
ejemplo,
HPV.
Otras
vacunas
han
demostrado
proteger
frente
a
microorganismos
no
relacionados.
Esto
se
debe
a
la
capacidad
de
estimular
la
INMUNIDAD
ENTRENADA
(Trained
Immunity),
que
implican
una
activación
transitoria
de
las
células
del
sistema
inmune
innata,
la
cual
permiten
que
éstas
respondan
de
forma
más
rápida
y
potente
frente
al
ingreso
de
cualquier
microorganismo.
Un
ejemplo
muy
estudiado
de
este
tipo
de
vacunas
es
la
BCG
(figura
5).
Página 14 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
Figura 5: Esquema representativo de la Inmunidad Entrenada inducida por la BCG.
Vacunas contra cáncer
Hay
dos
grandes
formas
de
aplicar
la
vacunación
para
el
control
del
cáncer:
para
prevenir
la
ocurrencia
de
cáncer
(vacunas
profilácticas),
o
para
tratar
el
cáncer
una
vez
que
se
ha
desarrollado
(vacunas
terapéuticas).
El
virus
de
la
hepatitis
B
(HBV)
y
el
del
papilloma
humano
(HPV)
son
causantes
de
cáncer
de
hígado
y
cuello
de
útero
respectivamente,
y
ambos
son
muy
prevalentes
en
países
en
vías
de
desarrollo.
El
HPV
también
está
involucrado
en
la
etiología
de
otros
tipos
de
cáncer,
incluyendo
el
cáncer
de
faringe.
El
desarrollo
y
disponibilidad
de
vacunas
efectivas
contra
estos
patógenos
pueden
jugar
un
rol
fundamental
en
la
reducción
de
la
incidencia
de
cáncer.
Aunque
hay
muchos
tipos
de
HPV,
sólo
dos
de
ellos
(el
16
y
el
18)
serían
oncogénicos,
por
lo
que
las
vacunas
contra
HPV
disponibles
actualmente,
que
contienen
estos
dos
tipos,
van
a
ser
muy
efectivas
en
prevenir
este
tipo
de
cáncer.
El
objetivo
de
las
vacunas
terapéuticas
anti-‐
cáncer
es
aumentar
las
respuestas
inmunológicas
naturales
del
paciente,
que
son
capaces
de
controlar
muchos
tipos
de
cáncer.
La
importancia
de
estas
respuestas
queda
en
evidencia
por
el
aumento
de
riesgo
de
contraer
cáncer
de
los
individuos
inmunocomprometidos,
como
resultado
de
una
infección
por
HIV,
o
por
el
suministro
de
drogas
inmunosupresoras.
Las
vacunas
para
cáncer
deben
estar
dirigidas
contra
un
antígeno
específico
expresado
por
un
cáncer
específico,
y
por
lo
tanto
deben
ser
paciente-‐específicas.
Además,
deben
ser
capaces
de
sobreponerse
a
los
mecanismos
de
tolerancia,
y
a
la
inmunomodulación
inducida
por
el
cáncer,
en
un
intento
por
"asegurar
su
supervivencia".
Para
lograr
esto
último,
ha
sido
necesario
el
uso
de
potentes
adyuvantes.
Aunque
hay
ejemplos
de
éxito
transitorio
de
vacunación
anti-‐
cáncer
en
pacientes,
hasta
ahora
solo
han
sido
licenciadas
2
vacunas
anticáncer
en
EEUU
(Provenge®,
contra
el
cáncer
de
próstata
en
EEUU,
y
CIMAVax,
contra
el
cáncer
de
pulmón
en
Cuba).
Las
vacunas
terapéuticas
anti-‐cáncer,
especialmente
si
deben
ser
individualizadas
para
cada
paciente,
tienden
a
ser
muy
caras,
y
por
lo
tanto
a
tener
poco
impacto
en
la
lucha
contra
el
cáncer.
Por
el
contrario,
las
vacunas
dirigidas
contra
las
causas
de
cáncer,
profilácticas,
tienen
el
potencial
de
disminuir
en
gran
medida
la
incidencia
de
esta
enfermedad.
Página 15 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
Vacunas para enfermedades crónicas no-‐infecciosas
Hasta ahora las vacunas están dirigidas principalmente a niños, para proteger a los individuos desde el inicio
de la vida, pero existe un creciente interés en la posibilidad de usar las vacunas para el control de
enfermedades crónicas no-‐infecciosas en adultos. La lógica de este enfoque es apuntar contra uno o más
mediadores biológicos claves de estas enfermedades. En el caso de la hipertensión, hay resultados
preliminares exitosos que se lograron bajando la presión sanguínea mediante la vacunación con el péptido
de angiotensina II presentado en un constructo de partícula-‐tipo-‐virus (VLP), y enfoques similares se están
investigando para tratar la diabetes. Fumar es un factor de riesgo para contraer enfermedades
cardiovasculares y cáncer, y la vacunación podría jugar un rol importante en el control de estas
enfermedades, ayudando a los fumadores a superar su adicción a la nicotina. Mediante la vacunación es
posible inducir altos títulos de anticuerpos anti-‐nicotina mediante un péptido de nicotina expresado en una
VLP. Estos anticuerpos impiden que la nicotina active los centros de placer en el cerebro, y puede ayudar a
los fumadores a superar su adicción. El mismo enfoque se está utilizando para ayudar a personas adictas a
otras drogas. Aunque encontrar los blancos adecuados es muy desafiante, al igual que lograr desencadenar
una respuesta inmune contra ellos que no genere efectos colaterales no deseados, el uso de las vacunas
para controlar distintos tipos de enfermedades crónicas no-‐infecciosas está ganando interés, y en los
próximos años puede volverse una herramienta muy valiosa para controlar estas enfermedades crónicas.
Desarrollo de vacunas
El desarrollo de una nueva vacuna, desde su diseño hasta su implementación en la población es un proceso
complejo, interdisciplinario, involucrando desde científicos trabajando en ciencia básica, hasta economistas
y especialistas en comunicación. Es un proceso largo, que dura por lo general, al menos 10 años, pero puede
demorar décadas dependiendo de las dificultades que se vayan encontrando. Los costos de desarrollo
varían, dependiendo de la vacuna, pero están en rango de los cientos de millones de euros. Para lograr el
éxito, el desarrollo de una nueva vacuna necesita un equipo interdisciplinario implacable, y un buen
liderazgo con competencias para adaptarse a cambios, y solucionar problemas. El desarrollo se lleva
adelante con un documento que se conoce como Perfil del Producto Deseado (TTP del inglés "Target
Product Profile), que resume las características y el desempeño que se espera de la futura vacuna. Sin
embargo, este documento no es estático, se inicia en las etapas de investigación científica, y puede ir
evolucionando a medida que se avanza en el desarrollo. Presenta la necesidad médica de la nueva vacuna
(basándose en la epidemiología), las demandas del mercado (viabilidad económica), así como también las
dificultades técnicas y científicas. Siempre y cuando los cambios no amenacen la viabilidad económica de la
vacuna, el TTP se va a ir adaptando a la luz de los resultados obtenidos durante las etapas de investigación.
Los cambios propuestos son revisados por un comité de expertos de todas las áreas. Muchas veces, la
solicitud de cambios mayores puede dar lugar a la finalización del proyecto. El proceso se realiza mediante
una serie de etapas en un orden definido. El orden de las etapas no puede alterarse, aunque en caso de
falla de alguna de ellas, debe repetirse hasta lograr ser exitosa. De lo contrario no es posible pasar a la
siguiente etapa. En este sentido, es bastante común, que una vacuna vuelva a la primer etapa (de
investigación en el laboratorio), luego de fallar en alguna de las fases clínicas. Las fases principales para el
desarrollo de una vacuna son:
0. Necesidad de una nueva vacuna: justificación: epidemiología y estudio de mercado. Se crea el TTP.
1.
Etapa
de
descubrimiento:
es
llevada
adelante
por
un
"equipo
de
descubrimiento",
que
explora
diferentes
estrategias
de
vacunas,
con
el
fin
de
identificar
posibles
antígenos
protectivos,
producir
y
caracterizar
una
vacuna
"prototipo"
y
finalmente
demostrar
que
funciona
en
modelo
animal.
En
esta
etapa
es
cuando
se
generan
patentes
de
propiedad
intelectual.
2.
Estudios
pre-‐clínicos:
a
la
"vacuna
prototipo"
se
le
realizan
pruebas
de
toxicidad
y
potencia
en
animales
de
laboratorio
y
hasta
en
primates
no
humanos
(en
el
caso
de
vacunas
para
humanos)
mediante
procedimientos
que
cumplan
con
los
comités
de
ética
y
las
regulaciones
de
los
distintos
países.
El
objetivo
de
esta
etapa
es
demostrar
que
la
vacuna
es
segura
y
efectiva
en
animales.
Página 16 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
3. Desarrollo del proceso y scale-‐up a nivel de producción: se lleva la "vacuna prototipo", producida en
pequeña escala, a escala industrial. Se debe poner especial énfasis en la homogeneidad y calidad del
producto logrado, así como también el rendimiento del proceso para que el proyecto continúe siendo
económicamente viable.
4.
Ensayos
clínicos:
La
vacuna
es
evaluada
en
personas,
en
las
distintas
etapas
de
ensayos
clínicos,
mediante
procedimientos
que
cumplan
con
los
comités
de
ética
y
las
regulaciones
de
los
distintos
países,
así
como
también
con
el
consentimiento
informado
de
todos
los
participantes
de
los
ensayos.
El
objetivo
de
esta
etapa
es
demostrar
que
la
vacuna
es
segura
y
efectiva
en
humanos.
En
el
caso
de
vacunas
veterinarias,
se
realizan
pruebas
en
la
especie
de
destino
de
la
vacuna.
5.
Etapa
de
registro
frente
a
organismos
regulatorios:
se
realizan
los
trámites
legales
y
administrativos
frente
a
los
organismos
regulatorios
donde
será
comercializada
la
vacuna.
Se
debe
presentar
toda
la
evidencia
científica
generada.
6. Producción comercial: se realiza la producción a gran escala de la vacuna, en condiciones GMP,
cumpliendo con las regulaciones y estándares de los organismos regulatorios donde fue registrada la
vacuna.
7.
Lanzamiento
del
producto
al
mercado:
se
hace
un
lanzamiento
para
presentar
el
producto
al
mercado,
y
asegurar
su
comercialización.
8. Etapa de pos-‐comercialización: Farmacovigilancia, ensayos clínicos fase 4. Se registran los efectos
adversos asociados a las vacunas durante todo el tiempo en que se comercialicen. Con estos datos se hacen
estudios y estadísticas para corroborar que no existan efectos adversos a largo plazo inducidos por las
vacunas.
El
pasaje
de
una
etapa
a
la
siguiente
implica
la
revisión
formal
de
comités
constituidos
por
miembros
de
alta
jerarquía
del
laboratorio
donde
se
esté
desarrollando
la
vacuna,
y
es
luego
de
su
aprobación
que
se
puede
realizar
el
pasaje
a
la
siguiente
etapa.
Vacunología
Reversa
Una
de
las
grandes
revoluciones
en
el
desarrollo
de
vacunas,
está
ligado
al
advenimiento
de
las
tecnologías
de
secuenciación
de
genomas,
que
han
permitido
un
cambio
radical
en
el
desarrollo
de
la
vacunología,
que
avanzaba
muy
lentamente.
El
punto
de
quiebre
fue
la
publicación,
en
1995,
del
primer
genoma
secuenciado
de
un
organismo.
Mediante
la
secuenciación
del
genoma,
y
mediante
la
determinación
del
repertorio
antigénico
completo
de
un
agente
infeccioso,
es
posible
identificar
candidatos
que
resulten
protectivos
al
ser
utilizados
como
antígenos
vacunales.
El
método,
denominado
"vacunología
reversa",
y
desarrollado
por
Rino
Rappuoli,
ha
proporcionado
un
cambio
en
la
perspectiva
del
diseño
de
vacunas.
La
idea
de
RV
se
originó
para
superar
los
problemas
encontrados
al
intentar
desarrollar
una
vacuna
eficaz
contra
Meningococo
B
(MenB).
La
secuenciación
del
genoma
de
la
cepa
virulenta
MC58
de
MenB
permitió
seleccionar
de
los
datos
genómicos,
posibles
blancos
de
la
vacuna.
El
principio
de
las
bases
de
RV
fue
que
los
blancos
vacunales
exitosos
eran
proteínas
o
expuestas
en
la
superficie
del
patógeno,
o
secretadas
al
medio
extracelular.
El
análisis
bioinformático
predijo
que
MenB
codificaba
para
2158
proteínas,
de
las
cuales
más
de
600
estaban
expuestas
en
la
superficie
o
eran
excretadas.
De
éstas,
350
fueron
clonadas
en
E.
coli,
expresadas,
y
utilizadas
para
inmunizar
ratones.
El
suero
de
los
animales
inmunizados
fue
evaluado
en
un
ensayo
bactericida,
que
se
correlaciona
con
la
protección.
En
cada
paso,
los
candidatos
que
no
cumplieran
los
criterios
de
calidad,
eran
descartados.
Este
proceso
derivó
en
la
identificación
de
candidatos
vacunales
previamente
desconocidos.
En
este
proceso
se
identificaron
3
Ags
protectivos
para
varias
cepas
de
MenB
(fHbp,
NadA,
and
NHBA),
y
se
combinaron
con
una
vesícula
de
membrana
externa
(OMV,
outer
membrane
vesicle)
de
MenB,
resultando
en
la
primera
vacuna
anti-‐MenB.
Esta
fue
la
primera
vacuna
basada
en
RV
que
ha
tenido
una
opinión
positiva
de
la
EMEA
(European
Medicines
Agency),
y
fue
aprobada
con
el
nombre
comercial
de
Bexsero®.
Luego
del
éxito
del
proyecto
de
la
vacuna
de
MenB,
la
RV
ha
sido
aplicada
en
Página 17 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
vacunas contra numerosos patógenos, tales como S. pneumoniae, Streptococcus pyogenes, Chlamydia
pneumonia, Chlamydia trachomatis, Streptococcus agalactiae, E. coli, y Leishmania major. La estrategia
basada en genómica de RV puede proveer soluciones innovadoras para el diseño de vacunas difíciles o
incluso imposibles de desarrollar utilizando métodos convencionales.
Correlatos de protección
Los correlatos de protección frente a infecciones de distintos patógenos incluyendo virus, bacterias y
parásitos, son parámetros medibles del sistema inmune adaptativo que estadísticamente se correlacionan
con protección frente a una infección específica. El parámetro puede tener un mecanismo de protección
vinculado, o simplemente puede correlacionarse con la protección sin vínculo aparente o sin ser el efector
inmunológico que confiere protección. Stanley Plotkin definió terminología para describir diferentes tipos
de marcadores que se correlacionan con protección, y además hizo las siguientes consideraciones:
• No
tiene
por
qué
existir
una
correlación
lineal
entre
el
marcador
y
la
protección.
El
sistema
inmune
innato
puede
eliminar
pequeñas
dosis
de
desafío,
mientras
que
grandes
dosis
pueden
sobrecargar
al
sistema
inmune
adaptativo.
• Los
correlatos
de
protección
no
se
limitan
a
la
vacunación.
También
aplican
a
la
protección
resultante
de
una
infección
natural.
• El
mecanismo
de
protección
no
tiene
por
qué
ser
el
mismo
que
el
mecanismo
para
recuperarse
de
una
infección.
La
inmunidad
mediada
por
células
tiene
un
rol
más
relevante
en
la
resolución
de
una
infección
viral
que
en
su
prevención.
Por
ejemplo,
la
prevención
contra
viruela,
se
logra
mediante
anticuerpos
neutralizantes,
mientras
que
la
eliminación
de
la
infección
está
mediada
por
respuestas
celulares.
• La
identificación
de
un
correlato
de
protección
no
significa
que
no
pueda
estar
actuando
también
otro
brazo
del
sistema
inmune
y
contribuyendo
en
la
protección
(redundancia
de
los
mecanismos
biológicos).
Stanley
Plotkin
y
Peter
Gilbert
han
propuesto
una
definición
revisada
para
los
correlatos
de
protección.
El
concepto
central
es
que
"un
correlato
refleja
correlación
estadística
entre
un
marcador
inmunológico
y
la
protección,
pero
no
implica
necesariamente
que
el
marcador
sea
la
causa
de
la
protección".
Producción y mercado de vacunas
Productores de vacunas
En los países desarrollados hay 5 grandes compañías farmacéuticas que cuentan con el 80% del mercado
de las vacunas. La mayoría de los productores de vacunas eran históricamente independientes de las
grandes compañías farmacéuticas, pero las necesidades crecientes de capital y las perspectivas de
desarrollo, llevaron a una fase de fusión y concentración del capital, que todavía está en marcha. Los
mayores productores de vacunas son: GlaxoSmithKline (GSK) y su división GSK Vaccines, Sanofi con su
división de vacunas Sanofi Pasteur, Merck & Co también conocida como Merck Sharp & Dohme (MSD),
Pfizer, y Seqirus. Novartis salió del negocio de las vacunas en 2013, luego de vender su línea de producción
de vacunas (salvo influenza) a GSK, y su línea de producción de vacunas de influenza a CSL (Australia). La
división de influenza de CSL se conoce como Seqirus, y es el segundo productor más grande de vacunas
contra influenza luego de Sanofi Pasteur.
En los países desarrollados, el negocio de las vacunas está muy consolidado y hay poco espacio para nuevos
productores de vacunas, debido al alto costo de inversión necesario. En países emergentes, esto es más
fácil, como en el caso de Cuba y el Instituto Finlay, Senegal con la Fundación del Instituto Pasteur de Dakar,
India y China, y han aparecido nuevos productores de vacunas que compiten con las grandes farmacéuticas
por una parte muy pequeña del mercado. También hay numerosos productores locales que están
mejorando sus niveles de calidad, y están comenzando a exportar su producción. Los productores locales
son ayudados por algunos de sus países, en un intento por mantener soberanía en el abastecimiento de
vacunas para las enfermedades principales. El Instituto de Sueros de India se ha convertido en el 5to
Página 18 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
productor de dosis de vacunas del mundo. Algunos otros laboratorios locales han sido adquiridos por
grandes farmacéuticas del mundo desarrollado.
El panorama de la industria de vacunas está cambiando a gran velocidad, debido a los productores de
vacunas de los países emergentes. En 2001, la Global Alliance for Vaccines and Immunization (GAVI) que
suministra vacunas para países del tercer mundo, adquiría vacunas de un solo proveedor de países del
tercer mundo y de cuatro del primer mundo. En 2010 el número total de proveedores pasó a ser más del
doble, y más de la mitad son de países emergentes.
El mercado de las vacunas y los anti-‐vacunas
La vacunación es un tratamiento profiláctico que se administra a individuos sanos para protegerlos de
posibles enfermedades. Las vacunas son, entonces, muy diferentes de los medicamentos que se utilizan
para tratar individuos enfermos, y esta diferencia afecta drásticamente la forma en que las personas
perciben las vacunas. Las personas a vacunarse son individuos sanos, y reticentes a los riesgos relacionados
a la vacunación, especialmente si el riesgo de contraer la enfermedad es bajo. La responsabilidad de
mantener vacunada a la población recae entonces en los sistemas de salud de los países mediante
esquemas de vacunación obligatorios. La mayoría de las vacunas son financiadas por gobiernos o
fundaciones sin fines de lucro, por lo que cada vez se presiona más a los productores de vacunas para que
bajen el costo de las vacunas. Esto explica por qué el mercado de las vacunas es pequeño en comparación
al de los productos farmacológicos. Para las grandes corporaciones, en 2009, el mercado de vacunas
rondaba los 29 mil millones de euros, mientras que el de los productos farmacológicos era de 790 mil
millones de euros, es decir, el mercado de las vacunas es entre el 3 y el 4 % del mercado de los
farmacológicos. En 2013, el mercado de las vacunas creció un 10 a 15 % frente al crecimiento del mercado
de los farmacológicos del 5 al 7 %. Se han realizado inversiones significativas para el mercado de
inmunoterapias contra cáncer y enfermedades autoinmunes, que es mucho más lucrativo que el de las
vacunas. Sin embargo, los desafíos biológicos a superar para ese tipo de productos, son mucho mayores
que para los de las vacunas contra agentes infecciosos. En consecuencia, no se puede especular con la
evolución del mercado de las inmunoterapias.
Hay dos grandes mercados para las vacunas: El mercado público es para las vacunas que son consideradas
como prioridad por los sistemas de salud de los distintos países. Los estados compran directamente las
vacunas a las compañías, y son suministradas gratis a la población. Incluye las vacunas pediátricas
obligatorias. Para los productores de vacunas, estos mercados implican que deben competir con otras
empresas, lo que resulta en una disminución del precio, pero si logran hacer la venta, es una venta de gran
volumen. El mercado público es por lejos el mayor mercado de las vacunas.
El mercado privado es para vacunas que no son consideradas como prioridad por los sistemas de salud de
los países, y no son administradas gratis a la población ni reembolsadas por los seguros de salud. Las vacunas
para turistas (o por viajes) son parte de este mercado privado. Las vacunas de este mercado pueden ser
vendidas a buen precio, pero los volúmenes de venta son bajos, especialmente si en el sistema de salud del
país se ofrece una vacuna similar.
El mercado de las vacunas también se puede dividir de acuerdo a la edad de los individuos a ser vacunados.
Históricamente, el mercado de vacunas era dominado por las vacunas pediátricas, con pocas vacunas para
adultos. Una vez saturado este mercado, se empezaron a desarrollar los mercados de vacunas para
adolescentes, adultos y adultos mayores.
Geográficamente, los mayores mercados en términos económicos siguen estando en EEUU y Europa,
aunque el mercado ya está saturado, y hay una tendencia al decrecimiento debido a recortes en el
presupuesto de salud. El hecho de que las enfermedades prevenibles por vacunas estén casi desaparecidas
en el primer mundo, sumado a altos niveles de educación, y el aumento del individualismo, han alimentado
el escepticismo hacia las vacunas, e incluso generado movimientos "anti-‐vacunas". Por esta razón ha habido
una disminución de la cobertura de niños vacunados, principalmente contra sarampión, rubeola y paperas,
resultando en brotes de nuevos casos, y hasta en la muerte de niños en esta región del mundo por esas
Página 19 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
enfermedades. Las vacunas contra HPV que fueron aprobadas hace algunos años, también han presentado
resistencia en la población, y su implementación ha sido fuente de escándalos y numerosos artículos de
prensa con testimonios de personas del movimiento "anti-‐vacunas" con conceptos equivocados.
Sin embargo, el mercado de las vacunas aún tiene margen de crecimiento en los países subdesarrollados,
donde aún mueren niños de enfermedades prevenibles por vacunas, debido a malas condiciones sanitarias,
y a falencias en políticas de salud, política en general, y en recursos económicos mal distribuidos.
Las vacunas son productos biológicos más complejos de producir y de controlar que los productos
farmacéuticos convencionales. Como consecuencia, no hay "vacunas genéricas" como sí hay fármacos
genéricos. Para demostrar que las vacunas son seguras y eficaces, previo a su aprobación, y también
durante todo el tiempo que la vacuna esté en uso, deben someterse a rigurosos ensayos clínicos y a
farmacovigilancia.
Desafíos
Desafíos en la investigación en vacunas
La investigación es necesaria, no solo para el desarrollo de nuevas vacunas, sino también para optimizar las
formas de administración. El desarrollo de jeringas descartables disminuyó drásticamente el riesgo de
transmisión de infecciones debido a la vacunación, lo que fue un gran problema antes de las jeringas
descartables, principalmente en los países en vías de desarrollo. Sin embargo, sería también conveniente
que las vacunas que hoy deben administrarse por vía inyectable (lo que requiere personal capacitado para
ello, que en muchas zonas del mundo no se encuentra disponible), se pudieran administrar por una vía
alternativa. En este sentido, se están explorando diferentes métodos, tales como parches para la piel,
micro-‐agujas, y administración por vía intranasal. Otro gran aspecto a mejorar en las vacunas, es intentar
lograr que sean más termoestables, lo que reduciría o eliminaría la necesidad de mantener la cadena de
frío desde su producción, transporte, y almacenamiento, hasta que es administrada al individuo. Este
aspecto reduciría en gran medida el costo (económico) de las vacunas, logrando que sean más accesibles a
países en vías de desarrollo.
Implementación de nuevas vacunas
Antes de la introducción de una nueva vacuna en un programa nacional de inmunización, se deben llevar
adelante una serie de discusiones respecto al costo-‐beneficio de la introducción de esa nueva vacuna,
respecto a otras necesidades del sistema nacional de salud. Una vez que se resuelve la implementación de
una nueva vacuna, es necesario superar los siguientes desafíos:
-‐ Conseguir suficiente evidencia para que quienes toman la decisión, puedan hacerlo de forma racional.
-‐
Lograr
buenas
formas
de
comunicación
a
la
sociedad,
para
lograr
que
ésta
entienda
la
importancia
de
la
aplicación
de
la
nueva
vacuna,
y
la
acepte.
-‐ Lograr los medios económicos para brindar a la población la nueva vacuna de forma gratuita y universal.
-‐ Solucionar aspectos prácticos relacionados a la introducción de la nueva vacuna en el programa de
vacunación (tener stock suficiente, buenas condiciones de almacenamiento, mantenimiento de la cadena
de frío, contar con personal disponible para su administración)
Vaccine hesitancy & anti-‐vaxxers
Como se mencionó previamente, el surgimiento de corrientes de personas anti-‐vacunas pone en riesgo la
aceptación de las vacunas por parte de la población, haciendo que disminuya la cobertura vacunal, y dando
lugar al surgimiento de nuevos brotes de enfermedades que estaban, aunque no erradicadas, controladas.
Es un desafío de la comunidad científica y de todo el personal médico y de salud brindar información de
Página 20 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
forma responsable y respetuosa para que todas las personas entiendan cómo funcionan las vacunas y qué
es lo que ponen en riesgo al no vacunarse, que no solo es su propia vida, sino también la de personas que
por razones inmunológicas no pueden recibir las vacunas.
Vacunas Veterinarias y Salud Pública
Las vacunas veterinarias son importantes para la salud y bienestar animal, para la producción de alimentos,
y para la salud pública. Son un método costo-‐efectivo para prevenir enfermedades en los animales, así como
también para aumentar la eficiencia en la producción de alimento, y reducir las zoonosis y enfermedades
transmitidas por alimentos a las personas. Contar con vacunas veterinarias seguras y eficaces es
fundamental para la sociedad moderna. Sin prevenir epizootias en animales de producción, sería imposible
producir proteína animal para los 7mil millones de habitantes del planeta. Sin vacunas para animales de
compañía, (principalmente la vacuna contra la rabia), mucha gente no tendría mascotas, y no tendría la
experiencia del vínculo humano-‐animal. Sin vacunas efectivas, zoonosis tales como brucellosis y
leptospirosis serían mucho más prevalentes hoy en día.
El hecho de que tanta gente dependa del ganado y el rubro avícola para subsistir y como fuente de alimento
limita las opciones de políticas, complica decisiones comerciales a nivel local y global, y genera sensibilidad
política. Es inevitable que el mundo continúe experimentando la emergencia de nuevas enfermedades para
humanos y animales en las próximas décadas. Este desafío da cuenta de la necesidad de que las
comunidades médicas veterinarias, y de salud pública, trabajen en conjunto a nivel local e internacional.
Las enfermedades infecciosas aún siguen siendo un gran desafío para medicina humana y veterinaria, y la
interacción e interdependencia entre ambas se está reconociendo cada vez más mediante del concepto de
"una sola salud" ("one health" en inglés). Las vacunas veterinarias basadas en patógenos inactivados o
atenuados convencionalmente han hecho contribuciones esenciales manteniendo humanos y animales
sanos.
Referencias:
Greenwood et.al. Phil. Trans. R. Soc. B (2011) 366, 2733–2742 doi:10.1098/rstb.2011.0076
Finco
O
and
Rappuoli
R
(2014)
Designing
vaccines
for
the
twenty-‐first
century
society.
Front.
Immunol.
5:12.
doi:
10.3389/fimmu.2014.0001
Glick Medical Biotechnology
Adjuvants
for
Animal
Vaccines
Yulia
Burakova,1,2
Rachel
Madera,1
Scott
McVey,3
John
R.
Schlup,2
and
Jishu
Shi1
VIRAL
IMMUNOLOGY
Volume
00,
Number
00,
2017
Orchestrating
immune
responses:
How
size,
shape
and
rigidity
affect
the
immunogenicity
of
particulate
vaccines.
Naomi
Benne,
Janine
van
Duijn,
Johan
Kuiper,
Wim
Jiskoot,
Bram
Sl¨utter.
To
appear
in:
Journal
of
Controlled
Release.
2016.
Doi:
10.1016/j.jconrel.2016.05.033.
Duration
of
Humoral
Immunity
to
Common
Viral
and
Vaccine
Antigens.
Ian
J.
Amanna,
Ph.D.,
Nichole
E.
Carlson,
Ph.D.,
and
Mark
K.
Slifka,
Ph.D.
November
8,
2007.
N
Engl
J
Med
2007;
357:1903-‐1915.
DOI:
10.1056/NEJMoa066092.
Vaccine
Adjuvants:
from
1920
to
2015
and
Beyond.
Vaccines
2015,
3,
320-‐343;
doi:10.3390/vaccines3020320.
Vaccine
Potentiation
by
Combination
Adjuvants
Benoît
Levast
1,
Sunita
Awate
1,
Lorne
Babiuk
2,
George
Mutwiri
1,3,
Volker
Gerdts
1,4
and
Sylvia
van
Drunen
Littel-‐van
den
Hurk
1,5,*
Vaccines
2014,
2,
297-‐322;
doi:10.3390/vaccines2020297
Pre-‐training module 9 "Basic concepts in vaccinology" for the Vaccinology course -‐ Institute Pasteur 2019.
Página 21 de 22
CBCC6 -‐ Actividad 1: La vacunación como acto comunitario
Material de apoyo
M. Rivera, A. Mónaco & M.Moreno -‐ Setiembre 2020
Veterinary vaccines and their importance to animal health and public health. James A. Roth. Procedia in
Vaccinology 5 (2011) 127 – 136. Doi: 10.1016/j.provac.2011.10.009
https://www.gub.uy/ministerio-‐salud-‐publica/comunicacion/publicaciones/vacunas
John
TJ
&
Samuel
R
(2000).
Herd
immunity
and
herd
effect:
new
insights
and
definitions.
Eur
J
Epidem
16(7):601-‐6.
doi:
10.1023/a:1007626510002.
Página 22 de 22
También podría gustarte
- Vacunas: ¿La inmunidad colectiva justifica el daño permanente de unos pocos?De EverandVacunas: ¿La inmunidad colectiva justifica el daño permanente de unos pocos?Aún no hay calificaciones
- Análisis de la desigualdad en la vacunación contra la COVID-19: comparación México y ColombiaDe EverandAnálisis de la desigualdad en la vacunación contra la COVID-19: comparación México y ColombiaAún no hay calificaciones
- Investigación IIDocumento4 páginasInvestigación IIAlex GarciaAún no hay calificaciones
- Mpenabad,+01 MS22 17+ PORRAS VACUNACIONDocumento3 páginasMpenabad,+01 MS22 17+ PORRAS VACUNACIONCarlos DelgadoAún no hay calificaciones
- La Importancia de La Vacunación en La Prevención de EnfermedadesDocumento4 páginasLa Importancia de La Vacunación en La Prevención de Enfermedadesjeampiveme004Aún no hay calificaciones
- Las vacunas, una herramienta esencial para la salud públicaDocumento8 páginasLas vacunas, una herramienta esencial para la salud públicaJuan SimaoAún no hay calificaciones
- Plan Anual de InmunizacionesDocumento13 páginasPlan Anual de InmunizacionesHGannicusTowers100% (4)
- Sesion Educativa de VacunasDocumento10 páginasSesion Educativa de Vacunashans86% (14)
- VacunasDocumento7 páginasVacunascardosomariaemiliaAún no hay calificaciones
- Vacunas SADIDocumento7 páginasVacunas SADISMIBA MedicinaAún no hay calificaciones
- Inmunidad, VacunaciónDocumento10 páginasInmunidad, VacunaciónisaboAún no hay calificaciones
- Importancia vacunas prevenciónDocumento2 páginasImportancia vacunas prevenciónMery Mariza Amacifuen MacedoAún no hay calificaciones
- Importancia de Las VacunasDocumento2 páginasImportancia de Las Vacunasjuan jose sanchez sanchezAún no hay calificaciones
- Las Vacunas: Breve Historia, Efectos Secundarios e ImportanciaDocumento11 páginasLas Vacunas: Breve Historia, Efectos Secundarios e ImportanciaDaniela RondonAún no hay calificaciones
- Texto Científico Lissany Ortiz SánchezDocumento3 páginasTexto Científico Lissany Ortiz SánchezGuisella Nathalie Sanchez ZambranoAún no hay calificaciones
- INMUNIZACIONDocumento14 páginasINMUNIZACIONluznervis.rondon1998Aún no hay calificaciones
- Taller Plan Ampliado de InmunizacionesDocumento10 páginasTaller Plan Ampliado de InmunizacionesClaudia Liliana URON SUMALAVEAún no hay calificaciones
- Inmunidad y vacunación en el PerúDocumento31 páginasInmunidad y vacunación en el PerúAlexandra Caman de la CruzAún no hay calificaciones
- VACUNASDocumento5 páginasVACUNASDomenica CristinaAún no hay calificaciones
- Plan de Charla VacunasDocumento13 páginasPlan de Charla VacunasAna LauAún no hay calificaciones
- Plantilla de PA3 GDADocumento4 páginasPlantilla de PA3 GDApaulAún no hay calificaciones
- Plan de Sesion Educativa de VacunasDocumento21 páginasPlan de Sesion Educativa de VacunasKelicitha Vilca0% (2)
- Preguntas Frecuentes de Vacunas PRONAP 2016 (2) 4 - 1Documento41 páginasPreguntas Frecuentes de Vacunas PRONAP 2016 (2) 4 - 1Barbara TwitterAún no hay calificaciones
- Aspectos Generales de Las Inmunizaciones VDAD 2018 PDFDocumento64 páginasAspectos Generales de Las Inmunizaciones VDAD 2018 PDFYuruanys ChirinoAún no hay calificaciones
- 19 Rechazo DesafioDocumento9 páginas19 Rechazo DesafioBerenice CortinaAún no hay calificaciones
- "Lado B de La Salvación ": Xxix Feria de Ciencias Tecnología Del I.A.FDocumento26 páginas"Lado B de La Salvación ": Xxix Feria de Ciencias Tecnología Del I.A.Fsablek gamerAún no hay calificaciones
- Argumentos - ConclusionDocumento2 páginasArgumentos - ConclusionMILENE FERNANDA CALUA VASQUEZAún no hay calificaciones
- Ensayo AntivacunasDocumento22 páginasEnsayo AntivacunasYasmin Sheyla Zelada LabanAún no hay calificaciones
- VACUNASDocumento5 páginasVACUNASDomenica CristinaAún no hay calificaciones
- El Papel de La CienciaDocumento2 páginasEl Papel de La CienciaMilagros LópezAún no hay calificaciones
- MOVimiento ANTIVACUNASDocumento34 páginasMOVimiento ANTIVACUNASAngie HernandezAún no hay calificaciones
- Los antivacunas: Un movimiento con historiaDocumento11 páginasLos antivacunas: Un movimiento con historiaYasmin Sheyla Zelada LabanAún no hay calificaciones
- Pregunta 1,2Documento2 páginasPregunta 1,2César Luis QuiñonezAún no hay calificaciones
- ¿Qué Es El Programa Ampliado de Inmunización?: Características de Las Vacunas Del PaiDocumento12 páginas¿Qué Es El Programa Ampliado de Inmunización?: Características de Las Vacunas Del PaiNatasha RomeroAún no hay calificaciones
- Estrategia Sanitaria Nacional de Inmunizaciones Sesin 16Documento16 páginasEstrategia Sanitaria Nacional de Inmunizaciones Sesin 16Gianella jahaira Llachua casablancaAún no hay calificaciones
- Investigación Sobre Las Vacunas. Segunda ParteDocumento7 páginasInvestigación Sobre Las Vacunas. Segunda ParteCamila ContreraAún no hay calificaciones
- Toma de Decisiones en Situaciones de IncertidumbreDocumento2 páginasToma de Decisiones en Situaciones de IncertidumbreLAYESCA SOLANGE SANCHEZ MUGERSAAún no hay calificaciones
- Importancia de Las VacunasDocumento1 páginaImportancia de Las VacunasdinaAún no hay calificaciones
- Historia de La VacunacionDocumento7 páginasHistoria de La VacunacionJonathan Mares MorinAún no hay calificaciones
- Evaluacion Coef 2 de Junio III MedioDocumento11 páginasEvaluacion Coef 2 de Junio III Medio0 0Aún no hay calificaciones
- Teorías A Favor de Las VacunasDocumento4 páginasTeorías A Favor de Las VacunasJherson ZumaetaAún no hay calificaciones
- Qué Es Una VacunaDocumento2 páginasQué Es Una VacunaRemi SolisAún no hay calificaciones
- Proyecto Modular Técnicas de La Investigacion SocialDocumento7 páginasProyecto Modular Técnicas de La Investigacion SocialAlejandra G MartinezAún no hay calificaciones
- Las VacunasDocumento17 páginasLas Vacunasyanelys RosadoAún no hay calificaciones
- Plan de Inmunizaciones 2024 c.s. ConchucosDocumento14 páginasPlan de Inmunizaciones 2024 c.s. ConchucosKatherine Acuña UlloaAún no hay calificaciones
- Las pandemias ocurren cuando surge un nuevo virus (1)Documento1 páginaLas pandemias ocurren cuando surge un nuevo virus (1)Maria Gracia MartinezAún no hay calificaciones
- VacunasDocumento7 páginasVacunasMaria paulina Villa contrerasAún no hay calificaciones
- Informe PediatriaDocumento25 páginasInforme PediatriaWatson Inga ZuñeAún no hay calificaciones
- Seminario Inmunizaciones Listo.Documento32 páginasSeminario Inmunizaciones Listo.diego izquierdoAún no hay calificaciones
- Ensayo Lenguaje FinalDocumento5 páginasEnsayo Lenguaje Finalmathpai141Aún no hay calificaciones
- 5598-Texto Del Artículo-21677-1-10-20210125Documento12 páginas5598-Texto Del Artículo-21677-1-10-20210125Aby AbAún no hay calificaciones
- Informe 01 - Inmunología Sem - Grupo 19Documento8 páginasInforme 01 - Inmunología Sem - Grupo 19Jenny TarrilloAún no hay calificaciones
- Las Vacunas, Peligros y Beneficios - Wellintong Rosario PDFDocumento6 páginasLas Vacunas, Peligros y Beneficios - Wellintong Rosario PDFWellintong RosarioAún no hay calificaciones
- eglobal,+69R2Documento11 páginaseglobal,+69R2pamela castilloAún no hay calificaciones
- Las VacunasDocumento22 páginasLas VacunasDayron Stiven Penagos CardonaAún no hay calificaciones
- Presentación Propuesta Proyecto Juvenil Creativa Colorida Morado y Turques_20240329_190539_0000Documento21 páginasPresentación Propuesta Proyecto Juvenil Creativa Colorida Morado y Turques_20240329_190539_0000AlejandraAún no hay calificaciones
- Documento VacunasDocumento2 páginasDocumento VacunasXavi Paúl Mendoza FosterAún no hay calificaciones
- PLAN ANUAL Inmunizaciones ZarandaDocumento12 páginasPLAN ANUAL Inmunizaciones Zarandawillychirinos97% (33)
- La vacuna contra el covid-19: Esperanza para combatir la pandemiaDocumento13 páginasLa vacuna contra el covid-19: Esperanza para combatir la pandemiaAlianna GonzálezAún no hay calificaciones
- Taller # 4 Plan Ampliado de Inmunización y VacunaciónDocumento6 páginasTaller # 4 Plan Ampliado de Inmunización y Vacunaciónlaura sofiaAún no hay calificaciones
- Manual Conductas de BioseguridadDocumento29 páginasManual Conductas de BioseguridadDavid HuaweiAún no hay calificaciones
- 3 virus pielDocumento4 páginas3 virus pielYeisy Ruiz SierraAún no hay calificaciones
- Práctica #6 ''Métodos de Inoculación de Bacterias en Tubos''Documento5 páginasPráctica #6 ''Métodos de Inoculación de Bacterias en Tubos''Fátima GómezAún no hay calificaciones
- Virus - Control BiológicoDocumento21 páginasVirus - Control BiológicoricardoAún no hay calificaciones
- 3.especies Venenosas y Vectores. Juan SerranoDocumento9 páginas3.especies Venenosas y Vectores. Juan SerranoAna G Marcano SandovalAún no hay calificaciones
- Lyphochek Assayed Chemistry Control Levels 1 and 2Documento13 páginasLyphochek Assayed Chemistry Control Levels 1 and 2Mariam Manga100% (2)
- Genics WSSV Educatonal Resource Guide SpanishDocumento3 páginasGenics WSSV Educatonal Resource Guide SpanishAbraham Flores RendónAún no hay calificaciones
- Herpes 1Documento2 páginasHerpes 1Rafael Eduardo Gonzalez IbarraAún no hay calificaciones
- DENGUE. Diapositivas Kati.Documento10 páginasDENGUE. Diapositivas Kati.Luis Alfonso MorenoAún no hay calificaciones
- Agentes Etiológicos de GastroenteritisDocumento13 páginasAgentes Etiológicos de GastroenteritisCamila Filipeli ChiarelliAún no hay calificaciones
- Enfermedades Virales Del CerdoDocumento4 páginasEnfermedades Virales Del CerdoDianaAún no hay calificaciones
- MeningoencefalitisDocumento10 páginasMeningoencefalitisandry yulieth Andrade MedinaAún no hay calificaciones
- CLASE 4 Enfermedades Respiratorias IDocumento46 páginasCLASE 4 Enfermedades Respiratorias Ihugo f.cAún no hay calificaciones
- Resultados de Laboratorio Clinico Sede: Chia No ORDEN: 2021051810693 No INGRESO: 5073748Documento1 páginaResultados de Laboratorio Clinico Sede: Chia No ORDEN: 2021051810693 No INGRESO: 5073748chirryAún no hay calificaciones
- Dengue ResumenDocumento13 páginasDengue ResumenJuliana VesgaAún no hay calificaciones
- INVESTIGACIONDocumento10 páginasINVESTIGACIONGYCELA MARTINEZAún no hay calificaciones
- Plan de prevención COVID-19 para instituto de bellezaDocumento40 páginasPlan de prevención COVID-19 para instituto de bellezaAngel NHAún no hay calificaciones
- Capítulo 366 GeaDocumento4 páginasCapítulo 366 GeaWalter Manfredo Chavez MauricioAún no hay calificaciones
- FOR-SSO-175 Inspección SST Transporte de Personal Interno y ExternoDocumento1 páginaFOR-SSO-175 Inspección SST Transporte de Personal Interno y ExternoRonald PCAún no hay calificaciones
- Los virus: agentes infecciosos más pequeñosDocumento38 páginasLos virus: agentes infecciosos más pequeñoscarolAún no hay calificaciones
- Diagnóstico Diferencial en Medicina Interna PDFDocumento185 páginasDiagnóstico Diferencial en Medicina Interna PDFUniversitas Laverdadosharalibres50% (2)
- Un Viaje Hacia La VerdadDocumento2 páginasUn Viaje Hacia La VerdadAngela Correa100% (1)
- 1ro SEMANA 15Documento10 páginas1ro SEMANA 15Daniel Allende JoaquinAún no hay calificaciones
- Ucn - Biol.virus I 2023.Documento30 páginasUcn - Biol.virus I 2023.Alysson Hanoi Calero Castillo 8Aún no hay calificaciones
- Evaluacion de Microorganismos 7mosDocumento3 páginasEvaluacion de Microorganismos 7mosJULIA VASQUEZ SAEZAún no hay calificaciones
- ADN Recombinante II-1Documento3 páginasADN Recombinante II-1MARIO CRISPIN HERNANDEZ ALVAREZAún no hay calificaciones
- Natulardtresidential en EsDocumento1 páginaNatulardtresidential en EsFede RamirezAún no hay calificaciones
- Edafologia 13 Introducción A La BiorremediaciónDocumento2 páginasEdafologia 13 Introducción A La BiorremediaciónDanna SalameaAún no hay calificaciones
- Cells at Work!Documento2 páginasCells at Work!Morales Ordaz Maria FAún no hay calificaciones
- Mitos y Verdades COVID VacunacionDocumento24 páginasMitos y Verdades COVID VacunacionSMIBA MedicinaAún no hay calificaciones