Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Destilacion Diferencial
Cargado por
Leonardo Caro GonzalesTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Destilacion Diferencial
Cargado por
Leonardo Caro GonzalesCopyright:
Formatos disponibles
DESTILACIÓN SIMPLE O DIFERENCIAL
1. OBJETIVOS.
Aplicar los principios básicos de la destilación como proceso de separación.
Familiarizarse con las variables que impacten de la destilación simple.
Comparar los métodos para predecir las composiciones finales y cantidades de
destilado y residuo por los siguientes métodos.
a) K = Cte.
b) α = Cte.
c) K ≠ Cte. Y α = Cte.
Indicar como varía la composición del destilado respecto al residuo en función del
tiempo.
Determinar de forma analítica y experimental la composición máxima del
destilado.
Determinar la temperatura de las primeras gotas de destilado de forma
experimental y analítica.
Si el objetivo de la práctica fuese obtener un destilado con una fracción molar del
40% que volumen de destilado se deberá obtener.
2. MARCO TEORICO.
2.1. Destilación
La destilación es una técnica de separación de sustancias que permite separar los distintos
componentes de una mezcla. Esta técnica se basa fundamentalmente en los puntos de
ebullición de cada uno de los componentes de la mezcla. Cuanto mayor sea la diferencia
entre 2 los puntos de ebullición de las sustancias de la mezcla, más eficaz será la separación
de sus componentes; es decir, los componentes se obtendrán con un mayor grado de pureza.
(Andrade Benítez, 2008)
2.2. Destilación diferencial
LABORATORIO DE PROCESOS UNITARIOS
La destilación simple, abierta o diferencial es una operación intermitente en la que la
mezcla a destilar se carga en el balon, donde se suministra el calor necesario para llevarla a
su temperatura de burbuja. En ese instante comienza la ebullición, que se mantiene se va
eliminando continuamente el vapor generado. Este vapor se condensa en el exterior dando
lugar al producto destilado. Conforme transcurre el proceso se va modificando la
composición del líquido, ya que se eliminan preferentemente los componentes más
volátiles, con lo cual va aumentando consiguientemente la temperatura de burbuja de la
mezcla. Lógicamente, el vapor (siempre en equilibrio con el líquido en la caldera) también
cambiara continuamente su composición, empobreciéndose en el componente más volátil.
El calor debe suministrarse en la caldera de modo que en todo instante el vapor generado
este en equilibrio con el líquido en la caldera. (Andrade Benítez, 2008)
Destilación Diferencial(Henley, E. J; Seader, J.D., 2000, pp 397)
Características
Es una Operación discontinua (el material se carga en el equipo y el vapor generado
se retira en forma continua).
También llamada: Destilación simple por lotes, destilación por cargas.
Se realiza en una sola etapa, mediante calentamiento lento y no presenta reflujo.
Los vapores se extraen con la misma velocidad con que se forman (no hay
acumulación) y se condensan (destilado líquido).
Se admite que las composiciones del vapor generado (y) y del líquido remanente (x)
se hallan en estado de equilibrio.
Composición del líquido remanente varía con el tiempo.
PRACTICA 2 1 PRQ - 370
LABORATORIO DE PROCESOS UNITARIOS
2.3. Volatilidad relativa
La separación por destilación será tanto más sencilla cuanto más elevada (superior a 1)
fuese la volatilidad relativa de A en relación a B. Genéricamente la volatilidad Relativa αi,j
del componente i relativamente al j se define como la razón entre las razones de equilibrio
del componente i y del componente de referencia j. (González, 2012)
yi
xi ki
α ij = =
yj kj
xj
Ki e Kj son las razones de equilibrio para cada uno de los componentes. El componente de
referencia tiene que ser siempre un componente pesado (con punto de ebullición elevado).
(González, 2012)
2.4. Ecuaciones
Nomenclatura
D = Destilado, mol/h
Y = XD = composición del destilado, fracción molar
W = cantidad de líquido en la caldera de destilación
x = xw = composición del líquido del componente liviano
Balance de materia global
dW
−D=
dt
−Ddt=dW
Fuente: (Treybal, 1993, pp 407)
Balance por componente
d (W X W )
−D X D=
dt
PRACTICA 2 2 PRQ - 370
LABORATORIO DE PROCESOS UNITARIOS
Wd X W X W dW
−D X D= +
dt dt
−Ddt X D=Wd X W + X W dW
X D dW =Wd X W + X W dW
dW ( X D −X W )=Wd X W
WF X wf
dW d XW
∫ =∫
W X ( X D −X W )
WO wo
Xwf
wf d XW
ln =∫
w o X ( X D −X W )
wo
Fuente: (Treybal, 1993, pp 408)
3. MATERIALES Y EQUIPOS.
4. PROCEDIMIENTO DE LA PRÁCTICA.
5. REGISTRO DE DATOS.
5.1. DATOS EXPERIMENTALES.
PRACTICA 2 3 PRQ - 370
LABORATORIO DE PROCESOS UNITARIOS
6. CALCULOS Y GRAFICAS.
6.1. CALCULOS.
6.1.1. Cálculo de los volúmenes individuales de alcohol comercial y agua para
preparar la solución de 2000 ml con Xw0= 0.09
Para ello se realizara un sistema de ecuaciones: 3 ecuaciones con 3 incógnitas
Vol alcohol comercial∗%V /V ∗Densidad etanol∗1
N etanol =
PM etanol
N etanol
x etanol=
( N etanol + N agua )
N eta nol =0.09∗N totales
g
∗1
ml
0.09∗N totales =Vol alcohol comercial∗0,96∗0,789
g
46,069
mol
Vol alcohol comercial∗( 1−%V /V )∗ρagua∗1 Vol agua∗ρagua∗1
N agua = +
PM agua PM agua
N agua
x agual=
(N etanol + N agua )
N agua =0.91∗N totales
g g
∗1 ∗1
ml ml
0.91∗N T =Vol alc co∗ (1−0,96 )∗0,998 +Vol agua∗0,998
g g
18,015 18,015
mol mol
V total=V alcohol comercial +V agua
2000=V ealcohol comercial +V agua
V etanol =495 ml
PRACTICA 2 4 PRQ - 370
LABORATORIO DE PROCESOS UNITARIOS
V agua =1505 ml
6.1.2. Calculo de la carga inicial W0.
Calculo de la densidad de mezcla.
ρ Mezcla =ρ etanol∗x etanol + ρ agua∗x agua
g g
ρ Mezcla =0,789 ∗0,09+ 0,998 ∗0,91
ml ml
g
ρ Mezcla =0,979
ml
Calculo de la masa total inicial.
mmezcla =Vol ( solución )∗ρ Mezcla
g
m mezcla=2000 ml∗0,979
ml
m mezcla=1958 g
Calculo del peso molecular de mezcla.
PM Mezcla=PM etanol∗xetanol + PM agua∗x agua
g g
PM Mezcla =46,069 ∗0,09+18,015 ∗0,91
mol mol
g
PM Mezcla =20,540
mol
Calculo de la carga inicial.
m mezcla
W o=
PM Mezcla
1958 g
W o=
g
20,540
mol
W o =95,326 mol
6.1.3. Cálculo de la fracción molar de etanol y agua (Xetanol, Xagua) en las pruebas
realizadas.
Para todos los puntos el cálculo es el mismo
Ni
x i=
N total
PRACTICA 2 5 PRQ - 370
LABORATORIO DE PROCESOS UNITARIOS
N etanol N agua
x etanol= x agua =
( N etanol + N agua ) ( N etanol + N agua )
Para calcular las fracciones molares necesitamos el número de moles de etanol y de
agua
Destilado∗(%V /V )∗Densidad etanol∗1
N etanol =Vol .
PM etanol
( 100−%V /V )∗Densidad agua∗1
N agua =V
PM agua
Calculo de los moles del destilado:
g
∗1
ml
N etanol =315 ml∗0,612∗0.789
g
46,069
mol
N etanol =3.3016 mol
g
∗1
ml
N agua =315 ml(1−0.612)∗0,998
g
18 ,015
mol
N agua =6.7707 mol
Calculo de la fracción molar en el destilado :
3.3016
x etanol= =0,3278
( 3.3016+6.7707 )
6.7707
x agua = =0,6722
( 3.3016+ 6.7707 )
Calculo de los moles del residuo y fracción final en el balón:
g
∗1
ml
N etanol =1566 ml∗0,152∗0.789
g
46,069
mol
N etanol =4.0766 mol
g
∗1
ml
N agua =1566 ml (1−0.152)∗0,998
g
18 ,015
mol
PRACTICA 2 6 PRQ - 370
LABORATORIO DE PROCESOS UNITARIOS
N agua =73,5671 mol
Calculo de la fracción molar en el residuo (fracción final en el balón Xwf):
4.0766
x etanol= =0,0525
( 4.0766+73,5671 )
73,5671
x agua = =0,9475
( 4.0766+73,5671 )
6.2. CÁLCULO DE LA FRACCIÓN FINAL XWF Y LA CARGA FINAL WF
TEÓRICOS POR LOS TRES MÉTODOS.
Caso a) Cuando K = Cte. en todo el proceso.
Del informe 1 tomamos el promedio de la K de equilibrio:
Ketanol = 3,54178350
No K1
1 0,99982
2 1,03288
3 1,09357
4 1,28203
5 1,55878
6 1,93577
7 2,44339
8 3,13661
9 4,10663
10 5,52484
11 7,78277
12 11,6043
Kprom 3,541784
Xwf
Wf dXw
ln =∫
Wo Xwo KXw−Xw
PRACTICA 2 7 PRQ - 370
LABORATORIO DE PROCESOS UNITARIOS
Wf 1 Xwf
ln = ∗ln ( 1)
Wo K−1 Xwo
Wf∗Xwf −Wo∗Xwo
X D , prom= (2)
Wf −Wo
Calculo de XD,PROM:
Fracción molar en el residuo (fracción final en el balón Xwf):
A partir del Volumen de Residuo:
X WF =X etanol=0,0525
X agua=0,9475
Calculo de la densidad de mezcla.
ρ Mezcla=ρetanol∗x etanol + ρagua∗x agua
g g
ρ Mezcla =0,789 ∗0,0525+ 0,998 ∗0,9475
ml ml
g
ρ Mezcla =0.9870
ml
Calculo de la masa total inicial.
m mezcla=Vol ( solución )∗ρ Mezcla
g
m mezcla=1566 ml∗0,9870
ml
mmezcla =1545.6850 g
Calculo del peso molecular de mezcla.
PM Mezcla =PM etanol∗xetanol + PM agua∗x agua
g g
PM Mezcla =46,069 ∗0,0525+18,015 ∗0,9475
mol mol
g
PM Mezcla =19.4878
mol
Calculo de la carga final.
mmezcla
W f=
PM Mezcla
1545.6850 g
W f=
g
19.4878
mol
PRACTICA 2 8 PRQ - 370
LABORATORIO DE PROCESOS UNITARIOS
W f =79.3154 mol
79.3154 mol∗0,0525−95.326 mol∗0.09
X D , prom=
79.3154 mol−95.326 mol
X D , prom=0.2757
Valor para el XDpromedio = 0.2757
Resolviendo las dos ecuaciones para hallar WF y XWF finales teóricas:
Wf 1 Xwf
ln = ∗ln ( 1)
Wo K−1 Xwo
Wf∗Xwf −Wo∗Xwo
X D , prom= (2)
Wf −Wo
wF 1 x W ,f
ln = ∗ln
95.326 3,54178350−1 0,09
W F∗X Wf −95.326∗0,09
0.2757=
W Final−95.326
W Final=84,5806
x W , final =0,0664
Caso b) Cuando α = Cte. en todo el proceso.
A partir de un promedio de las constantes de equilibrio del primer informe calculamos la
volatilidad relativa (α).
No K1 K2
1 0,99982 1,00217
2 1,03288 0,89530
3 1,09357 0,81742
4 1,28203 0,71196
5 1,55878 0,64709
6 1,93577 0,60810
7 2,44339 0,58897
8 3,13661 0,58955
9 4,10663 0,61267
10 5,52484 0,66788
11 7,78277 0,78307
PRACTICA 2 9 PRQ - 370
LABORATORIO DE PROCESOS UNITARIOS
12 11,6043 1,00031
Kprom 3,541784 0,69458
K etanol =3,54178 K agua =0,69458
Ki Ketanol
α= =
Kj Kagua
3,54178
α= =5,09917
0,69458
Wo 1 Xwo 1− Xwf
ln =
Wf α −1
∗ ln (
Xwf
+ α∗ln
1−Xwo
(1) )
Wf∗Xwf −Wo∗Xwo
X D , prom= (2)
Wf −Wo
Resolviendo las dos ecuaciones con dos incógnitas tenemos:
95.326 1 0,09 1−Xwf
ln
Wf
=
5,09917−1 (
∗ ln
Xwf
+5,09917∗ln
1−0,09 )
Wf ∗Xwf −95.326∗0,09
0.2757=
Wf −95.326
Wf =78,7810 mol
xwf =0,051
Caso c) cuando k ≠ ctte ; α ≠ ctte en todo el proceso
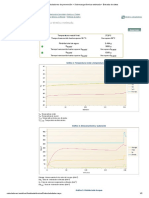
Utilizamos el diagrama de equilibrio X-Y de la primera práctica.
PRACTICA 2 10 PRQ - 370
LABORATORIO DE PROCESOS UNITARIOS
X-Y
1
0.9
0.8
0.7
0.6
Axis Title
0.5
0.4
0.3
0.2
0.1
0
0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1
Axis Title
Y1 X1
GRAFICA N° 1
Fuente: Elaboración Propia
GRAFICA N° 2
PRACTICA 2 11 PRQ - 370
LABORATORIO DE PROCESOS UNITARIOS
X-Y
0.6
0.55
0.5
0.45
0.4
0.35
0.3
0.25
0.2
0.15
0.1
0.05
0
0 0.01 0.02 0.03 0.04 0.05 0.06 0.07 0.08 0.09 0.1
Y1 X1
Fuente: Elaboración Propia
Ubicamos Xwo subimos hasta la curva de equilibrio y leemos yD=XDi
Generamos la siguiente tabla:
No XW XD 1/( XD- XW)
1 0,090 0,42 3,03
2 0,076 0,40 3,09
3 0,062 0,36 3,36
4 0,048 0,32 3,68
5 0,034 0,26 4,42
6 0,02 0,17 6,67
Fuente: Elaboración Propia
Xwf
wf dXw
ln =∫
wo Xwo xD− Xw
Realizamos la integración gráficamente para hallar el área bajo la curva:
PRACTICA 2 12 PRQ - 370
LABORATORIO DE PROCESOS UNITARIOS
Xwf
dXw
A= ∫
Xwo xD−Xw
A=−0,2716
wf
ln =−0,2716
wo
wf =95,326∗e−0,2716
wf =72,654 mol
Con la ecuación:
Wo∗Xwo−W∗Xw
X D , prom=
Wo−W
Calculamos W final
95.326∗0.09−72,654∗0.020
XDpromedio=
95.326−72,654
XDprom=¿ 0,314
De la gráfica leemos Xw
Xw =0.045
CALCULO DE LA COMPOSICISON MAXIMA DEL DESTILADO
A partir de la composición Xwo = 0.09 trazar una línea hasta la curva y leer el valor de
Xmax:
X-Y
1
0.9
0.8
0.7
0.6
0.5
0.4
0.3
0.2
0.1
0
0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1
GRAFICA N° 3
PRACTICA 2 13 PRQ - 370
LABORATORIO DE PROCESOS UNITARIOS
Fuente: Elaboración Propia
GRAFICA N° 4
X-Y
0.45
0.45
0.44
0.44
0.43
0.43
0.42
0.42
0.41
0.41
0.4
0.08 0.09 0.09 0.1 0.1
PRACTICA 2 14 PRQ - 370
LABORATORIO DE PROCESOS UNITARIOS
Fuente: Elaboración Propia
De la lectura de la gráfica, Xmax= 0.424
PRACTICA 2 15 PRQ - 370
También podría gustarte
- Control Automatico de ProcesosDocumento14 páginasControl Automatico de ProcesosLeonardo Caro GonzalesAún no hay calificaciones
- Fundamentos Del ComportamientoDocumento7 páginasFundamentos Del ComportamientoLeonardo Caro GonzalesAún no hay calificaciones
- Instalaciones de Gas Natural Doméstico y Comercial 2Documento32 páginasInstalaciones de Gas Natural Doméstico y Comercial 2Leonardo Caro GonzalesAún no hay calificaciones
- Espectrometría de Fluorescencia de RayosDocumento3 páginasEspectrometría de Fluorescencia de RayosLeonardo Caro GonzalesAún no hay calificaciones
- Instrumentos de Medicion de TemperaturaDocumento17 páginasInstrumentos de Medicion de TemperaturaLeonardo Caro GonzalesAún no hay calificaciones
- Mapa de ProcesosDocumento7 páginasMapa de ProcesosLeonardo Caro GonzalesAún no hay calificaciones
- Sefuridad IndustrialDocumento11 páginasSefuridad IndustrialLeonardo Caro GonzalesAún no hay calificaciones
- Construccion y Operacion de EE SSDocumento5 páginasConstruccion y Operacion de EE SSLeonardo Caro GonzalesAún no hay calificaciones
- Mapa de ProcesosDocumento7 páginasMapa de ProcesosLeonardo Caro GonzalesAún no hay calificaciones
- Laboratorio de Circuitos EléctricosDocumento23 páginasLaboratorio de Circuitos EléctricosAngel HCastAún no hay calificaciones
- Ejercicios 10,11,12Documento3 páginasEjercicios 10,11,12Santiago NievesAún no hay calificaciones
- Analisis de Reologica en AlimentosDocumento13 páginasAnalisis de Reologica en AlimentosSTIVEN ORTEGA QUINTEROAún no hay calificaciones
- Preinforme Movimiento ParabolicoDocumento4 páginasPreinforme Movimiento Parabolicocarolinarestrepov100% (1)
- Resumen Dilatación Lineal de Sólidos InformeDocumento3 páginasResumen Dilatación Lineal de Sólidos InformeHarwin Jose Moya VegaAún no hay calificaciones
- Repasoo 7Documento14 páginasRepasoo 7FerAún no hay calificaciones
- Activiad FisicaDocumento10 páginasActiviad FisicaJose JulioAún no hay calificaciones
- Sistema de Potencia EléctricaDocumento4 páginasSistema de Potencia EléctricaSantiago NMAún no hay calificaciones
- Chapter 2. Fluid MechanicsDocumento6 páginasChapter 2. Fluid MechanicsjmezapAún no hay calificaciones
- Calculadores de Prevención - Sobrecarga Térmica Estimada - Entrada de DatosDocumento2 páginasCalculadores de Prevención - Sobrecarga Térmica Estimada - Entrada de Datoscrismar2016Aún no hay calificaciones
- Laboratorio 3Documento10 páginasLaboratorio 3Felix Guitton TeranAún no hay calificaciones
- s03.s1 Estado LiquidoDocumento52 páginass03.s1 Estado LiquidofaftAún no hay calificaciones
- Fase 3 LSE. 2035534Documento12 páginasFase 3 LSE. 2035534roonaldo.corpus18Aún no hay calificaciones
- Ejercicios Sobre Motores de CCDocumento2 páginasEjercicios Sobre Motores de CCLuis BiglieriAún no hay calificaciones
- Tema 5Documento142 páginasTema 5Kisha LopezAún no hay calificaciones
- Temperatura ReporteDocumento5 páginasTemperatura ReporteOrdoñez Martínez Adriana ShanneiAún no hay calificaciones
- Instrumentos de Medición Eléctrica Semana 10Documento15 páginasInstrumentos de Medición Eléctrica Semana 10aidaAún no hay calificaciones
- Termodinamica Semana 8Documento9 páginasTermodinamica Semana 8Fernando Berrios VargasAún no hay calificaciones
- ATV11 ManualDocumento15 páginasATV11 ManualFabián Méndez BasoAún no hay calificaciones
- 1.2-Conceptos GeneralesDocumento22 páginas1.2-Conceptos GeneralesangieAún no hay calificaciones
- SISTEMAS TrifasicosDocumento19 páginasSISTEMAS TrifasicosÁlvaro CastroAún no hay calificaciones
- Cálculo Eléctrico de Una Instalación - Pa2Documento17 páginasCálculo Eléctrico de Una Instalación - Pa2RAUL CJUNO HOLGUINOAún no hay calificaciones
- Presentación Cortocircuito - Colegio de Ingeniero78946516Documento64 páginasPresentación Cortocircuito - Colegio de Ingeniero78946516CristopherDiazAún no hay calificaciones
- Presentacion de Motor MonofasicoDocumento36 páginasPresentacion de Motor MonofasicoMOISES MELGARAún no hay calificaciones
- Ejercicios-Analisis DimensionalDocumento2 páginasEjercicios-Analisis DimensionalhanAún no hay calificaciones
- Reacciones Quimicas 2021 IngDocumento63 páginasReacciones Quimicas 2021 IngJuan Carlos AlcedoAún no hay calificaciones
- TallEVA S14 CBA 2021 2Documento6 páginasTallEVA S14 CBA 2021 2Jhoymer García Arteaga100% (1)
- Ejercicios Propuestos Magnetismo (Fuerza, Campo y Flujo) PDFDocumento2 páginasEjercicios Propuestos Magnetismo (Fuerza, Campo y Flujo) PDFarbonixAún no hay calificaciones
- Mecánica de Fluidos CompresibilidadDocumento30 páginasMecánica de Fluidos CompresibilidadJAVQ0% (2)
- Tranferencia de Calor Tarea 2Documento21 páginasTranferencia de Calor Tarea 2cesar Garcia100% (1)