Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Cuestionario 6
Cuestionario 6
Cargado por
Jesus Saravia Mendoza0 calificaciones0% encontró este documento útil (0 votos)
54 vistas1 páginaEste documento presenta varias preguntas sobre termoquímica y la aplicación de la primera ley de la termodinámica. La primera pregunta define la termoquímica y explica brevemente su historia y aplicaciones. La segunda pregunta pide aplicar la primera ley de la termodinámica para determinar la eficiencia de un refrigerador. La tercera pregunta contiene cinco problemas que involucran calcular trabajo y cambios en energía y entalpía para procesos que involucran gases ideales y reales expandiéndose o
Descripción original:
Título original
CUESTIONARIO 6
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoEste documento presenta varias preguntas sobre termoquímica y la aplicación de la primera ley de la termodinámica. La primera pregunta define la termoquímica y explica brevemente su historia y aplicaciones. La segunda pregunta pide aplicar la primera ley de la termodinámica para determinar la eficiencia de un refrigerador. La tercera pregunta contiene cinco problemas que involucran calcular trabajo y cambios en energía y entalpía para procesos que involucran gases ideales y reales expandiéndose o
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
54 vistas1 páginaCuestionario 6
Cuestionario 6
Cargado por
Jesus Saravia MendozaEste documento presenta varias preguntas sobre termoquímica y la aplicación de la primera ley de la termodinámica. La primera pregunta define la termoquímica y explica brevemente su historia y aplicaciones. La segunda pregunta pide aplicar la primera ley de la termodinámica para determinar la eficiencia de un refrigerador. La tercera pregunta contiene cinco problemas que involucran calcular trabajo y cambios en energía y entalpía para procesos que involucran gases ideales y reales expandiéndose o
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 1
CUESTIONARIO N° 6
1.- TERMOQUIMICA: DEFINICION, HISTORIA Y APLICACIÓN DE
TERMODINAMICA DEL PRIMER PRINCIPIO DE TERMODINAMICA E
INPORTANCIA y QUE LEYES LA SUSTENTAN.
2.- APLICANDO LA PRIMERA LEY DE TERMODINAMICA DETERMINE LA
EFICIENCIA y FUNCIONAMENTO DE LA REFRIGERADORA
3.- RESOLVER LOS SIGUIENTES PROBLEMAS y FUNDAMENTE SU RESPUESTA
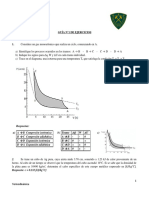
1.- Calcular el trabajo de expansión cuando se descompone
electrolíticamente 1 mol de agua a 25°C y 1 atm.
2.- Cuando dos de un gas ideal ocupando el volumen de un litro a 300°K, se
expanden isotérmicamente hasta 10,0 litros, calcular
a) El trabajo máximo (trabajo reversible) expresando en litro-atm; y
b) El trabajo mínimo (expansión contra presión cero)
3.- Calcular el trabajo hecho por el proceso de expansión adiabática de 8.00g
de oxígeno a 27°C y 10 atmosfera, cuando la presión final es 1 atmosfera
4.- Un mol de un gas monoatómico se guarda bajo una presión constante de
2atm. La temperatura se cambia de 100 a 25°C. Calcular los valores de W,
variación de energía y variación de entalpia.
5.- Un mol de un gas ideal monoatómico, inicialmente a 2 atm y 11,2 litros, se
pasa a la presión final de 3 atm, por un camino reversible definido por una
ecuación donde el parámetro: constante = PT. Calcular: a) T°K inicial; b) el
valor del parámetro de la ecuación; y c) La temperatura y volúmenes finales.
También podría gustarte
- Ingeniería química. Soluciones a los problemas del tomo IDe EverandIngeniería química. Soluciones a los problemas del tomo IAún no hay calificaciones
- Flujo de fluidos e intercambio de calorDe EverandFlujo de fluidos e intercambio de calorCalificación: 1 de 5 estrellas1/5 (1)
- Formalismo y métodos de la termodinámica. Volumen 1De EverandFormalismo y métodos de la termodinámica. Volumen 1Aún no hay calificaciones
- S16.s1 - Repaso para Examen FinalDocumento2 páginasS16.s1 - Repaso para Examen FinalJosue AltamiranoAún no hay calificaciones
- Primera Ley Termodinamica InfDocumento3 páginasPrimera Ley Termodinamica InfJuan Pablo Hilara MachacaAún no hay calificaciones
- S12.s3 - Problemas Sobre Gases. CV, CPDocumento15 páginasS12.s3 - Problemas Sobre Gases. CV, CPLuis Chocce PeñaAún no hay calificaciones
- Práctica Lab. Fisicoquímica Primer ParcialDocumento2 páginasPráctica Lab. Fisicoquímica Primer Parcialgrecia martinez ortiz100% (1)
- Problemas Video Clase 4Documento12 páginasProblemas Video Clase 4Andres GarciaAún no hay calificaciones
- 1 Bateria de Problemas de Gases Ideales y RealesDocumento6 páginas1 Bateria de Problemas de Gases Ideales y RealesKatherin SalasAún no hay calificaciones
- Practica 01 - FQ - 2018 PDFDocumento3 páginasPractica 01 - FQ - 2018 PDFjosue yanaAún no hay calificaciones
- Practica 02 FQ 2018Documento3 páginasPractica 02 FQ 2018juancalp81100% (1)
- TermodinamicaDocumento40 páginasTermodinamicaR Edith SJAún no hay calificaciones
- Problemas de Termodinamica 2010-1Documento8 páginasProblemas de Termodinamica 2010-1Sol Sanchez ArcosAún no hay calificaciones
- Taller 3 - TermodinámicaDocumento4 páginasTaller 3 - TermodinámicavanegasmarinAún no hay calificaciones
- Teoría CinéticaDocumento2 páginasTeoría Cinéticacerepl0% (1)
- Practica 01 FQ 2019Documento3 páginasPractica 01 FQ 2019AlexRodolfoMaytaVargasAún no hay calificaciones
- Ejercicios Propuestos Gases y Teoría Cinética 2021-IDocumento6 páginasEjercicios Propuestos Gases y Teoría Cinética 2021-IAyrton Lee Alfredo Aza�ero PerezAún no hay calificaciones
- Ejercicios Gases 2020-IDocumento6 páginasEjercicios Gases 2020-IOleggValVilAún no hay calificaciones
- Serie de Jercicios Primera LeyDocumento3 páginasSerie de Jercicios Primera LeyLuisCharrisAún no hay calificaciones
- Guia de Gases, W y QDocumento3 páginasGuia de Gases, W y QRosa MariaAún no hay calificaciones
- Problemas GasesDocumento7 páginasProblemas GasesMikhaelrams RamsAún no hay calificaciones
- Taller Primer CorteDocumento2 páginasTaller Primer Corteyeissy perezsAún no hay calificaciones
- Ejercicios Gases Ideales y Reales 2015Documento5 páginasEjercicios Gases Ideales y Reales 2015Wilo JaraAún no hay calificaciones
- TERMO Ejercicios (1) 2020 - II PDFDocumento8 páginasTERMO Ejercicios (1) 2020 - II PDFIrene Sánchez Arroyave0% (1)
- 2da Ley ENTROPIADocumento3 páginas2da Ley ENTROPIAStefany Elizabeth Crisostomo QuispeAún no hay calificaciones
- FseyndrxuDocumento4 páginasFseyndrxuMiguel SaavedraAún no hay calificaciones
- FQ1-2015.1 Tarea 01Documento2 páginasFQ1-2015.1 Tarea 01Jonathan DiazAún no hay calificaciones
- Práctica Lab. Fisicoquímica Primer ParcialDocumento2 páginasPráctica Lab. Fisicoquímica Primer ParcialALEJANDRA MELGAREJO PARDOAún no hay calificaciones
- Guia Numero 4Documento7 páginasGuia Numero 4eutectic19920% (1)
- Practica qmc-100 PDFDocumento9 páginasPractica qmc-100 PDFLouis FernandezAún no hay calificaciones
- Guia 1 Primera Ley GasesDocumento7 páginasGuia 1 Primera Ley GasesGeraldineAún no hay calificaciones
- Taller 1 Fisicoquimica Gases Ideales PDFDocumento2 páginasTaller 1 Fisicoquimica Gases Ideales PDFJuan CamiloAún no hay calificaciones
- Guia 1Documento2 páginasGuia 1Felipe Andrés Orellana0% (1)
- Estudio Dirigido QuímicaDocumento2 páginasEstudio Dirigido QuímicaDAPHNE NICOLLE SALAZAR GALÁNAún no hay calificaciones
- Práctica Lab. Fisicoquímica Primer Parcial 2023Documento2 páginasPráctica Lab. Fisicoquímica Primer Parcial 2023Juan Esteban Cordova AliAún no hay calificaciones
- Serie de Ejercicios Segunda LeyDocumento3 páginasSerie de Ejercicios Segunda LeyLuisCharrisAún no hay calificaciones
- Guia Fisicoquimica Segundo Parcial SumoDocumento17 páginasGuia Fisicoquimica Segundo Parcial SumoJanethe Cruz100% (1)
- Actividad N°1 - Procesos TermodinamicosDocumento4 páginasActividad N°1 - Procesos TermodinamicosJuan YañezAún no hay calificaciones
- Actividad N°1 - Procesos TermodinamicosDocumento4 páginasActividad N°1 - Procesos TermodinamicosJuan YañezAún no hay calificaciones
- Ejercicios Tema 3. Química GeneralDocumento3 páginasEjercicios Tema 3. Química GeneralPablo Molero MartínAún no hay calificaciones
- Trabajo Práctico #3 Gases Ideales y Reales Año 2020Documento6 páginasTrabajo Práctico #3 Gases Ideales y Reales Año 2020Luciano DanieleAún no hay calificaciones
- Guía Fisicoquímica IDocumento3 páginasGuía Fisicoquímica ITania GachusAún no hay calificaciones
- Gases Problemario de FisicoquimicaDocumento8 páginasGases Problemario de FisicoquimicaKriistian Rene QuintanaAún no hay calificaciones
- Examen Final de TermofluidosDocumento4 páginasExamen Final de TermofluidoscrackzarAún no hay calificaciones
- Guia 1 Termodinamica 2021Documento3 páginasGuia 1 Termodinamica 2021Victoria Paz Landeros ContrerasAún no hay calificaciones
- Actividad 01 - S8 - Ejercicios PropuestosDocumento3 páginasActividad 01 - S8 - Ejercicios PropuestosMARIA EMILIA ROCA ROJASAún no hay calificaciones
- Balotario 11+física 2 Primera Ley de La Termodinámica-Docente Ing. Henry Lama CornejoDocumento2 páginasBalotario 11+física 2 Primera Ley de La Termodinámica-Docente Ing. Henry Lama CornejoAlexHuamaniAún no hay calificaciones
- Trabajo de Fisico QuimicaDocumento87 páginasTrabajo de Fisico QuimicaRobertoLema125% (4)
- Problemas Tema 3 GrupalDocumento4 páginasProblemas Tema 3 GrupalnereaalbarranarocaAún no hay calificaciones
- Gases. Quimica de Procesos IDocumento5 páginasGases. Quimica de Procesos ICatherine AlmendralesAún no hay calificaciones
- Gua N1 Termodinmica 2015Documento9 páginasGua N1 Termodinmica 2015Elías Raphael Rubilar BugueñoAún no hay calificaciones
- Ejercicios de TermoDocumento2 páginasEjercicios de TermoCarlos AntonioAún no hay calificaciones
- Experiencias sobre la propiedad temperaturaDe EverandExperiencias sobre la propiedad temperaturaAún no hay calificaciones
- Psicología Industrial y Organizacional, Sesión 6Documento2 páginasPsicología Industrial y Organizacional, Sesión 6Jesus Saravia MendozaAún no hay calificaciones
- Psicología Industrial y Organizacional, Sesión 5Documento1 páginaPsicología Industrial y Organizacional, Sesión 5Jesus Saravia MendozaAún no hay calificaciones
- Rotulo y Medidas PDFDocumento1 páginaRotulo y Medidas PDFJesus Saravia MendozaAún no hay calificaciones
- DIBUJO Y GEOMETRÍA DESCRIPTIVA Sesión 01 - 02Documento46 páginasDIBUJO Y GEOMETRÍA DESCRIPTIVA Sesión 01 - 02Jesus Saravia MendozaAún no hay calificaciones
- Evolución de Las Tic's-WordDocumento27 páginasEvolución de Las Tic's-WordJesus Saravia MendozaAún no hay calificaciones
- Evolución de Las Tic'sDocumento13 páginasEvolución de Las Tic'sJesus Saravia MendozaAún no hay calificaciones
- Aplicacion de Las Tics en El Sector Salud-WordDocumento23 páginasAplicacion de Las Tics en El Sector Salud-WordJesus Saravia MendozaAún no hay calificaciones
- TRABAJOODocumento15 páginasTRABAJOOJesus Saravia MendozaAún no hay calificaciones