Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Explicacion Ecuaciones Hidroxidos PDF
Explicacion Ecuaciones Hidroxidos PDF
Cargado por
Yuleydy liceth Galvis arevaloTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Explicacion Ecuaciones Hidroxidos PDF
Explicacion Ecuaciones Hidroxidos PDF
Cargado por
Yuleydy liceth Galvis arevaloCopyright:
Formatos disponibles
http://rubenprofe.com.
ar
quimica@rubenprofe.com.ar
HIDRÓXIDOS
Los hidróxidos son sustancias que se forman a partir de la reacción química entre un óxido
básico y el agua.
Recordemos que el óxido básico (o simplemente óxido) está constituido por un metal
combinado con el oxígeno.
Es muy fácil escribir la fórmula de un hidróxido porque su molécula solo tiene un átomo del
metal y el radical (OH).
El radical oxhidrilo actua como un elemento que tiene una sola valencia.
Según lo dicho para escribir la fórmula de un hidroxido se procede de la siguiente forma:
1. Se escribe el metal.
2. Se escribe el radical (OH)
3. Se escribe como subíndice del radical un número igual a la valencia del
metal.
nota: el metal no lleva subíndice porque la valencia del radical (OH) es uno.
En la siguiente tabla se indican ejemplos paso a paso:
Nombre 1º paso 2º paso 3º paso
hidróxido de potasio K K(OH) K(OH)
hidróxido de Calcio Ca Ca(OH) Ca(OH)2
hidróxido de aluminio Al Al(OH) Al(OH)3
hidróxido plúmbico Pb Pb(OH) Pb(OH)4
Ejercicios:
1.- Escribir las fórmulas de los siguientes hidróxidos:
a) hidróxido de sodio b) hidróxido de litio c) hidróxido niqueloso d) hidróxido férrico
e) hidróxido de aluminio f) hidróxido auroso g) hidróxido cuproso h) hidróxido mercúrico
i) hidróxido de platino j) hidróxido plúmbico k) hidróxido de zinc l) hidróxido de indio
2.- Indicar con cuántas valencias actúa el metal en cada uno de los siguientes
hidróxidos:
a) Au(OH)3 b) Be(OH)2 c) Bi(OH)3 d) Cd(OH)2
e) Bi(OH)2 f) Ce(OH)3 g) Cs(OH) h) Ce(OH)4
3.- Escribir el nombre cada uno de los siguientes hidróxidos:
a) Ba(OH)2 b) Pb(OH)2 c) Fe(OH)2 d) Cu(OH)2
e) Au(OH)3 f) Hg(OH) 2 g) Ni(OH) 3 h) Ag (OH)
i) Zn(OH)2 j) In(OH)3 k) Fe(OH) 3 l) Lu(OH) 3
4.- Algunos de los hidróxidos de la siguiente tabla están mal escritos, táchelos.
a) Ca(OH) b) Pb(OH)2 c) Li(OH)2 d) Cu(OH)3
e) Au(OH)3 f) Hg(OH) 2 g) Ni(OH) 3 h) Ag (OH) 2
i) Zn(OH) j) In(OH)4 k) Fe(OH) 3 l) Cu(OH)
hidróxidos, ecuaciones de formación y balanceo
1
http://rubenprofe.com.ar
quimica@rubenprofe.com.ar
Ecuaciones de formación de hidróxidos
Como se dijo oportunamente, los hidróxidos se originan por la reacción química
entre un óxido básico o metálico con el agua.
A continuación plantearemos la forma de escribir las ecuaciones de formación y
equilibrarlas.
Para comenzar plantearemos el caso de un metal monovalente (1 valencia)
como el potasio:
hidróxido de potasio
óxido de potasio
K2O + H2O ⇒ 2 K (OH)
Vemos que la ecuación está equilibrada porque la cantidad de elementos a
derecha e izquierda de la fórmula son iguales
BALANCE
elemento izquierda derecha
2 átomos en la molécula de 2 átomos, uno en cada
potasio
óxido molécula de hidróxido
2 átomos, uno en la molécula 2 átomos, uno en cada
oxígeno de óxido y otro en la molécula molécula de hidróxido
de agua
2 átomos en la molécula de 2 átomos, uno en cada
hidrógeno
agua molécula de hidróxido
Vemos que el balance de átomos nos indica que la ecuación está equilibrada.
Segundo ejemplo, molécula bivalente (dos valencias) Ca
óxido de calcio hidróxido de calcio
OCa + H2O ⇒ Ca (OH) 2
Vemos que la ecuación está equilibrada porque la cantidad de elementos a
derecha e izquierda de la fórmula son iguales
BALANCE
elemento izquierda derecha
calcio 1 átomo en la molécula de 1 átomo, en la molécula de
óxido hidróxido
oxígeno 2 átomos, uno en la molécula 2 átomos, en la molécula de
de óxido y otro en la molécula hidróxido
de agua
hidrógeno 2 átomos en la molécula de 2 átomos, en la molécula de
agua hidróxido
Vemos que el balance de átomos nos indica que la ecuación está equilibrada.
TERCER EJEMPLO, elemento trivalente (tres valencias)
hidróxidos, ecuaciones de formación y balanceo
2
http://rubenprofe.com.ar
quimica@rubenprofe.com.ar
Usaremos en este caso el aluminio.
óxido de aluminio hidróxido de aluminio
O3Al2 + 3 H2O ⇒ 2 Al(OH) 3
BALANCE
elemento izquierda derecha
2 átomos en la molécula de 2 átomos, uno en cada una
aluminio óxido de las dos moléculas de
hidróxido
6 átomos, tres en la molécula 6 átomos, tres en cada una
de óxido y tres, uno en cada de las dos moléculas de
oxígeno
una de las tres moléculas de hidróxido
agua
6 átomos, dos en cada una 6 átomos, tres en cada una
hidrógeno de las tres moléculas de agua de las dos moléculas de
hidróxido
MÉTODO ALGEBRAICO PARA EL BALANCE DE ECUACIONES
El método de inspección que se usó en el desarrollo anterior suele ser un poco
difícil de elaborar, por ello existe un método algebraico que se suele usar para casos
complicados. En nuestro caso recomendamos usar este método solo en el caso en que
el alumno no pueda aplicar el anterior. El estudiante deberá escribir y balancear
ecuaciones de formación de óxidos, ácidos, hidróxidos y sales usando el método que le
resulte mas simple.
Usamos las mismas ecuaciones desarrolladas como ejemplos mas arriba.
Paso 1.- Se escribe la ecuación colocando como coeficiente una letra que será
una incógnita.
a K2O + b H2O ⇒ c K (OH)
Paso 2.- Se realiza el balance provisional usando letras indeterminadas
(incógnitas) que serán a, b y c.
BALANCE
elemento izquierda derecha
2 a átomos, uno en cada una c átomos, uno en cada una
potasio de las a moléculas de óxido de las c moléculas de
hidróxido
a átomos, uno en cada una c átomos, uno en cada
de las moléculas de óxido y b molécula de hidróxido
oxígeno
átomos en la molécula de
agua
2b átomos, dos en cada una c átomos, uno en cada
hidrógeno
de las b moléculas de agua molécula de hidróxido
hidróxidos, ecuaciones de formación y balanceo
3
http://rubenprofe.com.ar
quimica@rubenprofe.com.ar
Paso 3.- Se plantean las ecuaciones.
2a = c
a+b = c
2b = c
Paso 4.- Se resuelven las ecuaciones por el método de asignación.
Ahora le asignamos un valor cualquiera a una de las letras y luego resolvemos
el sistema, por ejemplo si hacemos a = 1 tendremos:
por ser a=1, 2 a se convierte en 2x1 = c luego a=1 y c = 2
1+b = 2 luego b = 1
Se verifica el
2x1 = 2 luego
sistema
1 K2O + 1H2O ⇒ 2 K (OH)
Paso 5.- Se escribe la solución.
Finalmente
K2O + H2O ⇒ 2 K (OH)
El segundo ejemplo no se desarrolla por el método algebraico porque su
balanceo es inmediato.
Tercer ejemplo:
Paso 1.- Se escribe la ecuación colocando como coeficiente una letra que será
una incógnita.
a O3Al2 + b H2O ⇒ c Al(OH) 3
Paso 2.- Se realiza el balance provisional usando letras indeterminadas
(incógnitas) que serán a, b y c.
BALANCE
elemento izquierda derecha
2 a átomos, uno en cada una c átomos, uno en cada una
aluminio de las a moléculas de óxido de las c moléculas de
hidróxido
3 a átomos, tres en cada una 3 c átomos, tres en cada una
de las a moléculas de óxido y de las c moléculas de
oxígeno
b átomos, uno en cada una hidróxido
de las b moléculas de agua
2 b átomos, dos en cada una 3 c átomos, tres en cada una
hidrógeno de las b moléculas de agua de las c moléculas de
hidróxido
Paso 3.- Se plantean las ecuaciones.
hidróxidos, ecuaciones de formación y balanceo
4
http://rubenprofe.com.ar
quimica@rubenprofe.com.ar
2a = c
3a+ = 3c
b
2b = 3c
Paso 4.- Se resuelven las ecuaciones por el método de asignación.
Ahora le asignamos un valor cualquiera a una de las letras y luego resolvemos
el sistema, por ejemplo si hacemos a = 1 tendremos:
por ser a = 1, a se convierte en = c luego a = 1 y c = 2
2x1
3x1+b = 6 luego b = 3
2b = 6 luego Verifica la solución
1 O3Al2 + 3 H2O ⇒2 Al(OH) 3
Paso 5.- Se escribe la solución.
Finalmente
O3Al2 + 3 H2O ⇒ 2 Al(OH) 3
Ejercicios:
5.- Resolver los ejercicios anteriores asignando valores a la letra b
verificando que se obtiene la misma solución. (los coeficientes finales deben ser
números enteros)
6.- Resolver los ejercicios anteriores asignando valores a la letra c
verificando que se obtiene la misma solución. (los coeficientes finales deben ser
números enteros)
7.- Escribir las ecuaciones de formación de los siguientes hidróxidos:
a) Ba(OH)2 b) Pb(OH)2 c) Fe(OH)2 d) Cu(OH)2
e) Au(OH)3 f) Hg(OH) 2 g) Ni(OH) 3 h) Ag (OH)
i) Zn(OH)2 j) In(OH)3 k) Fe(OH) 3 l) Lu(OH) 3
‘Rubén Víctor Innocentini-2010
hidróxidos, ecuaciones de formación y balanceo
5
También podría gustarte
- Examen QuimicaDocumento8 páginasExamen QuimicaClaudia Vasquez100% (13)
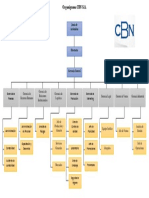
- Organigrama Cerveceria Nacional de BoliviaDocumento1 páginaOrganigrama Cerveceria Nacional de Boliviajose81% (43)
- Scrum KunagiDocumento36 páginasScrum Kunagijose100% (1)
- OxacidosDocumento5 páginasOxacidosAnonymous MSvUMLTApFAún no hay calificaciones
- Nomenclatura GuiaDocumento10 páginasNomenclatura GuiaMelany RiveraAún no hay calificaciones
- Valencia y OxidacionDocumento31 páginasValencia y OxidaciondafneAún no hay calificaciones
- Ácidos OxácidosDocumento1 páginaÁcidos OxácidosGuillermo MateoAún no hay calificaciones
- ANHIDRIDOSDocumento7 páginasANHIDRIDOSIlseAún no hay calificaciones
- Ácidos OxácidosDocumento24 páginasÁcidos Oxácidosgavic1995Aún no hay calificaciones
- Ecosistema PDFDocumento18 páginasEcosistema PDFHector RoldanAún no hay calificaciones
- Taller Nomenclatura 2019Documento8 páginasTaller Nomenclatura 2019Vanessa Velandia ÁvilaAún no hay calificaciones
- Nomenclatura Quimica Inorganica 2019Documento26 páginasNomenclatura Quimica Inorganica 2019Nubia Patricia Parada Rivera100% (1)
- Quimica NomenclaturaDocumento15 páginasQuimica NomenclaturaDomenica MendozaAún no hay calificaciones
- Taller Enlaces - Números de Oxidación 8º 2020 Semana 3 Julio PDFDocumento4 páginasTaller Enlaces - Números de Oxidación 8º 2020 Semana 3 Julio PDFJuan José MontesAún no hay calificaciones
- Taller de Función SalesDocumento1 páginaTaller de Función SalesJonesAún no hay calificaciones
- Ácidos HidrácidosDocumento11 páginasÁcidos HidrácidosLuis Carlos Andrade0% (1)
- Ejercicios de Nomenclatura 2009-2Documento3 páginasEjercicios de Nomenclatura 2009-2ShuletAR10Aún no hay calificaciones
- Guía de Nomenclatura STOCKDocumento8 páginasGuía de Nomenclatura STOCKMiguel Aliendres100% (1)
- Acidos OxacidoDocumento3 páginasAcidos OxacidoNataly Herrera bolivarAún no hay calificaciones
- Alcholes y FenolesDocumento21 páginasAlcholes y FenolesmarcoAún no hay calificaciones
- Hibridación de OrbitalesDocumento7 páginasHibridación de OrbitalesJesath Osvaldo Ramirez HernandezAún no hay calificaciones
- Nomenclatura QuimicaDocumento11 páginasNomenclatura QuimicaJpsè Marìa Pilamuga MirandaAún no hay calificaciones
- Nomenclatura StockDocumento11 páginasNomenclatura StockLESZLI KARINA ACOSTA MURTEAún no hay calificaciones
- RedoxDocumento10 páginasRedoxprofesor manuelAún no hay calificaciones
- 10 Química 06 II Fase 2021Documento6 páginas10 Química 06 II Fase 2021wilver condori chambiAún no hay calificaciones
- Ejercicios Basicos Sobre Celdas Galvanicas IDocumento2 páginasEjercicios Basicos Sobre Celdas Galvanicas IGalo YambayAún no hay calificaciones
- Alcanos para ClasesDocumento44 páginasAlcanos para ClasesvdiabloAún no hay calificaciones
- Nomenclatura Inorganica-Segunda ParteDocumento20 páginasNomenclatura Inorganica-Segunda ParteOdile VictoriaAún no hay calificaciones
- Compuestos QuímicosDocumento17 páginasCompuestos Químicosfernando rayoAún no hay calificaciones
- 12 - Función HidrurosDocumento3 páginas12 - Función HidrurosJoel Orellana LopezAún no hay calificaciones
- Balanceo de EcuacionesDocumento8 páginasBalanceo de EcuacionescalosraAún no hay calificaciones
- Masa MolarDocumento5 páginasMasa MolarÁngel MancillaAún no hay calificaciones
- Quimica InorganicaDocumento23 páginasQuimica Inorganicajoze2Aún no hay calificaciones
- Version 2013 Manual de NomenclaturaDocumento32 páginasVersion 2013 Manual de NomenclaturaJuan K MarroquinAún no hay calificaciones
- Números de Oxidación y Electrones de ValenciaDocumento15 páginasNúmeros de Oxidación y Electrones de ValenciaPilar Inga Solórzano100% (1)
- 03-F.o. Función ÁcidosDocumento23 páginas03-F.o. Función ÁcidosLenin Efio SosaAún no hay calificaciones
- Nomenclatura de Química Inorgánica PDFDocumento4 páginasNomenclatura de Química Inorgánica PDFJESSICA MARIANA LUGO FRAGOSOAún no hay calificaciones
- Reacciones Quimicas - Quimica 1° MedioDocumento15 páginasReacciones Quimicas - Quimica 1° MedioAndrea Fuentes GutierrezAún no hay calificaciones
- Compuestos Ternarios Grupo 2Documento18 páginasCompuestos Ternarios Grupo 2FranciscoPérezSAún no hay calificaciones
- Pre Presentacion 13 7v Nomenclatura 1 2023 1Documento27 páginasPre Presentacion 13 7v Nomenclatura 1 2023 1Nicolle Campos chamorroAún no hay calificaciones
- Nomenclatura Química InorgánicaDocumento14 páginasNomenclatura Química InorgánicaPatricia ChaileAún no hay calificaciones
- Tarea de Nomenclatura QuímicaDocumento3 páginasTarea de Nomenclatura QuímicaJeffry AriasAún no hay calificaciones
- Nomenclatura InorganicaDocumento6 páginasNomenclatura InorganicaJeremy Paul Zegarra CamposAún no hay calificaciones
- Nomenclatura - Binarios ModificadoDocumento18 páginasNomenclatura - Binarios ModificadoAmy Rodriguez ReyesAún no hay calificaciones
- Organismos Autótrofos y Heterótrofos 6º PDFDocumento15 páginasOrganismos Autótrofos y Heterótrofos 6º PDFPatriciaSanhuezaVillarrealAún no hay calificaciones
- Cuestionario de Tabla PeriodicaDocumento11 páginasCuestionario de Tabla PeriodicaWendy RodriguezAún no hay calificaciones
- EJE 7-NomenclaturaDocumento5 páginasEJE 7-NomenclaturaalamparonAún no hay calificaciones
- EVALUACION Funciones MDocumento10 páginasEVALUACION Funciones MMartín Leonardo Lacuta VaraAún no hay calificaciones
- Eteres Epoxidos y SulfurosDocumento31 páginasEteres Epoxidos y SulfurosCarlos Torres VelaAún no hay calificaciones
- Química Redox 3er. Curso Plan EspecíficoDocumento9 páginasQuímica Redox 3er. Curso Plan Específicoeliasfidelmartinezesquivel11Aún no hay calificaciones
- Que Son Las Reacciones QuímicasDocumento2 páginasQue Son Las Reacciones QuímicasMARY NOMESQUE0% (1)
- Ácidos OxacidosDocumento2 páginasÁcidos OxacidosJeniffer Robalino OrtizAún no hay calificaciones
- NomenclaturaDocumento24 páginasNomenclaturaaileengriselAún no hay calificaciones
- Que Pasa Cunado Chocan Los Atomos ActividadDocumento6 páginasQue Pasa Cunado Chocan Los Atomos ActividadHumberto CortezAún no hay calificaciones
- Sistemas de NomenclaturaDocumento5 páginasSistemas de Nomenclaturaluis miguel naranjo aguilarAún no hay calificaciones
- 0ac3e5f3875670ff2e15acb5fcef95b8 (1)Documento4 páginas0ac3e5f3875670ff2e15acb5fcef95b8 (1)Fredy CconzaAún no hay calificaciones
- Hidroxidos y OxoacidosDocumento2 páginasHidroxidos y OxoacidosALE MORETTI DJAún no hay calificaciones
- 3.5-Nomenclatura Sales InorgánicasDocumento6 páginas3.5-Nomenclatura Sales InorgánicasjlgzAún no hay calificaciones
- Quimica General 7 Sales Oxisales y HaloideasDocumento21 páginasQuimica General 7 Sales Oxisales y HaloideasRaul Milton Aquino BendezuAún no hay calificaciones
- Sustancias Simples y Compuestas PDFDocumento1 páginaSustancias Simples y Compuestas PDFGabrielaAún no hay calificaciones
- Ejercicios de Estados de OxidacionDocumento1 páginaEjercicios de Estados de Oxidacion5211241Aún no hay calificaciones
- Tema 8 Formulación Inorgánica. Teoría y Hojas de EjerciciosDocumento16 páginasTema 8 Formulación Inorgánica. Teoría y Hojas de EjerciciosCovadonga PerezAún no hay calificaciones
- ElectricaDocumento14 páginasElectricajoyceEvelynBenitezAún no hay calificaciones
- La EspinacaDocumento3 páginasLa Espinacajose100% (1)
- Circuitos Eléctricos en DC y Leyes de KirchoffDocumento5 páginasCircuitos Eléctricos en DC y Leyes de KirchoffjoseAún no hay calificaciones
- S05.s2 - Resolver Ejercicios - Grupo 02Documento3 páginasS05.s2 - Resolver Ejercicios - Grupo 02jossseantm10Aún no hay calificaciones
- Tema NomenclaturaDocumento31 páginasTema Nomenclaturaluchofernanflou90Aún no hay calificaciones
- Formulación InorgánicaDocumento39 páginasFormulación InorgánicaJesus Yamid Redondo RemolinaAún no hay calificaciones
- Triptico NomenglaturasDocumento2 páginasTriptico NomenglaturasEmma MirandaAún no hay calificaciones
- Fac. Ciencias de La Salud - Taller Quimica 2 2019Documento4 páginasFac. Ciencias de La Salud - Taller Quimica 2 2019MAIRA ALEJANDRA ARREDONDO SANCHEZAún no hay calificaciones
- Informe N7Documento11 páginasInforme N7Alexis LQAún no hay calificaciones
- Manual 2 Química 2013Documento54 páginasManual 2 Química 2013Rodrigo Rivas MoraAún no hay calificaciones
- Pre Presentacion 14 7s Nomenclatura 2 2023 1Documento30 páginasPre Presentacion 14 7s Nomenclatura 2 2023 1Nicolle Campos chamorroAún no hay calificaciones
- Obtenciòn de Carbonato de Plomo y CobreDocumento6 páginasObtenciòn de Carbonato de Plomo y CobreDaniel Gomez Galindo100% (1)
- Cantidad de Sustancias PurasDocumento39 páginasCantidad de Sustancias PurasJulio FriasAún no hay calificaciones
- Fomulación InorgánicaDocumento17 páginasFomulación InorgánicaLibertad Sanchez GonzalezAún no hay calificaciones
- Compuestos TernariosDocumento10 páginasCompuestos TernariosKevin MonterrosoAún no hay calificaciones
- Nomenclatura InorganicaDocumento42 páginasNomenclatura InorganicanadieAún no hay calificaciones
- Química - Formación de CompuestosDocumento4 páginasQuímica - Formación de CompuestosCecilia LopezAún no hay calificaciones
- 09 - El Lenguaje de La Química - RespuestasDocumento13 páginas09 - El Lenguaje de La Química - Respuestasmaria belen beltranAún no hay calificaciones
- Informe 7 (Secuencia de Reacciones Quimicas)Documento5 páginasInforme 7 (Secuencia de Reacciones Quimicas)Steven Valencia100% (2)
- Formulacion InorganicaDocumento8 páginasFormulacion Inorganicamadenicola10Aún no hay calificaciones
- Cartilla de Quimica InorganicaDocumento59 páginasCartilla de Quimica InorganicaXfoxtro FsaAún no hay calificaciones
- Capitulo 3a - Nomenclatura y Reacciones QuimicasDocumento28 páginasCapitulo 3a - Nomenclatura y Reacciones QuimicasaleinAún no hay calificaciones
- Quimica1Taller JhonHiguitaDocumento8 páginasQuimica1Taller JhonHiguitaHiguitaED100% (1)
- Daniel ZambranoDocumento25 páginasDaniel ZambranoIsabella TorresAún no hay calificaciones
- Marcha Analitica Cationes Aniones Completo 1 PDFDocumento44 páginasMarcha Analitica Cationes Aniones Completo 1 PDFJosé Benjamín Argumé Sandoval100% (1)
- Sales OxisalesDocumento3 páginasSales OxisalesPatrick Bustos MiteAún no hay calificaciones
- Para La PPT de QuimicaDocumento6 páginasPara La PPT de QuimicaFranko Mendoza SueldoAún no hay calificaciones
- Taller 3, Sobre Nomenclatura Química InorgánicaDocumento3 páginasTaller 3, Sobre Nomenclatura Química InorgánicaJannys CamargoAún no hay calificaciones
- Informe Grupo 2Documento39 páginasInforme Grupo 2Malú Sandy Contreras RodríguezAún no hay calificaciones
- Taller Numero 4 Quimica 10Documento7 páginasTaller Numero 4 Quimica 10Danilo Ramirez BarreraAún no hay calificaciones
- Tarea 2 Química NomenclaturaDocumento4 páginasTarea 2 Química Nomenclaturachristopher espinozaAún no hay calificaciones
- Consulta 4Documento24 páginasConsulta 4Godoy IgnacioAún no hay calificaciones